미나리 추출물의 기능성 원료 표준화를 위한 지표성분으로서 Hyperoside, Quercetin 3-glucoside의 분석법 검증
Abstract
In this study, we developed and validated a high-performance liquid chromatography/diode array method for the quantification of Hyperoside and quercetin-3-glucoside as a marker compound in water dropworth (Oenanthe javanica DC.) extract (WDE). Method validation was performed by measuring specificity, linearity, limit of detection (LOD), limit of quantitation (LOQ), accuracy, and precision. Hyperoside and quercetin-3-glucoside were separated without interference from other substances at the same retention time and spectrum as the standard solution, demonstrating the analytical specificity. Calibration curves of hyperoside and quercetin-3-glucoside exhibited high linearity (R2≥1.000). The LOD and LOQ of hyperoside and quercetin-3-glucoside were 0.16, 0.49 μg/mL and 0.14, 0.41 μg/mL, respectively. The recovery rate of hyperoside and quercetin-3-glucoside were obtained 97.20–99.78% and 99.44–104.37%, respectively, indicating that the results were highly accuracy. Relative standard deviation values for precision of hyperoside and quercetin-3-glucoside were 0.84–1.62% and 1.96–2.50%, respectively. These results indicate that the proposed HPLC/DAD method for the detection of hyperoside and quercetin-3-glucoside in WDE is simple, reliable, and reproducible. Therefore, this analytical method could be used as basic data for the development of functional ingredients for health functional food of WDE.
Keywords:
Water dropworth(Oenanthe javanica DC.), Hyperoside, Quercetin-3-glucoside, Validation, Functional Ingredient미나리(Oenanthe javanica DC)는 미나리과 산형목에 속하는 쌍떡잎식물로 습지에서 자라고 논에서 재배되는 다년생 초본이며, 습지에 자생하여 수근(水芹), 수영(水英)등으로 불리며, 한국, 일본, 중국 등의 온대 북부지역과 타이완, 말레이시아, 인도 등 동남아 등 아시아 전역에 분포한다.1)
미나리는 94%의 수분과 단백질, 지질, 당질이 1-2% 나머지 무기질과 비타민으로 이루어져 있으며, 섬유질이 풍부한 대표적인 알칼리 식품으로 Ca, P, Fe, Na, K이 많이 포함되어 있고 특히 비타민 A, B, C가 풍부하다.2) 또한 미나리에는 플라보노이드 계열의 화합물이 다량 존재하며 지금까지 apigenin, isorhamnetin-3-O-β-D-glucopyranoside, quercetin, isorhamnetin, isorhamnetin-3-O-galactoside, persicarin, afzelin, hyperoside, luteolin, kaempferol, rutin, nictoflorin, and quercetin-3-L-rhamnoside를 포함하여 10가지 이상의 플라보노이드가 분리 및 확인되었다.3)
미나리는 오래전부터 계절채소로 이용되어 왔으며, 일부 한방에서는 잎과 줄기를 수근이라고 하여 건조품을 약재로 사용하기도 한다.4) 미나리의 독특한 향과 맛은 입맛을 돋우어 주고 각종 독소를 배출하는 해독작용이 뛰어나며, 혈압을 낮추어 주는 효과가 있어 고혈압 환자에게 좋은 식품이고, 간장 질환에 좋아 황달이나 급·만성 간염 및 간경변증에 많이 이용되고 음주 후 주독을 제거하는데 사용하기도 했으며5-7) 또한 항염증,8,9) 항산화10,11) 및 항바이러스12,13) 등의 효능이 보고되어 있다.
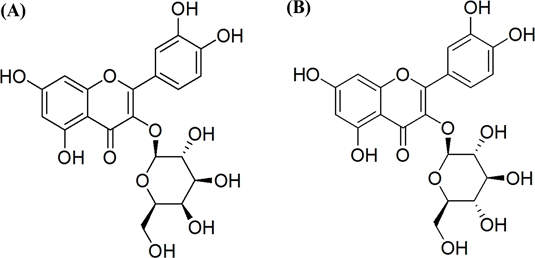
이러한 생리적 기능성을 함유한 미나리를 소재로 건강기능식품을 개발하기 위해서 지표성분 설정과 원료 표준화 연구가 선행되어야 하고 원료의 품질과 기능성을 판단할 수 있는 지표성분 함량의 기준 및 규격 설정을 위한 분석법의 유효성 검증 자료가 요구된다. 미나리 추출물의 지표성분 분석연구가 일부 보고되어14) 있으나 이는 미나리 에탄올 추출물의 지표성분으로 설정한 isorhamnetin의 high performance liquid chromatography (HPLC) 분석법이고 산 가수분해를 진행하지 않은 미나리 열수 추출물에서는 isorhamnetin의 함량을 확인할 수 없었다. 본 연구에서는 전주 미나리 열수 추출물 내 플라보노이드 중 하나인 hyperoside와 quercetin-3-glucoside를 지표성분으로 선정(Fig. 1) 하고 두 성분의 동시 분석을 위한 HPLC 분석법을 확립하고 유효성을 검증하였다.
재료 및 방법
실험재료 - 본 실험에 사용한 미나리는 전북특별자치도 전주시에서 재배한 미나리로서 3~5월에 채취한 것을 사용하였고, 미나리 원물을 정제수로 3회 세척하여 불순물을 제거한 후 열풍건조기(HDG-230T, Hyundai Enertec Co.)로 16시간 건조하였다. 건조된 미나리를 분쇄한 후 정제수 50배수를 가하여 추출농축시스템(EES-1200, HS TECH Co.)에서 95℃ 열수 추출 및 여과를 2회 진행한 다음 1차, 2차 추출물을 혼합 농축하여 분무 건조기(SD-01, KoreaBio Solutions Co.)로 분말화 하였다. 미나리 추출물의 분석에 사용된 표준물질 hyperoside (00180585, Sigma-Aldrich Co.)와 quercetin-3-glucoside (16654, Sigma-Aldrich Co.)는 Sigma-Aldrich에서 구입하여 사용하였다.
표준용액의 조제 - Hyperoside와 quercetin-3-glucoside 표준물질 5 mg을 정밀하게 달아 10 mL의 정용 플라스크에 취한 후 70% Methanol을 가해 초음파 추출하여 완전히 녹인 다음 1 mg/mL이 되도록 표준원액을 제조한 후 4℃에서 냉장 보관하였다. 표준 원액은 70% methanol로 단계적으로 희석하여 hyperoside (1.656–68.500 μg/mL), quercetin-3-glucoside (1.672–70.000 μg/mL) 농도범위 내에서 6개 농도의 표준용액을 조제한다. 전주 미나리 추출물 1000 mg을 취하여 70% 메탄올 20 mL에 녹여 30분간 초음파 추출하고 방냉 후 정용하여 0.45 μm filter로 여과한 것을 시험용액으로 사용하였다.
HPLC 분석 - 전주 미나리 추출물에 함유된 hyperoside와 quercetin-3-glucoside는 Diode Array Detector (DAD)가 장착된 HPLC (1260 Infinity, Agilent co.)를 통해 분석되었으며, 분석조건은 Table I과 같다. 분석 컬럼은 Cadenza Column C18 (4.6 × 250 mm, 3 μm)을 사용하였고, 이동상은 0.1% formic acid가 포함된 증류수(A)와 0.1% formic acid가 포함된 acetonitrile (B)을 사용하여 0.5 mL/min의 유량으로 하고 컬럼 온도는 30°C를 유지하였다. 검출파장은 254 nm로 설정하였으며 gradient condition으로 시료 10 μL를 주입하여 분석하였다.
분석법 검증 - 분석법의 유효성 검증(method validation)은 전주 미나리 추출물 내 유효 성분의 개별인정형 건강기능식품 기능성 원료로 등록하기 위한 것으로 의약품 등 분석법의 벨리데이션에 대한 가이드라인을15) 근거로 하여 지표성분에 대한 특이성(specificity), 직선성(linearity), 정확성(accuracy) 및 정밀성(precision)을 조사하고 검출한계(limit of detection, LOD)와 정량한계(limit of quantification, LOQ)를 평가하여 분석법을 검증하였다.
a) 특이성(specificity): 특이성은 추출물, 불순문, 분해물 등의 혼재 상태에서 분석대상 물질은 선택적으로 정확하게 측정할 수 있는 능력으로 hyperoside와 quercetin-3-glucoside 표준용액과 시험용액을 HPLC로 분석하여 크로마토그램상의 머무름시간(retention time)과 spectrum을 비교하였다.
b) 직선성(linearity): 직선성은 검체 중 분석대상물질의 양(또는 농도)에 비례하여 일정 범위 내에 직선적인 측정값을 얻어낼 수 있는 능력으로 표준용액을 2.014–70.000 μg/mL 농도 범위 내에서 6개 농도로 제조하고 HPLC 분석 후 검출성분의 피크 면적과 표준용액 농도 간의 검량선을 작성하여 상관계수(correlation coefficient, R2)를 확인하였다.
c) 정확성(accuracy): 정확성은 분석물질의 이론값과 분석법에 의해 얻은 측정값의 근접한 정도를 확인하는 방법으로, 농도를 알고 있는 시험용액에 표준용액을 저농도, 중농도, 고농도로 첨가하여 HPLC로 농도별 3회 반복 측정하였다. 시험용액에 첨가된 표준용액의 이론값과 실측값에 대한 회수율(recovery, %)을 구하여 정확성을 평가하였다.
d) 정밀성(precision): 정밀성은 균일한 검체로부터 여러 번 채취하여 얻은 검체를 정해진 조건에 따라 측정하였을 때 각각의 측정값들 사이의 근접성을 말하는 것으로 일정 농도로 조제한 시험용액에 대해 HPLC로 5회 반복 측정하여 반복성(repeatability)을 확인하였으며, 서로 다른 시험자가 단일 농도의 시험용액을 각각 5회 반복 측정하고 그에 대한 상대표준편차(relative standard deviation, %RSD)를 구해 재현성(reproducibility)을 확인하여 정밀도를 판단하였다.
정량한계 및 검출한계 - 정량한계는 적절한 정밀성과 정확성을 가진 정량값으로 표현할 수 있는 검체 중 분석대상물질의 최소량을 의미하고 검출한계는 검체 중 분석대상물질의 검출 가능한 최소량을 뜻한다. 각 성분에 대한 정량한계와 검출한계는 표준용액의 크로마토그램을 사용하였고, 직선성 검증으로 구한 검량선의 기울기(slope)와 y절편의 표준편차(standard deviation)를 통해 정량한계 10×σ/s (σ: 표준편차, s: 표준검량선의 기울기), 검출한계 3.3×σ/s 식을 이용하여 확인하였다.
결과 및 고찰
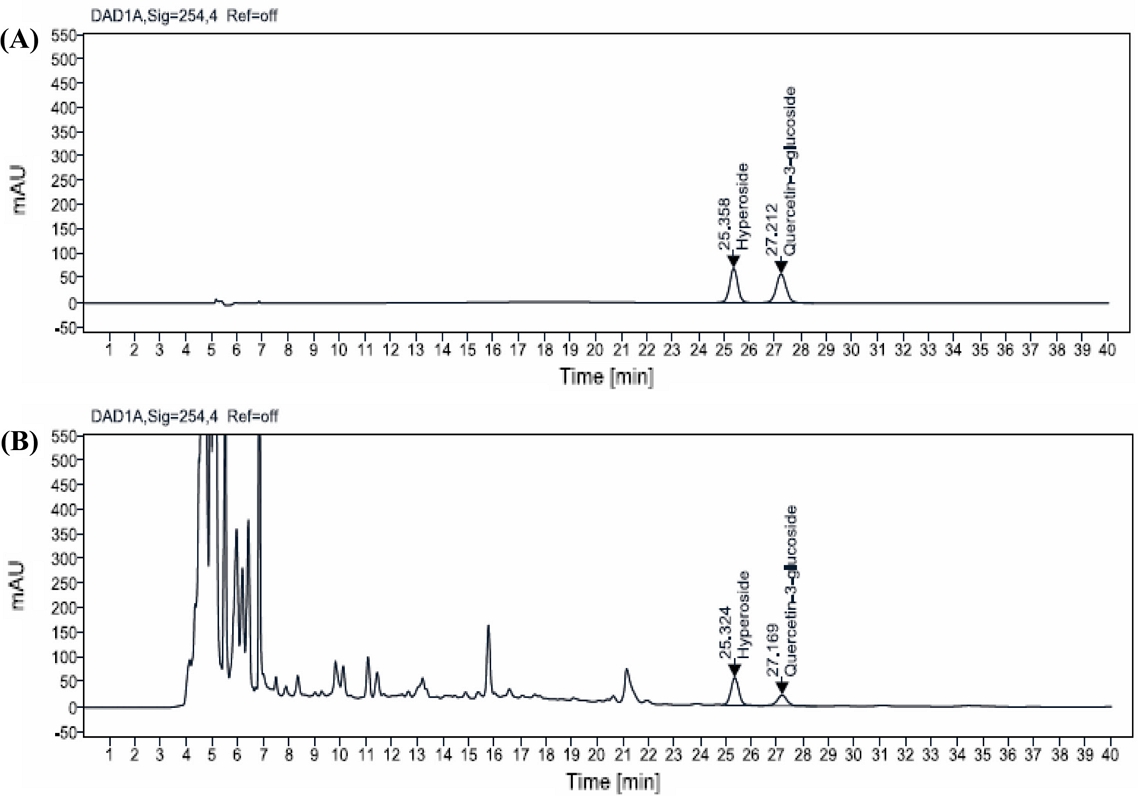
특이성 검증 - 특이성 검증은 여러가지 다른 성분들이 혼합되어 있는 미나리 추출 분말 중에서 hyperoside와 quercetin-3-glucoside를 선택적으로 정확하게 측정할 수 있는지 확인하기 위해 실시하였다. HPLC를 이용하여 표준용액에서의 hyperoside와 quercetin-3-glucoside 크로마토그램을 비교한 결과 다른 물질 간섭 없이 지표성분 2종이 분리된 것을 확인할 수 있었다(Fig. 2). 표준 용액과 미나리 추출물의 머무름 시간은 hyperoside에서 25분대, quercetin-3-glucoside에서 27분대로 표준용액의 피크 유지시간과 미나리 추출물의 피크 유지시간이 일치하였다. 또한, 표준 용액과 미나리 추출물의 DAD spectrum 측정에서도 같은 spectrum을 확인하였다(Fig. 3). 이러한 결과는 본 시험법이 hyperoside와 quercetin-3-glucoside의 분석을 위한 특이성이 있음을 의미한다.
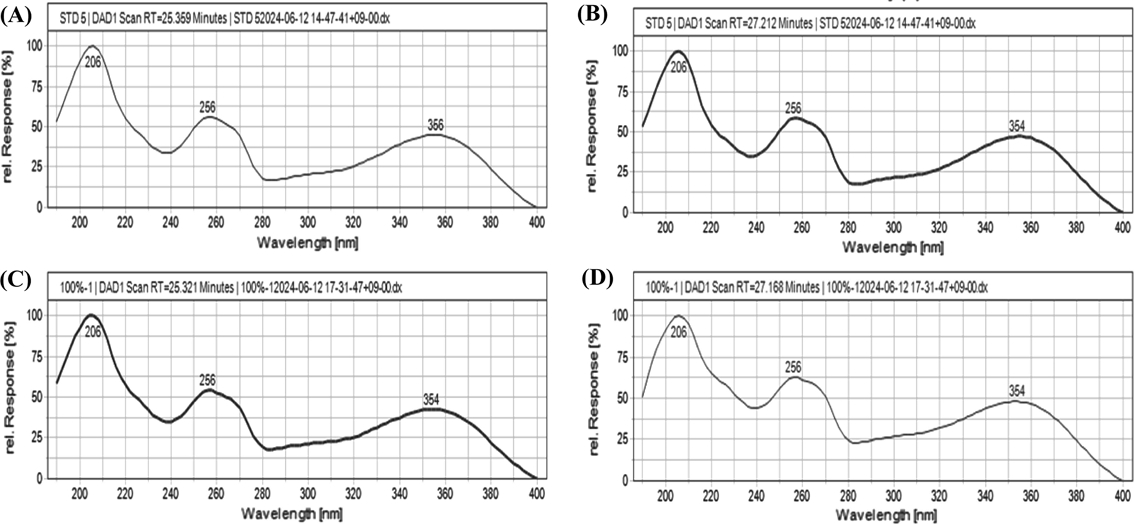
DAD (Diode Array Detector) spectrum of hyperoside and quercetin-3-glucoside. (A) Hyperoside standard solution, (B) Quercetin 3-glucoside standard solution, (C) Hyperoside in water dropwort extract, (D) Quercetin-3-glucoside in water dropwort extract.
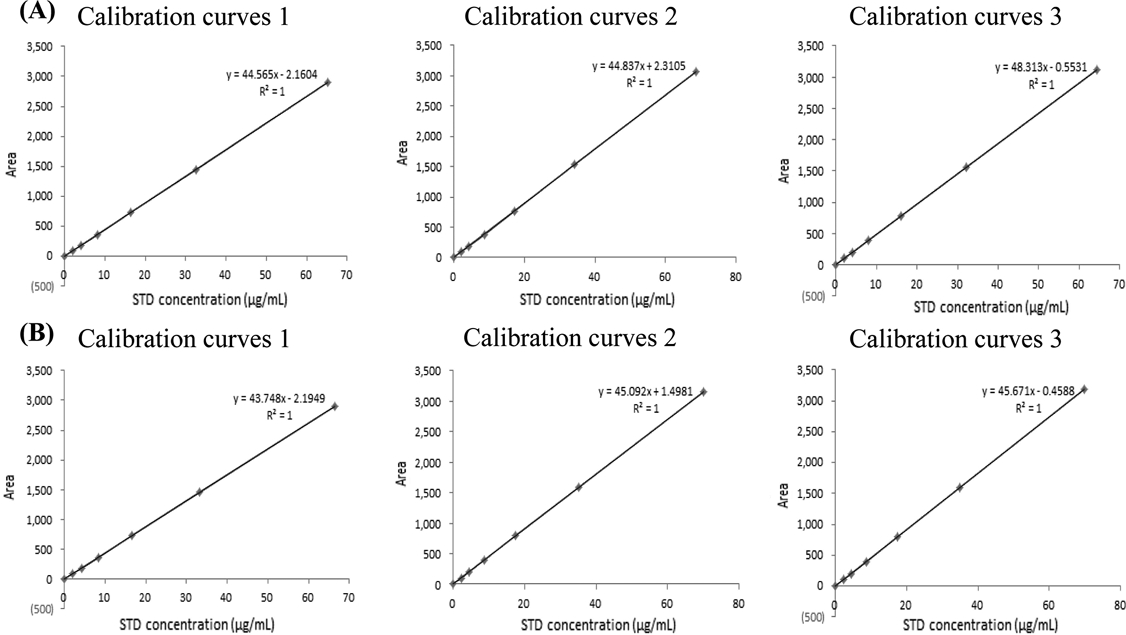
직선성 검증 - Hyperoside와 quercetin-3-glucoside 표준품을 1.656–70.000 μg/mL 농도 범위내에서 6개 농도의 표준용액으로 제조하고 HPLC를 이용하여 3회 반복 분석하였다. 검출된 hyperoside와 quercetin-3-glucoside 피크 면적을 통하여 검량선을 작성하였으며 검량선의 상관계수(R2)는 Fig. 4와 같이 hyperoside와 quercetin-3-glucoside 모두 1.000으로 나타나 높은 직선성을 보였다.
정확성 검증 - 전주 미나리 추출물 중 지표성분의 정확성을 측정하기 위해 시료에 표준용액을 넣은 후 분석에 의해 회수되는 회수율을 측정하였다. 미나리 추출물 1000 mg을 취한 후, 시료 중의 함유된 지표성분의 함량이 50%, 100%, 150%의 농도가 되도록 표준 용액을 hyperoside는 0.29 mL, 0.58 mL, 0.58 mL씩, quercetin-3-glucoside는 0.135 mL, 0.269 mL, 0.405 mL씩 첨가하여 정확도 시험을 수행하였다. HPLC를 이용하여 농도별로 3회 반복 분석하고 회수율은 기준농도를 고려하여 90–108%를 기준으로 하였다.16) 회수율 시험용액에 대한 표준값을 산출하고 동일 전처리 및 HPLC로 분석한 결과값을 이용하여 회수율을 계산하였다(Table II). 각 시험 용액에 대한 3개 농도의 hyperoside 회수율은 94.98–101.57%, quercetin-3-glucoside의 회수율은 95.72–105.72%로 나타나 본 시험법의 정확성을 확보하였다.
정밀성 검증
a) 반복성: 시료량의 변화에 따른 반복정밀도를 확인하기 위해 미나리 추출물을 500 mg, 1000 mg, 1500 mg의 3개 농도를 조제하여 HPLC조건으로 5회 반복 측정한 결과, hyperoside과 quercetin-3-glucoside의 RSD는 각각 0.73– 1.93%, 0.91–2.90%로 나타났다(Table III). 이는 지표성분 함량을 고려하여 설정된 기준(4% 이내)에 부합하는 것으로 나타나 반복성이 있음을 확인하였다.16)
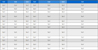
Content of hyperoside and quercetin-3-glucoside according to sample weight in water dropwort extract
b) 재현성: 시료량을 정량하여 시험자, 기기, 일자를 달리하여 5회 반복 측정하여 상대표준편차(RSD)를 구하였다. 3일간 반복하여 분석한 결과 전체 평균값은 hyperoside가 0.54±0.007 mg/g, quercetin-3-glucoside가 0.26±0.009 mg/g 이였으며, RSD 값은 각각 1.45%와 3.47%로 나타났다. 이는 AOAC 재현성(0.01%(0.1 mg/g)일 때, RSD 8% 이내) 범위에 부합하여 재현성이 있음을 확인하였다(Table IV). 위의 반복성과 재현성 결과를 통해 본 시험법의 정밀도를 확보하였다.

Content of hyperoside and quercetin-3-glucoside according to interday precision in water dropwort extract
정량한계 및 검출한계 - 직선성 검증을 통해 얻은 검량선의 기울기와 y절편을 통해 기울기 평균값과 y절편의 표준편차를 계산하고 이를 통해 정량한계와 검출한계를 구한 결과는 Table V와 같다. Hyperoside의 경우 S는 45.90, σ는 2.265로 정량한계와 검출한계는 각각 0.49, 0.16 μg/mL였으며, quercetin-3-glucoside의 경우 S는 44.84, σ는 0.14로 정량한계와 검출한계는 각각 0.41, 0.14 μg/mL로 확인되었다.

The limit of detection (LOD) and limit of quantitation (LOQ) for hyperoside and quercetin-3-glucoside analysis in water dropwort extract
전주 미나리 추출물의 hyperoside 와 quercetin-3-glucoside 함량 - 본 시험법의 검증 과정을 통해 개발된 HPLC분석법이 미나리 추출물의 지표성분 hypreoside와 quercetin-3-glucoside의 정량분석법으로 충분한 감도, 특이성, 직선성, 정확성 및 정밀성을 갖고 있음을 확인하였다. 검증된 분석법을 이용하여 미나리 추출물의 지표 성분 함량을 분석한 결과, hyperoside와 quercetin-3-glucoside의 평균 함량은 추출물 g당 각각 0.54 mg과 0.26 mg이었으며(Table VI), 건강기능식품 기능성 원료 인정 규정에17) 따라 80–120%의 지표 성분 함량 범위를 고려할 경우 Hyperoside는 0.432–0.648 mg/g, quercetin-3-glucoside는 0.208–0.312 mg/g으로 확인되었다.
결 론
본 연구는 전주 미나리 추출물을 개별인정형 건강기능식품 원료로 개발하기 위해 지표성분으로 hyperoside와 quercetin-3-glucoside를 설정하고, 이를 정량 분석하기 위한 HPLC/DAD 분석법을 확립하여 그 유효성을 검증하였다. 분석법 검증은 특이성, 직선성, 검출한계(LOD), 정량한계(LOQ), 정확성 및 정밀성을 측정하여 수행하였으며, 국내외 가이드라인에 부합하는 결과를 확인하였다. 이에 본 시험법이 신뢰성 있는 분석이 가능함을 검증하였으며, 본 HPLC/DAD 분석법이 향후 미나리의 개별인정형 건강기능식품 기능성 원료개발을 위한 기초 자료로 활용될 것으로 기대된다.
Acknowledgments
본 논문은 (재)전주농생명소재연구원 전주시책연계사업 수행과제 결과의 일부이며 전주시의 지원을 받아 이루어진 것으로 이에 감사드립니다.
References
-
Won, B. H., Shin, K. Y., Ha, H. J., Yun, Y. S., Kim, Y. R. and Lee, H. G. (2015). Changes in nutritional composition of dropwort (Oenanthe javanica) ethanol extracts. J. Korean Soc. Food Sci. Nutr. 44: 882-887.
[https://doi.org/10.3746/jkfn.2015.44.6.882]

- Park, S. J., Lee, K. S. and An, H .L. (2007) Effects of dropwort powder on the quality of castella. J. East Asian Soc. Dietary Life 17: 834-839.
-
Lu, C. L. and Li, X. F. (2019) A review of Oenanthe javanica (Blume) DC. as traditional medicinal plant and its therapeutic potential. Evid. Based Complement Alternat. Med. 2019: 6495819.
[https://doi.org/10.1155/2019/6495819]

- Jo, H. W., Lee, S. H., Nam, D. H., Kim, J. Y., Lim, S. K., Lee, J. S. and Park J. C. (2008) Antioxidant activity and phytochemical study on the aerial parts of Oenanthe javanica. Korean J. Pharmacogn. 39: 142-145.
- Jeon, E. J., Kim, J. S., Park, Y. K., Kim, T. S. and Kang, M. H. (2003) Protective effect of yellow-green vegetable juices on DNA damage in Chinese hamster lung cell using comet assay. Korean J. Nutr. 36: 24-31.
-
Ai, G., Huang, Z. M., Liu, Q. C., Han, Y. Q. and Chen, X. (2016) The protective effect of total phenolics from Oenanthe javanica on acute liver failure induced by D-galactosamine. J. Ethnopharmacol. 186: 53-60.
[https://doi.org/10.1016/j.jep.2016.03.024]

-
Lee, D. H., Lee, J. S., Lee, I. H. and Hong, J. T. (2020) Therapeutic potency of fermented field water-dropwort (Oenanthe javanica (Blume) DC.) in ethanol-induced liver injury. RSC Adv. 10: 1544-1551.
[https://doi.org/10.1039/C9RA08976D]

-
Ahn, H. and Lee, G. S. (2017) Isorhamnetin and hyperoside derived from water dropwort inhibits inflammasome activation. Phytomedicine 24: 77-86.
[https://doi.org/10.1016/j.phymed.2016.11.019]

-
Bae, U. J., Jang, H. N., Lee, S. H., Kim, J. Y. and Kim, G. C. (2022) Oenanthe javanica ethanolic extract alleviates inflammation and modifies gut microbiota in mice with DSS-induced colitis. Antioxidants (Basel). 11: 2429.
[https://doi.org/10.3390/antiox11122429]

-
Tae, H. J., Park, J. H., Cho, J. H., Kim, I. H., Ahn, J. H., Lee, J. C., Kim, J. D., Park, J., Choi, S. Y. and Won, M. H. (2014) Oenanthe javanica extract increases immunoreactivities of antioxidant enzymes in the rat kidney. Chin. Med. J. (Engl). 127: 3758-3763.
[https://doi.org/10.3760/cma.j.issn.0366-6999.20141863]

-
Lee, C. H., Park, J. H., Cho, J. H., Kim, I. H., Ahn, J. H., Lee, J. C., Chen, B. H., Shin, B. N., Tae, H. J., Bae, E. J., Kang, I. J., Won, M. H. and Kim, J. D. (2015) Effect of Oenanthe javanica extract on antioxidant enzyme in the rat liver. Chin. Med. J. (Engl). 128: 1649-1654.
[https://doi.org/10.4103/0366-6999.158363]

-
Wang, W. N., Yang, X. B., Liu, H. Z., Huang, Z. M. and Wu, G. X. (2005) Effect of Oenanthe javanica flavone on human and duck hepatitis B virus infection. Acta Pharmacol. Sin. 26: 587-592.
[https://doi.org/10.1111/j.1745-7254.2005.00055.x]

-
Han, Y. Q., Huang, Z. M., Yang, X. B., Liu, H. Z. and Wu, G. X. (2008) In vivo and in vitro anti-hepatitis B virus activity of total phenolics from Oenanthe javanica. J. Ethnopharmacol. 118: 148-153.
[https://doi.org/10.1016/j.jep.2008.03.024]

-
Won, B. Y., Shin, K. Y., Ha, H. J., Wee, J. H., Yun, Y. S., Kim, Y. R., Park, Y. J., Jung, K. O., Sung, H. M. and Lee, H. G. (2016) Inhibitory effects of dropwort(Oenanthe javanica) extracts on memory impairment and oxidative stress and the qualitative analysis of isorhamnetin in the extracts. J. Korean Soc. Food Sci. Nutr. 45: 1-11.
[https://doi.org/10.3746/jkfn.2016.45.1.001]

- MFDS (2015) Guide-lines for validation of analysis method in pharmaceuticals. Ministry of Food and Drug Safety.
- AOAC (2023) Appendix K: Guidelines for dietary supplements and botanicals. In: Official Methods of Analysis AOAC International. 20th ed. AOAC International. p.9-11.
- MFDS (2023) Regulations concerning recognition of Functional ingredients and standards and specifications for health Functional Foods. Ministry of Food and Drug Safety. p.12.