국내 기능성 식물의 생리활성 대사체 정량 분석
Abstract
Functional plants cultivated in Korea are recognized as rich sources of bioactive metabolites with potential health benefits. In this study, seventeen metabolites were quantified from thirty different Korean functional plant species using liquid chromatography–tandem mass spectrometry (LC-MS/MS). As these seventeen compounds exhibit diverse bioactivities, they can serve as indicators to explore and suggest the potential functional properties of the plants.
Keywords:
Functional plants, Bioactive metabolites, LC-MS, Quantification전 세계적으로 식물은 수천 년에 걸쳐 인간의 삶 속에서 식용 및 약용 자원으로 광범위하게 활용되어 왔다. 인류는 식물을 통해 영양소를 공급받는 것은 물론, 다양한 생리활성 성분을 기반으로 질병을 치료하거나 건강을 증진해왔다. 2022년 기준 전 세계 건강기능식품 시장 규모는 약 1,761억 7천 달러(230조 1,600억원)에 달하며, 전년 대비 성장세를 보이고 있다.1) 식물은 다양한 생리활성 대사체를 함유하고 있는데, 특히 플라보노이드, 테르페노이드, 알칼로이드 등은 항산화, 항염증, 항암, 면역 조절 등 다양한 생리작용을 통해 인체 건강에 긍정적인 영향을 미치는 것이 알려져 있다.2-4) 이러한 생리활성 물질들은 건강기능식품의 핵심 소재로 활용되고 있을 뿐만 아니라, 천연물 의약품, 화장품 및 향수 등 다양한 산업 분야에도 매우 중요한 가치가 있다.5) 국내에서는 식물이 약용과 식용으로 사용되고 있으며,6) 천연물 신약 연구 개발 촉진법 시행령이 공포된 이후,7) 식물 대사체에 대한 분석과 응용 연구는 더욱 활발히 이루어지고 있다.
식물은 동물이나 미생물과 비교해 훨씬 더 다양한 이차 대사 산물을 생성하는 것으로 알려져 있는데, 일반적으로 수십만 개에 이르는 대사산물이 식물체에 존재하는 것으로 추정되며,8,9) 개별 식물 종마다 수천 개 수준의 대사산물을 포함하고 있는 것으로 여겨진다.10) 이러한 대사체의 조성 및 함량은 식물의 종뿐만 아니라, 재배 환경, 수확 시기, 가공 방법 등에 따라 크게 달라질 수 있다. 따라서 국내에서 재배되는 기능성 식물들에 존재하는 생리활성 대사체를 정량하는 연구는, 해당 식물의 기능성에 대한 과학적 근거를 확보하고 품질 표준화를 위한 기초자료를 마련하는 데 필수적이다. 본 연구에서는 국내에서 재배된 30가지 기능성 식물을 대상으로, LC-MS 기반 분석을 수행하여 총 17종의 생리활성 대사체를 정량하였다. 이를 통해 식물 종별 생리활성 대사체 특성을 분석하고, 해당 식물의 잠재적 기능성을 탐색하고자 하였다.
재료 및 방법
시약 및 재료 − 전반적인 분석 과정은 이전에 보고된 논문을11) 참고했다. MS grade water, MS grade methanol (MeOH), LC grade acetonitril, LC grade ethanol (EtOH)은 J.T. Baker (Phillipsburg, NJ, USA)에서 구매했고, formic acid는 Sigma Aldrich (St. Louis, MO, USA)제품을 사용했다. 국내에서 재배된 기능성 채소류 및 과일류 30종(갓, 개똥쑥, 겨자, 고사리, 곤드레, 곰취, 근대, 더덕, 돌나물, 모시풀, 민들레, 바디나물, 방아풀, 병품쌈, 블루베리, 뽀리뱅이, 산마늘, 셀러리, 시금치, 쑥갓, 삼채, 양상추, 어수리, 연, 유채나물, 참나물, 케일, 콜라비, 헛개나무, 화살나무)은 국립식량과학원으로부터 건조된 분말 형태로 제공받았으며, 분석 전까지 4℃에서 냉장보관되었다.
대사체추출 − 각 30종 식물 시료에 70% EtOH 또는 MeOH를 100 mg/mL 로 첨가하여, 상온에서 1시간동안 초음파 추출을 수행했다. 이후 10,000 g에서 10분간 원심분리하여 상층액을 회수했고, 0.2 µm syringe filter로 여과한 뒤 질량 분석에 사용하였다.
질량 분석 − 분석에는 Agilent 1290 Infinity II LC coupled with 6530 Q-TOF LC/MS를 사용했다. 컬럼은 Waters (Milford, MA, USA)의 acquity bridged ethyl hybrid C18 (1.7 µm, 2.1 mm×100 mm)를 썼고, 온도는 40℃로 유지했다. 이동상은 A: water + 0.1% formic acid, B: acetonitrile + 0.1% formic acid였다. Gradient와 flow rate은 Table I과 같다. 시료는 2 µL를 주입했다. Electrospray ionization (ESI) mode로 positive mode와 negative mode를 모두 적용해, 데이터 의존적 분석(data-dependent analysis, DDA)을 수행했는데, 상세한 질량 분석 조건은 Table II와 같다.
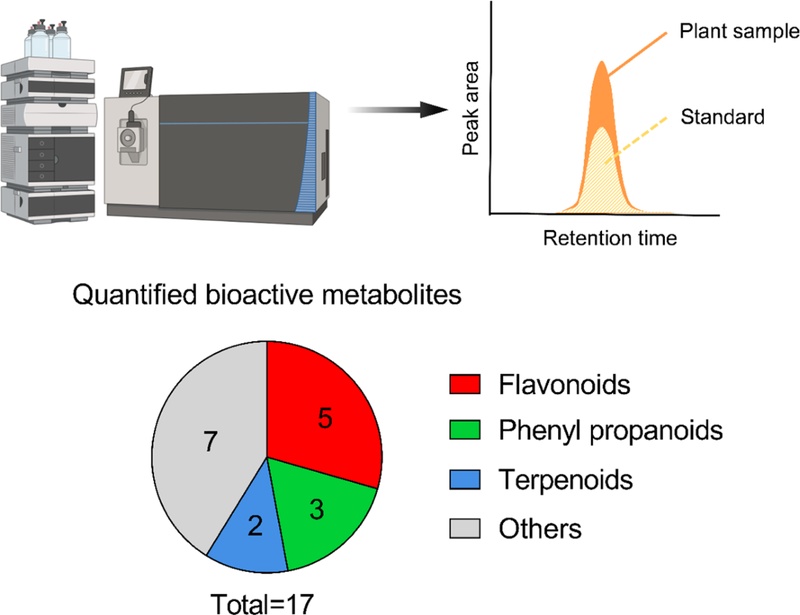
대사체 정량 분석 − 식물 대사체 정량을 위해 Sigma Aldrich에서 제공하는 PHYTOMOLS (phytochemical metabolite library of standards)을 사용해, 각 표준물질이 80% MeOH에서 최종 농도가 0.5 ppm이 되도록 식물 대사체 표준물질 혼합물을 제조했다.12) 이후 LC-MS 분석을 통해 각 표준물질의 precursor m/z, retention time(RT) 및 MS2 fragmentation 정보(MS/MS)를 확보했고, 이를 기반으로 시표에 포함된 대사체를 식별했다. m/z와 RT의 similarity score 가 900 이상이고, 동시에 MS/MS의 Rev. dot score 값이 750 이상인 경우에 한하여 해당 대사체를 식별했다. 대사체 정량으로 single point external standard method를 사용했다.13) 표준물질에서 얻은 peak area와 시료에서 관측되는 peak area를 비교해, 식물 대사체를 정량하였다(Fig. 1). 정량 값은 소수점 셋째 자리에서 반올림하였으며, 재현성을 확보하기 위해 3회 반복 측정에서 싱대표준편차가 30% 미만인 대사체만을 정량에 포함하였다. 데이터는 MS data independent analysis (DIAL)와 GraphPad Prism 9.5.1 소프트웨어로 처리 및 시각화되었다.
결과 및 고찰
본 연구에 사용한 식물 대사체 분석법을 통해 국내에서 재배된 30종의 기능성 식물에서 17종의 생리 활성 대사체를 정량할 수 있었다(Fig. 1). 정량된 17종의 생리활성 대사체는 식물에서 흔히 발견되는 주요 대사체 계열(flavonoid, phenylpropanoids, terpenoid)에 해당되며, 항산화, 항염증, 항암, 항당뇨 등 다양한 생리활성 범주를 포함하고 있어,14-30) LC–MS 정량법의 범용성을 검증하기 위한 대상으로 선정되었다. 이들 17종 대사체의 정량분석 결과는 Table III에 제시하였다. 각 성분에서 함량이 가장 높은 식물은 *표시로 나타냈다. 두 추출 조건에서 얻은 정량 값이 다소 차이를 보이는 경우도 있었으나, 많은 경우, 70% EtoH로 추출한 정량값과 MeOH로 추출한 정량값이 서로 유사했다.
본 연구에서 정량된 17종의 대사체는 각 식물의 잠재적 기능성을 탐색하는 지표로 활용될 수 있다. 예를 들어, 블루베리(Vaccinium corymbosum)와 바디나물(Angelica decursiva)에서 검출된 aesculin과 ginkgolide A는 해당 식물에서 보고된 항염증 활성과의31,32) 관련 가능성을 시사한다. 방아풀(Isodon japonicus)과 케일(Brassica oleracea)에서 확인된 asiatic acid와 ginkgolide C 역시 해당 식물의 항암 활성을33,34) 지지하는 대사적 단서 중 하나로 해석될 수 있다. 또한, glycerophosphocholin, hesperidine, isoliquiritigenin 은 각각 갓(Brassica juncea), 바디나물, 개똥쑥에서 검출되어, 이들 식물의 뇌기능 개선,35) 순환계 개선,36) 항비만 활성과의37) 잠재적인 연관성을 보여주는 지표로 활용될 수 있다. 바디나물에서 확인된 지질 개선 활성이 있는 eriocirtrin, 항 비만 효능이 있는 phenylpropionylglycine, 항멜라닌 활성을 가진 umbelliferone는 해당 식물이 다양한 기능성과 연관될 가능성을 시사하는 대사적 단서가 될 수 있다. 또한 어수리에서 검출된, 순환계에 작용하는 imperatorin는 이 식물의 순환계 활성을 탐색하는 참고 지표로 해석될 수 있다. 식물의 생리활성은 다수의 대사체가 상호작용하여 발현되기 때문에, 식물의 기능성을 검증하기 위해서는 추가적인 실험적 검증이 필요하다.
본 연구에서 적용한 single point external standard method는 검량선 작성이 불필요하므로 표준물질 사용량을 줄일 수 있으며, 표준물질이 고가이거나 확보가 어려운 경우, 특히 식물 등 천연물 분석에서 유용한 장점이 있다. 또한 분석 시간을 단축할 수 있어, 다수의 대사체를 신속하게 정량 분석하는데 적합하다. 그러나 검량선 기반의 정량분석에 비해 정확도가 제한될 수 있으며, matrix effect나 이온화 효율 차이에 따른 편차가 발생할 가능성이 있다. 따라서 향후 연구에서는 검량선을 포함한 정량법을 적용하여 보다 정확한 정량을 수행할 필요가 있다.
결 론
본 연구에 사용된 30종의 기능성 식물들은 항산화, 항염증, 항암 등 다양한 생리 활성과 관련된 대사체를 함유하고 있으며, 본 연구에서는 이들 대사체를 정량하여 각 식물의 잠재적 기능성을 탐색하였다. 이러한 결과는 식물 기능성에 대한 과학적 근거를 마련하는 기초 자료로 활용될 수 있으며, 새로운 기능성의 가능성을 제시하는 데에도 기여할 수 있다.
Acknowledgments
This research was supported by a grant from the Rural Development Administration of Korea (RS-2022-RD010385).
References
- 김종성 (2024) 미국 식물 기능성 식품 시장의 현황과 전망. 식품산업과 영양 29: 45-52.
-
Zhao, Y., Liu, G., Yang, F., Liang, Y., Gao, Q., Xiang, C., Li, X., Yang, R., Zhang, G. and Jiang, H. (2023) Multilayered regulation of secondary metabolism in medicinal plants. Molecular Horticulture 3: 11.
[https://doi.org/10.1186/s43897-023-00059-y]

-
D’auria, J. C. and Gershenzon, J. (2005) The secondary metabolism of arabidopsis thaliana: Growing like a weed. Current Opinion in Plant Biology 8: 308-316.
[https://doi.org/10.1016/j.pbi.2005.03.012]

-
Wang, S., Alseekh, S., Fernie, A. R. and Luo, J. (2019) The structure and function of major plant metabolite modifications. Molecular Plant 12: 899-919.
[https://doi.org/10.1016/j.molp.2019.06.001]

- Hassan, B. (2012) Medicinal plants (importance and uses). Pharmaceut. Anal. Acta 3: 2153-2435.
- 이용섭 and 이용화. (2017) 한방소재의 기능성 탐색 및 제 품화연구. 한국유화학회 학술대회 논문집 2017: 28-28.
- Bae, J. M., Kim, J. H., Cho, H. R., Shin, Y. J. and Bae, M. J. (2022) Activation plan of functional food market with domestic ingredients. Food Industry and Nutrition 27: 17-21.
-
Rai, A., Saito, K. and Yamazaki, M. (2017) Integrated omics analysis of specialized metabolism in medicinal plants. Plant Journal 90: 764-787.
[https://doi.org/10.1111/tpj.13485]

-
Fang, C., Fernie, A. R. and Luo, J. (2019) Exploring the diversity of plant metabolism. Trends in Plant Science 24: 83-98.
[https://doi.org/10.1016/j.tplants.2018.09.006]

-
Fernie, A. R., Trethewey, R. N., Krotzky, A. J. and Willmitzer, L. (2004) Metabolite profiling: from diagnostics to systems biology. Nature Reviews Molecular Cell Biology 5: 763-769.
[https://doi.org/10.1038/nrm1451]

-
Min, Y., Kim, T., Jung, C., Cho, I., Jang, H., Hwang, I. and Kwon, S. (2024) Global profiling of metabolites in korean medicinal and functional plants by an in-house library. Korean Journal of Pharmacognosy 55: 229-246.
[https://doi.org/10.22889/KJP.2024.55.4.229]

-
Tsugawa, H., Nakabayashi, R., Mori, T., Yamada, Y., Takahashi, M., Rai, A., Sugiyama, R., Yamamoto, H., Nakaya, T. and Yamazaki, M. (2019) A cheminformatics approach to characterize metabolomes in stable-isotope-labeled organisms. Nature Methods 16: 295-298.
[https://doi.org/10.1038/s41592-019-0358-2]

-
Kakouri, E., Trigas, P., Daferera, D., Skotti, E., Tarantilis, P. A. and Kanakis, C. (2023) Chemical characterization and antioxidant activity of nine hypericum species from greece. Antioxidants 12: 899.
[https://doi.org/10.3390/antiox12040899]

-
Benameur, T., Giacomucci, G., Panaro, M. A., Ruggiero, M., Trotta, T., Monda, V., Pizzolorusso, I., Lofrumento, D. D., Porro, C. and Messina, G. (2022) New promising therapeutic avenues of curcumin in brain diseases. Molecules 27: 236.
[https://doi.org/10.3390/molecules27010236]

-
Barbagallo, M., Giordano, M., Meli, M. and Panzarasa, R. (1994) Alpha-glycerophosphocholine in the mental recovery of cerebral ischemic attacks. An italian multicenter clinical trial. Annals of the New York Academy of Sciences 717: 253-269.
[https://doi.org/10.1111/j.1749-6632.1994.tb12095.x]

-
Mas-Capdevila, A., Teichenne, J., Domenech-Coca, C., Caimari, A., Del Bas, J. M., Escoté, X. and Crescenti, A. (2020) Effect of hesperidin on cardiovascular disease risk factors: the role of intestinal microbiota on hesperidin bioavailability. Nutrients 12: 1488.
[https://doi.org/10.3390/nu12051488]

-
Cao, Y.-J., He, X., Wang, N. and He, L.-C. (2013) Effects of imperatorin, the active component from radix angelicae (baizhi), on the blood pressure and oxidative stress in 2k, 1c hypertensive rats. Phytomedicine 20: 1048-1054.
[https://doi.org/10.1016/j.phymed.2013.04.021]

-
Liou, C.-J., Wu, S.-J., Shen, S.-C., Chen, L.-C., Chen, Y.-L. and Huang, W.-C. (2020) Phloretin ameliorates hepatic steatosis through regulation of lipogenesis and sirt1/ampk signaling in obese mice. Cell & Bioscience 10: 1-14.
[https://doi.org/10.1186/s13578-020-00477-1]

-
Jian, J., Sun, L., Cheng, X., Hu, X., Liang, J. and Chen, Y. (2015) Calycosin-7-o-β-d-glucopyranoside stimulates osteoblast differentiation through regulating the bmp/wnt signaling pathways. Acta Pharmaceutica Sinica B 5: 454-460.
[https://doi.org/10.1016/j.apsb.2015.06.005]

-
Jung, M. S., Jin, H. U., Kim, M. S. and An, C. E. (2024) Anti-melanogenic effects of umbelliferone: In vitro and clinical studies. Molecules 29: 5571.
[https://doi.org/10.3390/molecules29235571]

-
Domitrović, R., Rashed, K., Cvijanović, O., Vladimir-Knežević, S., Škoda, M. and Višnić, A. (2015) Myricitrin exhibits anti-oxidant, anti-inflammatory and antifibrotic activity in carbon tetrachloride-intoxicated mice. Chemico-Biological Interactions 230: 21-29.
[https://doi.org/10.1016/j.cbi.2015.01.030]

-
Lv, J., Sharma, A., Zhang, T., Wu, Y. and Ding, X. (2018) Pharmacological review on asiatic acid and its derivatives: a potential compound. SLAS TECHNOLOGY: Translating Life Sciences Innovation 23: 111-127.
[https://doi.org/10.1177/2472630317751840]

-
Hu, D., Wang, H.-J., Yu, L.-H., Guan, Z.-R., Jiang, Y.-P., Hu, J.-H., Yan, Y.-X., Zhou, Z.-H. and Lou, J.-S. (2024) The role of ginkgo folium on antitumor: bioactive constituents and the potential mechanism. Journal of Ethnopharmacology 321: 117202.
[https://doi.org/10.1016/j.jep.2023.117202]

-
Vincent, M. F., Marangos, P. J., Gruber, H. E. and Van Den Berghe, G. (1991) Inhibition by aica riboside of gluconeogenesis in isolated rat hepatocytes. Diabetes 40: 1259-1266.
[https://doi.org/10.2337/diab.40.10.1259]

-
Wu, Y., Liu, Y., Gulbins, E. and Grassmé, H. (2021) The anti-infectious role of sphingosine in microbial diseases. Cells 10: 1105.
[https://doi.org/10.3390/cells10051105]

-
Ju, S., Tan, Y., Wang, Q., Zhou, L., Wang, K., Wen, C. and Wang, M. (2024) Antioxidant and anti-inflammatory effects of esculin and esculetin. Experimental and Therapeutic Medicine 27: 248.
[https://doi.org/10.3892/etm.2024.12536]

-
Li, Y., Wu, Y., Yao, X., Hao, F., Yu, C., Bao, Y., Wu, Y., Song, Z., Sun, Y. and Zheng, L. (2017) Ginkgolide a ameliorates lps-induced inflammatory responses in vitro and in vivo. International Journal of Molecular Sciences 18: 794.
[https://doi.org/10.3390/ijms18040794]

-
Miyake, Y., Suzuki, E., Ohya, S., Fukumoto, S., Hiramitsu, M., Sakaida, K., Osawa, T. and Furuichi, Y. (2006) Lipid‐lowering effect of eriocitrin, the main flavonoid in lemon fruit, in rats on a high‐fat and high‐cholesterol diet. Journal of Food Science 71: S633-S637.
[https://doi.org/10.1111/j.1750-3841.2006.00192.x]

-
Zhao, L., Li, M., Zhu, Q., Yang, H. and Zhao, Y. (2025) Anti-obesity effect of isoliquiritigenin in the 3t3-l1 cell line and a high-fat diet-induced obesity mice model. Journal of Functional Foods 127: 106735.
[https://doi.org/10.1016/j.jff.2025.106735]

-
Jung, H. R., Oh, Y., Jang, D., Shin, S., Lee, S.-J., Kim, J., Lee, S. E., Oh, J., Jang, G. and Kwon, O. (2023) Gut bacteria-derived 3-phenylpropionylglycine mitigates adipocyte differentiation of 3t3-l1 cells by inhibiting adiponectin-ppar pathway. Genes & Genomics 45: 71-81.
[https://doi.org/10.1007/s13258-022-01332-y]

-
Pervin, M., Hasnat, M. A., Lim, J.-H., Lee, Y.-M., Kim, E. O., Um, B.-H. and Lim, B. O. (2016) Preventive and therapeutic effects of blueberry (Vaccinium corymbosum) extract against dss-induced ulcerative colitis by regulation of antioxidant and inflammatory mediators. The Journal of Nutritional Biochemistry 28: 103-113.
[https://doi.org/10.1016/j.jnutbio.2015.10.006]

-
Zhao, D., Islam, M. N., Ahn, B. R., Jung, H. A., Kim, B.-W. and Choi, J. S. (2012) In vitro antioxidant and anti-inflammatory activities of angelica decursiva. Archives of Pharmacal Research 35: 179-192.
[https://doi.org/10.1007/s12272-012-0120-0]

-
Hwang, Y.-J., Kim, J., Park, D.-S. and Hwang, K.-A. (2012) Study on the immunomodulation effect of Isodon japonicus extract via splenocyte function and nk anti-tumor activity. International Journal of Molecular Sciences 13: 4880-4888.
[https://doi.org/10.3390/ijms13044880]

-
Brandi, G., Schiavano, G. F., Zaffaroni, N., De Marco, C., Paiardini, M., Cervasi, B. and Magnani, M. (2005) Mechanisms of action and antiproliferative properties of Brassica oleracea juice in human breast cancer cell lines. The Journal of Nutrition 135: 1503-1509.
[https://doi.org/10.1093/jn/135.6.1503]

-
Thakur, A. K., Chatterjee, S. S. and Kumar, V. (2013) Beneficial effects of Brassica juncea on cognitive functions in rats. Pharmaceutical Biology 51: 1304-1310.
[https://doi.org/10.3109/13880209.2013.789917]

-
Yang, X., Na, C. and Wang, Y. (2023) Angelica decursiva exerts antihypertensive activity by inhibiting l-type calcium channel. Journal of Ethnopharmacology 313: 116527.
[https://doi.org/10.1016/j.jep.2023.116527]

-
Baek, H. K., Shim, H., Lim, H., Shim, M., Kim, C.-K., Park, S.-K., Lee, Y. S., Song, K.-D., Kim, S.-J. and Yi, S. S. (2015) Anti-adipogenic effect of Artemisia annua in diet-induced-obesity mice model. Journal of Veterinary Science 16: 389-396.
[https://doi.org/10.4142/jvs.2015.16.4.389]