한약(생약)제제 중 비추출물제제의 7종 지표성분 동시정량법 확립
Abstract
Assay of herbal medicinal product should be complied with the Korean Herbal Pharmacopoeia. Currently, assay test requires individual analysis of marker compound and involve complicated pretreatment steps, leading to considerable analysis time. Thus, it needs to be improved in these aspects. In this study, we aimed to develop a simultaneous quantitative method for 7 marker compounds (loganin, gentiopicroside, poncirin, saikosaponin A, decursin, decursinol angelate, and magnolol) that can be applied to 28 herbal medicinal products (pills) in the Korean Herbal Pharmacopoeia. We developed and validated the simultaneous quantitative method for these 7 marker compounds, assessing linearity, limit of detection, limit of quantitation, accuracy, and precision. The R2 values for linearity of each marker compounds were ≥ 0.999, and the accuracy ranged from 82.64~108.68%, with relative standard deviations (%RSD) for precision ranging from 0.43~3.49%, all within acceptable limits (≤ 15%). Furthermore, a comparison between the current and improved test methods confirmed the similarity of quantification. As a result, we intend to incorporate this developed analytical method into the Korean Herbal Pharmacopoeia to facilitate its utilization in the quality control of herbal medicinal products.
Keywords:
The Korean herbal pharmacopoeia, Herbal medicinal products, Pills, HPLC-DAD, Simultaneous quantitative method, Validation대한민국약전 및 대한민국약전외한약(생약)규격집에는 구성 생약을 추출 및 정제하여 만든 가미소요산엑스 과립 등 추출물 한약(생약)제제 117품목과 추출물 형태가 아닌 한약(생약) 원물에 부형제 등 첨가제를 넣어 구상의 형태로 가공한 가감팔미환 등 비추출물 한약(생약)제제 40품목이 수재되어 있다.1,2)
제제의 품질관리를 위하여 일부 정량이 가능한 생약에는 지표성분을 이용하여 정량 기준을 설정하고 있으나 현행 지표성분별 정량법을 수행해야하는 측면에서 시간적, 경제적 어려움이 상존한다.4,6) 선행연구에서 추출물 및 비추출물 제제 중 총 12종의 지표성분 동시분석법을 개발하였으나,3) 비추출물 제제에 설정된 7종 지표성분에 대한 동시분석법이 부재하므로 시험법 마련이 필요하다. 이에 본 연구에서는 HPLC/DAD법을 이용하여 비추출물제제에 해당하는 7가지 지표성분의 동시분석법을 개발하고자 하였다. 가감팔미환 등 40품목의 비추출물제제에는 당귀 등 30개의 구성 생약에 대한 함량시험법이 설정되어 있으며 그 중 용담(龍膽, Gentian Root and Rhizome), 당귀(當歸, Angelica Gigas Root), 산수유(山茱萸, Cornus Fruit), 시호(柴胡, Bupleurum Root), 지실(枳實, Poncirus Immature Fruit), 후박(厚朴, Magnolia Bark) 등 6품목은 비추출물제제에만 적용된다. 이에 따라 비추출물제제에 적용가능한 한약(생약)의 지표성분인 gentiopicroside (용담), decursin/decursinol angelate (당귀), loganin (산수유), saikosaponin A (시호), poncirin (지실), magnolol (후박)에 대한 동시분석법을 개발하고자 하였다. 확립된 동시분석법은 의약품등 시험방법 밸리데이션 가이드라인 및 AOAC 가이드라인에 따라 직선성, 특이성, 정밀성, 정확성, 검출한계, 정량한계, 시스템적합성 평가를 수행하여 시험법 타당성을 검토하였으며 확립된 동시분석법을 이용하여 시중에 유통되는 비추출물 제제의 함량을 분석하여 본 분석법의 응용가능성을 검토하였다.
재료 및 방법
시약 및 표준물질 − HPLC 분석을 위한 증류수과 아세토니트릴은 Merck사의 HPLC급 용매를 구입하였고, 인산은 Sigma aldrich사의 ACS급 시약를 구입하여 사용하였다. 지표물질인 loganin, gentiopicroside, poncirin, saikosaponin A, decursin, decursinol angelate, magnolol는 Chemfaces사에서 순도 98% 이상인 표준물질을 구입하였으며, 이들의 화학적 구조는 Fig. 1과 같다.
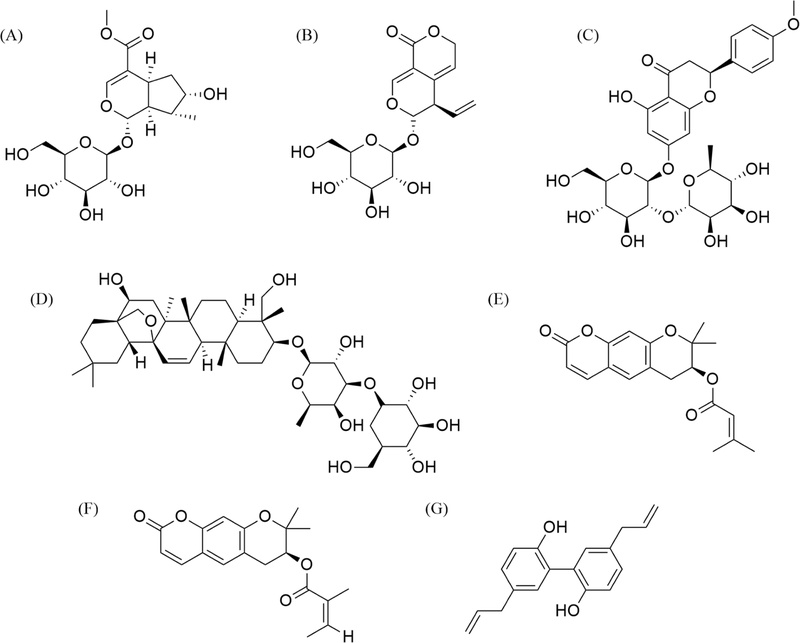
Chemical structures of (A) loganin, (B) gentiopicroside, (C) poncirin, (D) saikosaponin A, (E) decursin, (F) decursinol angelate, and (G) magnolol.
표준용액의 조제 − Loganin, gentiopicroside, poncirin, saikosaponin A, decursin, decursinol angelate, magnolol은 각각 80 mg씩 정밀히 칭량하여 methanol 20 mL로 녹여 4,000 μg/mL의 농도로 표준원액을 제조하였다. loganin, gentiopicroside, saikosaponin A 표준원액 각 4.0 mL, poncirin 표준원액 1.0 mL, decursin, decursinol angelate, magnolol 표준원액 각 0.4 mL씩 정확하게 취하여 methanol 20 mL로 맞추어 loganin, gentiopicroside, saikosaponin A는 800 μg/mL 농도로, poncirin 200 μg/mL, decursin, decursinol angelate, magnolol 80 μg/mL 농도가 되도록 혼합표준액을 조제한 다음, 단계적으로 희석하여 직선성 표준용액으로 사용하였다.
검액 제조 − 본 연구에 사용한 비추출물 한약(생약)제제는 시판되고 있는 제품을 구입하여 사용하였으며, Table I에 나타내었다. 제제의 1회량을 50 mL 코니칼튜브에 정밀히 취하여 50% methanol 40 mL을 넣고 30분간 초음파 추출한 후 여과지(Whatman, Grade 4,Φ 90 mm)를 사용하여 여과하여 다시 50% methanol을 넣고 정확하게 100 mL로 정용한 뒤 검액으로 사용하였다.
HPLC 분석조건 − HPLC는 Agilent 1260 infinity (Agilent, Santa, CA, USA)를 사용하였고 컬럼은 YMC Pack ODS-A (250×4.6 mm, 5 μm)을 사용하였다. 이동상은 0.05% 인산을 포함한 증류수(A)와 아세토니트릴(B)을 사용하여 7종 지표성분의 최적의 이동상 조건을 확립하였다(Table II). 확립된 분석에 따라 검액 10 mL를 주입하여 1.0 mL/min 유속으로 215 nm (PDA) 파장에서 분석하였다.
확립된 분석법의 검증(Validation) − 비추출물 한약(생약) 제제 7종 지표성분 동시 정량법을 검증하기 위하여 ‘의약품 등 시험방법 밸리데이션 가이드라인’을 참고하여 직선성, 특이성, 정밀성, 정확성, 검출한계, 정량한계 및 시스템적합성 을 검토하였다.
직선성 확인(Linearity) − 유의성 있는 검량선을 얻기 위해 제조한 표준원액 loganin, gentiopicroside, saikosaponin A 각 4 mL, poncirin 1 mL, decursin, decursinol angelate, magnolol 각 0.4 mL 씩 20 mL 부피 플라스크에 정확하게 취하여 넣고 methanol로 희석하여 loganin, gentiopicroside, saikosaponin A는 최종 농도 800 μg/mL, poncirin은 200 μg/mL, decursin, decursinol angelate, magnolol은 80 μg/mL로 제조하여 표준용액으로 사용하였으며, 7가지 농도에서 실험을 실시하였다. Regression equation을 y=ax+b (y와x는 각각 peak의 면적과 시료의 함량)의 형태로 식을 구하여 상관계수(R2)의 값을 통해 직선성을 판단하였으며, R2의 값이 0.99 이상인 경우 지표성분의 함량을 평가하는 검량선으로 사용하였다.
특이성 검토(Specificity) − 7가지의 지표성분을 혼합한 표준액을 제조하여 matrix와 분리되고 구별되었는지 PDA 검출기를 이용하여 스펙트럼과 분리도를 확인하였다.
검출한계(LOD) 및 정량한계(LOQ) − 검출한계 및 정량한계는 반응의 표준편차와 검량선의 기울기에 근거하는 방법으로 산출되었으며, 검량선을 3회 반복하여 얻은 기울기의 평균과(S) 표준편차(σ)를 아래의 수식을 사용해 계산하였다.
검출한계(LOD) = 3.3 × σ/S
정량한계(LOQ) = 10 × σ/S
σ : 반응의 표준편차, S: 검량선의 기울기
정밀성(Precision) 및 정확성(Accuracy) − 정확성과 정밀성 평가를 위해 사용한 검액은 동일한 방법으로 제조하여 각 지표성분의 피크면적 값을 비교하는 방법으로 측정하였다. 평가용 검액은 육미지황환을 시료로 하여 3가지 농도로 희석한 혼합표준액을 처리한 다음, 50% 메탄올에 추출해 검액으로 사용하였다.
정확성은 3가지 농도의 혼합표준액을 첨가한 검액을 3회 반복 실험하여 회수율(Recovery)과 상대표준편차(% RSD)를 측정하는 방법으로 평가하였다.
정밀성은 동일한 방법으로 조제된 검액을 intra-day test를 통해 각 농도별로 3회 반복 측정한 결과의 상대표준편차(% RSD)를 산출하고 inter-day test를 통해 3일간 반복 실험하여 측정한 검액 농도의 상대표준편차(% RSD)를 산출하여 정밀성을 확인하였다.
시스템 적합성 평가(System Suitability) − 시스템 적합성은 분석기기, 분석조작, 분석대상검체 등으로 구성된 전체 시스템이 적절하게 수행되는지 증명하기 위한 것으로 혼합된 표준액을 9회 조제하여 측정하고 각 지표성분의 피크면적에 대한 상대표준편차(% RSD)를 확인해 시스템 재현성을 증명하였다.
확립된 동시분석법을 통한 함량평가 − 확립된 동시 정량법의 적용성을 평가하기 위해 시판되어 구매가 가능한 비추출물 한약(생약)제제 12종을 확보하여 지표성분 함량을 평가하였다.
결과 및 고찰
분석조건의 확립 − 7종 지표성분 동시 정량법은 지표성분별 최대 흡수파장과 이동상 조성을 고려하여 최적의 분석 조건을 확립하였다. 이동상은 0.05% 인산 포함한 증류수와 아세토니트릴로 구성하고, 용매 조성 비율은 시간대 별로 달리하여 분리능을 높인 gradient 조건으로 확립하였다(Table II). PDA detector의 파장 조건은 각 지표성분의 최대 흡수파장을 고려하여 7종 지표성분을 모두 검출할 수 있는 215 nm로 측정파장으로 설정하였으며(Fig. 2), 지표성분의 peak는 분리도가 1.5 이상이 될 수 있도록 유지시간과 UV 스펙트럼을 비교하여 최종 확립하였다.
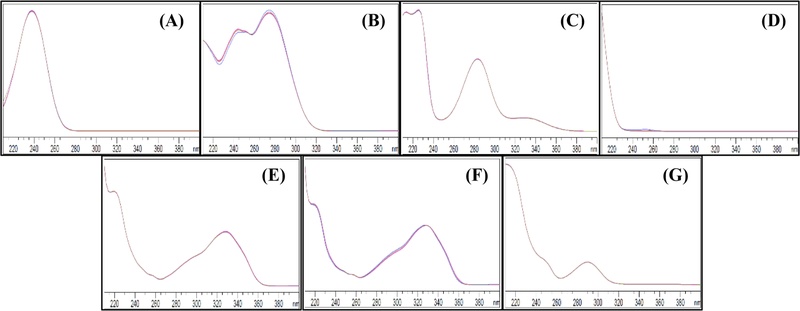
UV spectra of (A) loganin, (B) gentiopicroside, (C) poncirin, (D) saikosaponin A, (E) decursin, (F) decursinol angelate, and (G) magnolol.
동시분석법 밸리데이션 − 확립된 동시 정량법에 대하여 식품의약품안전처 ‘의약품등 시험방법의 밸리데이션 가이드라인’에 따라 직선성, 검출한계, 정량한계, 정확성, 정밀성 및 시스템적합성을 평가하였다.
직선성(Linearity), 검출한계(LOD), 정량한계(LOQ) − 7종 지표성분의 표준용액을 6가지 농도(직선성표준용액 ×1/2, ×1/4, ×1/8, ×1/16, ×1/40) 로 희석하여 HPLC 분석을 3회 반복 실시하였다. 분석 결과에 따라 y축을 피크면적, x축을 표준용액의 농도로 하여 y=ax+b 형태의 검량선을 작성하였다. 작성된 검량선을 통해 7종 지표성분의 R2 값은 모두 0.9994 이상으로 직선성이 확보되었다(Tabel III). 검량선을 분석하여 얻은 표준편차 값과 기울기를 이용해 지표성분에 대한 검출한계(LOD) 및 정량한계(LOQ)를 산출한 결과, 7종 지표성분의 LOD는 0.27~6.35μg/mL로 측정되었고, LOQ는 0.83~19.24 μg/mL로 측정되었다(Table III).
정확성(Accuracy) 정밀성(Precision) − 개발된 동시정량법의 정확성을 검토하기 위하여 검체에 3가지 농도를 시료에 첨가한 후 추출하여 회수율 및 상대표준편차(% RSD)를 확인한 결과, 회수율은 82.64~108.68%의 범위로 상대표준편차(% RSD)SMS 15% 이하로 확인되어 정확성이 확보됨을 확인하였다. 또한, 정밀성 평가를 위해 일내 및 일간 시험을 실시한 결과, 일내 시험에서는 상대표준편차(% RSD)가 0.03~0.92% 범위를 나타내었으며, 일간 시험에서는 상대표준편차(% RSD)가 0.43~3.49%로 확인되어 정밀성이 확보됨을 확인하였다. 정밀성, 정확성은 모두 식품의약품안전처 ‘의약품등 시험방법 밸리데이션 가이드라인’을 만족하였다(Tabel IV).
시스템적합성(System Suitability) − 7종 지표성분 동시정량법의 시스템 적합성을 검토하기 위하여 혼합표준액을 9회 조제하여 피크면적을 측정하였다. 측정된 각 지표성분의 피크면적에 대한 상대표준편차(% RSD)는 1.5% 이하였으며, 확립된 분석법의 시스템이 적절함을 확인하였다(Table V).
확립된 분석법을 이용한 비추출물 한약(생약)제제 함량분석 − 이와 같이 확립된 분석법을 이용하여 유통되고 있는 비추출물 한약(생약)제제를 대상으로 7가지 지표성분에 대하여 함량분석을 수행하였다. 각각의 지표성분들은 Matrix의 간섭을 받지 않았으며, 안중조기환, 태화환을 분석하였을 때 제제의 함유된 다른 성분의 피크에 영향을 받지 않고 각 지표성분의 피크가 분석 가능하였다(Fig. 3). 시판되는 비추출물 한약(생약)제제 중 구입 가능한 12품목에 대해 분석한 결과, 모든 시판제제에서 설정된 정량법 지표성분이 허가 기준 이상으로 적합하였다(Table VI).
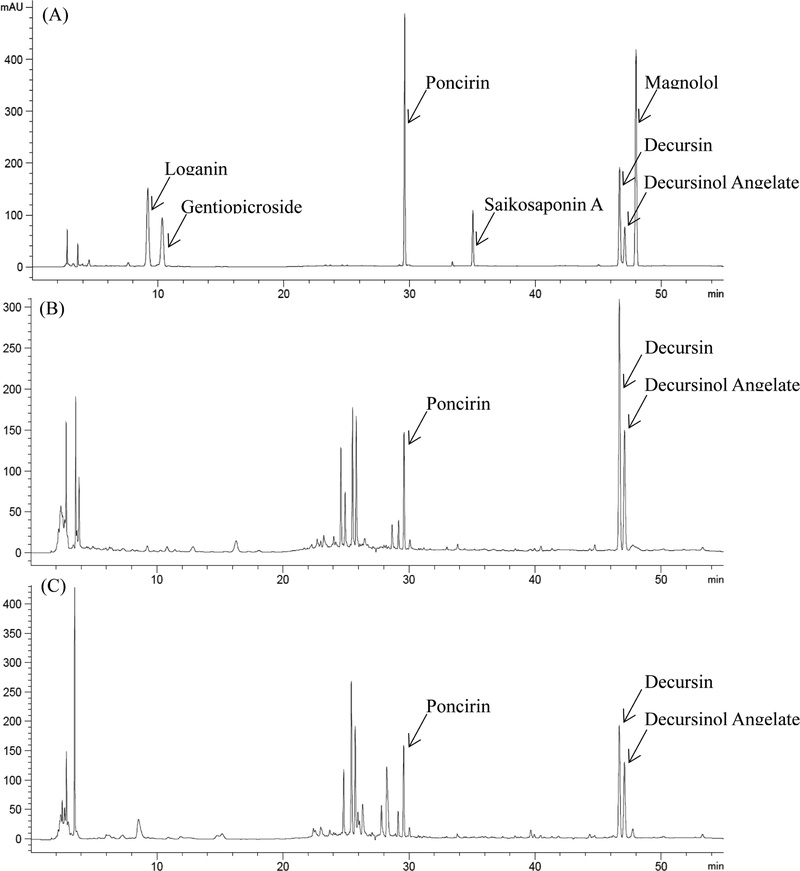
HPLC Chromatogram of (A) standard mixture, (B) taehwahwan pill sample, and (C) anjungjogihwan pill sample.
결 론
본 연구에서는 한약(생약)제제 중 비추출물제제에만 적용되는 loganin, gentiopicroside, poncirin, saikosaponin A, decursin, decursinol angelate, magnolol, 총 7가지 지표성분에 대하여 HPLC-DAD 기반 동시 정량법을 확립하고자 하였다. 이는 식품의약품안전처 ‘의약품등 시험방법 밸리데이션 가이드라인’ 및 AOAC 가이드라인에 따라 특이성, 직선성, 정밀성, 정확성 및 시스템적합성 항목으로 개발된 동시정량법의 유효성을 검증하였다. 또한, 시중에 유통되고 있는 비추출물 한약(생약)제제를 대상으로 7종 지표성분에 대해 matrix의 간섭 없이 분리 및 분석 가능함을 확인하였다. 개발된 분석법은 비추출물 한약(생약)제제를 생산하는데 있어 품질평가 시 7종 지표성분을 효율적으로 분석 가능하도록 하며, 품질 관리시 발생되는 시간적, 경제적 손실을 감소시킬 수 있을 것으로 예상된다.
Acknowledgments
본 연구는 2024년도 식품의약품안전처의 연구개발비(22201MFDS144)로 수행되었으며 이에 감사드립니다.
References
- 식품의약품안전처. (2019) 대한민국약전 제12개정.
- 식품의약품안전처. (2021) 대한민국약전외한약(생약)규격집 제6개정.
-
Ko, E. H., Jeong, J. E., Ha, J. S., Lee, S. M., Park, J. Y., Kim, K. H., Kim, J. C., Lee, S. M., Kim, J. H., Hwang, I. Y. and Hwang, J. H. (2025) Development of a HPLC-PDA method for simultaneous determination of twelve marker compounds of traditional Korean medicinal products. Kor. J. Pharmacogn. 56: 37-49.
[https://doi.org/10.22889/KJP.2025.56.1.37]

- Yang, H. J., Weon, B. J., Ma, J. Y. and Ma, C. J. (2010) Simultaneous Determination of six bioactive components in Guibi-tang by HPLC-DAD. Kor. J. Pharmacogn. 41: 313-318.
-
Lee, M. K., Park, J. H., Cho, J. H., Kim, D. H., Baek, J. H., Kim, H. J., Lee, K. Y., Kim, S. D., Kim, Y. C. and Sung, S. H. (2008) Simultaneous determination of hesperidin and glycyrrhizin in Pyungwi-san by HPLC/DAD. Kor. J. Pharmacogn. 39: 199-202.
[https://doi.org/10.4333/KPS.2009.39.1.023]

- Lee, B. H., Ma, J. Y., Weon, J. B., Yang, H. J., Yun B. R. and Ma, C. J. (2012) Simultaneous determination of three compounds in Ejung Tang by HPLC-DAD and LC-ESI-MS. Kor. J. Pharmacogn. 43: 10-15.
- Yoo, N. H., Kwon, Y. S. and Kim, M. J. (2019) Establishment of HPLC-UV analysis method validation for simultaneous analysis of standard compounds of Oplopanax elatus Nakai stem Kor. J. Pharmacogn. 50: 133-140.
- Kang, K. B., Jun, J. B., Yoo, G. J., Kwon, E. A., Yun, J. W., Kang, B. C., Kim, S. H., Sung, S. H., Jang, Y. P. and Yang, H. J. (2017) Simultaneous determination of gastrodin and gastrodigenin in Gastrodia elata by HPLC-UV. Kor. J. Pharmacogn. 48: 232-236.