덱사메타손으로 유도한 근 위축 세포 모델에서 니카라과 자생식물 100종의 근 세포 보호 활성 탐색
Abstract
Sarcopenia, characterized by age-related loss of skeletal muscle mass and strength, leads to serious health complications and increased societal costs. With its recent classification as an official disease in Korea, interest in developing therapeutic and functional food ingredients has grown. In this study, we screened 100 native Nicaraguan plant extracts to identify potential candidates for sarcopenia intervention. Using the MFDS-guided in vitro assay, mouse C2C12 myoblasts were differentiated into myotubes, pre-treated with extracts, and exposed to dexamethasone to induce muscle atrophy. Cytoprotective effects were evaluated by MTT assay. Anti-inflammatory activity was assessed by quantifying TNF-α and IL-6 secretion levels via ELISA. Several plant extracts exhibited significant protective and anti-inflammatory effects, indicating their potential as novel functional materials for muscle health. Among the 100 Nicaraguan native plant extracts evaluated, 15 extracts exhibited more than 20% cytoprotective activity against dexamethasone-induced muscle cell damage at concentrations of 100 μg/mL and 200 μg/mL. Of these, six extracts significantly reduced TNF-α and IL-6 secretion by more than 40% at 200 μg/mL. Notably, Crescentia alata Kunth (No. 36) showed superior cytoprotective and anti-inflammatory effects compared to the positive control, L-carnitine, without exhibiting cytotoxicity at the maximum concentration. To date, no scientific literature or patents have reported the muscle-protective or anti-inflammatory effects of this plant in muscle cells, suggesting its strong potential for development as a therapeutic agent or functional food for improving muscle function.
Keywords:
Muscle atrophy, Dexamethasone, C2C12 cells, Native Nicaraguan plants, Crescentia alata Kunth노화에 따른 골격근량 및 근력의 상실로 정의되는 근감소증(Sarcopenia)은 운동 능력을 저하시켜 신체 기능 저하, 낙상 위험 증가, 그리고 사망률 증가와 밀접한 연관을 지닌 질환이다.1) 근감소증은 발생 원인에 따라 일차성과 이차성으로 나눌 수 있다. 일차성 근감소증(Primary sarcopenia)은 자연 노화와 관련된 골격근 손실로 알려졌으며 대표적인 근감소증의 원인으로 설명된다. 운동량 및 단백질 섭취 감소 등 생활습관의 변화, 테스토스테론 및 성장호르몬 감소 등 내분비 이상, 그리고 염증 유발 사이토카인의 증가는 이차성 근감소증(Secondary sarcopenia)의 원인이 된다.1,2) 초고령 사회로 급속히 진입함에 따라 근감소증과 관련된 부상 및 합병증으로 막대한 사회적 비용이 발생하며 전세계적으로 근감소의 예방과 개선, 치료의 필요성이 대두되고 있다. 세계보건기구(WHO)는 2016년, 우리나라는 2021년에 제8차 한국표준질병사인 분류에 근감소증(M62.5) 진단명이 포함되었다. 이는 진단 알고리즘과 기준에 대한 국제적 합의에 따라 근감소증을 질병으로 분류한 것으로 전 세계가 근감소증 질병의 중요성과 가치에 주목함을 알 수 있다.3) 하지만 근감소에 대한 기전 연구 및 치료를 위한 약물 개발 연구는 여전히 부족한 실정이다.4)
덱사메타손(Dexamethasone)은 글루코코르티코이드(Glucocorticoid)계 화합물로, 항염제 및 항암제로 임상 환경에서 널리 사용되고 있지만 장기간 적용 시 단백질 분해 속도를 증가시키는 유비퀴틴 프로테아좀 시스템(Ubiquitin-proteasome system)을 활성화해 골격근의 단백질 합성 속도를 저해한다.5-7) 또한, 스트레스 상황(패혈증, 기아, 악액질 등)에서 방출되는 내분비 호르몬으로서 골격근 위축을 유발할 수 있다.8) 덱사메타손은 PI3K/Akt/mTOR pathway를 저해하는 역할을 하고, 이는 Downstream effectors인 4E-BP1 (Eukaryotic translation initiation factor 4E-binding protein 1)과 S6K1 (Ribosomal protein S6 kinase beta-1)등의 활성을 저해시켜 eIF4G (Eukaryotic translation initiation factor 4 G) 및 eIF4E (Eukaryotic translation initiation factor 4 E)의 작동을 막아 근섬유 위축을 야기한다.9) 따라서 덱사메타손은 근감소증에서 나타나는 제2형(Type II) 근섬유의 감소를 동반한다. 자연 노화 생쥐와 덱사메타손 유도 생쥐를 활용하여 모델 간 근육 특성의 유사점과 차이점을 조사한 결과, 두 모델 모두에서 앞다리 체지방량 감소, 근섬유 크기 축소, 악력 및 근육 수축력 저하가 유사하게 나타났고 단백질 분해 관련 유전자의 발현 증가 또한 두 모델 모두에서 관찰되었다.2) 이처럼, 덱사메타손 유도 생쥐 모델의 병태는 자연 노화로 인한 일차성 근감소증의 병태와 유사하기에 근감소증의 기전과 약물 효능평가 연구에 덱사메타손 유도 근위축 동물 모델이 널리 사용되고 있다.10,11)
본 연구는 식품의약품안전처가 발간한 ‘건강기능식품 기능성 평가 가이드(근력 및 근기능 관련)’에 따른 in vitro 약효 스크리닝을 통한 새로운 근 위축 개선 식의약소재 발굴을 위해 수행하였다.
재료 및 방법
실험재료 − 니카라과 현지에서 채집한 식물은 그늘에서 건조하여 분말화 한 후 메틸알코올 99.9% (v/v) 1 L에 첨가한 다음, 초음파 추출기(SDN-900H, SD-Ultrasonic Co. Ltd., Seoul, Republic of Korea)를 이용하여 추출하였다. 초음파 추출조건은 40 kHz, 1500 W로 하고, 한 사이클은 15분간의 초음파 처리와 120분간의 정치로 구성하여 이러한 과정을 총 30회 반복하여 추출을 진행하였다. 추출물은 여과(Qualitative Filter No. 100, Hyundai Micro Co. Ltd., Seoul, Republic of Korea)한 후 감압 건조함으로써 제작하였다. 본 연구에 사용한 니카라과 추출물 100종은 한국생명공학연구원 해외생물소재센터에서 분양 받아 사용하였으며, 각 표본은 한국생명공학연구원 식물표본관에 보관하고 있다. 니카라과 자생식물 메탄올 추출물 100종은 100 mg/mL의 농도로 DMSO에 녹여 실험에 사용하였다. 실험에 사용된 식물 시료의 목록은 Table I에 나타냈다.
C2C12 세포 배양 및 분화 유도 − 실험에 사용된 마우스 근아세포 C2C12 (Mouse myoblast cell line)는 American type culture collection (ATCC, Manassas, VA, USA)에서 구입하여 10% (v/v) fetal bovine serum (FBS, Gibco, Grand Island, NY, USA)과 1% penicillin/streptomycin (PS, Hyclone, Logan, UT, USA)이 함유된 Dulbecco’s modified eagle’s medium (DMEM, Hyclone, Logan, UT, USA) 배지를 사용하여 37℃, 5% CO2 incubator에서 2일에 한 번씩 교환하였다. 근관세포(Myotube)로의 분화 유도를 위하여 분주한 C2C12세포가 80% confluent 상태에 도달하면 2% horse serum (HS, Hyclone, Logan, UT, USA) 및 1% PS가 함유된 DMEM 배지(분화배지)를 사용하여 매 2일마다 교체하여 6일 동안 분화를 진행하였다.
Cell viability − 96 well plate에 C2C12 myoblast를 1×104 cells/well이 되도록 분주한 다음 근관세포로 분화를 유도하였다. 이후 농도별(10~200 μg/mL) 추출물 및 양성대조군 (Positive control, PC) L-carnitine (Sigma Aldrich, St. Louis, MO, USA) 200 μg/mL을 1시간 동안 처리한 후 근위축 유도용 Dexamethasone (Water soluble, Sigma Aldrich, St. Louis, MO, USA) 100 μM을 첨가하여 24시간 동안 추가 배양하였다. 그 후 3-(4,5-dimethylthiazoL-2-yl)-2,5-diphenyl tetrazolium bromide (MTT, Sigma Aldrich, St. Louis, MO, USA) 시약 (5 mg/mL)을 well 당 20 μL 첨가 후 4시간 동안 37℃, 5% CO2 조건에서 반응시켰다. 반응이 끝난 후 배지를 조심스럽게 제거하고 DMSO 100 μL를 가한 뒤 생성된 Formazan을 충분히 용해시킨 다음, Microplate reader (BioTek, Winooski, VT, USA)로 540 nm 파장에서 흡광도를 측정하여 세포생존율을 확인하였다. 근위축 유도에 적정한 덱사메타손 농도는 100 μM로 설정하였으며, 덱사메타손만 처리한 군을 음성대조군(Negative control, NC)으로, L-카르니틴(L-carnitine)을 첨가한 군을 양성대조군으로 하였다. MTT assay 결과 덱사메타손 처리군 대비 20~25%의 생존율 향상을 보인 농도 (200 μg/mL)를 L-카르니틴 처리 농도로 설정하였다.
ELISA − 덱사메타손 처리로 근세포 사멸을 유도한 모델에서 근 세포 보호 효능을 평가하기 위해 12 well plate에 C2C12 myoblast를 5 × 105 cells/well이 되도록 분주하여 24시간 배양하였다. Cell viability와 동일한 방법으로 근관세포로 분화 후 추출물 처리 1시간 뒤 덱사메타손과 L-카르니틴을 처리하여 24시간 동안 37℃, 5% CO2 조건에서 반응시켰다. 24시간 후 배양 배지를 원심분리(600×g, 5 min)하여 얻은 상층액으로 전염증성 사이토카인 TNF-α (Tumor necrosis factor-α), IL-6 (Interleukin 6)의 분비량을 측정하였다. TNF-α, IL-6는 Enzyme-linked immunosorbent assay (ELISA, BioLegend, San Diego, CA, USA) manual kit를 구입하여 사용하였으며 Microplate Reader (BioTek, Winooski, VT, USA)로 450 nm 파장에서 흡광도를 측정하였다.
통계처리 − 모든 실험은 3회 반복으로 실시하였고, 그 결과를 평균 ± 표준편차(Mean ± SD)로 표시하였다. 통계 분석은 IBM SPSS statistics 30 (SPSS Inc., Chicago, IL, USA)를 사용하여 수행하였으며 세 그룹 이상 간의 차이는 One-way analysis of variance (ANOVA)을 이용하여 분석하였으며, 실험군 들과의 유의차를 알아보기 위한 다중비교방법으로 Tukey’s multiple comparison test 검정을 실시하였다. 그룹간 통계적 유의성은 p<0.05 일 때 유의성이 있는 것으로 간주하였다.
결과 및 고찰
니카라과 자생식물 100종의 근 세포 보호 효능평가를 통한 1차 스크리닝 − 한국생명공학연구원 해외생물소재센터에서는 신약개발 및 첨단 생명공학산업에 활용하고자 해외생물소재 라이브러리를 구축하고 있으며, 2013년부터는 니카라과 국립자치대와 공동으로 니카라과의 식물자원 확보 및 활용사업을 진행하여 식물 추출물 라이브러리를 제작하였다.
골격근 내 세포생존율의 감소는 근감소증의 주요 지표이며, 덱사메타손은 세포 사멸에 관여하는 BAD (BcL-2-associated death promoter) 단백질의 활성화를 통해 세포사멸을 유도하는 것으로 보고하고 있다.12) 본 연구에서 C2C12 근관세포에 덱사메타손 100 μM로 처리한 음성대조군은 세포생존율이 정상대조군의 50~60% 정도로 유의하게 감소하였다. 한편, L-카르니틴은 산화 스트레스 억제와 단백질 합성 경로 활성화를 동시에 유도함으로써, 근육 퇴화와 기능 저하를 예방하는 이중적인 치료 효과를 지닌다고 보고되어,13) 이를 양성대조군으로 사용하였다. L-카르니틴을 200 μg/mL로 처리했을 때 음성대조군 대비 20~25% 범위로 세포생존율이 증가하였다. 평가 대상 추출물은 덱사메타손과 함께 10~200 µg/mL 농도로 처리하였고, 그 결과 니카라과 자생식물 100종 중 15종(Zuelania guidonia (Sw.) Britton & Millsp (No.28), Crescentia alata Kunth (No.36), Enterolobium cyclocarpum (Jacq.) Griseb (No.40), Guazuma ulmifolia Lam (No.46), Cnidoscolus urens (L.) Arthur (No.53), Cascabela thevetia (L.) Lippold (No.62), Spondias mombin L (No.66), Salix humboldtiana Willd (No.69), Furcraea cabuya Trel (No.71), Convolvulus nodiflorus Desr (No.72), Cassia grandis L. f (No.75), Cyperus giganteus Vahl (No.83), Capparis mollicella Standl (No.95), Pseudolmedia glabrata (Liebm.) C.C. Berg (No.98), Petiveria alliacea L (No.100))은 100 μg/mL 이상의 처리군에서 음성대조군에 비해 20% 이상 세포생존율이 증가하였다. 한편, 100 µg/mL에서 가장 높은 세포생존율을 보인 종은 4종(S. mombin (No.66), F. cabuya (No.71), C. grandis (No.75), C. mollicella (No.95))이었으나, 이들을 200 µg/mL로 처리했을 때는 오히려 세포생존율이 낮아졌다. 이는 이들 추출물 자체가 세포독성을 야기한 것이 주요 원인으로 판단된다(Fig. 1A). 1차로 선발된 15종의 추출물 중 200 µg/mL로 처리했을 때 세포독성이 없으면서 L-carnitine에 비해 유의하게(p<0.05) 강한 세포보호 활성을 가지는 소재는 Z. guidonia (No.28)와 C. alata (No.36)이었다(Fig. 1B).
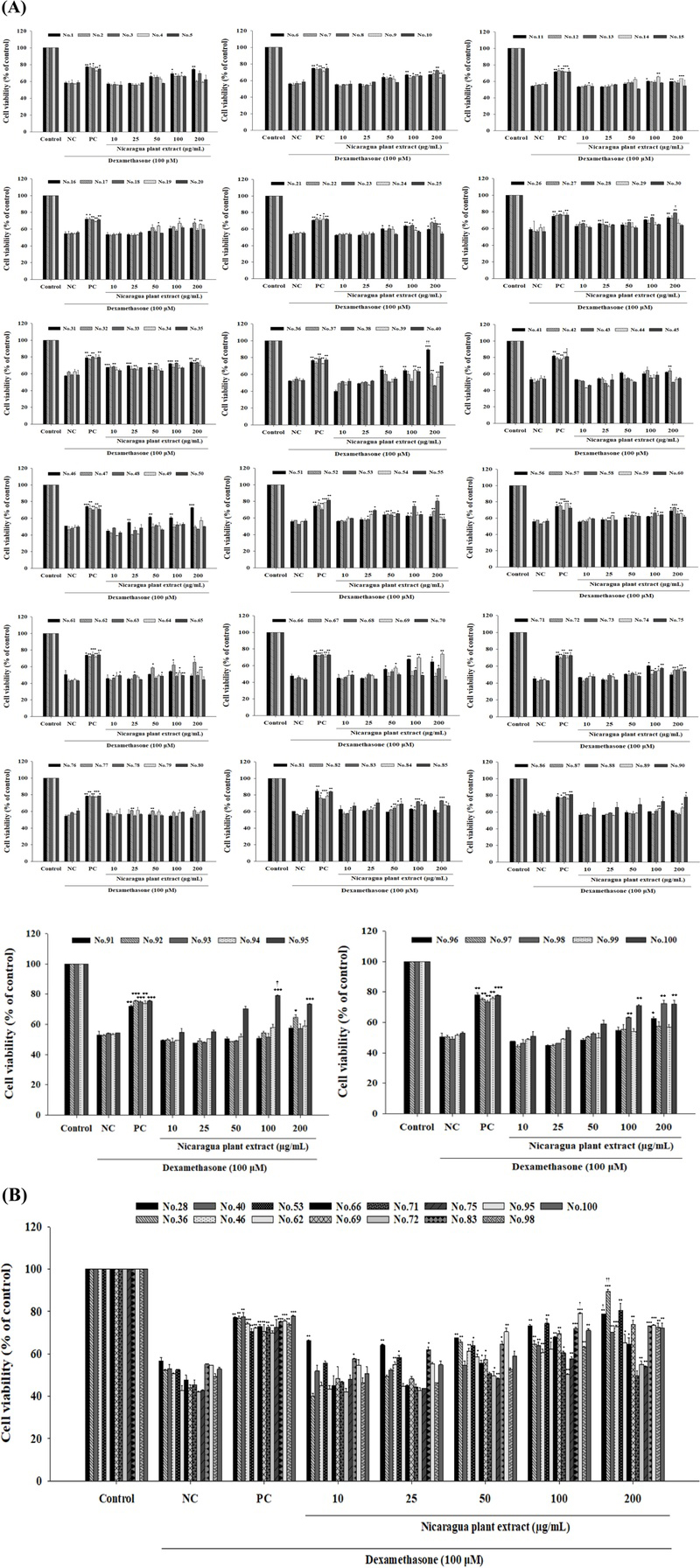
Cytoprotective effects of 100 Nicaraguan native plant extracts based on cell viability assay. (A) About C2C12 (1×104 cells/well) were seeded in 96-well microplates and maintained to sub-confluence in DMEM containing 10% FBS. To induce myoblast differentiation, the growth medium was replaced with DMEM supplemented with 2% horse serum (HS) and maintained for 6 days until myotube formation. Subsequently, the medium was replaced with 2% HS-DMEM containing 100 Nicaraguan native plant extracts (10~200 μg/mL) and L-carnitine (200 μg/mL). After a 1hour pre-treatment, dexamethasone (100 μM) was added and incubated for 24 hours. Cell viability was assessed using the MTT assay. (B) Comparative cytoprotective effects of 15 selected Nicaraguan plant extracts and L-carnitine in dexamethasone-treated C2C12 cells. These results are presented as mean ± SD of three independent experiments. ***p<0.001, **p<0.01, *p<0.05 vs. NC, ††p<0.01, †p<0.05 vs. PC.
니카라과 자생식물의 항염증 효능평가를 통한 2차 스크리닝 − MTT assay 결과로 근 세포 보호 활성을 확인한 후 2차적으로 항염증 활성 평가를 통해 근원 섬유단백질 분해 억제 가능성이 있는 소재를 탐색하였다. 1차 스크리닝에서 음성대조군보다 20% 이상 근 세포 보호 효과를 가졌던 니카라과 자생식물 15종을 대상으로 덱사메타손으로 근위축을 유도한 C2C12 근관세포에서 TNF-α 및 IL-6 분비량을 측정하였다. 측정 결과, 최대 처리 농도인 200 μg/mL에서 덱사메타손 대비 TNF-α, IL-6 분비량을 감소시킨 소재는 6종(C. alata (No.36), C. urens (No.53), C. thevetia (No.62), S. humboldtiana (No.69), C. mollicella (No.95), P. glabrata (No.98))이었다. TNF-α는 각각 55.5%, 50.9%, 40.8%, 44.9%, 49.3%, 52.7%를, IL-6의 경우 각각 56.5%, 45.3%, 54.6%, 40.6%, 64.5%, 47.6% 감소시켰다. 이 중, 세포독성이 없으면서 양성대조군에 비해 TNF-α와 IL-6 분비량 모두 유의하게(p<0.001) 감소시킨 소재는 C. alata (No.36)로 각각 33.4%, 37.8% 감소시켰다(Fig. 2). 1, 2차 스크리닝 결과를 종합해 볼 때, 동일 처리농도(200 μg/mL)에서 L-카르니틴보다 근 세포 보호 및 항염증 활성이 우수한 소재는 C. alata (No.36)가 유일했다.
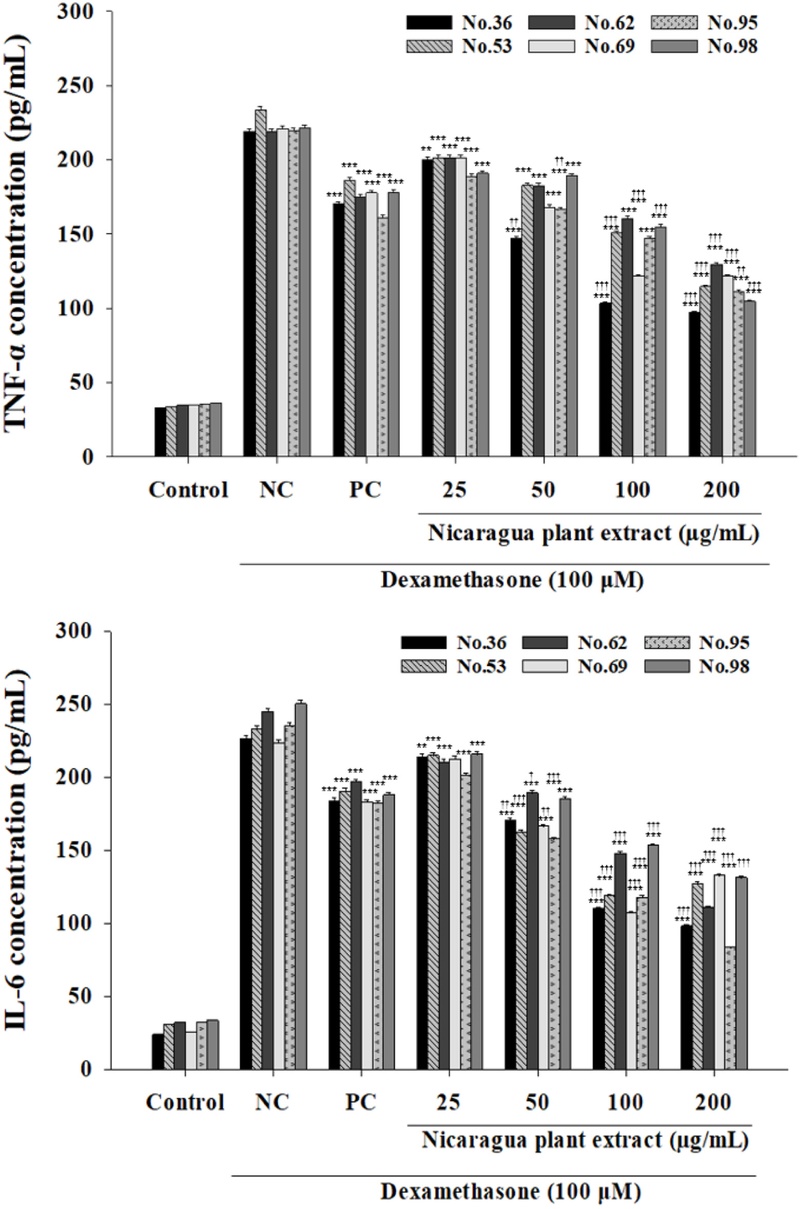
Anti-inflammatory activity of Nicaraguan native plants based on cytokine release. Inhibitory effects of 6 selected Nicaraguan native plant extracts on pro-inflammatory cytokine secretion of TNF-α, IL-6 in dexamethasone-induced C2C12 cells. These results are presented as mean ± SD of three independent experiments. ***p<0.001, **p<0.01, *p<0.05 vs. NC, †††p<0.001, ††p<0.01, †p<0.05 vs. PC.
Crescentia alata Kunth (Bignoniaceae)는 니카라과 식물로, 멕시코와 같은 중남미에 주로 분포하며 열매는 식용하고, 전통적으로 기침, 감기 등 호흡기 질환 치료에 사용되는 것으로 알려져 있다.14) C. alata는 한국의 능소화과 식물들인 능소화(Campsis grandiflora) 및 개오동(Catalpa ovata)과 비교하였을 때, 모두 통꽃 구조와 곤충·조류 매개 수분 등 능소화과 식물의 공통 형질을 공유하나, 생활형과 열매 형태에서는 뚜렷한 차이를 보인다. C. alata는 열대 기원의 교목으로서 목질의 구형 열매를 형성하는 반면, 한국의 능소화과 식물들은 주로 덩굴성 또는 낙엽성 교목으로서 삭과를 형성하는 것이 특징적이다. 2021년 Abinaya 등은 C. alata 잎 80% 메탄올 추출물, 용매분획 및 분리한 Stigmasterol에 대한 항균활성과 HeLa cell에 대한 세포독성을,14) 2001년 Autore 등은 C. alata 잎 메탄올 추출물의 항염증 활성과 Kaempferol, Kaempferol-3-O-rutinoside, rutin과 같은 플라보노이드 성분을 분리하여 보고15)한 바 있으나, 그 밖에 C. alata 잎을 소재로 한 연구는 발견할 수 없었으며, C. alata 잎의 근세포 보호 활성은 본 연구를 통해 처음으로 보고하는 바이다.
결론
한국생명공학연구원 해외생물소재센터에서 분양 받은 니카라과 자생식물 메탄올 추출물 총 100종에 대하여 덱사메타손 유도 근위축 세포모델을 이용하여 근 위축 감소 활성을 탐색한 결과, 음성대조군 대비 20% 이상 근세포 보호 활성을 가지는 15종의 소재 중 L-카르니틴 보다 우수한 활성을 보인 소재는 2종(Z. guidonia (No.28)과 C. alata (No.36))이었다. 상기 1차 선발된 15종의 소재를 대상으로 염증성 사이토카인(TNF-α와 IL-6) 분비 억제능을 평가한 결과, L-카르니틴에 비해 유의하게(p<0.05) 강한 항염증 활성을 가지는 소재는 C. alata (No.36)이었고, 최대 처리 농도인 200 μg/mL 에서 세포독성이 관찰되지 않으면서 근세포 보호활성 및 항염증 활성이 L-카르니틴 보다 우수한 소재는 C. alata (No.36)로 확인되었다. 추후 해당 소재의 유효성분, in vivo 효능평가 및 작용기전 규명 등 상용화를 위한 추가 연구가 필요할 것으로 사료된다.
References
-
Hong, S. M. and Choi, W. H. (2012) Clinical and physiopathological mechanism of sarcopenia. Korean J. Med. 83: 444-454.
[https://doi.org/10.3904/kjm.2012.83.4.444]

-
Wang, B. Y. H. and Hsiao, A. W. T. (2023) Is dexamethasone-induced muscle atrophy an alternative model for naturally aged sarcopenia model? J. Orthop. Translat. 39: 12-20.
[https://doi.org/10.1016/j.jot.2022.11.005]

- Lim, J. Y. (2020) Consensus update on definition and diagnosis for sarcopenia. Journal of KAGRM 10: 39-45.
-
Seo, D. Y., Bae, J. H., Bang, H. S. and Kwak, Y. S. (2020) Role of exercise in skeletal muscle atrophy: A mechanistic investigation. Exercise Sci. 29: 202-207.
[https://doi.org/10.15857/ksep.2020.29.3.202]

-
Chen, C., Yang, J. S. and Lu, C. C. (2020) Effect of quercetin on dexamethasone-induced C2C12 skeletal muscle cell injury. Molecules 25: 32-67.
[https://doi.org/10.3390/molecules25143267]

-
Massaccesi, L., Goi, G. and Tringali, C. (2016) Dexamethasone-induced skeletal muscle atrophy increases O-GlcNAcylation in C2C12 cells. J. Cell Biochem. 117: 1833-1842.
[https://doi.org/10.1002/jcb.25483]

-
Menconi, M., Gonnella, P. and Petkova, V. (2018) Dexamethasone and corticosterone induce similar, but not identical, muscle wasting responses in cultured L6 and C2C12 myotubes. J. Cell Biochem. 105: 353-364.
[https://doi.org/10.1002/jcb.21833]

-
Schakman, O., Gilson, H., Kalista, S. and Thissen, J. P. (2009) Mechanisms of muscle atrophy induced by glucocorticoids. Horm. Res. Paediat. 72: 36-41.
[https://doi.org/10.1159/000229762]

-
Schakman, O., Kalista, S., Barbé, C., Loumaye, A. and Thissen, J. P. (2013) Glucocorticoid-induced skeletal muscle atrophy. Int. J. Biochem. Cell Biol. 45: 2163–2172.
[https://doi.org/10.1016/j.biocel.2013.05.036]

-
Mallidis, Ma. K., Bhasin, C., Mahabadi, S., Artaza, V. and Gonzalez-Cadavid, N. (2003) Glucocorticoid-induced skeletal muscle atrophy is associated with upregulation of myostatin gene expression. Am. J. Physiol. Endocrinol. Metabol. 285: 363–371.
[https://doi.org/10.1152/ajpendo.00487.2002]

-
Seto, J. T., Roeszler, K. N., Meehan, L. R., Wood, H. D., Tiong, C. and Bek, L. (2021) ACTN3 genotype influences skeletal muscle mass regulation and response to dexamethasone. Sci. Adv. 7: eabg0088.
[https://doi.org/10.1126/sciadv.abg0088]

-
Bonnefoy Berard, N., Aouacheria, A. and Verschelde, C. (2004) Control of proliferation by Bcl-2 family members. Biochim. Biophys. Acta Mol. Cell Res. 1644: 159-168.
[https://doi.org/10.1016/j.bbamcr.2003.10.014]

-
Montesano A., Senesi, P., Luzi, L., Benedini, S. and Terruzzi, I. (2015) Potential therapeutic role of L-carnitine in skeletal muscle oxidative stress and atrophy conditions. Oxid. Med. Cell Longev. 13: 646171.
[https://doi.org/10.1155/2015/646171]

-
Abinaya, R. (2021) Isolation, characterization and biological activities of stigmasterol from leaf part of Crescentia alata Kunth (Bignoniaceae). Eur. J. Med. Plant. 32: 9-21.
[https://doi.org/10.9734/ejmp/2021/v32i330377]

-
Autore G, Rastrelli. R., Lauro, M. R., Marzocco, S., Sorrentino, R., Sorrentino, U., Pinto, A. and Aqu, A. (2001) Inhibition of nitric oxide synthase expression by a methanolic extract of Crescentia alata and its derived flavonols. Life Sci. 70: 523-534.
[https://doi.org/10.1016/S0024-3205(01)01425-4]