
해마에서 칼슘 투과성 AMPA 수용체를 통한 genkwanin의 장기강화 촉진 효과
Abstract
Mild cognitive impairment (MCI) is regarded as a prodromal stage of Alzheimer’s disease (AD), and enhancing cognitive function during this period is a crucial strategy to delay progression to dementia. This study investigated the effects of genkwanin on hippocampal synaptic plasticity, particularly long-term potentiation (LTP), a cellular mechanism underlying learning and memory. Genkwanin significantly enhanced LTP in acute hippocampal slices, suggesting its potential role in improving memory function. Moreover, genkwanin increased phosphorylation of the GluA1 subunit of AMPA receptors, indicating a mechanism contributing to synaptic strengthening. Notably, the LTP-enhancing effect of genkwanin was abolished by IEM-1460, a selective antagonist of calcium-permeable AMPA receptors (CP-AMPARs). These results suggest that genkwanin facilitates hippocampal synaptic plasticity via the GluA1–CP-AMPAR pathway, providing a potential mechanism for cognitive improvement in early neurodegenerative conditions.
Keywords:
Genkwanin, Calcium-permeable AMPA receptor (CP-AMPAR), GluA1 phosphorylation, Long-term potentiation (LTP), Mild cognitive impairment (MCI)경도인지장애(Mild Cognitive Impairment, MCI)는 일상생활능력은 보존되어 있지만 기억력, 주의력, 실행 기능 등 인지기능이 나이 및 교육 수준을 기준으로 예상되는 것보다 뚜렷한 저하가 나타나는 상태를 의미한다.1) 정상 노인에서 연간 1-2%가 치매로 이환되는, 경도인지 장애 환자를 추적 관찰 시 연간 10-15%, 6년 이내 약 80%가 치매로 이환 되는 것으로 알려졌다. 이는 경도인지장애가 신경퇴행성 변화와 연관되어 치매로 진행될 위험이 높으며, 경도인지장애 환자가 치매로 이환되기 이전에 적극적 관리가 필요하다는 점을 시사한다.2)
인지 기능 개선 약물은 주로 신경전달물질 조절 또는 병리단백질 억제에 기반한다. Donepezil 등의 아세틸콜린에스테레이스 억제제는 아세틸콜린 분해를 억제하여 콜린성 신호를 강화한다.1) Memantine 등의 N-Methyl-D-aspartate (NMDA) 수용체 길항제는 과도한 글루탐산성 자극을 줄여 흥분독성을 완화한다. Lecanemab 등의 항아밀로이드 항체 치료제들은 아밀로이드 베타에 결합해, 뇌에 축적된 아밀로이드 플라크를 제거한다.3,4)
이러한 접근은 주로 증상 완화나 진행 지연에 초점을 두고 있어 학습과 기억의 분자적 기반인 시냅스 가소성(long-term potentiation, LTP)을 직접적으로 강화하는 효과는 제한적이다.5,6) 이러한 한계를 보완할 수 있는 새로운 접근으로 칼슘 투과성 AMPA 수용체(calcium-permeable AMPA receptor, CP-AMPAR)가 대두되고 있다. CP-AMPAR은 GluA2 서브유닛이 결여된 형태로 칼슘 투과성을 지니며, 해마에서 LTP가 유도될 때 PKA 의존적 GluA1 인산화에 의해 시냅스에 일시적으로 삽입된다. 이 과정에서 CP-AMPAR을 통한 Ca2+ 유입이 발생하고, 이 신호가 CaMKII와 CREB 등 하위 경로를 활성화하여 LTP 형성의 핵심 분자적 기전으로 작용한다.7,8)
기초 연구에서도 이러한 메커니즘이 확인되었다. 해마 절편에서 LTP 유도시 CP-AMPAR의삽입과함께강한 Ca2+ 유입이 관찰되며, 선택적 차단제(IEM-1460, NASPM) 처리 시 Ca2+ 신호가 차단되고 LTP가 억제된다.9) 또한 GluA1 결손 마우스는 공간기억과 작업기억 과제 수행에 결함을 보이지만, GluA1 신호가 정상적으로 작동할 경우 LTP와 학습 기능이 회복된다.10) 최근 천연물 연구에서도 3,4,5-trimethoxycinnamic acid methyl ester (TMCA)가 해마 절편에서 PKA–GluA1–CP-AMPAR 경로를 통한 Ca2+ 유입과 LTP 촉진을 유발하며, 이 효과는 CP-AMPAR 차단제 처리 시 소실되는 것으로 보고되었다.11) 이러한 결과들은 CP-AMPAR이 기존 약물 기전과 차별화되며, Ca2+ 유입을 매개로 학습과 기억 형성을 직접 조절하는 중요한 표적임을 보여준다.
Genkwanin은 플라보노이드 계열 화합물로, 미세아교세포 억제, 항염증, 항산화 기능을 통해 신경보호에 기여할 수 있음이 보고되었다.5,12,13) 그러나 이러한 신경보호 효과에도 불구하고, 시냅스 가소성의 핵심 요소인 CP-AMPAR를 매개로 한 기전 연구는 아직 부족하다. 따라서 본 연구는 genkwanin이 PKA 의존적 GluA1 인산화를 유도하고, 이를 통해 CP-AMPAR의 시냅스 삽입과 Ca2+ 유입을 촉진하여 장기강화(long-term potentiation, LTP)를 증진시킬 수 있다는 가설을 세워 증명하고자 한다. 이를 통해 genkwanin이 PKA 의존적 GluA1 인산화를 매개로 CP-AMPAR의 시냅스 삽입과 Ca2+ 유입을 촉진하고, 이에 따른 시냅스 강화에 기여할 수 있음을 제시하고자 한다. 본 연구는 genkwanin의 시냅스 수준 기전을 규명함으로써, 향후 경도인지장애 및 치매와 같은 인지기능 장애의 치료 전략 탐색에 기초 자료를 제공할 수 있을 것이다.
재료 및 방법
재료 − Genkwanin (≥98% purity, Sigma-Aldrich, St. Louis, MO, USA)은 dimethyl sulfoxide (DMSO)에용해하여 10 mM stock solution으로 제조하였으며, 사용 직전에 인공뇌척수액(aCSF)으로 희석하여 최종 농도 10, 30 및 100 μM로 처리하였다. CP-AMPAR 선택적 차단제 IEM-1460 (Tocris Bioscience, Bristol, UK)은 100 μM 농도로 사용하였다. PKA 저해제 H89 (10 μM, Tocris Bioscience)는대조실험에서사용하였다. 모든 시약은 실험 직전에 준비하여 사용하였다.
실험동물 − 실험에는 6주령의 수컷 ICR 마우스(26–28 g, OrientBio, Seongnam, Korea)를 사용하였다. 동물은 22 ± 2°C, 상대습도 55 ± 5%, 12시간 명암주기(07:00–19:00)의 일정한 환경에서 사육하였으며, 물과 사료는 자유 급여하였다. 모든 동물실험은 건국대학교의 동물실험윤리위원회(Institutional Animal Care and Use Committee, IACUC)의 승인(KU25009)을 받아 수행되었다.
해마 절편 준비 − 실험동물은 isoflurane으로 마취한 후 신속히 희생시켜 뇌를 적출하였다. 적출한 뇌는 얼음에 차갑게 냉각된 산소포화 인공뇌척수액(aCSF; 124 mM NaCl, 3 mM KCl, 1.25 mM NaH2PO4, 26 mM NaHCO3, 10 mM glucose, 2 mM CaCl2, 1 mM MgCl2) 내에서보관하였다. Leica VT1200S vibratome (Leica Microsystems, Germany)을 사용하여 400 μm 두께의 해마 절편을 제작하였으며, 95% O2와 5% CO2로 포화된 aCSF에서 30°C로 유지하며 1시간 동안 회복시킨 후 전기생리학적 실험에 사용하였다.
전기생리학적 기록 − Field excitatory postsynaptic potentials (fEPSPs)는해마 CA1 영역의 stratum radiatum에서 extracellular recording 방식으로 측정하였다. 자극 전극은 Schaffer collateral에, 기록전극은 CA1 영역에각각배치하였다. Baseline 반응은 0.05 Hz로 20 분간 안정적으로 기록하였으며, 장기강화(long-term potentiation, LTP)는 100 Hz의 고주파 자극(high-frequency stimulation, HFS)을 1 초 동안 3회, 20 초 간격으로 가하여 유도하였다. 기록된 fEPSP 기울기(slope)는 baseline 평균값 대비 백분율로 정규화(normalized)하여 분석하였다. 해마 절편을 genkwanin (10, 30 or 100 μM)을 포함한 aCSF에 2시간 동안 배양시켰고, IEM-1460 (100 μM)은 genkwanin 처리 30분전부터전처리하였다. 이후해마절편을 recording chamber에 놓고 측정을 시작하였다. 데이터 수집은 Axoclamp 700B amplifier와 pClamp 10.0 software (Molecular Devices, CA, USA)를 이용하였다.
Western blot − 해마절편은 genkwanin (10, 30 or 100 μM)을 2시간 동안 처리한 후 ice-cold PBS로 세척하고, RIPA buffer (1% NP-40, 0.5% sodium deoxycholate, 0.1% SDS)를 이용하여 단백질을 추출하였다. 단백질 농도는 BCA protein assay kit (Thermo Fisher Scientific, USA)로 정량하였다. 50 μg의 단백질을 10% SDS-PAGE로 분리한 후 PVDF membrane (Millipore, USA)으로 전이하였다. 1차 항체는 anti-pGluA1 (Ser845, 1:1000, Cell Signaling Technology, USA), anti-GluA1 (1:1000, Millipore), anti-β-actin (1:5000, Sigma-Aldrich)을 사용하였다. 2차항체는 HRP-conjugated goat anti-rabbit 또는 anti-mouse IgG (1:5000, Jackson ImmunoResearch, USA)를 적용하였다. 밴드는 ECL detection reagent (GE Healthcare, USA)로 검출하였으며, band intensity는 ImageJ software (NIH, USA)를 이용해 정량하였다.
통계 분석 − 모든데이터는 mean ± SEM으로표시하였다. 통계 분석은 GraphPad Prism 10.0 (GraphPad Software, USA)을 이용하였으며, 두 집단 간 비교는 Student’s t-test, 세 집단 이상 비교는 one-way ANOVA 후 Tukey’s post hoc test를 실시하였다. p < 0.05를 통계적으로 유의한 차이로 간주하였다.
결과 및 고찰
해마 시냅스 장기강화에 미치는 genkwanin의 영향 − Genkwanin이 시냅스 가소성에 미치는 영향을 확인하기 위해, 해마 절편의 Schaffer collateral–CA1 시냅스에서 field excitatory postsynaptic potential (fEPSP)을 기록하여 장기강화(long-term potentiation, LTP)를 분석하였다. 대조군에서는 고빈도자극(high-frequency stimulation, HFS) 처리시에도 normalized fEPSP slope은 소폭 증가 후 일정하게 유지되었다(Fig. 1A and 1D). 이는 대조군에서 LTP가 유도되었음을 의미한다. 반면, genkwanin (10, 30, 100 μM) 전처리군에서는 고빈도자극을 처리하였을 때, 농도 의존적으로 normalized fEPSP slope이 증가하는 것을 관찰할 수 있었다(Fig. 1B–1D). 고빈도자극 후 60분 후 fEPSP slope 평균값을 LTP 비율로 정량화(LTP ratio)한 결과, 100 μM genkwanin 처리군에서 대조군보다 뚜렷한 LTP 증가가 나타났으며, 이는 통계적으로 유의하였다(Fig. 1D, **p < 0.01). 이러한 결과는 genkwanin이 해마 시냅스에서 LTP를 증가시킴을 나타낸다.
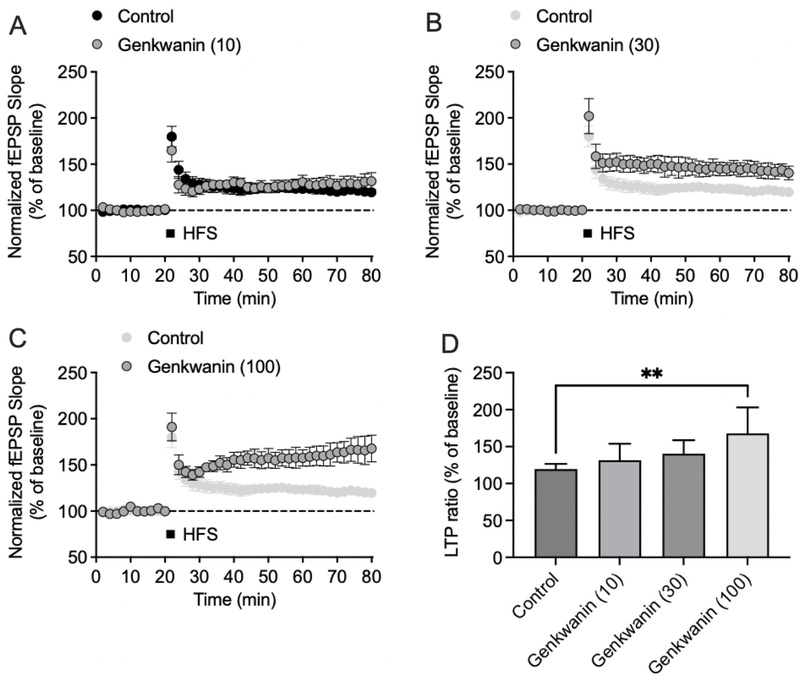
Effect of genkwanin on LTP in acute hippocampal slices. Representative field excitatory postsynaptic potential (fEPSP) traces recorded from Schaffer collateral–CA1 synapses are shown. (A–C) Time course of normalized fEPSP slope (% baseline) following high-frequency stimulation (HFS; 100 Hz, 1 s × 3 trains) in control and genkwanin-treated slices (10, 30, 100 μM). Genkwanin treatment markedly enhanced both the initial potentiation and the sustained increase in fEPSP slope for over 60 min, indicating a facilitation of long-term potentiation (LTP) induction. (D) Summary bar graph showing the mean LTP magnitude (normalized fEPSP slope, % baseline) measured 60 min after HFS. Genkwanin at 30 μM and 100 μM significantly increased LTP compared with the control in a concentration-dependent manner. Data are presented as mean ± SEM. Statistical significance was analyzed by one-way ANOVA followed by Tukey’s post hoc test (n = 6–8, **p < 0.01).
해마 GluA1의 인산화에 미치는 genkwanin의 영향 − Genkwanin이 AMPA 수용체의 기능에 미치는 영향을 평가하기 위하여, 다양한 농도의 genkwanin (0, 10, 30, 100 µM)을 처리한 후 GluA1의 Ser845 위치에서의 인산화 수준(pGluA1-S845)을 Western blot을 통해 분석하였다. Genkwanin은 pGluA1-S845의 발현을 농도 의존적으로 증가시켰다(Fig. 2A and 2B). 반면, 총 GluA1 단백질 및 loading control로 사용된 actin의 발현 수준은 모든 조건에서 일정하게 유지되었다. pGluA1-S845의 발현을 총 GluA1에 대해 정량화한 결과, 100 µM genkwanin 처리군에서 대조군(0 µM)에 비해 유의하게 증가된 인산화 수준을 나타내었으며(*p < 0.05) (Fig. 2A and 2B), 이는 genkwanin이 GluA1으로 구성된 calcium-permeable AMPA 수용체의 시냅스 발현을 증가시킬 가능성이 있음을 의미한다.
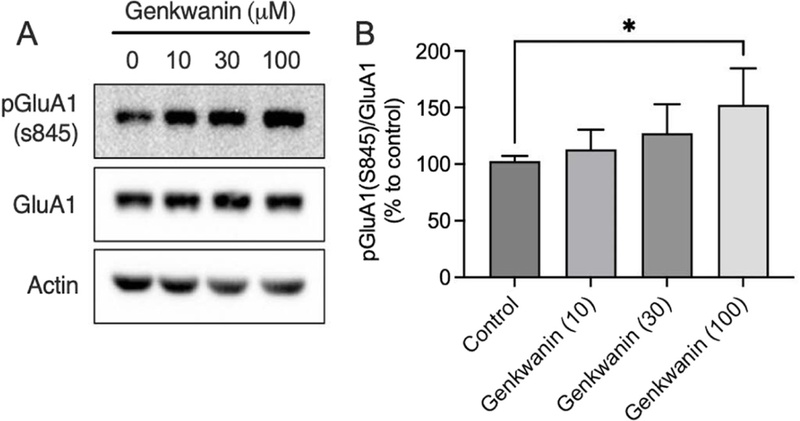
Effect of genkwanin on GluA1 phosphorylation. Western blot analysis of phosphorylated GluA1 at Ser845 (pGluA1) after genkwanin (10, 30 and 100 uM). Genkwanin significantly increased the pGluA1/GluA1 ratio, suggesting an enhancement of PKA-dependent GluA1 phosphorylation. β-actin was used as a loading control. Data are expressed as mean ± SEM, and statistical comparisons were made using one-way ANOVA followed by Tukey’s post hoc test (n = 3, *p < 0.05).
Genkwanin의 효과에 대한 칼슘 투과성 AMPA 수용체의 역할 − Genkwanin의 LTP 증가 효과가 GluA1으로 구성된 칼슘 투과성 AMPA 수용체의 영향을 받는지 확인하기 위해 CP-AMPAR의 선택적 길항제인 IEM-1460의 genkwanin의 효과에 대한 영향을 분석하였다. Genkwanin 단독 처리군에서는 대조군에 비해 유의적으로 높은 LTP가 나타났다(Fig. 3A and 3D). IEM-1460 단독 처리군에서 측정한 normalized fEPSP slope는 처리하지 않은 대조군과 비교하여 유의한 차이가 없었다(Fig. 3B and 3D). 반면, genkwanin이 촉진한 LTP가 IEM-1460과 병용 처리 시 억제되어, 대조군과 유사한 수준의 LTP가 관찰되었다(Fig. 3C and 3D). 이는 genkwanin이 CP-AMPAR 활성에 의존적으로 LTP를 촉진함을 시사한다.
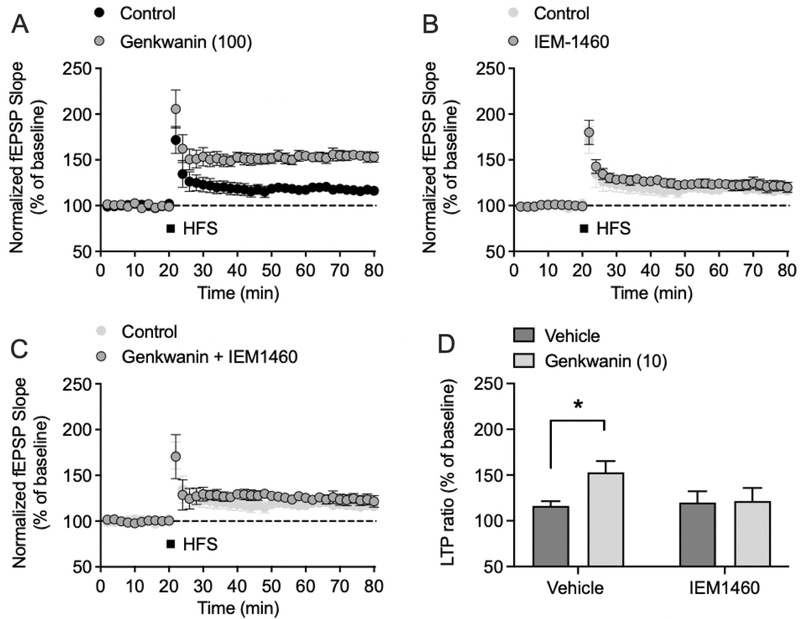
Correlation between genkwanin and CP-AMPAR. (A) Representative fEPSP traces recorded from Schaffer collateral–CA1 synapses are shown. (B–C) Pretreatment with the CP-AMPAR-selective antagonist IEM-1460 (50 μM) suppressed the genkwanin (10 μM)-induced increase in fEPSP slope. Although a transient potentiation was observed immediately after HFS, LTP decayed rapidly during the maintenance phase in the IEM-1460-treated group. (D) Bar graph summarizing the mean LTP magnitude measured 60 min after HFS. Co-application of IEM-1460 significantly attenuated Genkwanin-induced LTP enhancement compared with Genkwanin alone, indicating that the synaptic potentiation by Genkwanin is dependent on Ca2+ influx through CP-AMPARs. Data are presented as mean ± SEM. Statistical significance was analyzed by one-way ANOVA followed by Tukey’s post hoc test (n = 6–8, *p < 0.05).
경도인지장애(Mild Cognitive Impairment, MCI)는 정상 노화와 알츠하이머병(Alzheimer’s disease, AD) 사이의 중간 단계로, 치매로의 전환 위험이 높은 것으로 알려져 있다.14,15) 선행연구에 따르면 MCI 환자의약 50–60%가 수년내 AD로 진행하며, 정상 노인에 비해 30배 이상 높은 발병 위험을 보인다.16) 이러한 점에서 MCI는치매예방및조기치료전략의 핵심 단계로 간주된다.2)
그러나 현재까지의 치료 접근은 주로 신경전달물질 조절(예: 아세틸콜린에스터레이스 억제제, NMDA 수용체 길항제) 또는 병리 단백질(Aβ, tau) 축적 억제에 집중되어 있으며, 시냅스 수준에서의 기능 회복을 직접적으로 유도하는 기전 연구는 제한적이다.17,18)
시냅스 가소성(synaptic plasticity)은 학습과 기억의 분자적 기반으로, 그 손상은 MCI 및 AD의 초기 병태생리와 밀접하게 연관되어 있다.19,20) 특히 해마에서의 장기강화(long-term potentiation, LTP)는 인지기능 유지에 필수적인 과정으로, AMPA 수용체의 활성 및 조절이 그 핵심에 위치한다. AMPA 수용체의 GluA1 서브유닛 인산화는 CP-AMPAR의 시냅스 삽입을 유도하여 Ca2+ 유입을 매개하고, 이는 시냅스 강화 및 기억 형성에 중요한 역할을 한다.21-23) 이러한 기전은 시냅스 수준의 조절을 통해 신경가소성을 회복시키는 물질의 탐색이 MCI의 조기 치료 전략에 있어 새로운 접근이 될 수 있음을 시사한다.24-26)
최근 천연물 연구에서도 AMPA 수용체 조절을 통한 시냅스 가소성 증진 기전이 주목받고 있다. 예컨대, 3,4,5-trimethoxycinnamic acid methyl ester (TMCA)는 해마 절편에서 PKA–GluA1 인산화를 유도하여 CP-AMPAR 삽입과 LTP를 촉진하였으며, 선택적 CP-AMPAR 차단제(IEM-1460, NASPM) 처리 시 이러한 효과가 소실되는 것으로 보고되었다.11) 더불어 플라보노이드 계열 화합물들도 PKA–CREB 경로를 활성화하여 시냅스 강화와 기억 향상을 유도한 바 있다.27,28)
본 연구에서는 genkwanin이 해마 절편에서 LTP 유도를 유의하게 향상시킴을 확인하였다. HFS(High-frequency stimulation)에 의해 유도된 fEPSP 기울기는 대조군에 비해 genkwanin 처리군에서 현저히 증가하였으며, 이는 장기강화의 유도 및 유지가 촉진되었음을 의미한다. Western blot 분석 결과, genkwanin은 GluA1의 Ser845 인산화를 유의하게 증가시켰다. 더불어 CP-AMPAR 선택적 차단제 IEM-1460 전처리 시 LTP 촉진 효과가 소실된 것은 genkwanin의 작용이 CP-AMPAR 매개 Ca2+ 유입을 통한 시냅스 강화에 의존함을 시사한다. 이러한 결과는 genkwanin이 GluA1–CP-AMPAR 경로를 활성화하여 시냅스 수준에서 LTP를 직접적으로 조절할 수 있음을 보여준다. 본 연구의 메커니즘은 TMCA 등 유사 천연물 연구들과 기저 경로를 공유하면서도 genkwanin은 GluA1 서브유닛의 Ser845 인산화를 촉진함으로써 PKA 활성화 경로를 자극하였으며, 그 결과 CP-AMPAR의 시냅스막 삽입이 증가하고 이를 통한 세포 내 Ca2+ 유입이라는 보다 구체적이고 기전을 제시한다는 점에서 차별성을 가진다. 더불어, CP-AMPAR은 LTP 유도 초기 단계에서 일시적으로 발현되어 Ca2+ 신호를 매개하며, 이는 CaMKII 및 CREB 경로 활성화를 통해 시냅스 후 구조의 재조직화와 장기적 시냅스 강화로 이어지는 것으로 알려져 있다.18,22,29) 이러한 결과는 genkwanin이 단순한 항산화 또는 항염증 작용을 넘어서 시냅스 수준에서 직접적으로 가소성 변화를 유도할 수 있음을 시사한다.
한편, 본 연구는 해마 절편(ex vivo) 수준에서 수행되었기에 genkwanin의 시냅스 강화 효과가 in vivo 수준의 학습 및 기억 능력 향상으로 이어지는지는 추가적인 행동 실험을 통해 확인해야 한다. 또한 GluA1 인산화 및 CP-AMPAR 조절 외에도 genkwanin이 MAPK, CREB, BDNF 등 다른 신호경로에 미치는 영향을 통합적으로 분석할 필요가 있다. 향후 연구에서는 장기 투여 모델 및 동물 행동 실험을 통해 genkwanin의 시냅스 가소성 조절이 실제 인지 기능 향상으로 연결되는지를 규명하는 것이 중요하다.
결 론
종합하면, 본 연구는 genkwanin이 GluA1 인산화를 유도하여 CP-AMPAR의 시냅스막 삽입 및 Ca2+ 유입을 촉진함으로써 LTP를 강화한다는 기전을 규명하였다. 이러한 결과는 genkwanin이 시냅스 가소성을 직접 조절하는 새로운 분자적 메커니즘을 통해 인지기능 개선에 기여할 가능성을 제시하며, 이는 MCI 및 AD와 같은 인지기능 장애의 치료 전략 개발을 위한 유용한 기초 근거를 제공한다.
Acknowledgments
본 연구는 (재)보건장학회의 2023년도 연구지원 장학생 프로그램의 지원을 받아 수행되었다.
The conflict of Interest Statement
The authors declare no conflict of interest.
References
-
Petersen, R. (2000) Mild cognitive impairment: transition between aging and Alzheimer’s disease. Neurologia (Barcelona, Spain) 15: 93-101.
[https://doi.org/10.1016/S0197-4580(00)82678-0]

-
Petersen, R. C. (2004) Mild cognitive impairment. Continuum Lifelong Learn. Neurol. 10: 9-28.
[https://doi.org/10.1212/01.CON.0000293545.39683.cc]

-
Cummings, J., Apostolova, L., Rabinovici, G., Atri, A., Aisen, P., Greenberg, S., Hendrix, S., Selkoe, D., Weiner, M. and Petersen, R. (2023) Lecanemab: appropriate use recommendations. J. Prev. Alzheimers Dis. 10: 362-377.
[https://doi.org/10.14283/jpad.2023.30]

-
Karran, E., Mercken, M. and Strooper, B. D. (2011) The amyloid cascade hypothesis for Alzheimer’s disease: an appraisal for the development of therapeutics. Nat. Rev. Drug Discov. 10: 698-712.
[https://doi.org/10.1038/nrd3505]

-
El Menyiy, N., Aboulaghras, S., Bakrim, S., Moubachir, R., Taha, D., Khalid, A., Abdalla, A. N., Algarni, A. S., Hermansyah, A. and Ming, L. C. (2023) Genkwanin: An emerging natural compound with multifaceted pharmacological effects. Biomed. Pharmacother. 165: 115159.
[https://doi.org/10.1016/j.biopha.2023.115159]

-
Passeri, E., Elkhoury, K., Morsink, M., Broersen, K., Linder, M., Tamayol, A., Malaplate, C., Yen, F. T. and Arab-Tehrany, E. (2022) Alzheimer’s disease: treatment strategies and their limitations. IJMS 23: 13954.
[https://doi.org/10.3390/ijms232213954]

-
Gaidin, S. G. and Kosenkov, A. M. (2023) Calcium-permeable AMPA receptors: an underestimated pharmacological target for the therapy of brain pathologies. Neural Regen. Res. 18: 2669-2670.
[https://doi.org/10.4103/1673-5374.373714]

-
Whitehead, G., Regan, P., Whitcomb, D. J. and Cho, K. (2017) Ca2+-permeable AMPA receptor: A new perspective on amyloid-beta mediated pathophysiology of Alzheimer’s disease. Neuropharmacology 112: 221-227.
[https://doi.org/10.1016/j.neuropharm.2016.08.022]

-
Park, P., Georgiou, J., Sanderson, T. M., Ko, K.-H., Kang, H., Kim, J.-i., Bradley, C. A., Bortolotto, Z. A., Zhuo, M. and Kaang, B.-K. (2021) PKA drives an increase in AMPA receptor unitary conductance during LTP in the hippocampus. Nat. Commun. 12: 413.
[https://doi.org/10.1038/s41467-020-20523-3]

-
Sanderson, D. J., McHugh, S. B., Good, M. A., Sprengel, R., Seeburg, P. H., Rawlins, J. N. P. and Bannerman, D. M. (2010) Spatial working memory deficits in GluA1 AMPA receptor subunit knockout mice reflect impaired short-term habituation: evidence for Wagner’s dual-process memory model. Neuropsychologia 48: 2303-2315.
[https://doi.org/10.1016/j.neuropsychologia.2010.03.018]

-
Lee, Y., Jeon, J., Son, S. R., Cho, E., Moon, S., Park, A. Y., Chae, H. J., Bae, H. J., Moon, M. and Jeon, S. J. (2024) 3, 4, 5-trimethoxycinnamic acid methyl ester isolated from Polygala tenuifolia enhances hippocampal LTP through PKA and calcium-permeable AMPA receptor. Biochem. Pharmacol. 230: 116622.
[https://doi.org/10.1016/j.bcp.2024.116622]

- Khandagale, T. T., Singh, K., Sinha, S. and Puri, A. (2022) In silico study of phytochemicals for anticholinesterase activity as a potential drug target against Alzheimer’s disease. Chem. Biol. Lett. 9: 310.
-
Zeng, P., Fang, M., Zhao, H. and Guo, J. (2021) A network pharmacology approach to uncover the key ingredients in Ginkgo Folium and their anti-Alzheimer’s disease mechanisms. Aging (Albany NY) 13: 18993.
[https://doi.org/10.18632/aging.203348]

-
Geslani, D. M., Tierney, M. C., Herrmann, N. and Szalai, J. P. (2005) Mild cognitive impairment: an operational definition and its conversion rate to Alzheimer’s disease. Dement. Geriatr. Cogn. Disord. 19: 383-389.
[https://doi.org/10.1159/000084709]

-
Petersen, R. C. (2007) Mild cognitive impairment. Continuum Lifelong Learn. Neurol. 13: 15-38.
[https://doi.org/10.1212/01.CON.0000267234.69379.4e]

-
Gauthier, S., Reisberg, B., Zaudig, M., Petersen, R. C., Ritchie, K., Broich, K., Belleville, S., Brodaty, H., Bennett, D. and Chertkow, H. (2006) Mild cognitive impairment. Lancet 367: 1262-1270.
[https://doi.org/10.1016/S0140-6736(06)68542-5]

-
Gąsiorowski, K., Brokos, J. B., Sochocka, M., Ochnik, M., Chojdak-Łukasiewicz, J., Zajączkowska, K., Fułek, M. and Leszek, J. (2022) Current and near-future treatment of alzheimer’s disease. Curr. Neuropharmacol. 20: 1144-1157.
[https://doi.org/10.2174/1570159X19666211202124239]

-
Zarini-Gakiye, E., Amini, J., Sanadgol, N., Vaezi, G. and Parivar, K. (2020) Recent updates in the Alzheimer’s disease etiopathology and possible treatment approaches: A narrative review of current clinical trials. Curr. Mol. Pharmacol. 13: 273-294.
[https://doi.org/10.2174/1874467213666200422090135]

-
Galasko, D., Xiao, M., Xu, D., Smirnov, D., Salmon, D. P., Dewit, N., Vanbrabant, J., Jacobs, D., Vanderstichele, H. and Vanmechelen, E. (2019) Synaptic biomarkers in CSF aid in diagnosis, correlate with cognition and predict progression in MCI and Alzheimer’s disease. Alzheimers Dement. (NY) 5: 871-882.
[https://doi.org/10.1016/j.trci.2019.11.002]

-
Ikonomovic, M. D., Mufson, E. J., Wuu, J., Cochran, E. J., Bennett, D. A. and DeKosky, S. T. (2003) Cholinergic plasticity in hippocampus of individuals with mild cognitive impairment: correlation with Alzheimer’s neuropathology. J. Alzheimers Dis. 5: 39-48.
[https://doi.org/10.3233/JAD-2003-5106]

-
Diering, G. H. and Huganir, R. L. (2018) The AMPA receptor code of synaptic plasticity. Neuron 100: 314-329.
[https://doi.org/10.1016/j.neuron.2018.10.018]

-
Park, P., Sanderson, T. M., Amici, M., Choi, S. L., Bortolotto, Z. A., Zhuo, M., Kaang, B. K. and Collingridge, G. L. (2016) Calcium-permeable AMPA receptors mediate the induction of the protein kinase A-dependent component of long-term potentiation in the hippocampus. J. Neurosci. 36; 622-631.
[https://doi.org/10.1523/JNEUROSCI.3625-15.2016]

-
Wiltgen, B. J., Royle, G. A., Gray, E. E., Abdipranoto, A., Thangthaeng, N., Jacobs, N., Saab, F., Tonegawa, S., Heinemann, S. F. and O'Dell, T. J. (2010) A role for calcium-permeable AMPA receptors in synaptic plasticity and learning. PLoS One 5: e12818.
[https://doi.org/10.1371/journal.pone.0012818]

-
Colavitta, M. F. and Barrantes, F. J. (2023) Therapeutic strategies aimed at improving neuroplasticity in Alzheimer disease. Pharmaceutics 15: 2052.
[https://doi.org/10.3390/pharmaceutics15082052]

-
Navakkode, S. and Kennedy, B. K. (2024) Neural ageing and synaptic plasticity: prioritizing brain health in healthy longevity. Front. Aging Neurosci. 16: 1428244.
[https://doi.org/10.3389/fnagi.2024.1428244]

-
Vialko, A., Chałupnik, P. and Szymańska, E. (2025) Positive AMPA and kainate receptor modulators and their therapeutic potential in CNS diseases: A comprehensive review. IJMS 26: 6450.
[https://doi.org/10.3390/ijms26136450]

- Mehan, S., Parveen, S., Kaur, G., Kukkar, U., Dudi, R., Rajput, M. and Kalra, S. (2017) Targeting phytochemical driver in AC/cAMP/PKA/CREB activation: The next frontier for alleviating Huntington’s type neurodegenerative disorders in 3-NP animal model: A complete review. EC Neurol. 6: 77-131.
-
Sharma, P., Kumar, A. and Singh, D. (2019) Dietary flavonoids interaction with CREB-BDNF pathway: An unconventional approach for comprehensive management of epilepsy. Curr. Neuropharmacol. 17: 1158-1175.
[https://doi.org/10.2174/1570159X17666190809165549]

-
Park, P., Kang, H., Georgiou, J., Zhuo, M., Kaang, B.-K. and Collingridge, G. L. (2021) Further evidence that CP-AMPARs are critically involved in synaptic tag and capture at hippocampal CA1 synapses. Mol. Brain 14: 26.
[https://doi.org/10.1186/s13041-021-00737-2]
