
구증구포 강황 Methylene chloride 분획의 예쁜 꼬마선충 내의 항산화 효과
Abstract
In the process of searching for antioxidants in plants, the methylene chloride fraction of guzeungupo-processed Curcuma longa L. was observed to have a strong scavenging effect on DPPH radicals. In the study using Caenorhabditis elegans, the methylene chloride fraction reduced the level of reactive oxygen species (ROS), while the oxidative stress resistances of superoxide dismutase (SOD) and catalase were improved. The methylene chloride fraction was also found to cause the transgenic strain CF1553 to produce resistant proteins that resist oxidative stress.
Keywords:
Guzeunggupo-processed Curcuma longa L., Caenorhabditis elegans, Antioxidant effect, SOD, Catalase, ROS노화는 유전적 및 환경적 요인, 영양 상태, 생활 습관으로 인해 조직과 장기 기능이 점진적으로 상실되는 과정이다. 산화 스트레스는 세포 노화의 가장 중요한 메커니즘 중 하나로, 여러 관련된 비전염성 질환으로 유전체 불안정성, 텔로미어 단축, 프로테옴 항상성 감소, 줄기세포 기능의 변화, 세포 간 신호 전달기능의 감소, 미토콘드리아 기능 장애, 대사 불균형 등을 초래한다.1) 활성산소종(ROS)의 과잉 생산은 산화 스트레스를 유발하여 질병 발병에 있어 중요한 요인이 되며, 이는 삶의 질을 현저히 떨어뜨리고 심혈관 질환과 같은 사망의 원인이 되기도 한다. ROS는 핵산, 단백질, 지질, 탄수화물, 심지어 작은 무기물까지 다양한 인체 분자를 산화시킬 수 있는 작지만 반응성이 높은 물질이며, 항산화제는 ROS와 상호 작용하여 산화 과정을 억제할 수 있는 내인성 및 외인성 물질이다.2) 정상적인 생리적 조건에서는 소량의 ROS가 세포 내에서 생성되며, 이는 세포 신호 전달에 필요한 기능을 한다. 과잉의 ROS는 생체 내에 존재하는 항산화 방어 시스템에 의해 쉽게 감지되고 제거되지만 병태생리학적 조건에서는 항산화 방어 시스템의 완충 능력을 초과하여 세포 손상을 초래하는 것으로 보고되고 있다.3-5) 과도한 ROS는 산화 스트레스를 유발하여 생체분자 손상을 초래하며, 암, 당뇨병, 염증성 장질환과 같은 질병과 밀접한 관련이 있다. 생체 내에서 superoxide dismutase (SOD), catalase, glucose oxidase, glutathione peroxidase와 같은 항산화 효소는 시너지 작용을 통해 ROS 수치를 효과적으로 감소시켜 산화 스트레스를 완화하는데 중요한 역할을 한다.6) 그러나 인체는 공해, 과도한 스트레스와 같은 상황에서 이와 같은 항산화 시스템으로 부족한 경우가 발생하게 되어 이러한 효소들과 더불어 외부에서 공급하는 vitamin C, E나 flavonoid와 같은 polyphenol 화합물 등의 천연물 항산화제의 보충이 필요하다. 노화는 자연스럽게 진행되는 현상이지만 바람직한 노화의 진행을 위해서는 체내의 항산화 방어 시스템을 건강하게 유지하고 ROS의 과도한 생성을 초래하지 않는 과로나 오염된 음식이나 환경을 개선할 필요가 있으며, 비교적 안전성이 있을 것을 판단되는 천연물로부터 지속적인 항산화제의 개발이 필요하다.7,8)
강황(Curcuma longa L., Zingiberaceae)은 인도에서 가장 많이 재배되고 국내에서도 중부이남에서 재배하고 있는 식물이다. 전 세계적으로 한약재로 또는 식품의 원료나 천연색소로 식품에 다양하게 이용되고 있다. 식용 및 다양한 질병에 대한 전통적인 치료제로 이용되는 독특한 향을 가진 초본식물이다.9) 강황 추출물은 항암, 관절염 및 자가면역질환 개선효과, 신경보호 효과 등 다양한 효능이 보고되어 있다.9-11)
본 연구는 식물에서 항산화 활성 물질을 찾는 과정에서 강황의 methanol 추출물이 우수한 항산화 효능을 나타내고 강황을 구증구포한 methanol 추출물이 더 우수한 DPPH radical 소거활성을 나타내어 구증구포한 강황의 용매 계통 분획물을 제조하여 예쁜꼬마선충을 이용하여 항산화 실험을 진행한 내용이다. 식물 재료의 구증구포의 장점은 항산화 성분의 증가로 인한 약리성분의 증가와 숙성 과정 중 생성되는 배당체들의 가수분해로 인한 비당체의 생성을 비롯하여 난소화성 물질들의 소화가 용이하게 되어 활성성분의 흡수와 소화에 도움이 되는 특징이 있다.12) 구증구포 강황 methanol 추출물을 용매 계통 분획물로 제조하여 DPPH radical 소거 능력을 통해 가장 효능이 좋은 methylene chloride (CH2Cl2) 분획을 대상으로 예쁜꼬마선충 내의 항산화 효소인 SOD, catalase 활성과 산화 스트레스 및 ROS 축적 억제에 미치는 영향을 확인하였다. 또한, 산화 스트레스에 저항하는 단백질의 생성 여부를 확인하기 위해 형광이 삽입된 돌연변이 꼬마선충인 CF1553을 이용하여 실험하였으며, 몇 가지 지견을 얻었기에 이를 보고하고자 한다.
재료 및 방법
실험재료 − 실험에 사용한 강황은 시중에서 구입하여 김대근 교수가 검증한 후에 세척하여 물기를 말린 후 사용하였으며, 표준품은 우석대학교 약학대학 생약표본실에 보관하고 있다(WS-25-009). 구증구포 강황은 국산 강황을 전기건조기(발효증숙과학시스템, (농)앤제이메디칼㈜)를 이용하여 65℃에서 건조 및 증숙과정을 9번 시행하여 실험에 사용하였다.
추출 및 분획 − 잘 건조한 구증구포 강황 200 g을 50℃에서 methanol로 5시간씩 2회 추출하였다. 추출액을 수욕상에서 농축하여 methanol 엑스 약 30 g을 얻은 후 증류수로 현탁하여 동량의 n-hexane (0.4 g), methylene chloride (1.3 g), ethyl acetate (0.2 g)과 n-butanol (2.8 g)으로 분획하였다.
DPPH free radical 소거능 측정 − 구증구포 강황 CH2Cl2 분획을 농도별로 조제한 각각의 시료를 96 well plate에 분주하여, 0.2 mM의 1,1-diphenyl-2-picrylhydrazyl (DPPH) ethanol 용액을 일정량 씩 가하여 10초간 진탕하고 25℃에서 30분간 반응시켜서 517 nm에서 microplate reader로 vitamin C를 대조군으로 하여 흡광도를 측정하였다.13)
예쁜꼬마선충(Caenorhabditis elegans) 배양 − 예쁜꼬마선충은 E. coli OP50를 도말하고 20℃에서 Nematode Growth Medium (NGM) agar plate상에서 배양하여 사용하였고, DMSO에 용해한 구증구포 강황 시료를 0.1% (v/v)의 DMSO에 용해시킨 후 NGM plate에서 배양하였다.14)
선충 체내의 SOD, catalase 활성 측정 − 구증구포 강황 시료를 농도별로 조제한 plate에 선충을 배양하였고, 성체가 된 2일째에 M9 buffer(10 mM Tris-HCl, 150 mM NaCl, 0.1 mM EDTA, pH 7.5)로 세척하고 선충을 분쇄한 후 효소의 활성을 측정하였다. SOD 활성은 pH 8.0의 10 mM phosphate buffer를 용매로 하여 반응 혼합물(1.6 mM xanthine과 0.48 mM NBT 0.49 mL)을 제조하고 시료 10 μL를 가하여 37℃에서 5분간 pre-incubation시켰다. Xanthine oxidase 100 μL (0.05 U/mL)를 첨가한 후 37℃에서 20분 동안 incubation시킨 다음 69 mM SDS로 반응을 멈춘 후 570 nm에서 흡광도를 측정하였다.15) Catalase 활성은 25 mM H2O2에 농도별로 제조된 마늘 시료 50 μL씩을 가하여 3분 동안 반응시킨 후 240 nm에서 흡광도를 측정하였다.16)
선충 세포 내 활성 산소종(ROS) 분석 − 선충 내의 ROS의 양은 H2DCF-DA (2',7'-dichlorodihydro fluorescein diacetate)를 사용하여 측정하였고, 구증구포 강황 시료를 농도별 첨가한 plate에 나이가 동일한 성체가 된 후 4일째 되는 선충을 50 μM juglone 함유 M9 buffer에 넣고 2시간 방치한 후 50 μL의 M9 buffer가 담긴 96 well plate에 3마리씩 옮기고, 100 μM의 H2DCF-DA 50 μL를 첨가한 뒤 흡광도를 여기 485 nm, 방출 535 nm에서 측정하였다.17)
산화적 스트레스 저항성 측정 − 구증구포 강황 시료의 농도별 산화적 스트레스 저항성 측정은 선충이 성체가 된 지 7일째에 선충을 산화 스트레스를 유도하는 1 mM juglone이 함유된 M9 buffer가 담긴 96 well plate에 옮기고 시간 별로 생존율을 확인하였다.18)
형질 전환 선충 내 SOD-3::GFP 형광 측정 − SOD-3::GFP 유전자를 가지고 있는 돌연변이 선충 CF1553을 구증구포 강황 시료를 농도별로 투여된 배지에서 배양하였고, 성체가 된 후 3일째인 선충을 sodium azide (4%)로 마취시키고 발현된 GFP를 형광 실체 현미경(Olympus, Japan)을 이용하여 관찰하였으며, 발현강도의 정량분석은 현미경 사진과 ImageJ 소프트웨어를 이용하여 분석하였다.19)
통계 분석 − 통계 자료의 값은 평균값 ± 표준오차(mean ± S.E.M.)로 표시하였고, 통계적 유의성의 검증은 ANOVA를 통해서 분석하였다. 선충의 연속적인 생존도는 Log-rank test 분석 방법을 이용하였고, p값은 *p<0.05, **p<0.01, ***p<0.001 일 때 유의성이 있는 것으로 판단하였다.
결 과
DPPH radical 소거 효과 − 일반 강황의 methanol 엑스와 구증구포 강황의 methanol 엑스의 DPPH radical 소거 효과는 구증구포 강황이 더 좋은 활성을 나타냈다(data 미제시). 구증구포 강황의 methanol 엑스와 용매 분획의 DPPH radical 소거 효과는 Fig. 1에 나타난 바와 같이 구증구포 강황의 methylene chloride 분획물(CH2Cl2, IC50 value, 37.7 μg/mL)이 가장 좋은 radical 소거 효과를 나타냈다(vitamin C, IC50 value, 4.8 μg/mL) (Fig. 1).
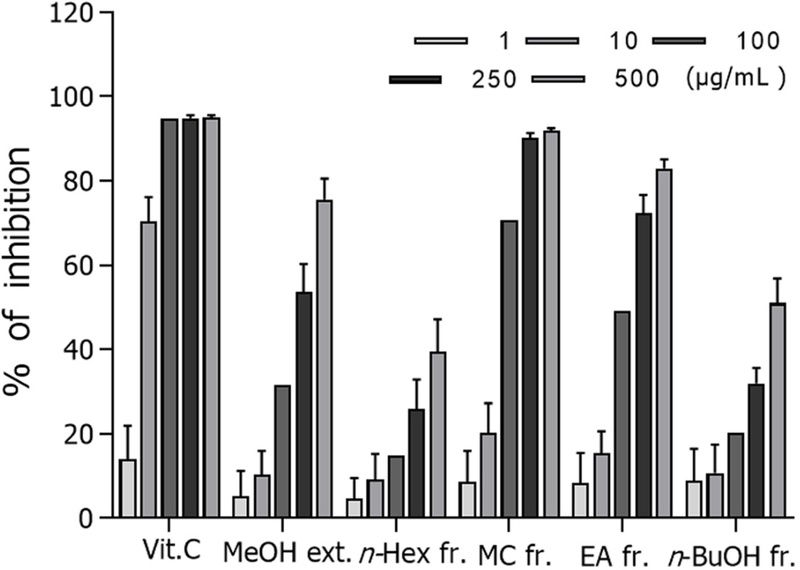
DPPH radical scavenging effects of the methanol extract and their fractions from the guzeunggupo-processed C. longa A.
SOD, Catalase 효소 활성 증가 효과 − 구증구포 강황 CH2Cl2 분획물의 xanthine oxidase로부터생성되는 superoxide anion을 활용하여 SOD의 활성을 측정하였다. 구증구포 강황 CH2Cl2 분획물 투여군은 예쁜꼬마선충의 SOD의 활성을 농도의존적으로 증가시켰으며, CH2Cl2 분획물 250 μg/mL과 500 μg/mL 투여군은 대조군에 비해 각각 18.1% (*p<0.05)와 25.1% (***p<0.001) 증가시켰다(Fig. 2A). Hydrogen peroxide를 소거시키는 능력을 측정하여 catalase의 활성을 측정하였다. CH2Cl2 분획물 250 μg/mL, 500 μg/mL 투여군은 대조군에 비해 각각 18.9% (**p<0.01), 32.4% (**p<0.01)를 증가시켰다(Fig. 2B).
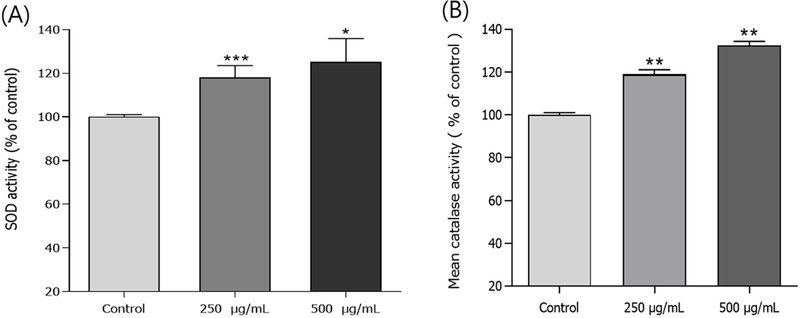
Effects of methylene chloride fraction from the guzeunggupo-processed C. longa on the antioxidant enzyme activity of wild-type N2 nematode. (A) The enzymatic reaction of xanthine with xanthine oxidase was used to generate •O2- and the SOD activity was estimated spectrophotometrically through formazan formation by NBT reduction. The SOD activity was showed as a percentage of superoxide-scavenged amount per control. (B) Catalase activity was calculated from the concentration of residual H2O2, as determined by a spectrophotometric method. The catalase activity was expressed in U/mg protein. Data are expressed as the mean ± S.E.M. of three independent experiments. Differences compared to the control were considered significant at *p<0.05, **p<0.01 and ***p<0.001 by the one-way ANOVA.
ROS 축적 감소 효과 − 구증구포 강황 CH2Cl2 분획물의 선충 내 ROS의 축적 억제 효능은 H2DCF-DA와 선충 내에서 생성되는 ROS를 반응시켜 생성되는 형광을 관찰하였다. ROS의 감소 효능은 대조군에 비해 구증구포 강황 CH2Cl2 분획 250 μg/mL, 500 μg/mL 투여군에서 각각 11.4% (***p<0.001), 15.1% (**p<0.01)를 감소시키는 효능을 보여주었다(Fig. 3).
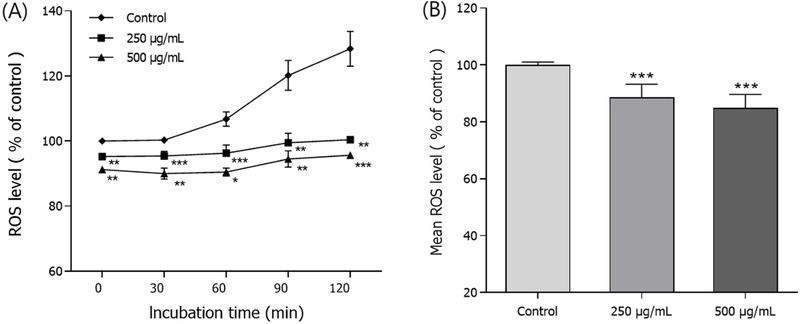
Effects of methylene chloride fraction from the guzeunggupo-processed C. longa on the intracellular ROS levels of wild-type N2 nematodes. Intracellular ROS accumulation was examined in a microplate fluorescence reader at 535 nm (emission) and 485 nm (excitation). (A) Plates were read for 120 min. (B) The average percentages of intracellular ROS accumulation were presented. Differences compared with the control were considered significant at *p<0.05, **p<0.01 and ***p<0.001 by the one-way ANOVA.
산화적 스트레스 저항성 증가 효능 − 구증구포 강황의 CH2Cl2 분획의 juglone을 이용한 선충의 산화 스트레스 저항 실험에서 CH2Cl2 분획을 미처리한 대조군이 28시간의 최대 생존시간을 보여주었고, CH2Cl2 분획 250 µg/mL, 500 µg/mL 농도에서의 최대 생존시간은 각각 34시간 및 40시간으로 증가시켰다. 대조군의 평균 생존 시간이 19.7±0.8시간이었으며, CH2Cl2 분획 250 µg/mL, 500 μg/mL 투여군은 각각 26.3±0.8시간(19.6%, ***p<0.001, 32.0±0.9시간(38.3%, ***p<0.001)으로 생존 시간을 연장시켰다(Fig. 4, Table I).
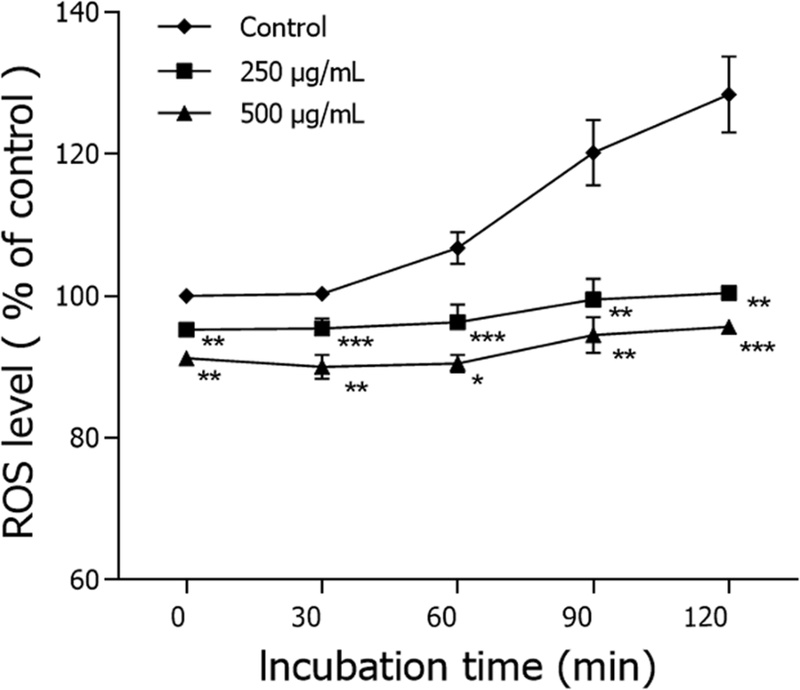
Effects of methylene chloride fraction from the guzeunggupo-processed C. longa on the stress tolerance of wild-type N2 nematodes. For the oxidative stress assays, worms were transferred to 96-well plate containing 1 mM of juglone liquid culture, and then their viability was scored. Statistical difference between the curves was analyzed by log-rank test. Differences compared with the control were considered significant at *p<0.05, **p<0.01 and ***p<0.001 by one-way ANOVA.
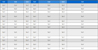
Effects of methylene chloride fraction from the guzeunggupo-processed C. longa on the oxidative stress tolerance of C. elegans
형질 전환 선충 내 SOD-3의 발현 증가 효과 − 구증구포 강황의 CH2Cl2 분획의 선충 내의 산화 스트레스에 대하여 저항성 단백질의 생성 여부는 C. elegans의 mutant CF1553을 이용하였다. 강황의 CH2Cl2 분획 250 μg/mL, 500 μg/mL 처리군이 대조군보다 각각 7.7% (*p<0.05), 11.5% (**p<0.01)의 증가된 형광이 관찰되어 SOD-3::GFP의 발현이 증가됨이 확인되었다(Fig. 5A, 5B).
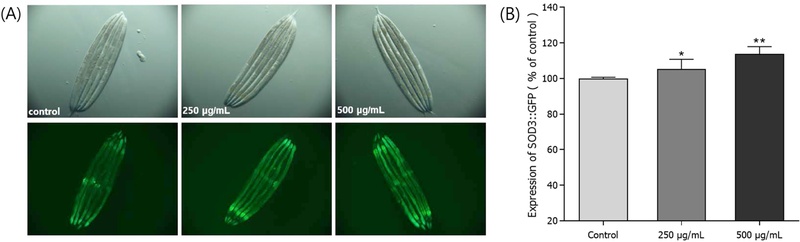
Effect of methylene chloride fraction from the guzeunggupo-processed C. longa on the expression of SOD-3 was determined using transgenic nematodes. (A) Images of SOD-3::GFP expression of CF1553 worm in the presence or absence of ethyl acetate fraction. (B) The mean GFP intensity of mutant was represented as mean ± S.E.M. of values from 19 to 25 animals per each experiment. Differences compared with the control were considered significant at *p<0.05 and **p<0.01 by one-way ANOVA.
고 찰
예쁜꼬마선충(C. elegans)은 유전자 정보가 모두 해독되어 기초 과학 연구에서 자주 사용되는 실험모델이 되었다.20,21) 특히 수명이 20일 전후로 짧아 노화와 수명 연장 관련 연구에 응용되고 있는데 특정 유전자의 조절을 통하여 수명을 연장할 수 있는 가능성을 제시하여 노화연구에 새로운 모델로 각광을 받게 되었다.22) 본 연구는 C. elegans를 이용하여 구증구포 강황의 methanol 추출물 분획 중 DPPH radical 소거능이 강한 CH2Cl2 분획을 대상으로 항산화 효능을 측정하였다. CH2Cl2 분획의 선충 내 SOD, catalase의 활성을 유의성 있게 상승시켰으며, 반면에 C. elegans 내 ROS 축적 수준을 농도 의존적으로 감소시키는 효능을 보여 주었다. Juglone으로 유도된 산화 스트레스는 구증구포 강황 CH2Cl2 분획을 처리한 실험군이 대조군과 비교하여 농도 의존적인 생존율 증가가 나타나 산화 스트레스를 억제하는 활성이 있음을 보여 주었다. 단백질 유전자 활성시에 형광을 나타내는 mutant (GFP-fused transgenic strain)인 선충 CF1553을 이용한 산화 스트레스를 이겨내는 단백 발현 여부를 측정하는 실험에서는 mutant 내의 형광이 농도 의존적으로 유의성 있게 크게 증가됨이 관찰되어 산화 스트레스에 저항하는 단백질의 생성되었음을 확인할 수 있었다.23) 노화 관련 이론은 여러 실험을 통해 알려지고 있지만 그 중에 전통적으로 인정받고 있는 가설 중의 하나는 자유 라디칼 노화 이론으로 ROS의 역할을 중시하고 있다. 이 이론은 미토콘드리아 내의 ROS 생산이 보편성(universal), 내인성(endogenous), 점진성(progressive), 유해성(deleterious)이 있고 노화와 상관관계가 있어 강력한 노화 이론으로 거론되고 있으며, 다양한 종에서 수많은 실험을 통해 ROS와 그 발암 특성의 돌연변이 효과가 입증되기도 하였다.24,25)
구증구포 강황의 CH2Cl2 분획은 C. elegans 내의 SOD와 catalase의 활성을 유의성 있게 올려 주었으며, ROS의 농도는 유의성 있게 낮추었고, 산화 스트레스에 저항할 수 있는 단백질의 생성을 확인할 수 있었다. 이 결과로 볼 때 구증구포 강황의 CH2Cl2 분획은 C. elegans 항산화 능력을 상승시켜 수명 연장에도 도움을 줄 수 있을 것으로 생각된다. 이러한 결과는 강황에 다량 존재하는 curcumin 유도체와 같은 polyphenol 화합물에 기인하는 효능일 것으로 판단된다.26,27) 본 연구의 결과물은 몇 가지 가능성 있는 항산화 관련 효능으로 이후에 구증구포 강황 추출물의 항노화와 관련된 단일 물질을 확보하여 물질 수준에서의 효능과 항산화, 항노화 기전에 대한 연구가 더 필요할 것으로 사료된다.
결 론
구증구포 강황 CH2Cl2 분획은 DPPH free radical 소거 효능을 농도의존적으로 높여 주었으며, C. elagans 내의 SOD, catalase의 활성을 유의성 있게 높여 주었다. C. elagans 내 ROS의 축적 수준을 낮추어 주었고, 산화 스트레스 조건에서는 C. elagans의 생존율을 유의성 있게 증가시켰다. C. elagans의 mutant인 CF1553을 이용한 산화 스트레스에 주는 영향을 관찰한 실험에서는 구증구포 강황 CH2Cl2 분획을 처리했을 때 C. elagans의 형광 발현율을 크게 상승시키는 것이 확인되어 산화 스트레스를 감소할 수 있는 저항 단백질의 증가 가능성이 확인되었다. 결론적으로 구증구포 강황 CH2Cl2 분획은 노화와 관련된 항산화 효능이 있는 것으로 사료되며 이와 관련된 질병의 예방 또는 치료의 후보 원료가 될 수 있을 것으로 판단된다.
Acknowledgments
본 연구는 2025년도 교육부 및 전북특별자치도의 재원으로 전북RISE센터의 지원을 받아 수행된 지역혁신중심 대학지원체계(RISE)의 결과입니다(2025-RISE-13-WSU).
References
-
Martemucci, G., Portincas, P., Di Ciaula, A., Mariano, M., Centonze, V. and D'Alessandro, A. G. (2022) Oxidative stress, aging, antioxidant supplementation and their impact on human health: An overview. Mech. Ageing Dev. 206: 111707.
[https://doi.org/10.1016/j.mad.2022.111707]

-
Młynarska, E., Hajdy,s J., Czarnik, W., Fularski, P., Leszto, K., Majchrowicz, G., Lisińska, W., Rysz, J. and Franczyk, B. (2024) The role of antioxidants in the therapy of cardiovascular diseases-A literature review. Nutrients 16: 2587.
[https://doi.org/10.3390/nu16162587]

-
van der Pol, A., van Gilst, W. H., Voors, A. A. and van der Meer, P. (2019) Treating oxidative stress in heart failure: past, present and future. Eur. J. Heart Fail 21: 425-435.
[https://doi.org/10.1002/ejhf.1320]

-
Sahoo, B. M., Banik, B. K., Borah, P. and Jain, A. (2022) Reactive oxygen species (ROS): Key components in cancer therapies. Anticancer Agents Med. Chem. 22: 215-222.
[https://doi.org/10.2174/1871520621666210608095512]

-
He, Z., Xu, Q., Newland, B., Foley, R., Lara-Sáez, I., Curtin, J. F. and Wang, W. (2021) Reactive oxygen species (ROS): utilizing injectable antioxidative hydrogels and ROS-producing therapies to manage the double-edged sword. J. Mater. Chem. B. 9: 6326-6346.
[https://doi.org/10.1039/D1TB00728A]

-
Yayun J, Qianqian, G., Xihang, S., Yang, H., Zhenping, H., Yuying, L., Xiancheng, M., Qian, J. and Pengjun, S. (2025) Metal-organic framework-mediated antioxidant enzyme delivery in disease treatment. Redox. Biol. 85: 103778.
[https://doi.org/10.1016/j.redox.2025.103778]

-
Jena, A. B., Samal, R. R., Bhol, N. K. and Duttaroy, A. K. (2023) Cellular Red-Ox system in health and disease: The latest update. Biomed. Pharmacother. 162: 114606.
[https://doi.org/10.1016/j.biopha.2023.114606]

-
Galasso, M., Gambino, S., Romanelli, M. G., Donadelli, M. and Scupoli, M. T. (2021) Browsing the oldest antioxidant enzyme: catalase and its multiple regulation in cancer. Free Radic. Biol. Med. 172: 264-272.
[https://doi.org/10.1016/j.freeradbiomed.2021.06.010]

-
Akaberi, M., Sahebkar, A. and Emami, S. A. (2021) Turmeric and curcumin: from traditional to modern medicine. Adv. Exp. Med. Biol. 1291: 15-39.
[https://doi.org/10.1007/978-3-030-56153-6_2]

-
Gondokesumo, M. E., Rasyak, M. R. and Ibrahim, M. (2025) Anticancer activity prediction of Curcuma longa and Phyllanthus urinaria through computational analysis. J. Adv. Pharm. Technol. Res. 16: 53-60.
[https://doi.org/10.4103/JAPTR.JAPTR_209_24]

-
Zeng, L., Yang, T., Yang, K., Yu, G., Li, J., Xiang, W. and Chen, H. (2022) Efficacy and safety of curcumin and Curcuma longa extract in the treatment of arthritis: A systematic review and meta-analysis of randomized controlled trial. Front. Immunol. 13: 891822.
[https://doi.org/10.3389/fimmu.2022.891822]

- Kim, H. Y., Seo, H.-Y., Seo, W. D., Lee, M. J., Choi, M.-S. and Ham, H. (2020) Effect on angiotensin-Ⅰ converting enzyme inhibition and antioxidant activities of soybean (Glycine max L.) following steaming and drying nine times. Korean J. Food Nutr. 33: 167-173.
-
Baliyan, S., Mukherjee, R., Priyadarshini, A., Vibhuti, A., Gupta, A., Pandey, R. P. and Chang, C. M. (2022) Determination of antioxidants by DPPH radical scavenging activity and quantitative phytochemical analysis of Ficus religiosa. Molecules 27: 1326.
[https://doi.org/10.3390/molecules27041326]

-
Roux, A. E., Langhans, K., Huynh, W. and Kenyon, C. (2016) Reversible age-related phenotypes induced during larval quiescence in C. elegans. Cell Metab. 23: 1113-1126.
[https://doi.org/10.1016/j.cmet.2016.05.024]

-
Mekheimer, R. A., Sayed, A. A. and Ahmed, E. A. (2012) Novel 1,2,4-triazolo[1,5-a]pyridines and their fused ring systems attenuate oxidative stress and prolong lifespan of Caenorhabditis elegans. J. Med. Chem. 55: 4169-4177.
[https://doi.org/10.1021/jm2014315]

-
Zhang, J., Chen, R., Yu, Z. and Xue, L. (2017) Superoxide dismutase (SOD) and catalase (CAT) activity assay protocols for Caenorhabditis elegans. Bio. Protoc. 7: e2505.
[https://doi.org/10.21769/BioProtoc.2505]

-
Hernández-Cruz, E. Y., Eugenio-Pérez, D., Ramírez-Magaña, K. J. and Pedraza-Chaverri, J. (2023) Effects of vegetal extracts and metabolites against oxidative stress and associated diseases: Studies in Caenorhabditis elegans. ACS Omega 8: 8936-8959.
[https://doi.org/10.1021/acsomega.2c07025]

-
Ahmad, T. and Suzuki, Y. J. (2019) Juglone in oxidative stress and cell signaling. Antioxidants (Basel) 8: 91.
[https://doi.org/10.3390/antiox8040091]

-
Motta, H. S., Roos, D., Tabarelli, G., Rodrigues, O. E. D., Ávila, D. and Quines, C. B. (2020) Activation of SOD-3 is involved in the antioxidant effect of a new class of beta-aryl-chalcogenium azide compounds in Caenorhabditis elegans. An. Acad. Bras. Cienc. 92(suppl 2): e20181147.
[https://doi.org/10.1590/0001-3765202020181147]

-
C. elegans Sequencing Consortium (1998) Genome sequence of the nematode C. elegans: a platform for investigating biology. Science 282(5396): 2012-2018.
[https://doi.org/10.1126/science.282.5396.2012]

-
Nechipurenko, I. and Sengupta, P. (2025) C. elegans: An elegant experimental system for the study of cilia biology. Semin. Cell Dev. Biol. 174: 103636.
[https://doi.org/10.1016/j.semcdb.2025.103636]

-
Murphy, C. T., McCarroll, S. A., Bargmann, C. I., Fraser, A., Kamath, R. S., Ahringer, J., Li, H. and Kenyon, C. (2003) Genes that act downstream of DAF-16 to influence the lifespan of Caenorhabditis elegans. Nature 424(6946): 277-283.
[https://doi.org/10.1038/nature01789]

-
Waters, J. C. (2009) Accuracy and precision in quantitative fluorescence microscopy. J. Cell Biol. 185: 1135-1148.
[https://doi.org/10.1083/jcb.200903097]

-
Wang, R. J., Ni, Y. J. and Liu, Y. Q. (2024) Hesperetin Increases Lifespan and Antioxidant Ability Correlating with IIS, HSP, mtUPR, and JNK Pathways of Chronic Oxidative Stress in Caenorhabditis elegans. Int. J. Mol. Sci. 25: 13148.
[https://doi.org/10.3390/ijms252313148]

-
Baranov, V. S. and Baranova, E. V. (2017) Aging and ambiguous ROS. System genetics analysis. Curr. Aging Sci. 10: 6-11.
[https://doi.org/10.2174/1874609809666160921114504]

-
Chen, J. C., Wang, R. and Wei, C. C. (2024) Anti-aging effects of dietary phytochemicals: From Caenorhabditis elegans, Drosophila melanogaster, rodents to clinical studies. Crit. Rev. Food Sci Nutr. 64: 5958-5983.
[https://doi.org/10.1080/10408398.2022.2160961]

-
Dehzad, M. J., Ghalandari, H., Nouri, M. and Askarpour, M. (2023) Antioxidant and anti-inflammatory effects of curcumin/turmeric supplementation in adults: A GRADE-assessed systematic review and dose-response meta-analysis of randomized controlled trials. Cytokine 164: 156144.
[https://doi.org/10.1016/j.cyto.2023.156144]
