베트남인삼(Panax vietnamensis)의 효과에 대한 체계적 문헌 고찰
Abstract
Vietnamese ginseng (Panax vietnamensis) is a species of ginseng native to Vietnam and is known to be one of the species rich in ginseng saponins. Nevertheless, research aimed at revealing the effects of Vietnamese ginseng, such as clinical trials and animal studies, has not been actively conducted. In this study, the effects of Vietnamese ginseng were summarized through a systematic review, and the current research trends were presented. Out of a total of 123 papers, 18 animal and clinical trial papers were selected, and 13 papers were analyzed, excluding 5 papers that did not present direct efficacy. As a result, studies have showed that the most prevalent research on Vietnamese ginseng has focused on its anti-stress and organ protective effects, and studies on anti-cancer, anti-inflammatory, and immunoenhancement effects were also conducted. Vietnamese ginseng is widely known to provide mental benefits, and among the studies, five of the most extensively researched papers specifically focused on anti-stress effects. Four used social stress models and one used environmental stress model. All studies reported improvements in stress resistance. In the case of social stress, reduced sleep time was recovered, and oxidative damage was improved, and in the case of environmental stress, the subjects were able to endure the situation better. The only clinical trial among the analyzed papers was a study that demonstrated anti-diabetic efficacy. A significant reduction in blood sugar levels was observed in comparison with the placebo group, while other ginseng species such as Panax japonicus showed no changes or an increase in blood sugar, leading to different results. As revealed by component analysis, this could be due to the higher levels of protopanaxadiol (PPD) ginsenoside compared to other species. Further diverse clinical trials and animal studies are needed to verify the functional properties of Vietnamese ginseng.
Keywords:
Panax vietnamensis, Clinical study, In vivo study, Systematic review인삼(ginseng)은 다양한 건강 상태에 대한 전통적인 치료제로써 사용되어 왔다.1) 예로부터 한국, 중국 및 일본과 같은 아시아 국가에서 중요한 약용식물로써 사용되어 왔으며, 중추신경계 치료효과, 기분 개선, 장기 보호 등 여러 가지 이점이 있다고 여겨진다.2-5) World Flora Online Plant List (wfoplantlist.org)에서는 23종, Plant of the World Online (POWO, powo.science.kew.org)에서는 15종을 인삼의 종으로서 수록하는 등 문헌마다 인정하는 인삼 종의 수는 상이하며, 다양한 인삼종 중 고려인삼(Panax ginseng), 미국인삼(Panax quinquefolius), 삼칠(Panax notoginseng)이 가장 활발히 연구되고 있다.6-9) 특히, 고려인삼은 제2 당뇨병과 같은 대사질환 및 심장질환 발병의 위험도 개선 등 다양한 효과가 있음이 밝혀졌다.10-14) 이외에도 암 환자 삶의 질 개선, 성기능 개선, 알츠하이머 환자의 기억력 향상과 같은 효과에 관련된 연구도 진행된 바 있다.15-17)
베트남인삼(Panax vietnamensis)은 두릅나무과(Araliaceae)에 속하는 종으로, 1973년 베트남 중부의 고원지대에서 발견되어 1985년 발표된 인삼의 종이다.18,19) 위도상 가장 남쪽에서 자라는 인삼으로 알려져 있으며 베트남 소수민족에서 전통 의학으로 사용된 것으로 알려졌다.1) 베트남인삼의 세포 수준의 연구에서 항암, 항산화, 항균 등 여러 효과가 보고되었다.18-22) 또한, 성분 분석에서 majonoside R2, pseudoginsenoside RT4, ocotillol, panaxynol, protopanaxadiol과 같은 ginseng saponins의 비율이 다른 인삼종보다 높은 비율로 함유한 것으로 연구되기도 하였다.23-25) 이러한 주요 성분들의 화학 구조를 Fig. 1에 제시하였다. 이러한 성분들은 인삼 효과에 기여하는 성분으로 여겨지기에 베트남인삼은 가치 있는 인삼종 중의 하나임을 의미한다.26-28) 그럼에도, 베트남인삼에 대한 임상시험 및 동물시험을 통한 효능의 규명은 활발히 진행되고 있지는 않다.
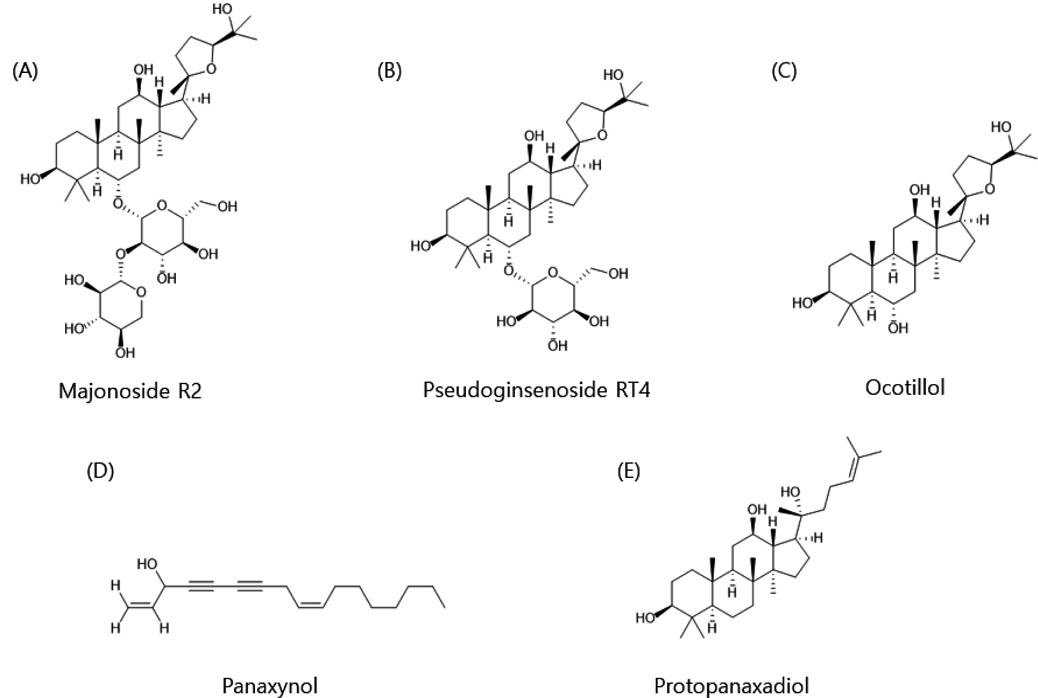
Chemical structures of bioactive compunds from Vietnamese ginseng: (A) majonoside R2; (B) pseudoginsenoside RT4; (C) ocotillol; (D) panaxynol; and (E) protopanaxadiol.
체계적 문헌 고찰(systematic review)은 기준에 따라 모든 관련 연구 문헌을 수집하고 분석하여 이전에 출간되어 발표되었던 연구 결과들을 종합하는 연구의 방법이다.29) 이는 엄격하고 객관적인 과정을 기반으로 하여 정해진 배제 기준에 따라 논문을 선별하는 과학적인 접근법이다. 일반적인 종설 연구와 비교하였을 때 품질 평가 과정에서 두 명 이상의 전문가가 개입하여 독립적으로 논문의 분류에 참여하고, 자료의 편향(bias)을 줄인다는 장점이 있다.30,31) 또한, 문헌의 결과만을 통한 공통점, 모순점과 같은 부분을 발견하고 토론하기에 더 높은 객관성을 확보할 수 있다는 차별성이 있다.32)
본 연구에서는 임상시험 및 동물시험을 통해 규명한 베트남인삼의 효능에 초점을 두어 체계적 문헌 고찰을 진행하였다. 또한, 과거부터 현재까지의 모든 관련 문헌이 제공하는 정보 및 특성들에 대해 비교 분석을 시행하였다. 그에 따라 베트남인삼의 동물 모델 이상의 연구에서 밝혀진 효능에 대한 정보를 요약하고 연구 동향을 제시하였다.
재료 및 방법
문헌 검색 - 베트남인삼의 기능성을 in vivo를 통하여 확인한 문헌을 검색하기 위해, PubMed, Embase, CENTRAL (Cochrane), ClinicalTrials.gov 에서 검색을 진행하였다. 해당 사이트들에 베트남인삼의 학명인 ‘Panax vietnamensis’와 더불어 이명인 ‘vietnamese ginseng’, ‘Ngọc Linh ginseng’을 검색어로 이용하였다. 문헌은 2024년 7월 30일에 일괄 수집하였으며, 이후 주기적으로 출간 여부를 확인하기 위한 검색을 진행하였다.
포함 및 배제 기준 – 본 연구에서는 베트남인삼의 기능성을 조사하였으며, 포괄적인 선정을 위하여 베트남인삼의 단일 처리 실험과 병용 처리 실험을 모두 포함하였다. 포함된 논문이 (1) in vivo, 임상시험이 아닌 연구, (2) 성장 조건, 생합성 경로와 같은 본 연구와 관련 없는 주제의 문헌, (3) 2차 자료 분석 문헌, (4) 기능성이 제시되지 않은 문헌, (5) 초록이나 전체 문헌을 이용할 수 없는 경우, (6) 중복 논문 중 하나에 해당 시에는 적합하지 않다고 판단하여 배제하였다. 정보 추출 단계를 위해 각 문헌의 전문을 읽어 평가를 진행하였다. 선별 과정에서는 두 명의 저자가 독립적으로 수행하고 결과를 비교한 후 일치하지 않는 경우 제 3자가 개입하여 평가하고 결정했다. 최종 선별이 완료된 후 정보 추출 단계를 위해 각 문헌의 전문을 읽고 평가를 수행하였다.
정보 추출(Data extraction) – 포함된 문헌에 대한 저자, 출간 연도, 실험 디자인, 사용 부위, 실험 모델, 섭취 방법, 실험군의 인원 및 복용량, 대조군의 인원 및 복용량, 기저상태, 평가 항목 및 주요 결과를 추출하였다. 베트남인삼의 성분을 포함한 혼합물질이 처리된 경우 모든 성분을 조사하였으며, 문헌에서 제시된 모든 성분을 추출하였다. 편향을 줄이기 위해 2명 이상의 저자가 독립적으로 정보를 추출한 후 상호 비교를 통해 평가자의 주관이 개입되지 않도록 하였다.
품질 평가(Quality assessment) – 문헌의 편향 위험성을 평가하기 위해 동물시험 연구는 Cochrane risk of bias tool을 기반으로 한 SYRCLE’s risk of bias tool for animal studies를, 임상시험 연구는 National Institutes of Health에서 제공하는 Study Quality Assessment Tools를 이용하였다.33,34) 동물시험의 평가에서 질문의 각 항목에 대해 ‘Yes’, ‘No’, ‘Unclear’로 기록하였으며, 10개의 질문에서 Yes의 개수에 따라 문헌의 compliance를 계산하였다. 임상시험의 경우는 ‘Yes’, ‘No’, ‘Cannot Determine’으로 각 항목을 기록했고, 최종 결과에 따라 ‘Good’, ‘Fair’, ‘Poor’로 등급화 하였다. 평가자의 주관 개입에 따른 편향성을 막기 위하여 2명 이상의 저자가 투입되어 개별적으로 평가를 진행한 후 비교하였다. 비교 과정에서 일치하지 않는 항목에 대해서는 제3자의 개입 하에 다시 평가가 진행되었다.
결과 및 고찰
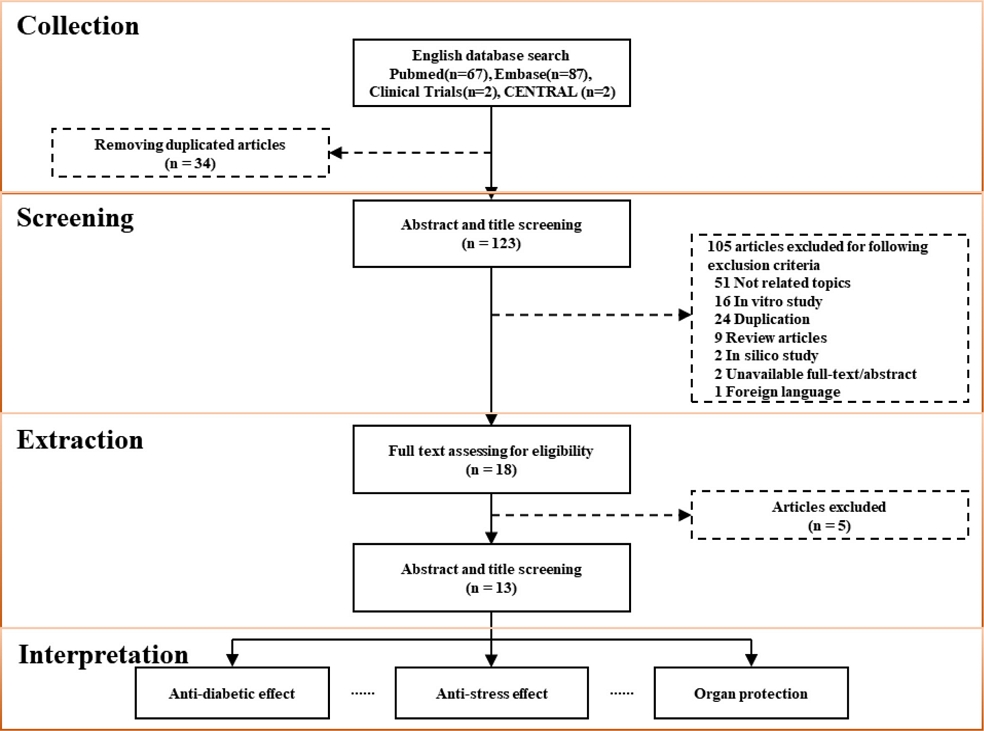
자료 선정 – 베트남인삼에 관련된 문헌을 PubMed, Embase, CENTRAL (Cochrane), ClinicalTrials.gov에서 조사하여 각각 67개, 87개, 2개, 2개를 찾았다. 그중 34개의 중복되는 문헌을 제거하여 123개를 선별하였으며, 남은 문헌들의 초록과 제목을 포함 및 배제 기준에 따라 18개의 문헌으로 추렸다. 선정된 문헌들의 전문을 내려받아 자료 추출을 하는 과정에서 배제 기준에 부합하는 논문을 5개 더 제거하여 13개의 문헌을 추출했다. 전반적인 흐름과 자세한 과정은 Fig. 2에 기재하였다.
선정 문헌 정리 및 분류 – 문헌의 저자 및 출간 연도, 사용 부위, 연구 디자인, 실험 모델, 투여 경로, 질병 및 증상의 종류, 처리군과 대조군의 수와 복용량, 처리 기간을 정리하여 Table Ⅰ에 자세히 기재하였다. 추출된 자료를 간단히 언급하면, 사용된 베트남인삼의 부위는 기재되지 않음 5건, 뿌리와 근경 5건, 뿌리 3건이었다. 투여 방법은 경구투여 10건, 복강투여 7건, 뇌실 내 주사 1건이었다. 총합이 13건 이상인 것은 한 연구 내에서 여러 투여 방법을 진행했기 때문이다. 투여 기간은 단회투여에서 25주까지 문헌에 따라 다양하였으나, 단회투여로 진행하는 경우가 6건으로 가장 많았다. 투여 성분의 경우, 단일 성분 majonoside-R2가 7건으로 가장 많았고, 단순 추출물 5건, total saponin 3건이 있었다. 그 밖의 자세한 사항은 Fig. 3에 기재하였다. 베트남인삼의 효능은 스트레스 완화가 5건으로 가장 많았으며, 다음으로 장기보호 4건, 항암, 항당뇨, 면역증진, 항염증 각 1건이 있었다. 자세한 효능과 평가 항목, 그리고 결론은 Table Ⅱ에 정리하였다. 또한, 효능은 Fig. 3에도 도식화하였다.

Study design and description of the included studies. p.o., oral administration; i.p., intraperitoneal; i.c.v., intracerebroventricular; DEN, N-nitrosodiethylamin; PB, phenobarbital; NOR1, (±)-(E)-methyl-2-[(E)-hydroxyimino]-5-nitro-6-methoxy-3-hexenamide; TPA, 12-O-tetradecanoyl-13-acetate; RND, randomized; DB, double-blind; MCS, multiple-crossover; DPC, double-placebo; VG, Vietnamese Ginseng
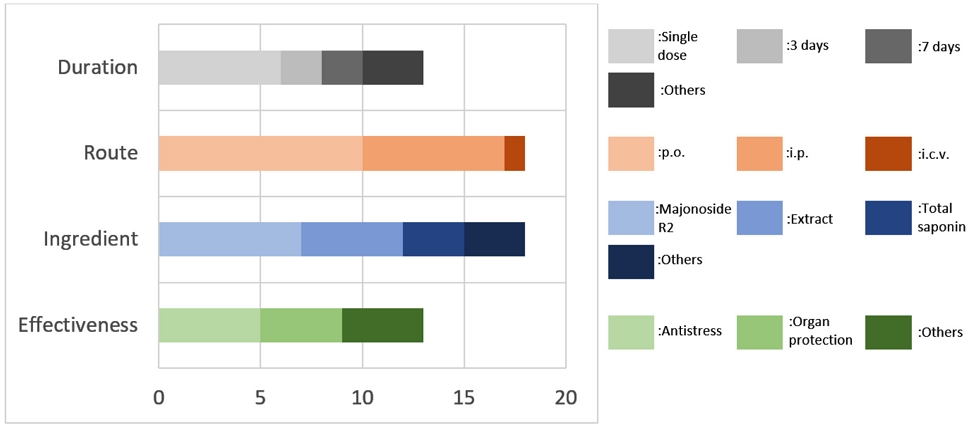
Several categorized features of all studies on Vietnamese ginseng. p.o., oral administration; i.p., intraperitoneal; i.c.v., intracerebroventricular.

Evaluation system, effectiveness and main result of the included studies. NOR1, (±)-(E)-methyl-2-[(E)-hydroxyimino]-5-nitro-6-methoxy-3-hexenamide; TPA, 12-O-tetradecanoyl-13-acetate
품질 평가(Quality assessment) – 평가한 12개의 동물시험 연구의 compliance 평가 결과, 50%가 5건으로 가장 많았고, 60% 4건, 40% 3건이 있었다. 모든 문헌에서 공통적으로 실험동물이 무작위 배정 여부와 평가자의 맹검 여부는 알 수 없었다. 임상문헌 1건은 14개의 질문 중 11개가 ‘Yes’로 평가되어 ‘Good’으로 등급화했다. 하지만, 표본이 12명으로 적었기에 대표성을 확보할 수 없을 것이라 판단한다.
베트남 인삼의 효능
스트레스 개선 효과 – 인삼은 진정 작용, 항스트레스와 같은 정신적인 이점이 있다고 알려졌다.35,36) 실제로, 베트남인삼에 대한 논문 추출 과정에서 구별된 문헌 중 5건이 항스트레스에 대한 연구로 가장 많았다. 5건 중 2건은 사회적 고립을 통한 스트레스 유도 모델(Social isolation-induced stress model), 2건은 communication box를 통한 심리적 스트레스 유도 모델(Communication box-induced psychologically stress model)을 사용하여 스트레스 개선 효과를 관찰했다.37-40) 나머지 1건은 스트레스 유도 모델이 아닌 Cold swimming test를 사용하여 스트레스 개선 효과를 관찰했다.41)
사회적 고립을 통한 스트레스 유도 모델을 사용한 문헌 2건 중 1건에서는 스트레스로 인한 수면시간 변화를 관찰하였다.37) 연구에서는 수면시간 개선정도를 관찰하기 위해 pentobarbital을 사용했다. 스트레스는 수면에 영향을 주는 것으로 알려져 있으며 pentobarbital과 같은 수면제의 효능에도 영향을 미친다.42) 5~7주 동안 스트레스를 가한 뒤, 실험 30분 전 베트남인삼 추출물의 유효성분인 majonoside-R2를 복강투여 또는 뇌실 내 주사하였으며, 두 실험군에서 유의미(p < 0.05)한 수준으로 수면시간을 회복하는 것을 확인하였다. 다른 1건의 문헌은 스트레스에 따른 지질 과산화(lipid peroxidation) 정도를 알아보기 위해 malondialdehyde (MDA), NO metabolite, total glutathione을 측정했다.38) 6주간 스트레스로 인해 증가했던 MDA, NO metabolite 수치와 감소했던 total glutathione 수치는 majonoside-R2를 3일 투여했을 때, 유의미(p < 0.05)하게 개선되는 것을 관찰했다.
Communication box를 통한 심리적 스트레스를 유도한 2건의 연구들은 사회적 고립을 통한 스트레스 유도 실험과 같이 pentobarbital을 사용해 수면시간을 관찰하고, 산화적 손상을 평가하기 위해 지질 과산화를 분석했다.39,40) 두 문헌에서 스트레스를 가한 시간은 상이하였다. 수면시간에 대한 연구에서는 베트남인삼 추출물과 베트남인삼에서 추출한 사포닌, majonoside-R2와 같은 다양한 형태의 성분이 투여되었다.39) 투여물질은 투여 방법에 따라 스트레스를 노출하기 30분~1시간 전 투여됐다. 수면 유도를 위한 pentobarbital는 심리적 스트레스를 30분 가한 후 투여되었다. 실험 결과, 대조군의 수면 시간에 비해 베트남인삼 및 유효성분을 투여군의 수면 시간은 증가되었으며, 특히 majonoside-R2 투여 실험군에서 80분 이상 유의미(p < 0.01)하게 증가했다. 그러나, majonoside-R2의 수면 개선 시간은 농도 의존적으로 나타나지는 않았다. 또한, 16시간 동안 스트레스를 가하여 스트레스성 위장 병변에 대한 효과도 연구하였다.39) 연구 결과, 발생하는 위장 병변의 발병률은 대조군(약 77%)에 비해 실험군(약 15%)에서 유의미(p < 0.01)하게 개선되었으며, 심각도 역시 50% 이상 유의미(p < 0.01)하게 개선됨을 확인하였다. 한편, 산화적 손상을 관찰한 논문의 경우, 실험군은 베트남인삼에서 추출한 사포닌, majonoside-R2, majonoside-R2 aglycone과 같은 다양한 유효성분을 스트레스를 받기 직전 경구 투여 또는 복강 투여하였다.40) 이후 4시간 동안의 스트레스를 가한 후, MDA 수치를 측정했다. 연구 결과, 실험군은 대조군에 비해 유의미(p < 0.05)하게 감소하는 것을 확인했다.
Cold swimming test는 추위, 피로와 같은 생리적 스트레스와 더불어 행동의 무력감에서 오는 심리적 스트레스를 견딜 수 있는 능력을 측정하는 방법이다.43) 수영의 latency time은 스트레스 상황에 얼마나 잘 견디는지를 나타내는 지표로 사용되었으며, 연구 결과 베트남인삼 추출물을 처리한 쥐에서는 대조군에 비해 수영 latency time이 유의미(p < 0.05)하게 증가하였다. 41)
정신약리학적(Psychopharmacological) 효과 – 앞선 cold swimming test를 진행한 연구 문헌은 open-field test, rota-rod test를 통해 정신운동(psychomotor) 개선 효과, pentobarbital을 이용한 진정 효과, elevated plus-maze test를 통한 불안 완화 효과, Y-maze test, passive-avoidance test를 통한 인지기능 개선 효과를 관찰하였다.41) 실험 결과, 진정효과를 제외한 모든 실험에서 유의한(p < 0.05) 차이가 나타났다. 이는 베트남인삼 추출물이 다른 인삼과 유사하게 정신운동 자극, 불안 완화, 기억력 향상과 같은 다양한 정신약리학적 효과가 있을 가능성을 시사한다.44) 한편, pentobarbital을 이용한 진정 효과 실험에서는 유의미한 결과가 관찰되지 않았다. 이는 앞서 언급했던 pentobarbital를 이용한 연구들과 상이한 결과였다. 다른 결과가 관찰된 것은 다른 연구와 달리 기저상태가 스트레스 유도 상태가 아닌 정상 상태였기 때문으로 추측된다. 베트남인삼이 스트레스에 의한 수면 감소를 완화하는 효과는 있으나, 정상 상태의 진정효과는 미미하거나 없을 수 있다는 것이다. 다만, 다른 인삼을 연구한 논문에서 진정효과가 있다고 보고되었으며, 베트남인삼의 경우는 정상상태에서 진정효과를 확인한 실험이 1건밖에 없기 때문에 확실한 판단은 불가능했다.35) 이에, 추가적인 연구가 필요할 것으로 보인다.
장기 보호 – 베트남인삼의 장기 보호 효과를 확인한 연구는 총 4건으로, 2건은 간 보호, 나머지는 각각 신장 보호와 심장 보호에 대한 연구였다.
간 보호에 대한 연구에서는 D-galactosamine (D-GalN), lipopolysaccharide (LPS) 유도 간 손상 모델, tetrachloride 유도 간 손상 모델을 사용했다.45,46) D-GlaN과 LPS유도 간 손상 모델을 사용한 연구에서는 sGPT (ALT)와 sGOT (AST)를 통해 유의미한 간 기능의 회복(p < 0.01)을 확인하였으며, TNF-α 수치도 유의미(p < 0.05)한 차이를 확인했다. Tetrachloride 유도 간독성 모델을 사용하여 베트남 인삼의 보호 효과를 관찰한 연구에서는 tetrachloride를 통해 증가했던 AST 수치와 GSTα 수치가 실험군에서 유의미(p < 0.05)하게 감소하는 것을 확인하였다.
신장 보호에 대한 연구에서는 cisplatin 유도 신장 독성 모델을 사용하였다.47) 다른 연구들과 달리 유일하게 베트남인삼의 유효성분 중 panaxynol를 투여한 연구이다. Cisplatin 투여 시 감소했던 체중이 실험군에서 유의미하게 회복되었고, serum creatinine, serum BUN 등 신장 기능 관련 지표들이 유의미 (p < 0.05)하게 개선되었다.
심장 보호에 대한 연구에서는 isoproterenol을 투여하여 허혈성 심근 손상을 유도하였다.48) 연구 결과, 베트남인삼 추출물 투여군에서 isoproterenol에 의한 S-T 분절 상승과 심박수의 증가를 억제함이 확인되었다. 또한, 추출물을 각 ginsenoside 단일성분으로 분리하여 세포 시험을 진행한 결과, ocotillol 유형의ginsenoside에서 H9c2 심근세포에 대한 보호 효과를 확인할 수 있었다. 그러나 단일성분에 대한 동물시험은 진행되지 않았다.
항암 효과 – 고려 인삼을 포함한 다양한 인삼이 항암효과가 있다고 알려져 있으며, 이는 베트남 인삼도 세포 수준은 물론 동물시험에서 관찰된 바 있다.22,49-51) 추출된 문헌 중 1편은 베트남인삼 추출물에서 유효성분인 majonoside-R2를 분리하여 ICR, SENCAR mice에 투여한 연구였다.52) ICR mice는 N-nitrosodiethylamin (DEN)+phenobarbital (PB)-유도 간암 모델, SENCAR mice는 (±)-(E-methyl-2-[E-hydroxyimino]-5-nitro-6-methoxy-3-hexenamide (NOR1)+12-O-tetradecanoyl phorbol-13-acetate (TPA)-유도 피부 유두종, peroxynitrite+TPA-유도 피부 유두종 모델로 사용하였다.
간암 모델을 이용한 실험 결과, 간에서의 hyperplastic nodule 수가 60% 이상 억제되었고, 결절이 있는 쥐의 비율은 55% 이상 감소하였다. 피부 발암 모델의 경우, NOR1과 TPA를 처리한 모델과 peroxynitrite와 TPA를 처리한 모델에서 모두 50% 이상의 억제 효과가 확인되었다. 따라서 발암의 개시와 촉진 효과가 모두 억제되어 majonoside-R2의 항암 예방제로서의 가능성을 나타냈다. 그러나, majonoside-R2의 발암 억제 기전은 밝혀져 있지 않아, 이에 대한 추가적인 연구가 필요할 것으로 판단된다.
항당뇨 효과 – Sievenpiper, J. L.의 연구는 추출된 논문 중 유일하게 인간을 대상으로 한 문헌이었다. 12명의 참여자가 8종류의 인삼을 복용하여 항당뇨 효과를 확인한 연구였다.53) 미국인삼과 베트남인삼은 90분 plasma glucose (PG)를 감소시키는 경향이 있었다. 다른 인삼 종의 경우, peak-PG와 AUC-PG가 증가하는 등 인삼의 품종에 따라 혈당에 미치는 영향이 상이했다. 본 결과에 대해 해당 연구진은 다른 인삼종에 비해 미국인삼, 베트남인삼에서 높게 관찰된 protopanaxadiol (PPD)가 원인일 수 있다고 언급했다. 성분 분석을 진행한 다른 연구에서도 베트남인삼이 높은 비율의 PPD를 가지고 있음이 밝혀졌으며, 연구 결과와 종합하여 PPD가 항당뇨 효과에 관여한다고 생각해 볼 수 있다.9) 그러나, 다양한 측정 요소 중 일부 요소들에서만 나타난 결과를 설명할 수 있었고, 2시간 후 PG (p = 0.18), peak-plasma insulin (p = 0.22) 등의 다른 평가 요소에서는 유의미한 결과가 나타나지 않았기에 일반화하기엔 어려울 것으로 판단한다. 또한 실험 인원이 12명으로 적은 표본에서 나온 결과이기에 대표성을 확보하기 어려워 보인다.
한편, 과체중 집단(6명)에서 AUC-PI (plasma insulin) 강하 효과가 유의하게 나타났다. 비만과 2형 당뇨병은 연관성이 있는 것으로 알려져 있으며, 비만 환자의 경우는 일반적으로 혈중 인슐린 농도가 높다는 연구 결과가 있다.54) 비만 환자에서 AUC-PI가 낮아졌다는 것은 인슐린 저항성이 낮아진 것으로 판단할 수 있으며, 인슐린 저항성을 낮추는 기전으로 당뇨병을 치료하는 약물인 thiazolidinedione, metformin 등과 유사할 수도 있을 것이라 유추해 볼 수는 있을 것이다.55-57) 그러나, 앞서 언급한 바와 같이 실험 인원이 적어 대표성을 지닌다고 하기 어려운 점, 당뇨병과 비만에 관련 있는 대사증후군에서는 인슐린 저항성 외에도 다양한 원인이 관여할 수 있다는 점, 8종의 인삼 중 베트남인삼에서만 AUC-PI의 강하 효과가 나타난 점을 명확히 밝히지 못했다는 점 등을 고려하였을 때, 이를 위한 추가연구가 필요해 보인다.58)
면역증진 효과 – 베트남인삼의 면역증진 효과를 보기 위하여 swiss albino mice와 BALB/c mice에 대해 대장균을 직접적으로 복강주사 하였다.59) 베트남인삼 추출물과 유효성분인 majonoside-R2를 투여하였으며, 연구 결과 실험군에서 식세포(phagocyte) 활성이 유의미하게 증가하였으며, 72시간 이후 생존율 역시 p < 0.05로 유의미하게 증가하는 것이 확인되었다.
항염증 효과 – 항염증 효과를 제시한 1건의 연구로서, 베트남인삼에서 분리된 majonoside-R2와 대사체인 pseudoginsenoside RT4 (PRT4)와 ocotillol에 대한 문헌이 있었다.60) 세포 시험에서 이들이 Th17 세포로의 분화를 억제하는 것이 확인되었으며, ocotillol을 2,4,6-trinitrobenzenesulfonic acid (TNBS)-유도 대장염 모델에 투여하여 항염증 효과를 확인하였다. 연구 결과, 대장의 단축, myeloperoxidase 활성, 질소산화물과 PGE2의 생성이 유의미(p < 0.05)하게 억제되었다. 이외에도 TNF-α, IL-1β, IL-10, IL-17과 같은 염증지표가 개선되었기에 베트남인삼의 유효성분 중 하나인 ocotillol이 염증성 질환을 개선할 수 있음을 시사한다.
결 론
본 연구에서는 베트남인삼의 효과를 알아보기 위해 문헌 고찰을 통해 13편의 문헌을 조사하였다. 문헌에서 제시된 효능은 항스트레스 효과가 5건으로 가장 많았고, 행동 스트레스 사회적 스트레스 등 다양한 스트레스의 환경에서 이에 대한 영향을 유의미하게 완화할 수 있다는 결과가 제시되었다. 다음으로 4건의 문헌이 장기 보호에 관한 연구로, 2건은 간, 나머지는 각각 신장과 심장에 대한 보호 효과를 제시하였다. 이외에도 항암 1건, 면역증진 1건, 항염증 1건의 연구가 있었다. 항암효과에 대한 문헌에서는 간암의 결절 수와 발생률, 피부 유두종의 발병을 유의미하게 억제하는 것을 확인할 수 있었다. 면역증진 효과에서는 식세포 활성과 72시간 후 생존율이 유의미하게 증가한 것을 확인하였다. 마지막으로 항염증 연구에서는 염증세포인 Th17 세포로의 분화를 억제하고 대장염 모델에서 염증지표와 매개 물질이 유의미하게 억제됨을 보였다.
체계적 문헌 고찰을 진행한 문헌 중 1건만이 인간을 대상으로 하는 연구였다.29) 무작위 배정, 이중 맹검, 다중 교차, 이중 위약 대조의 임상시험으로 항당뇨 효과를 위약과 다른 인삼종을 교차 복용하여 규명한 연구였으며, 베트남인삼과 미국인삼만이 유의하게 혈당을 낮추는 결과가 나타났다. 이는 성분 분석에서 나타난 PPD의 높은 비율 때문일 수 있다고 제시했다. 그러나, 당뇨를 나타낼 수 있는 다양한 지표 중 일부만을 설명하였기에 항당뇨 효과가 있다고 보기는 어렵다는 점과, 적은 표본인 12명을 대상으로 연구를 진행하였기에 대표성을 확보하기 어렵다는 한계가 존재한다.
본 연구에서는 임상시험 문헌 수의 부족으로 동물모델 연구까지 모두 포함하여 체계적 문헌 고찰을 진행하였다. 하지만, 공통된 결과와 문헌 수의 부족으로 메타분석을 진행할 수 없었다. 체계적 문헌 고찰 결과, 베트남인삼의 스트레스 완화, 장기 보호 등 다양한 효능이 세포 및 동물 수준의 연구에서 제시되었으나, 아직 연구 수가 적어 추가적인 실험이 필요할 것으로 보인다. 또한, 더 많은 평가 항목을 분석하는 등 더욱 체계적인 실험을 통해 효능에 대해 보다 심도 있고 객관성이 높일 수 있는 연구가 추가적으로 진행될 필요가 있을 것으로 판단된다.
Acknowledgments
This research was supported by the Rural Development Administration of Korea (RS-2022-RD010385).
References
-
Park, H. J., Kim, D. H., Park, S. J., Kim, J. M. and Ryu, J. H. (2012) Ginseng in traditional herbal prescriptions. Journal of Ginseng Research 36: 225-241.
[https://doi.org/10.5142/jgr.2012.36.3.225]

-
Kim, H. J., Kim, P. and Shin, C. Y. (2013). A comprehensive review of the therapeutic and pharmacological effects of ginseng and ginsenosides in central nervous system. Journal of Ginseng Research 37: 8.
[https://doi.org/10.5142/jgr.2013.37.8]

-
Zhao, H., Li, Q., Pei, X., Zhang, Z., Yang, R., Wang, J. and Li, Y. (2009) Long-term ginsenoside administration prevents memory impairment in aged C57BL/6J mice by up-regulating the synaptic plasticity-related proteins in hippocampus. Behavioural Brain Research 201: 311-317.
[https://doi.org/10.1016/j.bbr.2009.03.002]

-
Kennedy, D. O. and Scholey, A. B. (2003) Ginseng: potential for the enhancement of cognitive performance and mood. Pharmacology Biochemistry and Behavior 75: 687-700.
[https://doi.org/10.1016/S0091-3057(03)00126-6]

-
Lim, S. W., Luo, K., Quan, Y., Cui, S., Shin, Y. J., Ko, E. J., Chung, B. H. and Yang, C. W. (2020) The safety, immunological benefits, and efficacy of ginseng in organ transplantation. Journal of Ginseng Research 44: 399-404.
[https://doi.org/10.1016/j.jgr.2020.02.001]

-
Van Le, T. H., Lee, S. Y., Kim, T. R., Kim, J. Y., Kwon, S. W., Nguyen, N. K., Park, J. H. and Nguyen, M. D. (2014) Processed Vietnamese ginseng: Preliminary results in chemistry and biological activity. Journal of Ginseng Research 38: 154-159.
[https://doi.org/10.1016/j.jgr.2013.11.015]

-
Dela Pena, I., Yoon, S. Y., Kim, H. J., Park, S., Hong, E. Y., Ryu, J. H., Park, I. H. and Cheong, J. H. (2014) Effects of ginseol k-g3, an Rg3-enriched fraction, on scopolamine-induced memory impairment and learning deficit in mice. Journal of Ginseng Research 38: 1-7.
[https://doi.org/10.1016/j.jgr.2013.11.003]

-
Park, J. H., Cha, H. Y., Seo, J. J., Hong, J. T., Han, K. and Oh, K. W. (2005) Anxiolytic-like effects of ginseng in the elevated plus-maze model: comparison of red ginseng and sun ginseng. Progress in Neuro-Psychopharmacology and Biological Psychiatry 29: 895-900.
[https://doi.org/10.1016/j.pnpbp.2005.04.016]

-
Van Le, T. H., Lee, G. J., Vu, H. K. L., Kwon, S. W., Nguyen, N. K., Park, J. H. and Nguyen, M. D. (2015) Ginseng saponins in different parts of Panax vietnamensis. Chemical and Pharmaceutical Bulletin 63: 950-954.
[https://doi.org/10.1248/cpb.c15-00369]

-
Bang, H., Kwak, J. H., Ahn, H. Y., Shin, D. Y. and Lee, J. H. (2014) Korean red ginseng improves glucose control in subjects with impaired fasting glucose, impaired glucose tolerance, or newly diagnosed type 2 diabetes mellitus. Journal of Medicinal Food 17: 128-134.
[https://doi.org/10.1089/jmf.2013.2889]

-
Reay, J. L., Kennedy, D. O. and Scholey, A. B. (2006) Effects of Panax ginseng, consumed with and without glucose, on blood glucose levels and cognitive performance during sustained ‘mentally demanding’ tasks. Journal of Psychopharmacology 20: 771-781.
[https://doi.org/10.1177/0269881106061516]

-
Choi, H. S., Kim, S., Kim, M. J., Kim, M. S., Kim, J., Park, C. W., Seo, D., Shin, S. S. and Oh, S. W. (2018) Efficacy and safety of Panax ginseng berry extract on glycemic control: A 12-wk randomized, double-blind, and placebo-controlled clinical trial. Journal of Ginseng Research 42: 90-97.
[https://doi.org/10.1016/j.jgr.2017.01.003]

-
Liu, Q., Wu, H., Wang, J. and Li, X. M. (2018) Effects of Shenmai injection on the values of CO, SV, and EF in patients undergoing off-pump coronary artery bypass graft: A randomized, clinical trial. Medicine 97: e0085.
[https://doi.org/10.1097/MD.0000000000010085]

-
Kim, S. Y., Seo, S. K., Choi, Y. M., Jeon, Y. E., Lim, K. J., Cho, S., Choi, Y. S. and Lee, B. S. (2012) Effects of red ginseng supplementation on menopausal symptoms and cardiovascular risk factors in postmenopausal women: a double-blind randomized controlled trial. Menopause 19: 461-466.
[https://doi.org/10.1097/gme.0b013e3182325e4b]

-
Kim, J. H., Park, C. Y. and Lee, S. J. (2006) Effects of sun ginseng on subjective quality of life in cancer patients: a double‐blind, placebo‐controlled pilot trial. Journal of Clinical Pharmacy and Therapeutics 31: 331-334.
[https://doi.org/10.1111/j.1365-2710.2006.00740.x]

-
Farnia, V., Alikhani, M., Ebrahimi, A., Golshani, S., Bahmani, D. S. and Brand, S. (2019) Ginseng treatment improves the sexual side effects of methadone maintenance treatment. Psychiatry Research 276: 142-150.
[https://doi.org/10.1016/j.psychres.2019.05.004]

-
Heo, J. H., Lee, S. T., Chu, K., Oh, M., Park, H. J., Shim, J. Y. and Kim, M. (2008) An open‐label trial of Korean red ginseng as an adjuvant treatment for cognitive impairment in patients with Alzheimer’s disease. European Journal of Neurology 15: 865-868.
[https://doi.org/10.1111/j.1468-1331.2008.02157.x]

-
Van Le, T. H., Lee, S. Y., Lee, G. J., Nguyen, N. K., Park, J. H. and Nguyen, M. D. (2015) Effects of steaming on saponin compositions and antiproliferative activity of Vietnamese ginseng. Journal of Ginseng Research 39: 274-278.
[https://doi.org/10.1016/j.jgr.2015.01.006]

-
Yamasaki, K. (2000) Bioactive saponins in Vietnamese ginseng, Panax vietnamensis. Pharmaceutical Biology 38: 16-24.
[https://doi.org/10.1076/phbi.38.6.16.5956]

-
HOUNG, N. T. T., Matsumoto, K., Kasai, R., YAMASAKI, K. and WATANABE, H. (1998) In vitro antioxidant activity of Vietnamese ginseng saponin and its components. Biological and Pharmaceutical Bulletin 21: 978-981.
[https://doi.org/10.1248/bpb.21.978]

-
Thanh, N. T., Van, T. T. H., Hung, L. V., Van Khiem, N., Mai, L. Q., Xuyen, D. T., Oanh, P. T., Van Hai, D., Dien, N. D. and Nhut, D. T. (2023) Bioactive Compounds and Biological Activities of Vietnamese Ginseng (Panax vietnamensis Ha et Grushv.). Bioactive Compounds in the Storage Organs of Plants: 1-25.
[https://doi.org/10.1007/978-3-031-29006-0_23-1]

-
Minh Nguyen, H., Truong Nguyen, H., Win, N., Piow Wong, C., Vu Huynh, K. L., Hoang, N. N., Do, K. M., Thi Nguyen, H., Viet Ho, D. and Duc Nguyen, M. (2020) Antimelanogenic Activity of Ocotillol‐Type Saponins from Panax vietnamensis. Chemistry & Biodiversity 17: e2000037.
[https://doi.org/10.1002/cbdv.202000037]

-
Duc, N. M., NHAM, N. T., KASAI, R., ITO, A., YAMASAKI, K. and TANAKA, O. (1993. Saponins from Vietnamese ginseng, Panax vietnamensis Ha et Grushv. collected in central Vietnam. I. Chemical and Pharmaceutical Bulletin 41: 2010-2014.
[https://doi.org/10.1248/cpb.41.2010]

-
Duc, N. M., Kasai, R., Ohtani, K., Ito, A., Yamasaki, K., Nham, N. T. and Tanaka, O. (1996) New saponins from Vietnamese ginseng: Highlights on biogenesis of dammarane triterpenoids. Saponins Used in Traditional and Modern Medicine: 129-149.
[https://doi.org/10.1007/978-1-4899-1367-8_13]

-
Nguyen, H. T., Vu-Huynh, K. L., Nguyen, H. M., Le, H. T., Le, T. H. V., Park, J. H. and Nguyen, M. D. (2021) Evaluation of the saponin content in Panax Vietnamensis acclimatized to lam dong province by HPLC–UV/CAD. Molecules 26: 5373.
[https://doi.org/10.3390/molecules26175373]

-
Jeong, S. M. and Nah, S. Y. (2005) Ginseng and ion channels: Are ginsenosides, active component of Panax ginseng, differential modulator of ion channels? Journal of Ginseng Research 29: 19-26.
[https://doi.org/10.5142/JGR.2005.29.1.019]

-
Nhut, D. T., Hai, N. T., Huy, N. P., Chien, H. X. and Nam, N. B. (2013) New achievement in Panax vietnamensis research. Biotechnology of Neglected and Underutilized Crops, (Springer), pp. 43-57.
[https://doi.org/10.1007/978-94-007-5500-0_3]

-
Tran, Q. L., Adnyana, I. K., Tezuka, Y., Nagaoka, T., Tran, Q. K. and Kadota, S. (2001) Triterpene Saponins from Vietnamese Ginseng (Panax v ietnamensis) and Their Hepatocytoprotective Activity. Journal of Natural Products 64: 456-461.
[https://doi.org/10.1021/np000393f]

-
Littell, J.H. (2008) Systematic reviews and meta-analysis (Oxford University Press).
[https://doi.org/10.1093/acprof:oso/9780195326543.001.0001]

- 김수영, 박지은, 서현주, 이윤재, 손희정, 장보형, 서혜선, and 신채민 (2011) NECA 체계적 문헌고찰 매뉴얼. 한국보건의료연구원: 1-287.
-
Gupta, S., Rajiah, P., Middlebrooks, E. H., Baruah, D., Carter, B. W., Burton, K. R., Chatterjee, A. R. and Miller, M. M. (2018) Systematic review of the literature: best practices. Academic Radiology 25: 1481-1490.
[https://doi.org/10.1016/j.acra.2018.04.025]

-
Giang, H. T. N., Ahmed, A. M., Fala, R. Y., Khattab, M. M., Othman, M. H. A., Abdelrahman, S. A. M., Thao, L. P., Gabl, A. E. A. E., Elrashedy, S. A. and Lee, P. N. (2019) Methodological steps used by authors of systematic reviews and meta-analyses of clinical trials: a cross-sectional study. BMC Medical Research Methodology 19: 1-11.
[https://doi.org/10.1186/s12874-019-0780-2]

-
Hooijmans, C. R., Rovers, M. M., De Vries, R. B., Leenaars, M., Ritskes-Hoitinga, M. and Langendam, M. W. (2014) SYRCLE’s risk of bias tool for animal studies. BMC Medical Research Methodology 14: 1-9.
[https://doi.org/10.1186/1471-2288-14-43]

- National Heart, L. and Blood Institute (2021) Quality Assessment of Controlled Intervention Studies. Systematic Evidence Reviews and Clinical Practice Guidelines.
-
Han, H. J., Kim, H. Y., Choi, J. J., Ahn, S. Y., Lee, S. H., Oh, K. W. and Kim, S. Y. (2013) Effects of red ginseng extract on sleeping behaviors in human volunteers. Journal of Ethnopharmacology 149: 597-599.
[https://doi.org/10.1016/j.jep.2013.07.005]

-
Koo, M. (1998) Effects of ginseng on ethanol induced sedation in mice. Life Sciences 64: 153-160.
[https://doi.org/10.1016/S0024-3205(98)00545-1]

-
Huong, N. T. T., Matsumoto, K., Yamasaki, K. and Watanabe, H. (1997) Majonoside-R2 reverses social isolation stress-induced decrease in pentobarbital sleep in mice: Possible involvement of neuroactive steroids. Life Sciences 61: 395-402.
[https://doi.org/10.1016/S0024-3205(97)00396-2]

-
Huong, N. T. T., Murakami, Y., Tohda, M., Watanabe, H. and Matsumoto, K. (2005) Social isolation stress-induced oxidative damage in mouse brain and its modulation by majonoside-R2, a Vietnamese ginseng saponin. Biological and Pharmaceutical Bulletin 28: 1389-1393.
[https://doi.org/10.1248/bpb.28.1389]

-
Huong, N. T. T., Matsumoto, K., Yamasaki, K., Duc, N. M., Nham, N. T. and Watanabe, H. (1996) Effects of majonoside-R2 on pentobarbital sleep and gastric lesion in psychologically stressed mice. Pharmacology Biochemistry and Behavior 53: 957-963.
[https://doi.org/10.1016/0091-3057(95)02147-7]

-
Yobimoto, K., Matsumoto, K., Huong, N. T. T., Kasai, R., Yamasaki, K. and Watanabe, H. (2000) Suppressive effects of Vietnamese ginseng saponin and its major component majonoside-R2 on psychological stress-induced enhancement of lipid peroxidation in the mouse brain. Pharmacology Biochemistry and Behavior 66: 661-665.
[https://doi.org/10.1016/S0091-3057(00)00257-4]

-
dela Peña, I. J. I., Kim, H. J., Botanas, C. J., De La Pena, J. B., Van Le, T. H., Nguyen, M. D., Park, J. H. and Cheong, J. H. (2017) The psychopharmacological activities of Vietnamese ginseng in mice: characterization of its psychomotor, sedative–hypnotic, antistress, anxiolytic, and cognitive effects. Journal of Ginseng Research 41: 201-208.
[https://doi.org/10.1016/j.jgr.2016.03.005]

-
Kim, E. J. and Dimsdale, J. E. (2007) The effect of psychosocial stress on sleep: a review of polysomnographic evidence. Behavioral Sleep Medicine 5: 256-278.
[https://doi.org/10.1080/15402000701557383]

-
Can, A., Dao, D. T., Arad, M., Terrillion, C. E., Piantadosi, S. C. and Gould, T. D. (2012) The mouse forced swim test. Journal of Visualized Experiments: JoVE.
[https://doi.org/10.3791/3638-v]

-
Lee, R., Kim, J. H., Kim, W. W., Hwang, S. H., Choi, S. H., Kim, J. H., Cho, I. H., Kim, M. and Nah, S. Y. (2024) Emerging evidence that ginseng components improve cognition in subjective memory impairment, mild cognitive impairment, and early Alzheimer's disease dementia. Journal of Ginseng Research.
[https://doi.org/10.1016/j.jgr.2024.02.002]

-
Le Tran, Q., Adnyana, I. K., Tezuka, Y., Harimaya, Y., Saiki, I., Kurashige, Y., Tran, Q. K. and Kadota, S. (2002) Hepatoprotective effect of majonoside R2, the major saponin from Vietnamese ginseng (Panax vietnamensis). Planta Medica 68: 402-406.
[https://doi.org/10.1055/s-2002-32069]

-
Nguyen, T., Villard, P., Barlatier, A., Elsisi, A., Jouve, E., Duc, N. M., Sauze, C., Durand, A. and Lacarelle, B. (2000) Panax vietnamensis protects mice against carbon tetrachloride-induced hepatotoxicity without any modification of CYP2E1 gene expression. Planta Medica 66: 714-719.
[https://doi.org/10.1055/s-2000-9603]

-
Lee, D., Lee, J., Vu-Huynh, K. L., Van Le, T. H., Tuoi Do, T. H., Hwang, G. S., Park, J. H., Kang, K. S., Nguyen, M. D. and Yamabe, N. (2019) Protective effect of panaxynol isolated from Panax vietnamensis against cisplatin-induced renal damage: in vitro and in vivo studies. Biomolecules 9: 890.
[https://doi.org/10.3390/biom9120890]

-
Xie, J., Li, X. B., Ma, C. H. and Jiang, W. W. (2022) Ocotillo-type ginsenosides from the Panax vietnamensis ha et grushv protect H9c2 cardiomyocytes against H2O2-induced apoptosis. Pharmacognosy Magazine 18.
[https://doi.org/10.4103/pm.pm_253_21]

-
Kim, S., Kim, N., Jeong, J., Lee, S., Kim, W., Ko, S. G. and Kim, B. (2021) Anti-cancer effect of Panax ginseng and its metabolites: from traditional medicine to modern drug discovery. Processes 9: 1344.
[https://doi.org/10.3390/pr9081344]

-
Hong, H., Baatar, D. and Hwang, S. G. (2021) Anticancer activities of ginsenosides, the main active components of ginseng. Evidence‐Based Complementary and Alternative Medicine 2021: 8858006.
[https://doi.org/10.1155/2021/8858006]

-
Vo, H. T., Ghimeray, A. K., Vu, N. T. and Jeong, Y. H. (2015) Quantitative estimation of ginsenosides in different ages of Panax vietnamensis and their anti-proliferation effects in hela cells. African Journal of Traditional, Complementary and Alternative Medicines 12: 79-83.
[https://doi.org/10.4314/ajtcam.v12i4.12]

-
Konoshima, T., Takasaki, M., Ichiishi, E., Murakami, T., Tokuda, H., Nishino, H., Duc, N. M., Kasai, R. and Yamasaki, K. (1999) Cancer chemopreventive activity of majonoside-R2 from Vietnamese ginseng, Panax vietnamensis. Cancer Letters 147: 11-16.
[https://doi.org/10.1016/S0304-3835(99)00257-8]

-
Sievenpiper, J. L., Arnason, J. T., Leiter, L. A. and Vuksan, V. (2004) Decreasing, null and increasing effects of eight popular types of ginseng on acute postprandial glycemic indices in healthy humans: the role of ginsenosides. Journal of the American College of Nutrition 23: 248-258.
[https://doi.org/10.1080/07315724.2004.10719368]

-
Kahn, B. B. and Flier, J. S. (2000) Obesity and insulin resistance. The Journal of Clinical Investigation 106: 473-481.
[https://doi.org/10.1172/JCI10842]

-
Jones, C. N., Abbasi, F., Carantoni, M., Polonsky, K. S. and Reaven, G. M. (2000) Roles of insulin resistance and obesity in regulation of plasma insulin concentrations. American Journal of Physiology-Endocrinology and Metabolism 278: E501-E508.
[https://doi.org/10.1152/ajpendo.2000.278.3.E501]

-
Quinn, C., Hamilton, P., Lockhart, C. and McVeigh, G. (2008) Thiazolidinediones: effects on insulin resistance and the cardiovascular system. British Journal of Pharmacology 153: 636-645.
[https://doi.org/10.1038/sj.bjp.0707452]

-
Herman, R., Kravos, N. A., Jensterle, M., Janež, A. and Dolžan, V. (2022) Metformin and insulin resistance: a review of the underlying mechanisms behind changes in GLUT4-mediated glucose transport. International Journal of Molecular Sciences 23: 1264.
[https://doi.org/10.3390/ijms23031264]

- Reaven, G. (2005) Insulin resistance, the insulin resistance syndrome, and cardiovascular disease. Panminerva Medica 47: 201-210.
-
Huong, N. T. T., Matsumoto, K., Nham, N., Quang, N., Duc, N., Yamasaki, K. and Watanabe, H. (1997) Effect of Vietnamese Ginseng on the phagocytosis in vitro and in vivo. Phytomedicine 4: 341-346.
[https://doi.org/10.1016/S0944-7113(97)80044-X]

-
Lee, S. Y., Jeong, J. J., Le, T. H. V., Eun, S. H., Nguyen, M. D., Park, J. H. and Kim, D. H. (2015) Ocotillol, a majonoside R2 metabolite, ameliorates 2, 4, 6-trinitrobenzenesulfonic acid-induced colitis in mice by restoring the balance of Th17/Treg cells. Journal of Agricultural and Food Chemistry 63: 7024-7031.
[https://doi.org/10.1021/acs.jafc.5b02183]