골격근 감소 개선 효과를 가지는 생지황의 성분 및 생지황 건조과정에서 주요 성분의 상대 함량 비교
Abstract
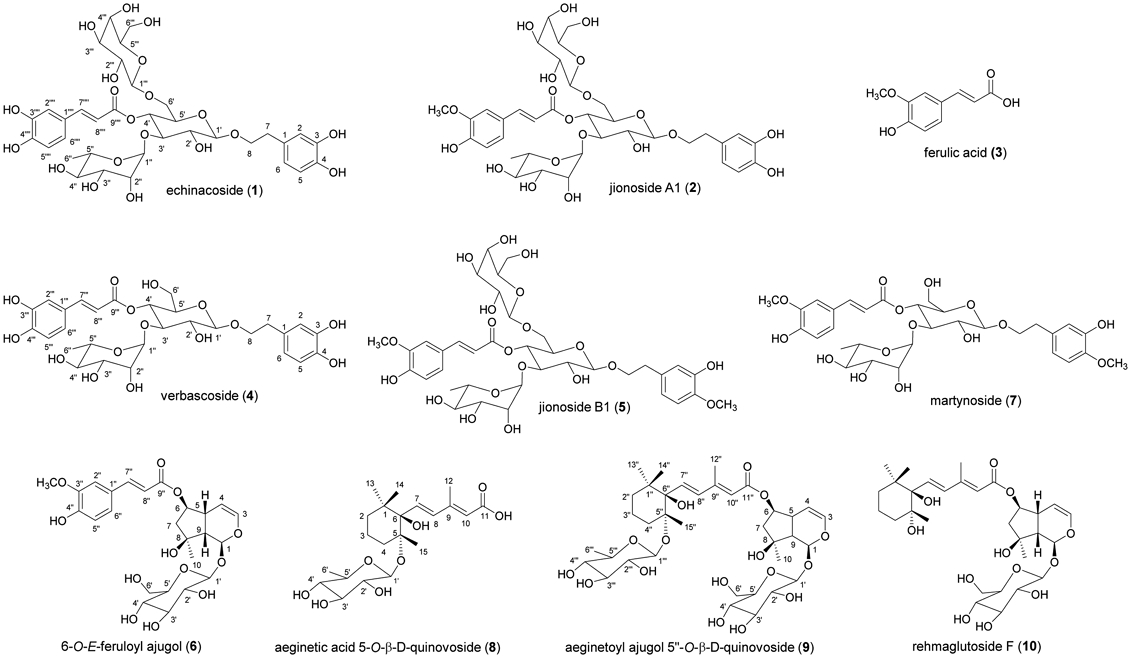
The fresh roots extract of Rehmannia glutinosa showed a preventive effect in a dexamethasone-induced C2C12 myotube atrophy model. Bioactivity-guided isolation using centrifugal partition chromatography and prep-HPLC yielded to ten compounds: five phenylethanoid glycosides (1, 2, 4, 5, and 7), three iridoids (6, 9, and 10), one phenylpropanoid (3) and one sesquiterpene glycoside (8). Their chemical structures were elucidated as echinacoside (1), jionoside A1 (2), ferulic acid (3), verbascoside (4), jinoside B1 (5), 6-O-E-feruloyl ajugol (6), martynoside (7), aeginetic acid 5-O-β-D-quinovoside (8), aeginetoyl ajugol 5"-O-β-D-qunovoside (9), and rehmaglutinoside F (10) by spectroscopic analysis. Among them, compounds 7 and 9 demonstrated preventive effects against dexamethasone-induced skeletal muscle atrophy in C2C12 myotubes. Furthermore, the during the drying process of fresh R. glutinosa, the relative content ratio of compound 6 increased by 7.8 fold, while the levels of compounds 5, 6, 8, and 9 decreased by more than 50%.
Keywords:
Rehmannia glutinosa (Gaertn.) Libosch. ex Steud., Phenylethanoid glycosides, Iridoid glycosides, Skeletal muscle atrophy, Drying지황(Rehmannia glutinosa (Gaertn.) Libosch. ex Steud.)은 현삼과(Scrophulariaceae)에 속하는 여러해살이풀로, 뿌리를 생약으로 활용한다. 지황은 가공 상태에 따라 신선한 뿌리를 생지황 (Rehmanniae Radix Recens), 건조한 것을 건지황(대한약전명: 지황, Rehmanniae Radix), 쪄서 말린 것을 숙지황(Rehmanniae Radix Preparata)으로 구분하며, 각각의 성미와 효능이 다르다. 생지황의 맛(味)은 달고 쓰며(甘苦) 성질(性)은 차갑고(寒) 청열생진(淸熱生津), 양혈지혈(凉血止血)의 효능이 있다. 건지황은 달고 쓰며(甘苦) 성질이 서늘(涼)하여 청열양혈 (淸熱凉血), 자음생진 (滋陰生津)의 효능이 있다. 숙지황은 자음보혈 (滋陰補血), 익정진수 (益精嗔髓)의 효능이 있다.1-3) 지황의 주요 성분으로는 iridoid 계열의 catalpol, aucubin, ajugol 등과, 페놀성화합물인 forsythiaside와 acetoside 등, oligosaccharide인 stachyose, verbascose, raffinose 등이 분리 보고되었다.4-6) 또한, 항산화, 항알러지, 항염, 당뇨병, 신경변성질환 등에 효능이 있는 것으로 알려져 있다.4,7-10)
본 연구에서는 생지황과 건지황의 덱사메타손으로 유도된 골격근세포의 위축을 개선하는 효능을 평가하고, 생지황추출물에서 10종의 화합물을 분리 정제하여 구조를 동정하였다. 또한 생지황의 건조 과정에서 주요 성분의 상대 함량 변화를 분석한 결과를 보고하고자 한다.
재료 및 방법
실험재료 − 본 실험에 사용한 생지황(3 kg)과 건지황(500 g)은 2022년 9월 광명당제약에서 경상북도에서 재배된 것을 구매하여 실험에 사용하였다. 표본(생지황: HYUP-RG-001, 건지황: HYUP-RG-002)은 한양대학교 에리카캠퍼스 약학대학 생약학 실험실에 보관하였다.
시약 및 기기 − 추출 및 분획용 시약과 TLC 및 column용 시약은 대정화학 1급 용매를 사용하였다. Centrifugal partition chromatography (CPC)는 Spot prep II LC system이 결합된 SCPC-100+1000 (Armen Instrument, Saint-Avé, France)을 사용하였다. HPLC 분석은 Agilent 1260 HPLC system (Agilent Technologies, Palo Alto, CA, USA)을 사용하였으며, 분취용으로는 Gilson 321 HPLC pump와 Waters 2487 검출기를 이용하였고 분취용 HPLC 칼럼으로는 Cosmosil 5C18-PAQ (20 × 150 mm)을 사용하였다.
HPLC 분석 – 추출물과 그리고 CPC를 수행하여 얻은 12개의 소분획은 HPLC를 이용하여 분석을 진행하였다. HPLC는 Agilent 1260 HPLC system (Agilent Technologies, Palo Alto, CA, USA)을 사용하였다. 분석용 HPLC 칼럼으로는 Shiseido Capcell Pak C18 UG 120 (4.6 × 250 mm, 5 µm, Shiseido, Japan)을 사용하였으며, 이동상으로는 acetonitrile (0.1% formic acid, 이동상 A)와 water (0.1% formic acid, 이동상 B)의 혼합액을 기울기 용리하였다. 용매의 농도 구배는 0-5분(5% 이동상 A), 5-10분(5g15% 이동상 A), 10-30분(15g30% 이동상 A), 30-40분(30g100% 이동상 A)이었으며, 유속은 1.0 ml/min이고, UV 스펙트럼은 파장범위 210-400 nm에서, 크로마토그램은 280 nm에서 얻었다.
추출물 분획 및 분리 정제 − 생지황(1.5 kg)을 ethanol로 환류추출 방법으로 1시간씩 3회 추출하였다. 감압농축기와 동결건조기를 이용하여 용매를 제거하여 에탄올추출물 145 g을 얻었다. 에탄올추출물(144 g)을 증류수 1000 ml에 현탁하여 n-butanol로 3회 분획한 후 농축하여 n-butanol 분획물(17 g)과 물 분획물(126 g)을 얻었다. 이후, n-butanol 가용 분획(13 g)을 n-hexane-ethyl acetate-acetonitrile-water (1:1:1.5:1, v/v/v/v)로 이루어진 three-phase solvent system (4050 ml)을 이용하여 분획을 수행하여 upper phase에서 1 g, middle phase에서 5 g, 그리고 lower phase에서 7 g의 분획물을 얻었다. 각 분획을 분석용 HPLC를 실시하여 모니터링 하였으며, 덱사메타손으로 유도한 C2C12 세포주의 diameter 감소 개선 효능을 평가하였다.
CPC를 이용한 화합물이 분리 – 골격근 감소 개선 효능을 나타낸 lower phase 분획물(7 g)은 기울기 용리 CPC를 이용하여 소분획으로 나누었다. CPC는 기존의 본 연구실에서 개발한 기울기 용리 시스템을 이용하여 실행하였다.11) CPC의 로터(roter)를 500 rpm으로 회전하며 고정상인 n-hexane-acetonitrile-water (10:2:8, v/v/v)의 하층을 채웠고, 이후 950 rpm으로 회전하고 이동상을 10 ml/min으로 흘렸다. 이동상으로는 n-hexane-acetonitrile-water (10:2:8, v/v/v)의 상층(이동상 A)과 ethyl acetate-acetonitrile-water (10:2:8, v/v/v)의 상층(이동상 B), 그리고 water-saturated n-butanol-acetonitrile-water (10:2:8, v/v/v)의 상층(이동상 C)을 기울기 용리하였다. 이동상은 0-60분(100% 이동상 A), 60-145분(100% 이동상 Ag100% 이동상 B), 145-250분(100% 이동상 Bg100% 이동상 C), 그리고 250-360분(100% 이동상 C)로 기울기 용리하였고, 검출은 280과 320 nm의 파장에서 수행하였다. CPC 수행이 끝난 후 methanol 2000 ml을 흘려 CPC에 도입된 모든 샘플을 회수(6943.9 mg)하였다. 샘플은 7 g을 이동상 20 ml과 고정상 20 ml의 혼합액에 녹여 주입하였으며, CPC를 수행한 후 크로마토그램에 따라 12개의 소분획(Fr. A-Fr. K, R*)으로 나누었고, 회수율은 99%이상이었다. 이후 각 소분획을 분취용 HPLC를 수행하여 10개의 화합물을 분리 정제하였다. Fr. C에서 화합물 3(5.5 mg), Fr. D에서 화합물 8(1.2 mg), Fr. F에서 화합물 10(2.2 mg), Fr. G에서 화합물 7(8.4 mg), Fr. H에서 화합물 4(7.4 mg), 화합물 6(26.1 mg), 화합물 9(6.7 mg), Fr. I에서 화합물 5(6.0 mg), Fr 10에서 화합물 2(4.9 mg), 그리고 Fr. K에서 화합물 1(1.3 mg)을 각각 분리하였다.
화합물의 구조 동정 − 분리한 화합물의 구조 분석을 위해 Bruker model digital AVANCE Ⅲ 400 (Bruker, Germany)을 이용하여 NMR을 측정하였으며, Waters ZQ single quadrupole-mass spectrometer (Waters Corp., Milford, MA)를 이용하여 ESI-MS값을 얻었다.
Echinacoside (1): ESI-MS (m/z): 809.3 [M+Na]+, 785.5 [M-H]-; 1H-NMR (400 MHz, CD3OD) δ: 7.60 (1H, d, J=15.8 Hz, H-7′′′′), 7.06 (1H, d, J=2.0 Hz, H-2′′′′), 6.96 (1H, dd, J=8.2, 2.4 Hz, H-6′′′′), 6.78 (1H, dd, J=8.2 Hz, H-5′′′′), 6.72 (1H, d, J=2.0 Hz, 1H, H-2), 6.68 (1H, d, J=8.0, H-5), 6.58 (1H, dd, J=8.0, 2.0 Hz, H-6), 6.28 (d, J = 15.9 Hz, 1H, H-8′′′′), 5.18 (1H, d, J=1.7 Hz, 1H, H-1″), 4.38 (1H, d, J=7.9 Hz, H-1′), 4.26 (1H, d, J=7.7 Hz, 1H, H-1‴), 2.80 (2H, m, H-7), 1.06 (3H, d, J=6.2 Hz, H-6″).
Jionoside A1 (2): ESI-MS (m/z): 823.2 [M+Na]+, 799.4 [M-H]-; 1H-NMR (400 MHz, CD3OD) δ: 7.67 (1H, d, J=15.9 Hz, H-7′′′′), 7.21 (1H, d, J=1.8 Hz, H-2′′′′), 7.09 (1H, dd, J=8.2, 1.8 Hz, H-6′′′′), 6.82 (1H, d, J=8.2 Hz, H-5′′′′), 6.72 (1H, d, J=1.9 Hz, 1H, H-2), 6.68 (1H, d, J=8.0, H-5), 6.58 (1H, dd, J=8.0, 1.9 Hz, H-6), 6.38 (d, J=15.9 Hz, 1H, H-8′′′′), 5.19 (1H, d, J=1.5 Hz, 1H, H-1″), 4.99 (1H, m, H-4′), 4.39 (1H, d, J=7.9 Hz, H-1′), 4.26 (1H, d, J=7.6 Hz, 1H, H-1‴), 3.89 (3H, s, OCH3), 2.79(2H, t, J=7.4 Hz, H-7), 1.09 (3H, d, J=6.2 Hz, H-6″); 13C-NMR (100 MHz, CD3OD) δ: 168.4 (C-9′′′′), 150.9 (C-3′′′′), 149.2 (C-4′′′′), 147.8 (C-7′′′′), 146.1 (C-4), 144.7 (C-3), 131.6 (C-1), 127.7 (C-1′′′′), 124.4 (C-6′′′′), 121.3 (C-6), 117.2 (C-5), 116.3 (C-2), 115.7 (C-5′′′′), 115.1 (C-8′′′′), 111.9 (C-2′′′′) , 105.3 (C-1‴), 104.1 (C-1′), 103.0 (C-1″), 81.4 (C-3′), 76.7 (C-5‴), 76.1 (C-2′), 75.0 (C-5′), 74.8 (C-3‴), 73.8 (C-4″), 72.6 (C-2‴), 72.4 (C-3″), 72.4 (C-8), 72.2 (C-2″), 70.4 (C-4′), 70.3 (C-4‴), 70.0 (C-5″), 69.2 (C-6′), 62.5 (C-6‴), 56.5 (OCH3), 36.5 (C-7), 18.4 (C-6″).
Ferulic acid (3): ESI-MS (m/z): 193.3 [M-H]-; 1H-NMR (400 MHz, CD3OD) δ: 7.57 (1H, d, J=15.9 Hz, H-7), 7.18 (1H, d, J = 2.0 Hz, H-2), 7.06 (1H, dd, J=8.2, 2.0 Hz, H-6), 6.81 (1H, d, J=8.2 Hz, H-5), 6.32 (1H, d, J=15.9 Hz, H-8), 3.91 (3H, s, OCH3).
Verbascoside (4): ESI-MS (m/z): 647.1 [M+Na]+, 623.3 [M-H]-; 1H-NMR (400 MHz, CD3OD) δ: 7.59 (1H, d, J=15.9, H-7‴), 7.05 (1H, d, J=2.0 Hz, H-2‴), 6.96 (1H, dd, J=8.2, 2.0 Hz, H-6‴), 6.78 (1H, d, J=8.2 Hz, H-5‴), 6.70 (1H, d, J=2.0 Hz, H-2), 6.68 (1H, J=8.0 Hz, H-5), 6.57 (1H, dd, J=8.0, 2.0, H-6), 6.27 (1H, d, J=15.9, H-8‴), 5.19 (1H, d, J=1.3, H-1″), 4.38 (1H, d, J=7.9 Hz, H-1′), 2.80 (2H, brt, J=7.3 Hz, H-7), 1.09 (3H, d, J=6.2, H-6″); 13C-NMR (100 MHz, CD3OD) δ: 168.0 (C-9‴), 149.7 (C-4‴), 148.0 (C-7‴), 146.8 (C-3‴), 146.1 (C-3), 144.6 (C-4), 131.5 (C-1), 127.6 (C-1‴), 123.1 (C-6‴), 121.2 (C-6), 117.1 (C-2), 116.5 (C-5‴), 116.3 (C-5), 115.2 (C-2‴), 114.7 (C-8‴), 104.2 (C-1′), 103.0 (C-1″), 81.6 (C-3′), 76.2 (C-2′), 76.0 (C-5′), 73.8 (C-4″), 72.3 (C-2″), 72.2 (C-8), 72.0 (C-5″), 70.6 (C-4′), 70.4 (C-3″), 62.3 (C-6′), 36.5 (C-7), 18.4 (C-6″).
Jiononoside B1 (5): ESI-MS (m/z): 837.3 [M+Na]+, 813.4 [M-H]-; 1H-NMR (400 MHz, CD3OD) δ: 7.67 (1H, d, J=15.9 Hz, H-7′′′′), 7.21 (1H, d, J=1.8 Hz, H-2′′′′), 7.09 (1H, dd, J=8.1, 1.8 Hz, H-6′′′′), 6.83 (1H, d, J=8.2 Hz, H-5), 6.81 (1H, d, J=8.1 Hz, H-5′′′′), 6.76 (1H, d, J=1.9 Hz, 1H, H-2), 6.70 (1H, dd, J=8.2, 1.9 Hz, H-6), 6.38 (d, J=15.9 Hz, 1H, H-8′′′′), 5.20 (1H, d, J=1.8 Hz, 1H, H-1″), 4.99 (1H, t, J=9.7 Hz, H-4′), 4.39 (1H, d, J=7.9 Hz, H-1′), 4.27 (1H, d, J=7.6 Hz, 1H, H-1‴), 3.89 (3H, s, OCH3), 3.82 (3H, s, OCH3), 2.83( 2H, t, J=7.3 Hz, H-7), 1.09 (3H, d, J=6.2 Hz, H-6″); 13C-NMR (100 MHz, CD3OD) δ: 168.4 (C-9′′′′), 150.9 (C-3′′′′), 149.4 (C-4′′′′), 148.1 (C-7′′′′), 147.6 (C-3), 147.4 (C-4), 133.0 (C-1), 127.7 (C-1′′′′), 124.4 (C-6′′′′), 121.2 (C-6), 117.1 (C-5), 116.5 (C-5′′′′), 115.1 (C-8′′′′), 112.9 (C-2), 111.8 (C-2′′′′), 105.3 (C-1‴), 104.2 (C-1′), 103.3 (C-1″), 81.5 (C-3′), 76.7 (C-5‴), 76.2 (C-2′), 75.0 (C-5′), 74.8 (C-3‴), 73.8 (C-4″), 72.6 (C-2‴), 72.4 (C-3″), 72.2 (C-8), 72.1 (C-2″), 70.5 (C-4′), 70.4 (C-4‴), 70.3 (C-5″), 69.2 (C-6′), 62.5 (C-6‴), 56.5 (OCH3), 36.5 (C-7), 18.4 (C-6″).
6-O-E-Feruloyl ajugol (6): ESI-MS (m/z): 547.1 [M+Na]+, 523.4 [M-H]-; 1H-NMR (400 MHz, CD3OD) δ: 7.63 (1H, d, J=15.9 Hz, H-7″), 7.19 (1H, d, J=2.0 Hz, H-2″), 7.07 (1H, dd, J=8.2, 1.9 Hz, H-6″), 6.81 (1H, d, J=8.2 Hz, H-5″), 6.39 (1H, d, J=15.9 Hz, 1H,H-8″), 6.22 (1H, dd, J=6.3, 2.2 Hz, H-3), 5.50 (1H, d, J=2.5 Hz, H-1), 4.98 (1H, dd, J=6.3, 2.6 Hz, H-4), 4.93 (1H, m, H-6), 4.67 (1H, d, J=7.9 Hz, H-1′), 3.91 (1H, dd, J=11.8, 1.8, H-6′a), 3.89 (3H, s, OCH3), 3.67 (1H, dd, J=11.8, 5.6 Hz, H-6′b), 3.39 (1H, d, J=11.8, 5.6 Hz, H-3′), 2.93 (1H, dd, J =9.2, 2.1 Hz, H-5), 2.58 (1H, dd, J=9.2, 2.2 Hz, H-9), 2.24 (1H, dd, J=14.2, 6.4 Hz, H-7a), 2.00 (1H, dd, J=14.2, 3.9 Hz, H-7b), 1.39 (3H, s, H-10); 13C-NMR (100 MHz, CD3OD) δ: 169.0 (C-9″), 150.6 (C-3″), 149.4 (C-4″), 146.9 (C-7″), 141.1 (C-3), 127.7 (C-1″), 124.1 (C-6″), 116.5 (C-5″), 115.7 (C-8″), 111.7 (C-2″), 104.6 (C-4), 99.4 (C-1′), 80.3 (C-6), 79.1 (C-8), 78.2 (C-3′), 78.0 (C-5′), 74.8 (C-2′), 71.7 (C-4′), 62.9 (C-6′), 56.4 (OCH3), 51.6 (C-9), 47.9 (C-7), 39.4 (C-5), 26.1 (C-10).
Martynoside (7): ESI-MS (m/z): 653.3 [M+H]+, 651.4 [M-H]-; 1H-NMR (400 MHz, CD3OD) δ: 7.66 (1H, d, J=15.9 Hz, H-7‴), 7.20 (1H, d, J=2.0 Hz, H-2‴), 7.09 (1H, dd, J=8.3, 1.8 Hz, H-6‴), 6.83 (1H, d, J=8.2 Hz, H-5‴), 6.81 (1H, d, J=8.2 Hz, H-5), 6.74 (1H, d, J=2.1 Hz, H-2), 6.69 (1H, dd, J=8.1, 2.1 Hz, H-6), 6.38 (1H, d, J=15.9 Hz,H-8‴), 5.20 (1H, d, J =1.7 Hz,H-1″), 4.92 (1H, t, J=9.4, H-4′), 4.38 (1H, d, J=7.9 Hz,H-1′), 3.89 (3H, s, OCH3), 3.82 (3H, s, OCH3), 2.83 (2H, brt, J=6.6 Hz, H-7), 1.10 (3H, d, J=6.2 Hz, H-6″); 13C-NMR (100 MHz, CD3OD) δ: 168.2 (C-9‴), 150.8 (C-4‴), 149.3 (C-3‴), 147.9 (C-7‴), 147.5 (C-3), 147.4 (C-4), 132.8 (C-1), 127.7 (C-1‴), 124.3 (C-6‴), 121.1 (C-6), 117.1 (C-5), 116.5 (C-5‴), 115.1 (C-8‴), 112.9 (C-2), 111.8 (C-2‴), 104.2 (C-1′), 103.0 (C-1″), 81.5 (C-3′), 76.2 (C-2′), 76.1 (C-5′), 73.8 (C-4″), 72.4 (C-2″), 72.1 (C-8), 72.1 (C-3″), 70.6 (C-4′), 70.4 (C-5″), 62.4 (C-6′), 56.4 (OCH3), 36.6 (C-7), 18.4 (C-6″).
Aeginetic acid 5-O-β-D-quinovoside (8): ESI-MS (m/z): 437.2 [M+Na]+, 413.3 [M-H]-; 1H-NMR (400 MHz, CD3OD) δ: 6.80 (1H, d, J=16.2 Hz, H-7), 6.37 (1H, d, J=16.2 Hz, H-8), 5.78 (1H, brs, H-10), 4.72 (1H, d, J = 7.6 Hz, H-1′), 3.00 (1H, t, J = 9.1 Hz, H-5′), 2.28 (3H, d, J=0.6, H-12), 2.09 (3H, s, H-12), 1.62 (1H, m, H-2a), 1.27 (1H, m, H-2b), 1.22 (3H, d, J=6.1 Hz, H-6′), 1.20 (3H, s, H-13), 1.15 (3H, s, H-15), 0.82 (3H, s, H-14); 13C-NMR (100 MHz, CD3OD) δ: 170.9 (C-11), 154.4 (C-9), 140.3 (C-7), 133.8 (C-8), 119.2 (C-10), 98.0 (C-1′), 83.62 (C-5), 80.3 (C-6), 78.8 (C-3′), 77.1 (C-5′), 75.8 (C-2′), 72.6 (C-4′), 39.9 (C-1), 37.1 (C-2), 32.9 (C-4), 27.6 (C-14), 25.9 (C-13), 21.9 (C-15), 18.7 (C-3), 18.4 (C-6′), 14.4 (C-12).
Aeginetoyl ajugol 5"-O-β-D-quinovoside (9): ESI-MS (m/z): 767.3 [M+Na]+, 743.5 [M-H]-; 1H-NMR (400 MHz, CD3OD) δ: 6.84 (1H, d, J=16.2 Hz, H-7″), 6.37 (1H, d, J=16.2 Hz, H-8″), 6.20 (1H, dd, J=6.3, 2.1 Hz, H-3), 5.82 (1H, s, H-10″), 5.48 (1H, d, J=2.4 Hz, H-1), 4.97 (1H, dd, J=6.3, 2.7 Hz, H-4), 4.66 (1H, d, J=7.9 Hz, H-1′), 4.42 (1H, d, J=7.6 Hz, H-1‴), 3.00 (1H, t, J=9.0, H-5‴), 2.88 (1H, d, J=9.2, H-5), 2.54 (1H, d, J=9.6, H-9), 2.31 (3H, d, J=0.8, H-12″), 2.21 (1H, dd, J=14.2, 6.4, H-7b), 1.95 (1H, dd, J=14.2, 3.3, H-7b), 1.37 (3H, s, H-10), 1.22 (3H, d, J=6.1, H-6‴), 1.19 (3H, s, H-13″), 1.14 (3H, s, H-15″), 0.81 (3H, s, H-14″); 13C-NMR (100 MHz, CD3OD) δ: 168.7 (C-11″), 154.7 (C-9″), 141.3 (C-7″), 140.9 (C-3), 133.6 (C-8″), 118.7 (C-10″), 104.8 (C-4), 99.4 (C-1′), 98.0 (C-1‴), 93.4 (C-1), 83.6 (C-5″), 80.4 (C-6″), 79.7 (C-6), 79.1 (C-8), 78.8 (C-3‴), 78.2 (C-5′), 78.0 (C-3′), 77.0 (C-5‴), 75.8 (C-2‴), 74.8 (C-2′), 72.6 (C-4‴), 71.7 (C-4′),62.9 (C-6′), 51.6 (C-9), 48.0 (C-7), 39.9 (C-1″), 39.3 (C-5), 37.1 (C-2″), 32.9 (C-4″), 27.6 (C-14″), 26.0 (C-10), 25.9 (C-13″), 21.9 (C-15″), 18.7 (C-3″), 18.5 (C-6‴), 14.5 (C-12″).
Rehmaglutoside F (10): ESI-MS (m/z): 621.2 [M+Na]+, 597.4 [M-H]-; 1H-NMR (400 MHz, CD3OD) δ: 6.73 (1H, d, J=16.3 Hz, H-7″), 6.42 (1H, d, J=16.3 Hz, H-8″), 6.21 (1H, dd, J=6.3, 2.3, H-3), 5.83 (1H, s, H-10″), 5.49 (1H, d, J=2.5, H-1), 4.66 (1H, d, J=7.9, H-1′), 2.33 (3H, d, J=1.1, H-12″), 1.37 (3H, s, H-10), 1.21 (3H, s, H-13″), 1.07 (3H, s, H-15″), 0.80 (3H, s, H-14″); 13C-NMR (100 MHz, CD3OD) δ: 168.6 (C-11″), 154.2 (C-9″), 141.0 (C-3), 140.4 (C-7″), 134.2 (C-8″), 119.1 (C-10″), 104.7 (C-4), 99.4 (C-1′), 93.4 (C-1), 80.7 (C-6″), 79.7 (C-6), 79.1 (C-8), 78.3 (C-3′), 78.0 (C-5′), 74.8 (C-2′), 71.7 (C-4′), 62.9 (C-6′), 51.6 (C-9), 48.0 (C-7), 39.7 (C-1″), 39.3 (C-5), 37.4 (C-2″), 36.7 (C-4″), 27.5 (C-14″), 27.4 (C-15″), 26.0 (C-10), 25.7 (C-13″), 18.9 (C-3″), 14.4 (C-12″).
C2C12 세포 배양 및 분화 유도 − 실험에서 사용된 C2C12 (mouse myoblast cell line)은 ATCC로부터 분양 받아 10% fetal bovine serum (Welgene, Gyeongsan, South Korea)과 1% penicillin/streptomycin (PS, Invitrogen Co., NY, USA)이 함유된 Dulbecco’s modified eagle’s medium (DMEM, Hyclone, UT, USA) 배지를 사용하여 37°C, 5% CO2 incubator에서 2일에 한 번씩 계대 배양하였다. 분화 유도를 위하여 C2C12 세포를 12 well plate에는 5 x 104 cells/well 분주하고, 2일 뒤 새로운 배지로 교환한 후, confluent 상태에 도달하면 2% horse serum (Welgene, Gyeongsan, South Korea), 1% PS가 함유된 DMEM 배지(분화배지)를 사용하여 매 2일마다 교체하여 6일동안 분화를 진행하였다. 분화된 C2C12 myotube에 10 μM의 덱사메타손을 처리하여 근 위축을 유도하고, 추출물(30 mg/ml), 분획물(표시한 농도) 및 화합물 1-10 (30 μM)을 24 시간 처리하여 결과를 확인하였다.
Myosin heavy chain (MHC)과 핵(nuclei) 염색 및 diameter 측정 – C2C12 myotube는 PBS로 2번 세척한 후 4% paraformaldehyde로 15분 동안 고정하였다. 고정된 세포에 0.5% Trion X-100로 15분 간 반응시키고, 1% BSA 용액에서 1시간 반응시킨 후 MHC 항체(1:100, Santa Cruz, TX, USA)와 함께 4°C에서 하룻밤 반응하였다. 0.1% Triton X-100이 포함된 1×PBS (PBS-T)를 이용하여 3번 세척한 후, 세포들은 Alexa Fluor 488 goat anti-rabbit IgG(1:500, Invitrogen, MA, USA)로 37°C에서 1시간 동안 반응시켰다. 0.1% PBS-T로 3번 세척한 후, 핵은 10 µM의 Hoechst 33342 (Sigma-Aldrich, MO, USA) 염색하였다. 염색된 C2C12 myotube는 형광현미경(JuLITM stage)을 사용하여 관찰하고 사진을 촬영하였다. C2C12 myotube의 직경(diameter), MHC 양성 면적 및 융합 지수(fusion index) 측정을 위하여 ImageJ 소프트웨어를 사용하였다.
생지황의 건조 과정에서 주요성분의 상대 함량 비교 – 생지황을 40℃에서 20 시간, 30 시간 및 45 시간 동안 건조한 후, 에탄올로 추출하여 농축하였다. 각 추출물을 10 mg/ml의 농도로 메탄올에 녹여 HPLC로 분석하고, 화합물의 상대 함량 변화를 각 peak의 면적비를 통하여 계산하여 비교하였다.
Peak의 상대 함량비(%) = (각 peak의 면적) / (각 peak 면적의 합) × 100%
통계처리 − 통계적 유의성은 SigmaPlot 12.1 (Systat Software Inc, San Jose, CA, USA) Student's t-test 사용하여 통계적 유의성을 평가하였으며, 3번의 독립적인 실험에 대한 평균 ± 표준편차에 대하여 *p < 0.05, ***p < 0.01 및 ***p < 0.001을 통계적으로 유의한 것으로 간주하였다.
결과 및 고찰
생지황과 건지황을 구입하여 골격근 감소 개선 효능을 C2C12 myotube에서 비교한 결과, 생지황 추출물이 더 우수한 효능을 나타냄을 확인하였으며, HPLC 분석을 통하여 생지황(FR)과 건지황(DR)에서 주요 화합물의 함량 변화도 확인하였다(Fig. 1). 이 결과를 바탕으로 생지황을 선정하여 에탄올로 추출한 뒤, 용매 분획과 CPC 및 prep-HPLC를 순차적으로 진행하여 활성 화합물을 분리 정제하였다. 먼저, 물과 n-butanol을 이용하여 용매 분획을 진행하였으며, n-butanol 분획물을 다시 n-hexane-ethyl acetate-acetonitrile-water (1:1:1.5:1, v/v/v/v)로 이루어진 three-phase solvent system을 사용하여 추가 분획을 실시하였다. 이 과정에서 가장 하층(lower layer)에서 활성을 확인하였고, 이를 gradient CPC를 이용하여 12개의 분획(A-K, Residue)을 얻었다(Fig. 2). CPC를 통해 획득한 소분획을 수율비(obtained weight ratios)에 따라 C2C12 세포에 처리하여 활성을 확인한 결과, 여러 개의 분획에서 활성이 나타남을 확인하여 각 소분획을 prep-HPLC로 분리 정제하여 10개의 화합물(1-10)을 얻었다. 화합물의 구조는 1H-NMR, 13C-NMR과 ESI-MS data를 문헌치와 비교하여 echinacoside (1),12) jionoside A1 (2),13) ferulic acid (3),14) verbascoside (4),15) jinoside B1 (5)13), 6-O-E-feruloyl ajugol (6),16) martynoside (7),17) aeginetic acid 5-O-β-D-quinovoside (8),18) aeginetoyl ajugol 5"-O-β-D-qunovoside (9)18) 및 rehmaglutinoside F (10)19)로 동정하였다(Fig. 3).
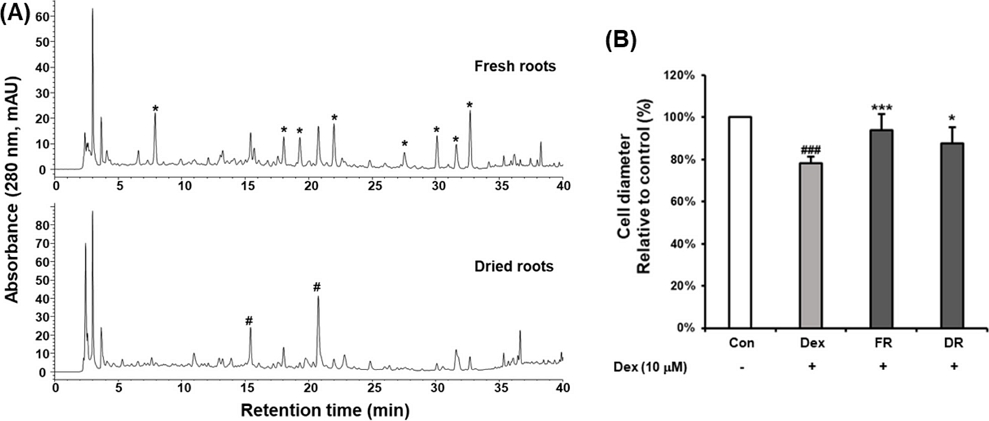
HPLC chromatograms of fresh and dried roots of R. glutinosa and their effects on myotube diameters in dexamethasone (Dex)-treated C2C12 myotubes. (A) HPLC chromatograms of fresh roots and dried roots. Each extract was dissolved in methanol at 10 mg/ml, injected 10 μl into HPLC, and monitored at 280 nm. *, decreased peaks of fresh roots compared with dried roots, #, increased peaks in dried roots compared with fresh roots. (B) Effects of fresh roots (FR) and dried roots (DR) extracts on Dex-induced atrophy in C2C12 myotubes. C2C12 myotubes were treated with 10 μM Dex in the presence or absence of 30 μg/ml of FR or DR for 24 h. The values were presented as percentages of the control. These results are presented as means ± SD of three independent experiments. ###p < 0.05 vs. control; *p < 0.05, ***p < 0.001 vs. Dex.
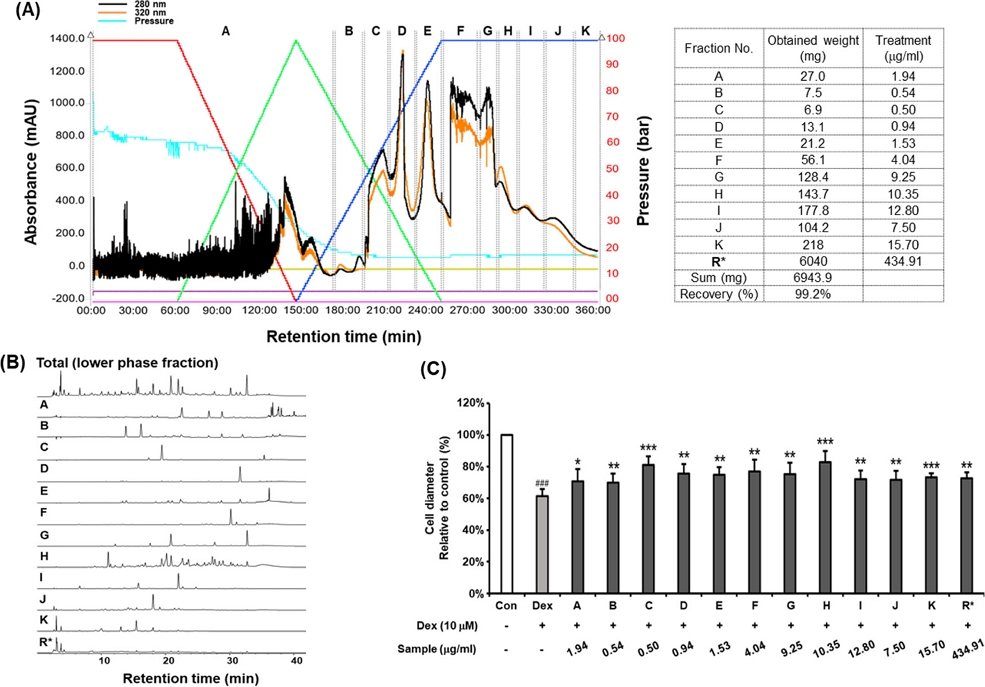
Activity-guided isolation process of fresh roots of R. glutinosa. (A) CPC chromatogram of lower phase fraction (7 g) in the three phases consisted of n-hexane-ethyl acetate-acetonitrile-water (1:1:1.5:1, v/v/v/v). Monitored at 280 nm and 320 nm. Stationary phase: lower aqueous phase of n-hexane-acetonitrile-water (10:2:8, v/v/v); flow rate: 10 mL/min; rotation speed: 950 rpm; ascending mode. (B) HPLC chromatograms of sub-fractions obtained by gradient CPC. (C) Effects of obtained sub-fractions on Dex-induced atrophy in C2C12 myotubes. C2C12 myotubes were treated with 10 μM Dex in the presence or absence of assigned weight ratio (based on 500 μg/ml of lower phase fraction) for 24 h. The values were presented as percentages of the control. These results are presented as means ± SD of three independent experiments. ###p < 0.05 vs. control; *p < 0.05, **p < 0.01, ***p < 0.001 vs. Dex.
분리 정제한 화합물(1-10)을 덱사메타손으로 유도한 C2C12 세포에서 근 위축에 대한 개선 효능을 평가하였다. 분화된 C2C12 myotube에 10 μM의 덱사메타손을 처리하여 근 위축을 유도하고, 화합물(1-10)을 30 μM의 농도로 24 시간 처리하여 근 위축을 보호하는 효능을 평가하였다(Fig. 4). 덱사메타손 처리로 인하여 C2C12 myotube의 MHC 염색 영역은 19.5%, 세포 직경(myotube diameter)은 18.2%, fusion index는 9.7% 감소하였다. 그러나 분리한 화합물을 처리하였을 때, MHC 염색 영역은 화합물 7과 9에서 효과가 나타났으며, 세포의 직경(diameter)은 화합물 1, 2와 6-10에서 활성이 나타났다. Fusion index는 화합물 2와 9가 증가시킴을 확인할 수 있었다. 특히, 화합물 9 (aeginetoyl 5"-O-β-D-qunovoside)가 가장 효과가 좋은 것으로 나타났다. 화합물 9를 처리했을 때, 덱사메타손 처리군에 비해 MHC 염색 영역은 9.1%, 세포의 직경은 27.7%, fusion index는 36.9% 증가하였다. 두번째로 활성이 우수했던 화합물 7을 처리하였을 때는, 덱사메타손 처리군 대비 MHC 염색 영역은 8.2%, 세포 직경(myotube diameter)은 39.2%, fusion index는 2.5% 증가하였다. 이러한 결과는 덱사메타손으로 유도한 골격근 감소를 개선하는 주요 유효 성분이 화합물 9와 7임을 보여주었다.
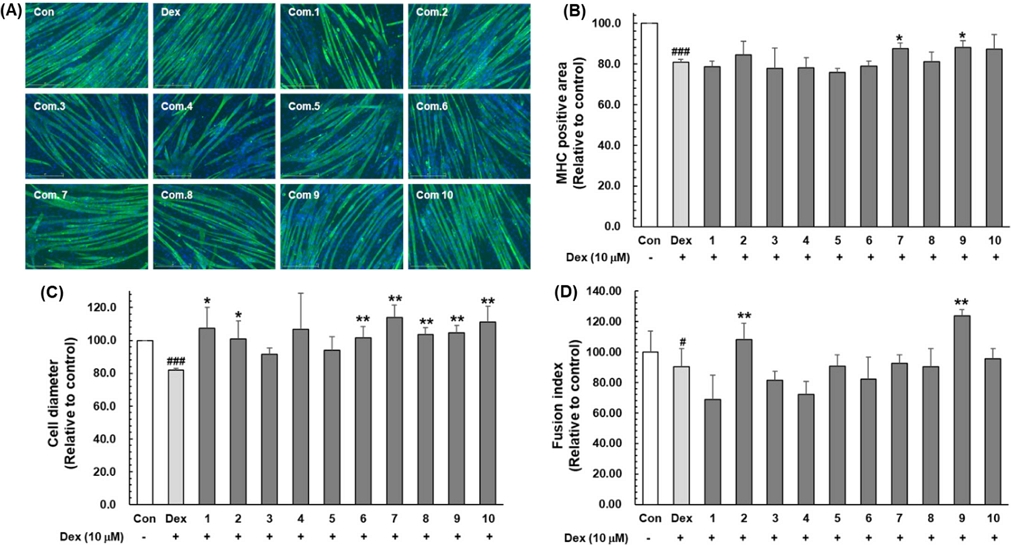
Effects of compounds 1-10 on Dex-induced atrophy in C2C12 myotubes. (A) C2C12 myotubes were stained with MHC (green) and DAPI (blue), and representative photographs were observed under a fluorescent microscope. (B) Relative changes in MHC-stained area in myotubes, (C) diameters, and (D) fusion index were measured from randomly selected fields and quantified using the ImageJ program. Data are presented as the means ± standard deviation (n = 3). #p < 0.05, ###p < 0.001 vs. control, *p<0.05, **p<0.01, vs. Dex.
이후, 생지황과 건지황의 골격근 감소 개선 효능에 차이가 있으며, 생지황과 건지황의 주요 성분의 peak의 면적 차이가 나타남을 확인하였다(Fig. 1A). 이를 기반으로, 생지황을 40℃에서 건조하며, 시간 별로 각 peak의 면적 비율의 변화를 분석하였다. 대부분의 peak가 나타나는 280 nm의 주요 peak (peaks: a, 1, 2, 4, 5, 6, 7, 8, 9)의 합을 100%로 설정하고, 건조 시간에 따른 각 peak의 상대적인 비율을 계산하였다(Fig. 5A). 분석 결과, 생지황 추출물에서는 peak a (unidentified)가 32.5%로 가장 많은 비율을 차지하였으나, 20 시간 건조한 후 분석하였을 때는 peak 4 (verbascoside)가 44.9%로 가장 큰 비율을 나타내었다(Fig. 5B). 45시간 건조 후 생지황(0 시간)과의 peak 면적비를 비교한 결과, peak a, 5, 6, 8과 9는 50% 이상 감소하였으며, peak 1과 2의 비율은 30% 이하로 감소하였다. 특히, Peak 4는 건조 시간이 증가함에 따라 비율이 지속적으로 증가하여, 45시간 후에는 생지황 대비 함량 비율이 7.8 배 증가하였다(Fig. 5C).
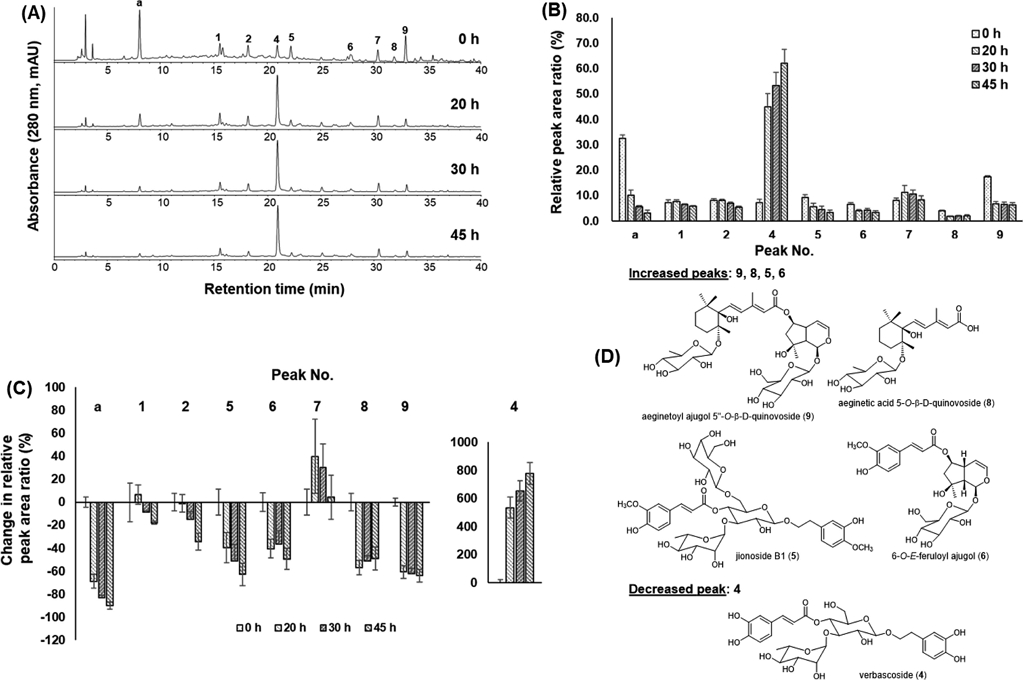
Comparison of the relative content of the main ingredients during the drying process. (A) HPLC chromatograms of R. glutinosa during drying (0 h, 20 h, 30 h, and 45 h) at 40℃. Peak a: unidentified, peak1: echinacoside (1), peak 2: jionoside A1 (2), peak 4: verbascoside (4), peak 5: jinoside B1 (5), peak 6: 6-O-E-feruloyl ajugol (6), peak 7: martynoside (7), peak 8: aeginetic acid 5-O-β-D-quinovoside (8), and peak 9: aeginetoyl ajugol 5"-O-β-D-qunovoside (9). (B) The relative peak area ratio (%) of each peak. Peak area ratio was calculated as [(individual peak area) / (sum of all peak area)] × 100 (%). (C) Changes in the relative peak ratio (%). (D) Chemical structures of increased peaks (9, 8, 5 and 6) and decreased peak (4).
결 론
생지황에서 3상 용매 분획, 기울기 용리 CPC, 그리고 prep-HPLC를 이용하여 총 10종의 화합물을 분리 정제하였다. 분리한 화합물은 분광학적 방법을 이용하여 echinacoside (1), jionoside A1 (2), ferulic acid (3), verbascoside (4), jinoside B1 (5), 6-O-E-feruloyl ajugol (6), martynoside (7), aeginetic acid 5-O-β-D-quinovoside (8), aeginetoyl ajugol 5"-O-β-D-qunovoside (9) 및 rehmaglutinoside F (10)로 그 구조를 동정하였다. 분리 정제한 화합물을 덱사메타손으로 유도한 근육세포의 위축을 개선하는 효능을 평가한 결과, martynoside (7)과 aeginetoyl 5"-O-β-D-qunovoside (9)이 가장 뛰어난 활성을 나타냄을 확인하였다. 또한, 생지황을 40℃에서 건조하며 주요 peak의 함량 비율 변화를 확인한 결과, iridoid 계열의 화합물인 9와 6, 그리고 화합물 8과 5의 함량은 감소한 반면, verbascoside (4)의 함량은 증가하였다. 이는 생지황을 건조하는 과정에서 주요 화합물의 함량 변화를 확인할 수 있으며, 향후 건조 온도와 시간에 따라 지황의 화합물 변화에 대한 연구가 더 진행되어야 한다.
Acknowledgments
본 연구는 한국연구재단의 기본연구(RS-2023-00251177), 창의도전연구기반지원사업(RS-2023-00245441)과 대학중점연구소지원사업(NRF-2020R1A6A1A03042854)의 연구비 지원을 통하여 수행되었습니다.
References
- 정보섭, 신민교(2003) 향약(생약)대사전, pp906-909. 도서출판영림사, 서울.
- 식품의약품안전처 대한민국약전 12개정판, 의약품각조 제2부.
- 식품의약품안전처 대한민국약전외한약(생약)규격집, 의약품각조 제1부.
-
Zhang, R. X., Li, M. X. and Jia, Z. P. (2008) Rehmannia glutinosa: Review of botany, chemistry, and pharmacology. J. Ethnopharmacol. 117: 199-214.
[https://doi.org/10.1016/j.jep.2008.02.018]

- Won, T. H., Ryu, S. K., Kang, S. S. and Shin, J. H. (2010) Simultaneous analysis of bioactive metabolites from Rehmannia glutinosa by HPLC-DAD-MS/MS. Nat. Prod. Sci. 16: 116-122.
-
Liang, Q., Ma, J., Ma, Z., Wang, Y., Tan, H., Xiao, C., Liu, M., Lu, B., Zhang, B. and Gao, Y. (2013) Chemical comparison of dried Rehmannia root and prepared Rehmannia root by UPLC-TOF MS and HPLC-ELSD with multivariate statistical analysis. Acta Pharm. Sin. B 3: 55-64.
[https://doi.org/10.1016/j.apsb.2012.11.001]

-
Jiang, B., Liu, J. H., Bao, Y. M. and An, L. J. (2004) Catalpol inhibits apoptosis in hydrogen peroxide-induced PC12 cells by preventing cytochrome c release and inactivating caspase cascade. Toxicon. 43: 53-59.
[https://doi.org/10.1016/j.toxicon.2003.10.017]

-
Waisundara, V. Y., Huang, M., Hsu, A., Huang, D. and Tan, B. K. H. (2008) Characterization of the anti-diabetic and antioxidant effects of Rehmannia glutinosa in streptozotocin-induced diabetic Wistar rats. American J. Chi. Med. 36: 1083-1104.
[https://doi.org/10.1142/S0192415X08006594]

-
Kim, H., Lee, E., Lee, S., Shin, T., Kim, Y. and Kim, J. (1998) Effect of Rehmannia glutinosa on immediate type allergic reaction. Int. J. Immunopharmacol. 20: 231-240.
[https://doi.org/10.1016/S0192-0561(98)00037-X]

-
Sung, Y. Y., Yoon, T., Jang, J. Y., Park, S. J. and Kim, H. K. (2011) Topical application of Rehmannia glutinosa extract inhibits mite allergen-induced atopic dermatitis in NC/Nga mice. J. Ethnopharmacol. 134: 37-44.
[https://doi.org/10.1016/j.jep.2010.11.050]

-
Kim, J. H., Jung, E. J., Lee, Y. J., Kim, C. Y. and Jeon, J. S. (2021) Application of linear gradient solvent system in centrifugal partition chromatography facilitating bioassay-guided fractionation of Yongdamsagan-Tang, traditional oriental decoction. Evid. Based Complement. Alternat. Med. 2021: 6624532.
[https://doi.org/10.1155/2021/7552169]

-
Becker, H., Hsieh, W. C., Wylde, R., Laffite, C. and Andary, C. (1982) Structure of echinacoside. Z. Naturforsch. C 37: 351-353.
[https://doi.org/10.1515/znc-1982-5-601]

-
Sasaki, H., Nishimura, H., Chin, M. and Mitsuhashi, H. (1989) Hydroxycinnamic acid esters of phenethylalcohol glycosides from Rehmannia glutinosa var. purpurea. Phytochemistry 28: 875-879.
[https://doi.org/10.1016/0031-9422(89)80134-7]

-
Liu, H., Gong, C., Liao, Z., Chen, T. and Li, Y. (2017) Isolation and purification of three analogues from Clematis akebioides by molecularly imprinted solid-phase extraction and HSCCC. Chromatographia 80: 1651-1658.
[https://doi.org/10.1007/s10337-017-3406-z]

-
Gómez-Aguirre, Y. A., Zamilpa, A., González-Cortazar, M. and Trejo-Tapia, G. (2012) Adventitious root cultures of Castilleja tenuiflora Benth. as a source of phenylethanoid glycosides. Ind. Crop. Prod. 36: 188-194.
[https://doi.org/10.1016/j.indcrop.2011.09.005]

-
Nishimura, H., Sasaki, H., Morota, T., Chin, M. and Mitsuhashi, H. (1989) Six iridoid glycosides from Rehmannia glutinosa. Phytochemistry 28: 2705-2709.
[https://doi.org/10.1016/S0031-9422(00)98072-5]

-
Calis, I., Lahloub, M. F., Rogenmoser, E. and Sticher, O. (1984) Isomartynoside, a phenylpropanoid glycoside from Galeopsis pubescens. Phytochemistry 23: 2313-2315.
[https://doi.org/10.1016/S0031-9422(00)80542-7]

-
Lee, S. Y., Kim, J. S., Choi, R. J., Kim, Y. S., Lee, J. H. and Kang, S. S. (2011). A new polyoxygenated triterpene and two new aeginetic acid quinovosides from the roots of Rehmannia glutinosa. Chem. Pharm. Bull. 59: 742-746.
[https://doi.org/10.1248/cpb.59.742]

-
Liu, Y. F., Liang, D., Luo, H., Hao, Z. Y., Wang, Y., Zhang, C. L., Zhang, Q. J., Chen, R. Y. and Yu, D. Q. (2012) Hepatoprotective iridoid glycosides from the roots of Rehmannia glutinosa. J. Nat. Prod. 75: 1625-1631.
[https://doi.org/10.1021/np300509z]