섬바디 줄기의 성분
Abstract
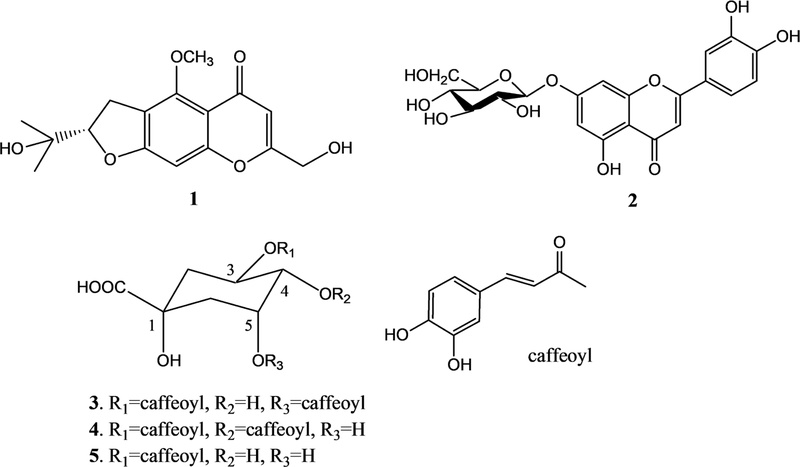
Five phenolic compounds were isolated from the stem of Dystaenia takeshimana. The structures of the isolated compounds were determined based on various spectroscopic analyses and identified as cimifugin (1), cynaroside (2), 3,5-dicaffeoylquinic acid (3), 3,4-dicaffeoylquinic acid (4), and chlorogenic acid (5). Among these, cimifugin (1), 3,5-dicaffeoylquinic acid (3), 3,4-dicaffeoylquinic acid (4), and chlorogenic acid (5) were isolated from this plant for the first time.
Keywords:
Dystaenia takeshimana, Stem, Quinic aicd derivatives, Flavonoid glycosdie, Chromone섬바디(Dystaenia takeshimana)는 산형과(Umbelliferae)에 속하는 다년초로 울릉도에 분포하고 줄기는 크고 윗부분에서 가지가 갈라지며 4 ~ 5개의 마디가 있고 높이 2m에 달한다. 잎은 호생하고 2회 우상복엽이며 엽병은 위로 갈수록 짧아지고 밑부분이 넓어져서 줄기를 감싸며 윗부분의 잎은 퇴화하여 엽병이 엽초로 된다. 열편은 간혹 2 ~ 3개로 깊이 갈라지고 정우편(頂羽片)은 넓은 피침형으로 가장 길며 가장자리에 결각상의 겹톱니가 있다. 꽃은 7월에 백색으로 피고 줄기와 가지 끝에 복산형화서로 달린다. 소산경이 많고 총포는 거의 없으며 소총포는 10 ~ 20개로 선형이다. 과실은 분과로 타원형이다.1) 뿌리는 울릉강활이라 하여 강활과 같은 용도로 사용하기도 한다.2) 이 식물의 성분연구로는 권 등3)이 뿌리로부터 psoralen, xanthotoxin, dimethylsuberosin 등의 coumarin 계열의 화합물을 분리, 보고하였고, 김 등은4) 뿌리에서 umbelliferone, skimmin, isoscopoletin, 및 phytosterol 혼합물을 분리하여 이를 보고하였다. 또한 김 등5)은 뿌리로부터 선행 연구자들이3,4) 분리, 보고한 성분들 외에 (+)-marmesin, 2-methoxy-2-(4′-hydroxyphenyl)ethanol, 2-hydroxy(4′-hydroxyphenyl)ethanol, apigenin, luteolin, cynaroside 및 daucosterol 등을 분리하고 그 구조를 동정한 후 항염증활성을 측정하여 그 결과를 보고하였다. 한편 이 등6)은 섬바디 추출물의 iNOS와 COX-2 등의 발현에 대한 효과를 측정하여 보고하였고, 김7)은 섬바디 뿌리 추출물에 대한 항산화, 항주름 및 미백 효능을 측정하여 보고하였으며, 오 등8)은 섬바디의 에탄올 추출물로부터 항균활성 물질로 falcarindiol을 분리, 보고하였다. 이상과 같이 섬바디의 연구는 비교적 다양하게 이루어 졌으며, 그 대상은 주로 뿌리를 이용한 것이 대부분이다. 저자 등은 연속되는 연구로 우리나라에 자생하는 산형과(Umbelliferae) 식물의 모든 부분에 대한 성분 연구를 계속하여 수행하고 있으며, 그 일부로 우리나라 특산 식물인 섬바디의 줄기에 대한 성분 연구를 수행하였으며, 그 결과 줄기 추출물의 n-BuOH 가용성 분획으로부터 5종의 화합물을 분리하고 그 구조를 밝혔기에 이를 보고하고자 한다.
재료 및 방법
재료 – 실험에 사용한 섬바디(D. takeshimana) 줄기는 2023년 8월 강원대학교 약학대학 구내에 식재되어 있는 것을 채집하여 강원대학교 약학대학 권용수 교수가 정확하게 감정한 후 음건하여 사용하였다. 확증표본 (KNUH-2023-S-1)은 강원대학교 약학대학 생약학 연구실에 보관중이다.
기기 및 시약 – 1H 및 13C-NMR은 Bruker사의 AVANCE 600을 이용하여 측정하였다. Mass spectra는 Waters 사의 Micromass Quattro micro API로 측정하였다. Column chromatography용 충진제로 silica gel은 Merck사의 Kieselgel 60 63-200 μm와 40-63 μm를 사용하였고, ODS는 YMC 사의 ODS-A (150μm)를 사용하였다. Flash column chromatography는 Teledyne Isco 사의 CombiFlash Flash chromatography system을 사용하였다. TLC plate는 Merck사의 precoated Kieselgel 60 F254s (layer thickness 0.25 mm, 20 × 20 cm, Merck Art. No. 5715), RP-18 F254s를 사용하였다. Open column chromatography에 사용한 용매는 특급시약을 증류하여 사용하였으며, TLC plate의 발색은 20% ethanol성 H2SO4 용액을 사용하였다.
추출 및 분리 – 채집하여 음건한 섬바디의 줄기 2.5 kg을 잘게 썰어 MeOH 10 L를 넣고 실온에서 1 주일간 추출하고 여과한 후 여액을 감압농축하여 MeOH ext. 245 g을 얻었다. 얻어진 MeOH ext.를 증류수로 현탁시키고 n-hexane, CHCl3 및 n-BuOH 순으로 분획하고 농축하여 n-hexane fraction 30.5 g, CHCl3 fraction 5 g 및 n-BuOH fraction 23.1 g을 각각 얻었다. 이들 분획 중 n-BuOH 분획에 함유되어 있는 성분을 분리하기 위하여 column chromatography를 실시하였다. 섬바디 줄기의 n-BuOH 가용성 분획 23 g을 silica gel (63-200 μm, 550 g) column (9.5 × 50 cm)에 걸고 EtOAc:MeOH:H2O를 용매로 8:1.5:0.5에서 6:3:1까지 순차적으로 용출시키고 다섯 개의 분획으로 나누었다(DTB-1 ~ DTB-5). 분획 DTB-2 (5.8 g)을 다시 silica gel (63-200 μm, 250 g) column (6.5 × 50 cm)에 걸고 CHCl3: MeOH:H2O = 3:1:0.1을 용매로 용출시키고 여섯 개의 분획(DTB-2-1 ~ DTB-2-6)으로 나누었다. 분획 DTB-2-1 (0.6 g)에 대하여 water-saturated EtOAc:MeOH = 19:1을 용매로 silica gel (40-63 μm, 70 g) column (3 × 50 cm) chromatography를 실시하고 여섯 개의 소분획(DTB-2-1-1 ~ DTB-2-1-6)으로 나누었다. 이중 소분획 DTB-2-1-2 (0.17 g)을 ODS (ODS-A 150 μm, 40 g) column (2.0 × 50 cm)에 걸고 MeOH:H2O = 50:50을 용매로 정제하고 화합물 1 (27 mg)을 얻었다. 분획 DTB-2-3 (0.08 g)을 MeOH로 세척하고 화합물 2 (36 mg)를 얻었다. 분획 DTB-2-5 (1.5 g)을 silica gel (63-200μm, 100 g) column (3.8 × 50 cm)에 걸고 EtOAc:MeOH:H2O = 8:1:0.5를 용매로 용출시켜 여섯 개의 분획(DTB-2-5-1 ~ DTB-2-5-6)으로 나누었다. 분획 DTB-2-5-2 (70 mg)를 다시 silica gel (40-63 μm, 70 g) column (3 × 50 cm)에 걸고 CHCl3:MeOH:H2O = 2:1:0.1을 용매로 용출시키고 다섯 개의 소분획(DTB-2-5-2-1 ~ DTB-2-5-2-5)으로 나누었다. 소분획 DTB-2-5-2-4 (38 mg)을 ODS (ODS-A 150 μm, 40 g) column (2.0 × 50 cm)에 걸고 MeOH:H2O = 30:70을 용매로 용출시키고 정제하여 화합물 3 (24 mg)과 4 (6 mg)을 얻었다. 분획 DTB-3 (7.8 g)을 silica gel (40-63 μm, 300 g) column (6.5 × 50 cm)에 걸고 EtOAc:MeOH:H2O = 7:2:1을 용매로 용출시켜 여섯 개의 분획(DTB-3-1 ~ DTB-3-6)으로 나누었다. 분획 DTB-3-4 (3.4 g)을 CombiFlash를 이용하여 silica gel column (Redisep® 80 g)에 CHCl3:MeOH:H2O = 2:1:0.1을 용매로 용출시켜 Flash chromatography를 실시하고 네 개의 분획(DTB-3-4-1 ~ DTB-3-4-4)으로 나누었다. 분획 DTB-3-4-3을 농축시켜 화합물 5 (0.3 g)을 얻었다.
Cimifugin (1) – White powder; 1H-NMR (600 MHz, CD3OD) δ: 6.61 (1H, s, H-8), 6.24 (1H, s, H-3), 4.77 (1H, dd, J=9.1, 8.1 Hz, H-2'), 4.45 (2H, br s, 2-CH2OH), 3.94 (3H, s, OCH3), 3.35 (2H, dd, J=9.1, 7.8 Hz, H-3'), 1.31, 1.25 (each 3H, s, gem-(CH3)2); 13C-NMR (150 MHz, CD3OD) δ: 179.76 (C-4), 168.66 (C-2), 167.10 (C-5), 161.14 (C-7), 157.03 (C-8a), 118.47 (C-6), 112.32 (C-4a), 109.28 (C-3), 94.53 (C-8), 92.63 (C-2'), 72.22 (C-4'), 61.04 (OCH3), 28.72 (C-3'), 25.40 (CH3), 25.33 (CH3); ESI-MS m/z 307 [M + H]+.
Cynaroside (2) – Brown powder; 1H-NMR (600 MHz, DMSO-d6) δ: 13.0 (1H, s, 5-OH), 7.44 (1H, dd, J=8.3, 2.2 Hz, H-6'), 7.41 (1H, d, J=2.2 Hz, H-2'), 6.89 (1H, d, J=8.3 Hz, H-5'), 6.78 (1H, d, J=2.1 Hz, H-8), 6.74 (1H, s, H-3), 6.43 (1H, d, J=2.1 Hz, H-6), 5.06 (1H, d, J=7.5 Hz, anomeric H), 3.68 (1H, br d, J=11.0 Hz, H-6″a), 3.51~3.15 (4H, overlapped, H-2″, 3″, 4″, 5″), 3.44 (1H, dd, J=11.0, 5.5 Hz, H-6″b); 13C-NMR (150 MHz, DMSO-d6) δ: 182.16 (C-4), 164.72 (C-7), 163.19 (C-2), 161.97 (C-5), 157.19 (C-9), 150.20 (C-4'), 146.03 (C-3'), 121.61 (C-1'), 119.43 (C-6'), 116.24 (C-5'), 113.78 (C-2'), 105.58 (C-10), 103.40 (C-3), 100.13 (C-1″), 99.78 (C-6), 94.99 (C-8), 77.39 (C-5″), 76.62 (C-3″), 73.35 (C-2″), 69.79 (C-4″), 60.86 (C-6″); ESI-MS m/z 449 [M + H]+.
3,5-Dicaffeoylquinic acid (3) – Light brown powder; 1H-NMR (600 MHz, CD3OD) δ: 7.63 (1H, d, J=15.9 Hz, H-3″), 7.61 (1H, d, J=15.8 Hz, H-3'), 7.11 (1H, d, J=2.1 Hz, H-5″), 7.08 (1H, d, J=2.1 Hz, H-5'), 6.99 (1H, dd, J=8.1, 2.1 Hz, H-9″), 6.97 (1H, dd, J=8.1, 2.1 Hz, H-9'), 6.79 (2H, d, J=8.1 Hz, H-8″, H-8'), 6.43 (1H, d, J=15.9 Hz, H-2″), 6.33 (1H, d, J=15.8 Hz, H-2'), 5.57 (1H, td, J=10.4, 5.1 Hz, H-3), 5.40 (1H, dd, J=6.6, 3.3 Hz, H-5), 3.92 (1H, dd, J=9.8, 3.5 Hz, H-4), 2.29 (1H, dd, J=15.3, 3.5 Hz, H-6ax), 2.15 (2H, m, H-2), 2.09 (1H, m, H-6eq); 13C-NMR (150 MHz, CD3OD) δ: 180.21 (COOH), 168.04 (C-1″), 167.55 (C-1′), 148.11 (C-7′), 147.97 (C-7″), 145.40 (C-3′, C-3″), 145.34 (C-6′, C-6″), 126.72 (C-4″), 126.49 (C-4′), 121.56 (C-9″), 121.50 (C-9′), 115.09 (C-8″), 115.04 (C-8′), 114.70 (C-2″), 114.22 (C-2′), 113.70 (C-5′, -5″), 74.93 (C-1), 73.13 (C-5), 71.92 (C-4), 71.09 (C-3), 39.65 (C-2), 36.33 (C-6); ESI-MS m/z 515 [M-H]-.
3,4-Dicaffeoylqunic aicd (4) – Light brown powder; 1H-NMR (600 MHz, CD3OD) δ: 7.60 (1H, d, J=15.9 Hz, H-3″), 7.53 (1H, d, J=15.8 Hz, H-3′), 7.03 (1H, d, J=2.1 Hz, H-5″), 7.01 (1H, d, J=2.1 Hz, H-5′), 6.92 (1H, dd, J=8.1, 2.1 Hz, H-9″), 6.90 (1H, dd, J=8.1, 2.1Hz, H-9′), 6.76 (1H, d, J=8.1 Hz, H-8″), 6.75 (1H, d, J=8.1 Hz, H-8′), 6.28 (1H, d, J=15.9 Hz, H-2"), 6.21 (1H, d, J=15.8 Hz, H-2'), 5.72 (1H, td, J=10.3, 5.8 Hz, H-3), 5.12 (1H, dd, J=10.3, 3.1 Hz, H-4), 4.34 (1H, dd, J=6.3, 3.2 Hz, H-5), 2.29 (1H, dd, J=14.9, 3.2 Hz, H-6a), 2.20 (2H, m, H-2), 2.02 (1H, dd, J=14.9, 5.9 Hz, H-6b); 13C-NMR (150 MHz, CD3OD) δ: 180.58 (COOH), 168.71 (C-1"), 168.64 (C-1'), 149.61 (C-7', C-7"), 147.53 (C-3"), 147.35 (C-3'), 146.74 (C-6', C-6"), 127.75 (C-4"), 127.68 (C-4'), 123.09 (C-9', C-9"), 116.47 (C-8′, C-8"), 115.09 (C-2′, C-2"), 77.57 (C-1), 77.32 (C-4), 70.87 (C-5), 69.65 (C-3), 40.99 (C-2), 38.97 (C-6); ESI-MS m/z 515 [M-H]-.
Chlorogenic acid (5) – Brown powder; 1H-NMR (600 MHz, CD3OD) δ: 7.54 (1H, d, J=15.5 Hz, H-3′), 7.02 (1H, d, J=2.0 Hz, H-5′), 6.90 (1H, dd, J=8.0, 2.0 Hz, H-9′), 6.75 (1H, d, J=8.0 Hz, H-8′), 6.25 (1H, d, J=15.5 Hz, H-2′), 5.35 (1H, dt, J=10.0, 5.0 Hz, H-3), 4.15 (1H, br d, J=2.5 Hz, H-5), 3.69 (1H, dd, J=9.5, 3.0, H-4), 2.14 (2H, dd, J=14.5, 2.5 Hz, H-2a, H-6a), 2.01 (2H, m, H-2b, H-6b); 13C-NMR (150 MHz, CD3OD) δ: 179.87 (COOH), 169.02 (C-1′), 149.47 (C-7′), 146.90 (C-3′), 146.74 (C-6′), 127.79 (C-4′), 122.93 (C-9′), 116.52 (C-8′), 115.48 (C-5′), 115.19 (C-2′), 74.54 (C-1), 72.62 (C-3), 72.28 (C-4, C-5), 40.14 (C-6), 38.60 (C-2); ESI-MS m/z 353 [M-H]-.
결과 및 고찰
화합물 1은 백색의 분말로 얻었으며, 1H-NMR의 δ 6.61과 6.24에서 나타나는 각각의 singlet으로부터 이 화합물은 전형적인 chromone계열의 화합물임을 알 수 있었다.9) δ 4.77에서 J=9.1과 8.1 Hz로 나타나는 수소 1개 분의 doublet of doublets, 3.35에서 J=9.1과 7.8 Hz로 나타나는 수소 2개 분의 doublet of doublets, 4.45에서 broad하게 나타나는 CH2에 의한 singlet, 1.31과 1.25에서 methyl기에 의한 singlet들을 확인할 수 있었다. 또한, δ 3.94에서 하나의 methoxyl기에 의한 singlet을 확인할 수 있었다. 이러한 1H-NMR spectrum으로부터 화합물 1은 dihydropyran ring 또는 dihydrofuran ring이 존재하는 chromone계열의 화합물로 추정하였다. 13C-NMR spectrum의 δ 92.63, 61.16 및 28.72에서 나타나는 signal들로부터 이 화합물은 dihydrofuran chromone계열의 화합물임을 알 수 있었고, 문헌10)에 기재된 값과 저자 등11)이 강활의 잎으로부터 분리한 cimifugin과 TLC분석을 비교하여 화합물 1을 cimifugin으로 동정하였다. 화합물 2는 1H- 및 13C-NMR spectrum을 분석하고, 그 결과를 문헌12)과 비교한 결과 선행연구자들5)이 섬바디의 뿌리로부터 분리, 보고한 cynaroside로 동정하였다. 화합물 3은 1H-NMR spectrum의 δ 7.63과 7.61에서 J=15.9와 15.8 Hz로 나타나는 각각의 doublet, δ 7.11과 7.08에서 J=2.1 Hz로 나타나는 각각의 doublet, δ 6.99와 6.79에서 J=8.1, 2.1 Hz로 나타나는 각각의 doublet of doublets 및 δ 6.43과 6.33에서 J=15.9와 15.8 Hz로나타나는각각의 doublet으로부터 이 화합물은 두 개의 caffeoyl기가 존재함을 알 수 있었으며, 13C-NMR spectrum의 δ 180.21, 74.93, 73.13, 71.92, 71.09, 39.65, 36.33에서 나타나는 signal들로부터 quinic acid의 존재를 확인할 수 있었다. 또한 1H-NMR spectrum의 δ 5.57에서 quinic acid의 3번수소의 signal이 J=10.4와 5.1 Hz의 triplet of doublets으로 나타나고, 5.40에서 5번 수소의 signal이 J=6.6, 3.3 Hz의 doublet of doublets으로 나타나며, 3.92에서 4번 수소의 signal이 J=9.8, 3.5 Hz의 doublet of doublet으로 나타났는데 이들의 signal들은 DQF-COSY, DEPT, HMBC 등의 분석을 통하여 확인하였다. 이 결과들을 문헌13)과 비교하여 화합물 3은 quinic acid의 3번과 5번 위치에 caffeoyl기가 치환되어 있는 3,5–dicaffeoylquinic acid로 동정하였다. 화합물 4도 1H- 및 13C-NMR spectra가 화합물 3과 매우 유사하지만 quinic acid의 3, 4 및 5번의 수소가 1H-NMR spectrum의 δ 5.72에서 J=10.3, 5.8 Hz의 triplet of doublets로, δ 5.12에서 J=10.3, 3.1 Hz의 doublet of doublets으로, 그리고 δ 4.34에서 J=6.3, 3.2 Hz의 doublet of doublets으로 각각 나타나므로 이 화합물은 quinic acid의 3번과 4번 위치에 caffeoyl기가 치환되어 있음을 알 수 있었으며, 이를 문헌15)과 비교하여 화합물 4는 3,4–dicaffeoylquinic acid로 동정하였다. 화합물 5는 문헌15)과 비교하여 chlorogenic acid로 동정하였다. 이상과 같이 그 구조를 동정한 화합물들의 활성에 관한 연구를 살펴보면 cimifugin (1)은 항염증작용,16) 건선에 의한 가려움증의 감소,17) 진통작용,18) 내장 장벽의 기능부전 개선작용19) 등이 보고되었다. Cynaroside (2)의 활성으로는 항염증작용,20) 항암작용,21) 간장보호작용,22) 골관절염 억제효과23) 등이 보고되었다. 3,5-dicaffeoyl quinic acid (3)의 활성으로는 피부보호작용,24) 항염증작용,25) HIV-1 억제작용26) 등이 보고되었다. 3,4–dicaffeoylquinic acid (4)의 활성으로는 동맥경화억제작용,27) 항산화작용,28) 항염증작용,29) antimutagenic acitivity,30) 항균활성31) 등이 보고되었다. Chlorogenic acid (5)의 활성으로는 괴양성대장염 완화작용,32) 항암작용,33) 폐섬유증 치료시 발생하는 epithelial-mesenchymal transition의 억제작용,34) 항산화작용,35) 골분화촉진작용36) 등이 보고되었다.
결 론
우리나라 특산 식물이며 울릉도에 주로 자생하고 있는 섬바디(D. takeshimana)의 줄기에 대한 성분을 밝혀 자원으로 사용할 수 있는지의 여부를 알아보기 위하여 연구에 착수하였으며, 줄기의 MeOH 추출물 중 n-BuOH 가용성 분획으로부터 5종의 화합물을 분리하고, NMR 등 분광학적 분석을 통하여 그 구조를 cimifugin (1), cynaroside (2), 3,5-dicaffeoyl quinic acid (3), 3,4-dicaffeoyl quinic acid (4) 및 chlorogenic acid (5)로 동정하였다. 이들 화합물 중 cynaroside (2)를 제외한 화합물들은 모두 이 식물로부터는 처음으로 분리 하였으며, 선행 연구자들이 보고한 활성을 보면 다양한 활성 연구를 위한 자원으로 섬바디(D. takeshimana)의 줄기가 이용될 수 있을 것으로 생각된다.
References
- 이우철 (1996) 원색 한국기준식물도감, 257, 아카데미 서적, 서울.
- 이춘녕, 안학수, 박수현 (1997) 한국농식물자원명감, 154, 일조각, 서울.
- Kwon, Y., Kim, C. W. and Kim, C. M. (1992) A study on the chemical components from the roots of Dystaenia takeshimana. Kor. J. Pharmacogn. 23: 218-220.
- Kim, B. H., Kwon, Y. and Kim, C. M. (1993) A study on the chemical components from the root of Dystaenia takeshimana. Kor. J. Pharmacogn. 24: 296-298.
-
Kim, J. S., Kim, J. C., Shim, S. H., Lee, E. J., Jin, W., Bae, K., Son, K. H., Kim, H. P., Kang, S. S. and Chang, H. W. (2006) Chemical constituents of the root of Dystaenia takeshimana and their anti-inflammatory activity. Arch. Pharm. Res. 29: 617-623.
[https://doi.org/10.1007/BF02968244]

-
Lee, J. Y., Yoo, D. H., Joo, D. H. and Chae, J. W. (2016) Inhibitory efficacy of Dystaenia takeshimana extract on iNOS, COX-2 protein and mRNA expression in Raw 264.7 cell. Microbiol. Biotechnol. Lett. 44: 571-576.
[https://doi.org/10.4014/mbl.1610.10006]

- Kim, Y. C. (2022) Antioxidant capacity, anti-wrinkle and whitening efficacies of Dystaenia takeshimana methanol extract in a cell-free system. J. Invest. Cosmetol. 18: 277-283.
- Oh, J. A., Shin, D. H. and Beak, N. I. (1999) Isolation and identification of growth inhibition substance on L. monocytogenes from Dystaenia takeshimana Kitagawa. Korean J. Food Sci. Technol. 31: 984-993.
-
Baba, K., Hata, K., Kimura, Y., Matsuyama, Y. and Kozawa, M. (1981) Chemical studies of Angelica japonica A. GRAY. Ⅰ. On the constituents of the ethyl acetate extract of the root. Chem. Pharm. Bull. 29: 2565-2570.
[https://doi.org/10.1248/cpb.29.2565]

-
Sasaki, H., Taguchi., Endo, T. and Yohioka, I. (1982) The constituents of Ledebouriella seseloides WOLFF. Ⅰ. Stuructures of three new chromones. Chem. Pharm. Bull. 30: 3555-3562.
[https://doi.org/10.1248/cpb.30.3555]

-
Byeon, W. B., Kim, Y. J., Lim, H. J., Hwang, J. S., Kim, M. J. and Kwon, Y. (2024) Chemical constituents of Ostericum koreanum Maximowicz leaves. Kor. J. Pharmacogn. 55: 67-71.
[https://doi.org/10.22889/KJP.2024.55.2.67]

- Jo, H. W. and Park, J. C. (2008) Phenolic compounds isolated from the leaves of Angelica keiskei showing DPPH radical scavenging effect. Kor. J. Pharmacogn. 39: 146-149.
-
Seo, Y. J., Kil, H. W., Rho, T. and Yoon, K. D. (2020) A new coumestan glucoside from Eclipta prostrata. Nat. Prod. Sci. 26: 289-294.
[https://doi.org/10.20307/nps.2020.26.4.289]

-
Basnet, P., Matsushige, K., Hase, K., Kadota, S. and Namba, T. (1996) Four Di-O-caffeoyl quinic acid derivatives from propoils. Potent hepatoprotective activity in experimetal liver injury models. Biol. Pharm. Bull. 19: 1479-1484.
[https://doi.org/10.1248/bpb.19.1479]

-
Baek, D. Y., Lee, M. J., Baek, N. I. and Seo, K. H. (2016) Phenolic compounds from the leaves of eggplant (Solanum melongena L.). J. Appl. Biol. Chem. 59: 103-106.
[https://doi.org/10.3839/jabc.2016.019]

-
Han, B., Dai, Y., Wu, H., Zhang, Y., Wan, L., Zhao, J., Liu, Y., Xu, S. and Zhou, L. (2019) Cimifugin inhibits inflammatory responses of RAW264.7 cells induced by lipopolysaccharide. Med. Sci. Moni. 25: 409-417.
[https://doi.org/10.12659/MSM.912042]

-
Yan, J., Ye, F., Ju, Y., Wang, D., Chen, J., Zhang, X., Yin, Z., Wang, C., Yang, Y., Zhu, C., Zhou, Y., Cao, P., Xu, Y., Yu, G. and Tang, Z. (2021) Cimifugin relieves pruritus in psoriasis by inhibiting TRPV4. Cell Calcium 97: 10249.
[https://doi.org/10.1016/j.ceca.2021.102429]

-
Lee, H. Y., Ki, Y. J., Park, S. Y., Cho, S. Y., Seo, J., Lim, K. J. and Jung, K. T.(2020) Antinociceptive effects of intrathecal cimifugin treatment: a preliminary rat study based on formalin test. Anesth. Pain Med. 15: 478-485.
[https://doi.org/10.17085/apm.20032]

-
Zhang, H., Xiong, Z., He, Y., Su, H. and Jiao, Y. (2025) Cimifugin improves intestinal barrier dysfunction by upregulating SIRT1 to regulate the NRF2/HO-1 signaling pathway. Naunyn Schmiedebergs Arch. Pharmacol. 398: 2897-2908.
[https://doi.org/10.1007/s00210-024-03433-9]

-
Zhou, Y., Huang, Y., Ye, W., Chen, Z. and Yuan, Z.(2024) Cynaroside improved depressive-like behavior in CUMS mice by suppressing microglial inflammation and ferroptosis. Biomed. Pharmacother. 173: 116425.
[https://doi.org/10.1016/j.biopha.2024.116425]

-
Lei, S., Cao, W., Zeng, Z., Wang, L., Lan, J. and Chen, T. (2024) Cynaroside induces G1 cell cycle arrest by downregulating cell division cycle 25A in colorectal cancer. Molecules 29: 1508.
[https://doi.org/10.3390/molecules29071508]

-
Wang, L., Ma, X., Wang, J. and Li, C. (2019) In vitro inhibitory effects of cynaroside on human liver cytochrome P450 enzymes. Pharmacology 104: 296-302.
[https://doi.org/10.1159/000502172]

-
Lee, S. A., Park, B. R., Moon, S. M., Hong, J. H., Kim, D. K. and Kim, C. S. (2020) Chondroprotective effect of cynaroside in IL-1 β-induced primary rat chondrocytes and organ explants via NF- κ B and MAPK signaling inhibition. Oxid. Med. Cell Longev. 2020: 9358050.
[https://doi.org/10.1155/2020/9358080]

-
Oh, J. H., Lee, J. I, Karadeniz, F., Park, S. Y., Seo, Y. and Kong, C. S. (2020) Antiphotoaging effects of 3,5-dicaffeoylepi-quinic acid via inhibition of matrix metalloproteinases in UVB-irradiated human keratinocytes. Evid. Based Complement Aternat. Med. 2020: 8949272.
[https://doi.org/10.1155/2020/8949272]

-
Nam, S. Y., Han, N. R., Rah, S. Y., Seo, Y., Kim, H. M. Jeong, H. J. (2018) Anti-inflammatory effects of Artemisia scoparia and its active constituent, 3,5-dicaffeoyl-epi-quinic acid against activated mast cells. Immunopharmacol. Immunotoxicol. 40: 52-58.
[https://doi.org/10.1080/08923973.2017.1405438]

-
Kwon, H. C., Jung, C. M., Shin, C. G., Lee, J. K., Choi, S. U., Kim, S. Y. and Lee, K. R.(2000) A new caffeoyl quinic acid from Aster scaber and its inhibitory activity against human immunodeficiency virus-1 (HIV-1) integrase. Chem. Pharm. Bull. 48: 1796-1798.
[https://doi.org/10.1248/cpb.48.1796]

-
Chiou, W. F., Chen, C. C. and Wei, B. L. (2011) 3,4-Di-O-Caffeoylquinic acid inhibits angiotensin-II-induced vascular smooth muscle cell proliferation and migration by down-regulating the JNK and PI3K/Akt signaling pathways. Evid. Based Complement Alternat. Med. 2011: 634502.
[https://doi.org/10.1093/ecam/nep140]

-
Retamozo, M. H., Silva, C. C., Tamayose, C. I., Carvalho, J. C. S., Romoff, P., Fávero, O. A, and Ferreira, M. J. P. (2023) Chemical constituents from leaves of Baccharis sphenophylla (Asteraceae) and their antioxidant effects. Plants 12: 1262.
[https://doi.org/10.3390/plants12061262]

-
Kim, S. Y., Shin, D. U., Eom, J. E., Jung, S. Y., Song, H. J., Lim, K. M., Kim, G. D., Yun, S. I., Kim, M. Y., Shin, H. S. and Lee, S. Y. (2022) Artemisia gmelinii attenuates lung inflammation by suppressing the NF-κB/MAPK pathway. Antioxidants 11: 568.
[https://doi.org/10.3390/antiox11030568]

-
Yoshimoto, M., Yahara, S., Okuno, S., Islam, M. S., Ishiguro, K. and Yamakawa, O. (2002) Antimutagenicity of mono-, di-, and tricaffeoylquinic acid derivatives isolated from sweet potato (Ipomoea batatas L.) leaf. Biosci. Biotechnol. Biochem. 66: 2336-2341.
[https://doi.org/10.1271/bbb.66.2336]

-
Han, J., Lv, Q. Y., Jin, S. Y., Zhang, T. T., Jin, S. X., Li, X. Y. and Yuan, H. L. (2014) Comparison of anti-bacterial activity of three types of di-O-caffeoylquinic acids in Lonicera japonica flowers based on microcalorimetry. Chin. J. Nat. Med. 12: 108-113.
[https://doi.org/10.1016/S1875-5364(14)60017-0]

-
Gao, W., Wang, C., Yu, L., Sheng, T., Wu, Z., Wang, X., Zhang, D., Lin, Y. Gong, Y. (2019) Chlorogenic acid attenuates dextran sodium sulfate-induced ulcerative colitis in mice through MAPK/ERK/JNK pathway. Biomed Res Int. 2019: 6769789.
[https://doi.org/10.1155/2019/6769789]

-
Gupta, A., Atanasov, A. G., Li, Y., Kumar, N. and Bishayee, A. (2022) Chlorogenic acid for cancer prevention and therapy: Current status on efficacy and mechanisms of action. Pharmacol Res. 186: 106505.
[https://doi.org/10.1016/j.phrs.2022.106505]

-
Mao, X., Xie, X., Ma, J., Wei, Y., Huang, Z., Wang, T., Zhu, J., Wang, Y., Zhao, H. and Hua, J. (2023) Chlorogenic acid inhibited epithelial-mesenchymal transition to treat pulmonary fibrosis through modulating autophagy. Biol. Pharm. Bull. 46: 929-938.
[https://doi.org/10.1248/bpb.b23-00071]

-
Tošović, J., Marković, S., Dimitrić, Marković, J. M., Mojović, M. and Milenković, D. (2017) Antioxidative mechanisms in chlorogenic acid. Food Chem. 237: 390-398.
[https://doi.org/10.1016/j.foodchem.2017.05.080]

-
Hu X, Wang L, He Y, Wei M, Yan H, Zhu H. (2021) Chlorogenic acid promotes osteogenic differentiation of human dental pulp stem cells through wnt signaling. Stem Cells Dev. 30: 641-650.
[https://doi.org/10.1089/scd.2020.0193]