계수나무(Cercidiphyllum japonicum) 가지에 함유된 엘라그산 성분과 생리활성
Abstract
3′-Di-O-methylellagic acid 4-O-β-D-glucopyranoside (1), 3,3′,4-tri-O-methylellagic acid (2), and methyl 4-hydroxybenzoate (3) were isolated from the ethyl acetate fraction of the twigs of Cercidiphyllum japonicum, and their structures were confirmed by spectroscopic methods. These three compounds were found for the first time in C. japonicum. The ethyl acetate and butanol extracts of C. japonicum exhibited stronger DPPH scavenging activity than ascorbic acid, which was used as a positive control. and among the isolated compounds, compound 1 showed inhibition of elastin-degrading enzyme activity. Compound 2 showed the strongest DPPH radical scavenging activity, and significant inhibition of tyrosinase activity. The antibacterial activity of the solvent extracts was highest in the ethyl acetate extract.
Keywords:
Cercidiphyllum japonicum, Ellagic acids, NMR, HPLC계수나무(Cercidiphyllum japonicum)는 계수나무과(Cercidiphyllaceae), 계수나무속(Cercidiphyllum)의 낙엽성 활엽교목으로서 일본과 중국 중남부에 분포하며 현재 한국의 중부이남에서 식재 되고 있다. 이 나무는 일본에서 들여온 품종으로서 1920년경 경기도 광릉에 처음으로 도입된 것으로 추정하고 있으며 그 모수가 현재 국립수목원에 존재하는 것으로 알려져 있다. 일본에서는 이 식물을 카츠라 나무(Katsura tree)라고 부르며 중국에서는 연향수(連香樹)라고 한다. 계수나무의 잎에서는 달콤한 캐러멜 향이 나는데 이는 식품산업에 다양하게 사용되는 방향성분인 말톨에 의한것으로 알려져 있다.1) 계수나무에는 gallotannin,2) ellagitannin,3) anomeric tannin과 flavonoide4) 같은 폴리페놀 화합물이 존재하는 것으로 보고 되어있다. Lee 등3)은 계수나무의 잎에서 hexa-O-galloyl-β-D-(+)-glucose과 그의 줄기 껍질에서 polyoxygenated ellagitannin의 일종을 분리하였으며 Lee 등5)은 계수나무의 줄기껍질에서 gallic acid, methyl gallate, kurigalin, 1,2,3,6-tetra-O-galloyl-β-D-glucose 및 1,2,3,4,6-penta-O-galloyl-β-D-glucose, isocorilagin과 같은 가수분해 형 탄닌을 발견한 바 있다. Min 등6)은 이 화합물들이 우수한 항산화 활성과 산화질소 생성 억제능을 나타낸다고 보고하였으며 Lee 등7)은 에틸아세테이트 분획이 당뇨개선 지표인 α-glucosidase 활성저해능을 보여주고 있음을 밝혔다. Kang 등8)은 HPL C로서 chlorogenic acid, quercetin, avicularin과 같은 플라보노이드 성분을 확인한 바 있다.
본 연구는 계수나무가 함유한 천연물질에 대한 다양한 자료를 확보하고 그의 생리활성을 규명하기 위하여 계수나무 가지로부터 3종의 화학성분을 분리하여 그의 물리화학적 자료로부터 화학구조를 동정하였다. 또한, 계수나무의 용매분획물 및 단리한 화합물에 대하여 항산화 효능으로서 DPPH 라디칼 소거능과 피부미백 효능으로서 타이로시네이즈 활성저해능, 피부탄력 효능으로서 엘라스틴분해효소 저해능을 검사하여 계수나무의 의약학적 유용성을 검토하였다.
재료 및 방법
실험재료 – 연구에 사용된 계수나무(C. japonicum)의 가지는 2018년 6월 대전광역시 목원대학교에 식재 된 것을 채집하여 사용하였고 국립수목원의 표본과 비교하여 동일 종임을 확인하였다. 실험에 사용된 표본(MOK-C001)은 목원대학교 식품제약학학부 천연물실험실에 냉동보관하였다.
시약 및 기기 – 계수나무 성분의 분리 및 분석에 사용된 용매는 모두 Duksan pure chemical (Korea)에서 구매하여 사용하였다. 증류수는 18 MΩ/cm 이상의 탈이온수를 제조하여 사용하였다. 화학성분 분리에 사용한 고정상은 실리카겔로서 Si 60 intertec 60-200 μm (Intertechnologies, Korea)과 Octadecyl (C18) Aqua (Yamazen Co, Japan)를 사용하였으며 TLC는 TLC Silica gel 60 F254 (Merck, USA)를 사용하였다. 함량분석을 위한 HPLC에 사용된 컬럼은 Discovery C18, 250 × 4.6 mm, 5 μm (Supelco, USA)이었다. 총 폴리페놀함량 측정을 위하여 사용한 시약은 Folin-ciocalteu (Sigma-Aldrich), Na2CO3 (Shinyo pure chemicals Co. Japan), galic acid (Samchun chemicals, Korea), 총 플라보노이드 함량측정을 위하여 AlCl3, NaNO2 (Duksan pure chemical, Korea), NaOH (Samchun chemicals, Korea), quercetin (ACROS Organics, USA), DPPH 라디칼 소거활성 측정용으로 2,2-diphenyl-1-picrylhydraxyl (Alfa Acer, USA), ascorbic acid (Sigma-Aldrich, USA), 타이로신 분해효소 저해활성 측정용으로 L-tyrosine, mushroom tyrosinase, kojic acid (Sigma-Aldrich, USA)를 사용하였다. 엘라스틴분해효소 저해활성 측정을 위하여 N-succinyl-(Ala)3-p-nitroanilide, elastase from porcine pancreas (PPE), ursolic acid (Sigma-Aldrich, USA)를 사용하였다. 항균활성 측정용 세균은 Staphylococcus aureus, Escherichia coli, Pseudomonas aeruginosa, Candida albicans, Aspergillus niger (KACC, Korea)를 사용하였다. 계수나무 함유 성분을 순수하게 분리하기 위하여 SHIMADZU LC (SCL-10A vp System controller, FRC-10A Fraction collector, LC-6AD Pump, SPD-10A vp UV-Vis Detector; Shimadzu, Japan)를 사용하였다. 분석에 사용된 HPLC는 Agilent Technologies HPLC 1200 series (G1322A Degasser, G1329A ALS, G1311A Quat Pump, G1316A TCC, G1315D DAD; Agilent Technologies, USA)를 사용하였다. 구조 동정에 사용한 13C-NMR, 1H-NMR은 Bruker Avance NEO 500 MHz (Bruker, USA)이며 UV spectrophotometer는 Jasco-760 (Jasco, Japan)이었다.
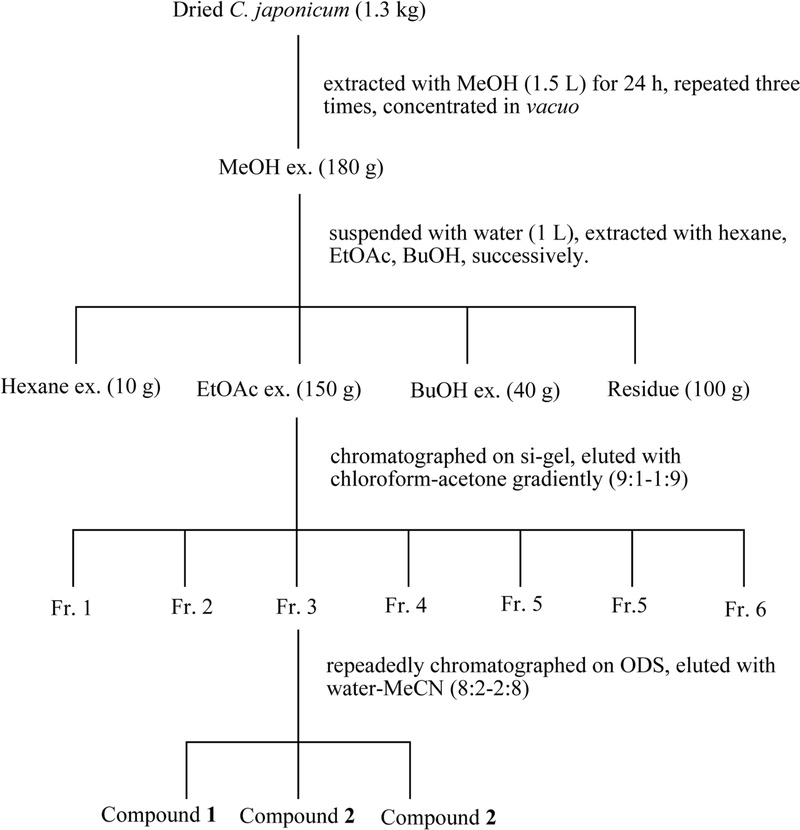
성분 추출, 분획 및 분리 – 건조한 계수나무 가지(1.3 kg)를 파쇄하여 메탄올(1.5 L)로 24시간 3회 환류추출하여 나온 추출액을 감압농축하여 메탄올 추출액(180 g)을 얻었다. 메탄올 추출액을 1 L의 증류수에 현탁한 후 헥산, 에틸아세테이트, 부탄올 각 1 L로서 순차적으로 용매 분획하였다. 이때 각 용매 당 2회 반복 분획하였다. 각 용매 분획을 감압농축하여 헥산 추출물(10 g), 에틸아세테이트 추출물(150 g), 부탄올 추출물(40 g), 물 잔사(100 g)를 얻었다. 에틸아세테이트 추출물(100 g)을 실리카겔(0.5 L)이 충진된 유리컬럼(60 × 5 cm)에 가하고 클로로포름-아세톤(9:1→1:9, v/v)을 이동상으로 용출하여 6개의 분획(Fr. 1~6)으로 나누었다. Fr. 3 (10.7 g)을 C18 수지(250 mL)를 충진한 유리컬럼(25 × 3 cm)에 가하고 이동상으로 물과 아세토니트릴 혼합용매로서(9:1→1:9) 용출하기를 반복 실시하여 compound 1, 2, 3을 분리하였다(Fig. 1).
화합물 1, 2, 3의 물리화학적 자료 – 계수나무 가지로부터 분리한 화합물의 화학적구조를 규명하기 위해 질량분석(UPLC-Q/TOF), 핵자기공명(NMR), 자외선분광분석(UV/vis)을 수행하였다. 각 화합물의 질량을 확인은 UPLC-Q/TOF MS으로 하였으며 Waters사의 Aquity Ultra Performance LC로서 각 화합물을 분리하여 확인하였다. 분리에 사용한 컬럼은 ACQUITY BEH C18 column이었다. 검출기는 Waters Xevo Q TOF MS로서 이온화 방식은 ESI이었다. NMR 스펙트럼을 얻기 위하여 각 성분은 DMSO-d6에 녹여 측정하였고 UV 스펙트럼을 얻기 위하여 각 성분은 메탄올에 녹여 측정하였다.
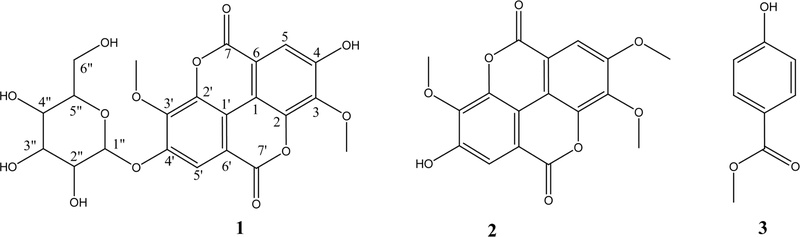
3,3′-Di-O-methylellagic acid-4′-O-β-D-glucopyranoside (1) – Yellow powder, UV (MeOH) λmax nm (log ε): 249 (4.09), 370 (0.70), ESI-MS: m/z 491 [M-H]-, 1H-NMR (500 MHz, DMSO-d6) δ: 7.57 (1H, s, H-5), 4.05 (3H, s, 3-O-CH3), 7.82 (1H, s, H-5′), 4.09 (3H, s, 3′-O-CH3), 5.15 (1H, d. J=7.04 Hz, H-1″). 3.4~3.7 (6H, m, H-2″~6″). 13C-NMR (125 MHz, DMSO-d6) δ : 112.4 (C-1), 141.4 (C-2), 140.9 (C-3), 61.6 (3-O-CH3), 151.7 (C-4), 112.5 (C-5), 113.1 (C-6), 158.8 (C-7), 114.9 (C-1′), 141.7 (C-2′), 142.1 (C-3′), 62.1 (3′-O-CH3), 154.8 (C-4′), 113.1 (C-5′), 113.6 (C-6′), 158.6 (C-7′), 101.8 (C-1″), 73.8 (C-2″), 77.8 (C-3″), 70.1 (C-4″), 76.9 (C-5″), 61.0 (C-6″).
3,3′,4-tri-O-methylellagic acid (2) – Yellow powder, UV (MeOH) λmax nm (log ε): 246 (4.24), 370 (0.74), ESI-MS: m/z 343 [M-H]-, 1H-NMR (500 MHz, DMSO-d6) δ: 7.84 (1H, s, H-5), 4.05 (3H, s, 3-O-CH3), 4.10 (3H, s, 3′-O-CH3), 4.01 (3H, s, 4′-O-CH3), 7.64 (1H, s, H-5′). 13C-NMR (125 MHz, DMSO-d6) δ : 112.1 (C-1), 142.1 (C-2), 141.4 (C-3), 62.2 (3-O-CH3), 153.7 (C-4), 108.8 (C-5), 113.8 (C-6), 158.8 (C-7), 110.8 (C-1′), 141.7 1(C-2′), 140.9 (C-3′), 61.5 (3′-O-CH3), 154.8 (C-4′), 56.8 (4′-OCH3), 112.8 (C-5′), 113.8 (C-6′), 158.6 (C-7′).
Methyl 4-hydroxybenzoate (3) – White powder, UV (MeOH) λmax nm (log ε): 255 (3.98), ESI-MS: m/z 151 [M-H]-, 1H-NMR (500 MHz, DMSO-d6) δ: 6.01 (2H, d, J=7.99 Hz, H-2,6), 7.05 (2H, d, J=8.02 Hz, H-3,5), 3.03 (3H, s, 7-O-CH3). 13C-NMR (125 MHz, DMSO-d6) δ: 160.1 (C-1), 113.9 (C-2, 6), 130.5 (C-3, 5), 120.0 (C-4), 166.5 (C-7), 50.0 (C-8).
HPLC를 이용한 계수나무 중 1, 2, 3의 함량 분석 – 계수나무 시료 분말 1 g을 정밀하게 달아 밀폐용기에 넣고 10 mL의 메탄올을 가한 후 24 시간 환류 추출하였다. 원심분리하여 나온 상징액을 막 여과기로 여과하여 시료용액으로 하였다. HPLC로 함량 분석을 하기 위한 이동상은 물과 아세토니트릴(MeCN) 혼합용매로서 0→20분(15→22% MeCN), 20→30분(22→30% MeCN), 30→40분(30→40% MeCN)를 1 mL/min의 유속으로 흘려주었다. 시료주입량은 10 μL이며 컬럼은 Discovery C18 (250 × 4.6 mm, 5 μm)이며 컬럼의 온도는 40°C 이었다. 254 nm에서 각 화합물들을 검출하였다(Fig. 3). 함량분석법의 검증은 ICH guideline에 따라 1, 2, 3을 일정 농도로 희석한 표준용액의 크로마토그램에서 보이는 각 피크의 넓이로부터 작성한 직선식에서 LOQ=3.3×(σ/S)와 LOD=10×(σ/S) 계산식을 이용하여 구하였으며 특이성은 머무름시간과 UV흡수패턴을 비교하여 확인하였으며 정밀성은 일간정밀성으로, 정확성은 회수율로 평가하였다.
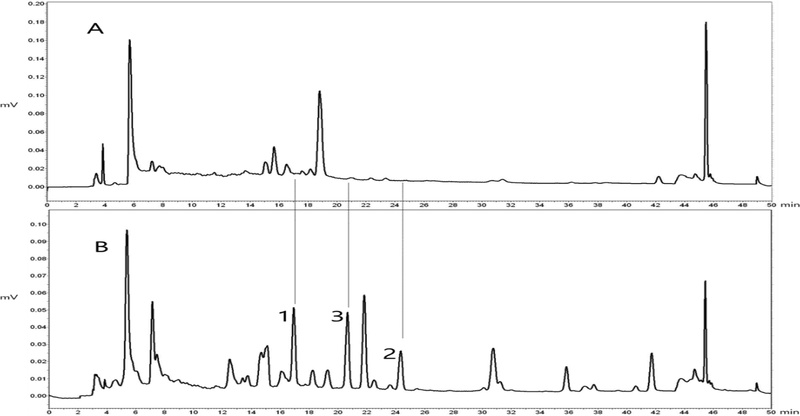
HPLC analysis of methanol extrat of C. japonicum. A: Leaf of C. japonicum, B: Twig of C. japonicum. Mobile phase for HPLC analysis: aquotic MeCN, 0→20 min (15→22%), 20→30 min (22→30%), 30→40 min (30→40%), flow rate 1 mL/min, detected at 254 nm, column temp.: 40℃.
총 폴리페놀함량 측정 시험 – 계수나무 가지 용매분획물들에 대한 총 폴리페놀 함량은 Folin-Denis방법을 응용하였다. 계수나무 가지 용매분획물인 헥산, 에틸아세테이트, 부탄올, 및 수층 추출물을 1, 5, 10, 50, 100 μg/mL의 농도로 DMSO에 녹여 시험용액으로 하였다. 96 well plate에 시료용액 20 μL와 100% Folin-Ciocalteu 40 μL를 주입하고 3 분간 25°C에 방치한 뒤 700 mM Na2CO3 포화용액 140 μL를 첨가하여 25°C에서 30 분간 암소에 반응시켰다. 반응시료는 765 nm에서 흡광도를 측정하고 gallic acid를 표준물질로 사용한 검량선에 대입하여 함량을 산출하였다. 측정 단위는 GAE (gallic acid equivalent) mg를 사용하였다.
총 플라보노이드 함량 측정 시험 – 총 폴리페놀함량 측정 시험과 동일한 방법으로 제조된 시험용액을 96 well plate에 20 μL 가하고 5% NaNO2 12 μL를 주입하여 25°C에서 6분간 반응시킨다. 그 후 10% AlCl3 24 μL를 첨가하고 25°C에서 5 분간 반응한 후 1 M NaOH 120 μL를 첨가한 후 25°C에서 15 분간 반응한 후 510 nm에서 흡광도를 측정하여 표준물질로 사용한 quercetin으로 작성한 검량선에 대입하여 함량을 산출하였다. 측정 단위는 QE (quercetin equivalent) mg/g이다.
항균활성 측정 – 계수나무 가지 용매분획물들에 대한 항균활성을 디스크 확산법으로 측정하였다. NA배지는 증류수 1 L에 nutrient agar 23 g, PDA배지는 증류수 1L에 potato dextrose agar 39 g를 혼합하고 NB 액체배지는 증류수 1 L에 nutrient broth 8 g, PDB액체배지는 증류수 1L에 potato dextrose broth 24 g을 혼합하여 멸균하여 사용하였다. 균주는 NA, NB에 접종하고 진균은 PDA, PDB에 접종하였다. 각 시료를 2 mg/mL의 농도로 DMSO에 녹여 disc에 10 μL 주입하고 37.5°C에서 24시간 배양하였다. 배양 후 disc의 직경을 포함한 clear zone의 크기를 측정하였다. 양성대조군은 phenoxyethanol을 사용하였다.
DPPH 라디칼 소거능 측정 – 계수나무 가지 용매분획물과 각 화합물(1, 2, 3)의 DPPH 라디칼 소거능은 Blois의 방법을 응용하였다. 용매분획물과 각 화합물의 농도는 각 시료를 96 well plate에 50 μL가할 때 최종 농도가 62.5, 125, 250, 500 μg/mL가 될 수 있도록 DMSO에 녹여 검액으로 하였다, 메탄올에 용해한 0.2 mM DPPH용액 150 μL를 가한 후 암소에서 25°C로 30 분간 반응하였다. 흡광도는 517 nm에서 측정하였으며 양성대조군으로 ascorbic acid를 사용하였다.
타이로시네이즈 활성 저해능 –각 화합물(1, 2, 3)의 농도는 각 시료를 96 well plate에 20 μL가할 때 최종 농도가 62.5, 125, 250, 500 μg/mL가 될 수 있도록 DMSO에 녹여 검액으로 하였다, 각 시료를 96 well plate에 20 μL 가하고 3 mM L-tyrosin 용액 40 μL를 주입한 후 pH 6.8로 조정한 0.1 M potassium phospate buffer에 용해하여 2000 unit/mL mushroom tyrosinase를 140 μL를 주입한 뒤 25°C에서 30 분간 반응하였다. 흡광도는 490 nm에서 측정하였으며 양성대조군은 kojic acid로 하였다.
엘라스틴 분해효소 저해능 – 각 화합물(1, 2, 3)의 농도는 각 시료를 96 well plate에 25 μL 가할 때 최종 농도가 62.5, 125, 250, 500 μg/mL가 될 수 있도록 DMSO에 녹여 검액으로 하였다. 각 검액을 96 well plate에 25 μL 가하고 2.5 unit/mL elastase from porcine pancreas 20 μL와 0.2 M Tris-HCl buffer 80 μL를 혼합 후 well에 가하고 37°C에서 15 분간 암소에서 반응하였다. N-succinyl-(alanin)3-p-nitroanilide 25 μL와 0.2 M Tris-HCl buffer 100 μL 첨가하여 37°C에서 20 분 간 암소에서 반응한 후 410 nm에서 흡광도를 측정하였다. 양성대조군은 ursolic acid였다.
결과 및 고찰
계수나무 가지 메탄올추출물의 에틸아세테이트 가용부로부터 계수나무에서 보고된 바 없었던 3종의 화합물을 분리하였다. 각 화합물은 추출 및 분리 과정 중에 확인한 TLC에서 특징적인 반점을 추적하여 분리하였으며 실리카겔 및 역상크로마토그래피를 반복 실시하여 용이하게 분리 정제할 수 있었다(Fig. 1). Compound 1은 1H-NMR 스펙트럼으로부터 방향성환에 존재하는 두 개의 수소 피크가 δ 7.57 (1H, s, 5-H), δ 7.82 (1H, s, 5′-H)에서 나타났으며 두 개의 메톡시 피크가 δ 4.05 (3H, s, 3-O-CH3), δ 4.09 (3H, s, 3′-O-CH3)에서 나타났다. 또한 δ 5.15 (d, J=7.04 Hz)에서 당의 anomeric 수소가 나타났으며 그의 짝지움 상수로부터 β anomer임을 확인하였다. δ 3.4~3.7에서 1개의 당으로부터 비롯된 수소 피크들이 관찰되었다. 13C-NMR에서 ellagic acid로부터 14개의 탄소 피크가 관찰되었으며 glucose로부터 기인한 6개의 피크가 관찰되었다. UV/vis 스펙트럼에서는 246 nm와 370 nm에서 흡수극대값을 보였다. 이 화합물의 분자량은 ESI-MS로서 측정하여 492 임을 확인하였고 이는 [M-H]- ion peak인 m/z 491 로부터 유추할 수 있었다. 이상의 결과들은 Nono 등9)이 Dissotis thollonii의 뿌리에서 분리하여 보고한 3,3′-di-O-methyllellagic acid 4′-O-β-D-glucopyranoside의 스펙트럼값과 정확히 일치하였다. Compound 2는 1과 마찬가지로 1H-NMR 스펙트럼으로부터 방향성환에 존재하는 두 개의 수소 피크가 δ 7.84 (1H, s, 5-H), δ 7.64 (1H, s, 5′-H)에서 나타났으며 세 개의 메톡시 피크가 δ 4.01 (s), δ 4.05 (s), δ 4.10 (s)에서 나타났다. 당으로부터 비롯한 수소피크들은 관찰되지 않았다. 13C-NMR에서 ellagic acid의 특징적인 14개의 탄소 피크가 관찰되었으며 UV/vis 스펙트럼에서는 246 nm와 370 nm에서 흡수극대값을 보였다. 이 화합물의 분자량은 ESI-MS로서 측정하여 344임을 m/z 343 [M-H]+ 이온 피크를 통하여 확인하였다. 이상의 결과로부터 compound 2는 Wardana 등10)이 Syzygium polycephalum에서 분리하여 보고한 3,3′,4-tri-O-methyllellagic acid으로 확인되었다. Compound 3은 1H-NMR 스펙트럼에서 방향성환에 존재하는 두 종류의 수소 피크가 AA′BB′ pattern 으로서 δ 6.01 (2H, d, J=7.99 Hz, H-2, 6), δ 7.05 (2H, d, J=8.02 Hz, H-3, 5)에서 나타났으며 한 개의 메톡시 피크가 δ 3.03 (3H, s, 7-O-CH3)에서 나타났다. 13C-NMR에서 방향성환에서 기인한 탄소가 113.9 (C-2,6), 130.5 (C-3,5) ppm에서 나타났으며 방향성환의 p-OH가 치환된 탄소가 160.1 (C-1) ppm에서 나타나며 acetoxy가 치환된 C-4는 120.0 ppm에서 acetyl에 존재하는 carbonyl carbone은 166.5, methyl carbone은 50.0 ppm에서 나타났다. UV/vis 스펙트럼에서는 255 nm에서 특징적인 흡수극대값을 보였다. 이 화합물의 분자량은 ESI-MS로서 측정한 m/z 151 (M-H)-로부터 152로 확인할 수 있었다. 이상의 결과로부터 compound 3은 식품에서 방부제로 사용되는 methyl 4-hydroxybenzoate (methyl paraben)로 확인되었다.
HPLC를 이용한 계수나무 중 1, 2, 3의 함량 – 서로 다른 네 그루의 계수나무 가지(AT, BT, CT, DT)와 잎(DL)을 파쇄하여 건조한 후 조말로 분쇄하여 나온 분말 시료를 각 1 g씩 정밀히 달아 밀폐용기에 넣고 10 mL 메탄올을 가하여 24시간 환류추출한 후 막여과한 추출액을 HPLC로 정량 하였다(Fig. 3, Table I). 이때 각 화합물에 대한 정량분석법 밸리데이션에 의하여 각 화합물의 검량선의 직선성은 결정계수(r2)가 0.9999로서 양호한 직선성을 보였으며 compound 1의 LOD는 7.72 μg/mL, LOQ는 23.34 μg/mL, compound 2의 LOD는 4.27 μg/mL, LOQ는 12.94 μg/mL, compound 3의 LOD는 8.41 μg/mL, LOQ는 25.48 μg/mL으로 확인되었다. 각 화합물의 정밀성은 상대표준편차로서 0.7% 미만이었으며 정확성은 회수율로서 105% 미만이었다. 분석특이성은 표준물질의 머무름시간과 UV흡수패턴를 비교하여 확인하였다. Compound 1은 각 네 그루의 가지에서 124~156 μg/g의 함량을 보이고 있었으며 10%의 상대표준편차를 보였다. Compound 2는 64~102 μg/g 함량을 보였다. 한 개체(DT)에서는 정량 한계 이하의 낮은 농도를 나타내고 있었으며 함량을 확인할 수 있는 시료의 상대표준편차는 10%이었다. Compound 3은 36~109 μg/g의 농도를 보이며 마찬가지로 한 개체(AT)에서는 정량 한계 이하의 농도로서 검량 할 수 없었다. 검량된 함량의 상대 표준편차는 48%로서 각 개체의 함량변이가 심하였다. 특이하게도 계수나무 잎에서는 분석대상 화합물이 검출되지 않았다. 따라서 계수나무 가지에 함유된 ellagic acid류를 다음 항에서 보여지는 생리효능을 좀더 보완하여 식의약학적으로 응용할 때 상대적으로 함량변이가 낮은 compound 1을 계수나무의 지표성분으로 하는 것이 바람직할 것으로 판단된다.
용매분획별 총 폴리페놀, 총 플라보노이드 함량 – 계수나무 가지의 헥산, 에틸아세테이트, 부탄올 및 물 가용분획물에 대하여 gallic acid를 표준물질로 이용한 총폴리페놀의 함량을 조사하였다(Fig. 4). 그 결과 헥산가용부는 69.04 ± 1.42 GAE mg/g, 에틸아세테이트 가용부는 485.86 ± 6.56 GAE mg/g, 부탄올가용부는 200.64 ± 2.96 GAE mg/g, 물가용부는 3.43 ± 0.86 GAE mg/g이었다. 총 플라보노이드의 함량은 quercetin을 표준물질로하여 측정하였을 때 헥산 가용부는 2.95 ± 0.19 GE mg/g, 에틸아세테이트 가용부는 395.97 ± 3.95 GE mg/g, 부탄올 가용부는 109.92 ± 2.19 GE mg/g, 물 가용부는 16.12 ± 2.19 GE mg/g였다. 에틸아세테이트 및 부탄올 가용부에서 총 폴리페놀 및 플라보노이드 함량이 높은 것은 서론에서 언급한 gallotannins, ellagitannins, anomeric tannins과 flavonoids 같은 폴리페놀화합물의 존재에 기인한 것으로 판단된다.
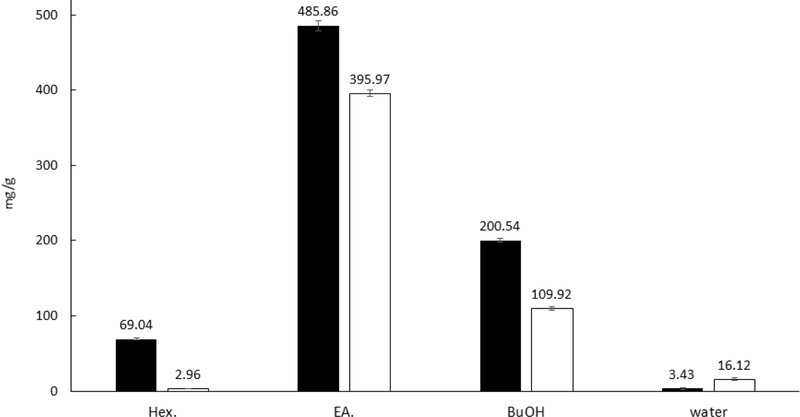
Total polyphenol (gallic acid equvalent, GAE mg/g, ■ black bar) and total flavonoide (quercetin equvalent, QE mg/g, □ white bar) in each solvent extracts from twigs of C. japonicum. Each quantitative value was obtained through three repetitions, and the error bars represent the standard deviation.
용매분획별 항균활성 – 계수나무 가지의 헥산, 에틸아세테이트, 부탄올 및 물 가용분획물에 대하여 phenoxyethanol을 양성대조군으로 하여 디스크확산법으로서 E. coli, S. aureus, P. aeruginosa, C. albicans, A. niger에 대한 생육저해능을 관찰하였다(Table II). 그 결과 에틸아세테이트 가용부에 대하여 E. coli, S. aureus, P. aeruginosa의 생육저지환의 지름은 순서대로 8.0, 14.0, 8.0 mm이었으며 헥산 가용부는 1.0, 1.2, 0.8 mm이었다 부탄올 가용부에서는 S. aureus에서만 8.0 mm로 항균활성을 나타내었다. 물 가용부에서는 항균활성이 나타나지 않았다. C. albicans, A. niger에 대하여서는 모든 가용부에서 생육저지환이 관찰되지 않았다. 따라서 에틸아세테이트 가용부에서만 유의미한 항균활성이 관찰되었으며 이는 에틸아세테이트 가용부에서 분리한 methyl 4-hydroxybenzoate (3)의 농도와 유관할 것으로 추정된다.
DPPH 라디칼 소거능 – 계수나무 가지의 헥산, 에틸아세테이트, 부탄올, 물 가용부 및 분리 정제한 compound 1, 2, 3에 대하여 ascorbic acid를 양성대조군으로 하여 DPPH 라디칼 소거능을 비교하였다(Table III). 양성대조군인 ascorbic acid의 라디칼 소거능은 IC50 값으로 45.1 μg/mL이었으며 헥산 가용부는 215.9 μg/mL, 에틸아세테이트 가용부는 9.9 μg/mL, 부탄올 가용부는 28.2 μg/mL 물 가용부는 효과가 관찰되지 않았다. 에틸아세테이트 가용부로부터 분리된 compound 1은 48.6 μg/mL, 2는 22.0 μg/mL, 3은 99/1 μg/mL이었다. 따라서 에틸아세테이트 가용부에서 분리한 화합물들 중 compound 2가 가장 강한 DPPH 라디칼 소거능을 보였으나 에틸아세테이트 가용부의 라디칼 소거능보다 현저하게 낮은 활성을 보였다. Min 등6)은 계수나무로부터 분리한 가수분해형탄닌이 강한 DPPH활성을 나타내고 있음을 보고한 바 있다. 따라서 에틸아세테이트 가용부에는 본 연구로서 밝히지 못한 강한 항산화 화합물이 존재함을 추정할 수 있다.
타이로시네이즈 활성저해 – 타이로시네이즈는 기질인 L-tyrosine이 DOPA를 거쳐 DOPA quinine으로 산화되는 과정을 촉매하여 멜라닌을 생성한다. Compound 1, 2, 3를 양성 대조군으로 사용된 kojic acid와 비교하여 타이로시네이즈 활성 저해정도를 IC50으로 측정하였다(Table III). 그 결과 양성 대조군인 kojic acid의 IC50 값이 5.6 μg/mL이었으며 compound 2는 70.3 μg/mL로서 양성대조군에 비하여 약하지만 저해능이 관찰되었다. Compound 1, 3는 타이로시네이즈 활성저해능이 없는 것으로 판단되었다.
엘라스틴 분해효소 억제 – 피부조직의 유연성, 신축성에 관여하고 있는 엘라스틴을 분해하는 효소인 elastase의 활성 억제능을 검사하였다. 활성억제정도는 IC50값으로 비교하였다(Table III). 양성대조군으로서 ursolic acid를 사용하였고 이의 IC50값은 306.0 μg/mL이었고 compound 1은 403.6 μg/mL, compound 3은 382.5 μg/mL 로서 양성대조군의 억제능과 비교할 때 의미 있는 엘라스틴분해효소 억제능을 보였다. Compound 2는 저해능이 없는 것으로 판단되었다. 일반적으로 양성대조군으로 사용되는 ursolic acid의 엘라스틴분해효소 억제능은 IC50 값으로서 100 μg/mL 정도에서 관찰되는 것으로 보고11)되어 있으나 본 실험에서는 306.0 μg/mL으로 나타나고 있다.
결 론
계수나무 가지의 에틸아세테이트 분획에서 3,3′-di-O-methylellagic acid-4-O-β-D-glucopyranoside (1), 3,3′,4-tri-O-methyllellagic acid (2), methyl 4-hydroxybenzoate (3)을 분리하여 분광학적 방법으로 구조를 확인하였다. 분리된 3종의 화합물은 계수나무에서 처음 규명된 화합물로 확인하였다. 분리된 화합물 중 compound 1은 계수나무 가지에서 가장 높고 안정적인 함유량을 보이고 있었다. 에틸아세테이트와 부탄올 추출물에서 양성대조군으로 사용된 ascorbic acid보다 강한 DPPH 소거능이 관찰되었으며 분리된 화합물 중에서는 compound 2가 가장 강한 DPPH 라디칼 소거능을 보여주고 있다. 그러나 분리 정제된 화합물보다 추출물 수준의 시료에서 높은 DPPH 라디칼 소거능을 나타내고 있는 것으로 보아 본 실험에서 분리 정제된 화합물들 보다 높은 항산화 성분이 함유되어 있을 것으로 사료된다. compound 2는 타이로시네이즈 활성저해능에 있어서 유의미한 결과를 보여주고 있으며 compound 1은 엘라스틴 분해효소 활성저해능을 나타내고 있다. 폴리페놀과 플라보노이드의 함량은 에틸아세테이트 추출물에서 가장 높게 나타나며 항균활성능도 동일 추출물에서 가장 높게 나타나는 것으로 보아 계수나무 가지의 에틸아세테이트 가용성분에서 다양한 생리활성을 가진 천연성분이 존재할 것으로 기대된다. 향후 계수나무가지에서 의약학적으로 보다 가치 있는 화학성분을 개발하기 위하여 에틸아세테이트 가용부에 함유된 천연물질을 보다 세밀히 분리하여 생리활성을 검사하고 더불어 플라보노이드 및 폴리페놀의 함량과 DPPH 소거 활성이 높은 계수나무 가지의 부탄올 가용부에 대한 성분 연구가 요구되어 진다.
References
-
Petra, T. and Ralf, G. B. (1993) Seasonal variation of the concentrations of maltol and maltol glucoside in leaves of Cercidiphyllum japonicum. J. Sci. Food Agric. 63: 59-61.
[https://doi.org/10.1002/jsfa.2740630110]

-
Lee, T. S. and Bae, Y. (2015) Gallotannin from Cercidiphyllum japonicum leaves. J. Korean Wood Sci. Technol. 43: 558-565.
[https://doi.org/10.5658/WOOD.2015.43.5.558]

-
Lee, M. S., Min, H. J., Kim, J. K. and Bae, Y. S. (2016) A polyoxygenated ellagitannin from Cercidiphyllum japonicum bark. J. Korean Wood Sci. Technol. 44: 551-558.
[https://doi.org/10.5658/WOOD.2016.44.4.551]

-
Si, C. L., Yang, X. H., Li, Z. J., Lu, J. S., Tao, X., Zhang, J. Y., Liu, W. and Bae, Y. S. (2018) Extractives of Cercidiphyllum japonicum twigs: isolation and structural elucidation of a new galloylflavonol glycoside, anomeric tannins and flavonoids. Holzforschung. 72: 719-725.
[https://doi.org/10.1515/hf-2018-0029]

-
Lee, M. S., Min, H. J., Si, C. L. and Bae, Y. S. (2016) Hydrolysable tannins from Cercidiphyllum japonicum bark. J. Korean Wood Sci. Technol. 44: 559-570.
[https://doi.org/10.5658/WOOD.2016.44.4.559]

- Min, H. J., Lee, M. S., Kim, Y. K. and Bae, Y. S. (2017) Evaluation of biological activity on the hydrolyzable tannins of Katsura Tree (Cercidiphyllum japonicum). J. Korean Wood Sci. Technol. 45: 250-257.
-
Lee, T. S., Ryu, W. G. and Bae, Y. S. (2015) α-Glucosidase inhibition activity of the extracts of Katsura tree (Cercidiphyllum japonicum Sieb. Et Zucc) leaves. J. Korean Wood Sci. Technol. 43: 238-247.
[https://doi.org/10.5658/WOOD.2015.43.2.238]

-
Kang, J. Y., Jang, H. S., Kim, J. Y., Lee, M. S., Bae, Y. S., Kwon, Y. S. and Yang, H. J. (2021) Simultaneous determination of four compounds from Cercidiphyllum japonicum using HPLC-UV analysis. Nat. Prod. Sci. 27: 280-283.
[https://doi.org/10.20307/nps.2021.27.4.280]

-
Nono, R. N., Barboni, L., Teponno, R. B., Quassinti, L., Bramucci, M. Vitali, L. A. D., Petrelli, G. and Lupidi, A. L. T. (2014) Antimicrobial, antioxidant, anti-inflammatory activities and phytoconstituents of extracts from the roots of Dissotis thollonii Cogn. (Melastomataceae). S. Afr. J. Bot. 93: 19-26.
[https://doi.org/10.1016/j.sajb.2014.03.009]

-
Wardana, A. P., Abdjan, M. I., Aminah, N. S., Mochamad, Z. F., Imam, S., Alfinda, N. K., Mirza, A. S. and Yoshiaki, T. (2022) 3,4,3′-Tri-O-methylellagic acid as an anticancer agent: in vitro and in silico studies. RSC Adv. 12: 29884-29891.
[https://doi.org/10.1039/D2RA05246F]

-
Kim, I. H. and Lee, J. H. (2022) Skin whitening and anti-wrinkle effects of Chambirum (Amaranthus mangostanus). Asian J. Beauty Cosmetol. 20: 21-31.
[https://doi.org/10.20402/ajbc.2021.0259]