Pseudocyphellaria freycinetii의 메탄올 추출물로부터 분리된 이차대사산물들 및 이들의 세포독성 효과
Abstract
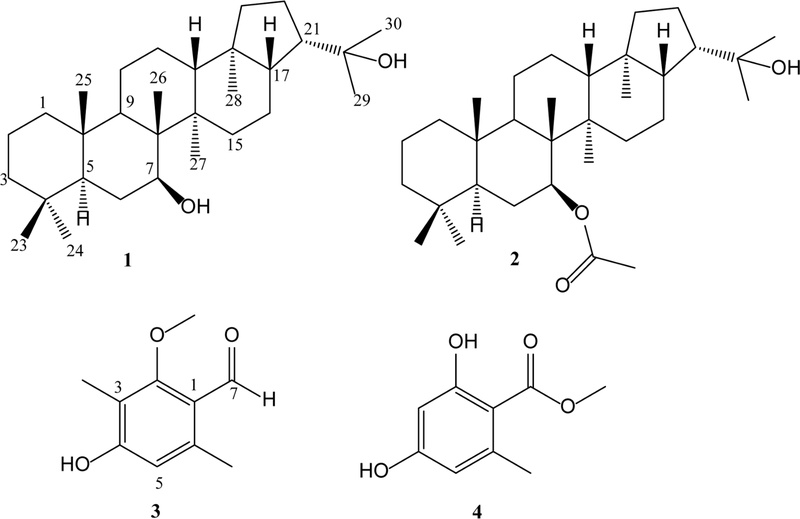
Phytochemical study of the lichen, Pseudocyphellaria freycinetii (Lobariaceae) led to the isolation of two hopane-type triterpenoids (1 and 2), along with two phenolic compounds (3 and 4). The structures of the compounds were identified by 1D and 2D NMR, and MS experiments, as well as by comparison of their data with published values. Compounds 2-4 were isolated for the first time in this species. All the compounds were evaluated for their cytotoxicity. Among the isolates, compound 1 showed considerable inhibitory activity against the Hela cell growth.
Keywords:
Pseudocyphellaria freycinetii, Lobariaceae, Lichen, Hopane-type triterpenoid, Cytotoxicity지의류는 곰팡이와 같은 균류와 녹조류와 같은 조류가 서로 영양분 및 광합성 에너지들을 교환하며 공생관계를 맺고 살아가는 복합 생명체이다.1) 지의류는 해발 6,000 m 이상의 고산, 사막, 적도에서 남.북극 지역까지 모든 환경에 서식하고 있으며 일반 생물들이 살기 어려운 화산 분화 지역 등을 포함한 전 세계 지역에 분포하고 있다.2) 지의류로부터 depsidone 류, dibenzofuran 류, anthraquinone 류 그리고 xanthone 류 등과 같은 다양한 화학성분들이 분리되었으며, 이러한 화합물들은 항생, 항염증, 항산화 및 항암 등의 다양한 생리활성들이 보고되고 있다.3,4)
Pseudocyphellaria (Lobariaceae)는 주로 남쪽의 온대 및 아 남극 지역에 널리 분포되어 있으며 약 170여종을 포함하고 있다.5) P. anthraspis, P. crocata 및 P. berberina들로부터 pulvinic acid 유도체 화합물6,7) P. divulsa, P. exanthematica, P. meyenii 그리고 P. nitide 종들로 부터 zeorin을 포함한 hopane triterpenoid, ergosterol peroxide, tenuiorin, constictic acid, cryptostictic acid, norstictic acid, hyposalazinic acid, stictic acid, leucotylin 등의 화합물들이 보고되었고,7) P. endochrysa 종에서는 calycin과 pulvinic dilactone이 분리되었다.8) 이들 화합물 중 일부 hopane-type triterpenoid는 기생충 억제 작용 및 항암 등의 활성이 있는 것으로 보고되었다.9,10) 우리의 이전 연구에서는 P. freycinetii로부터 분리된 7β,22-dihydroxyhopane 화합물의 교모 세포 종 줄기세포(Glioma Stem Cells)에 대한 억제 작용을 보고하였다.11)
남극 및 아 남극권의 지의류들을 이용한 계속적인 항암제 후보물질 개발 연구 중 P. freycinetii의 메탄올(MeOH) 추출물이 Hela cell (자궁경부암세포)에 대하여 암 세포의 성장을 억제하는 것으로 나타났다. 본 연구에서 P. freycinetii의 메탄올 추출물에 대한 이화학적 연구를 통하여 이미 보고된 7β,22-dihydroxyhopane과 함께 1 종의 hopane-type triterpenoid 유도체 및 2종의 phenol성 화합물들에 대한 물리화학적 분석 자료를 통한 구조 동정 및 분리된 물질들의 여러 암세포들에 대한 억제 활성을 보고한다.
재료 및 방법
실험재료 – 연구에 사용된 지의류는 2017년 1월 칠레의 푼타아레나스에서 채집되었다. 시료는(AL-100) 극지연구소 김지희 박사가 P. freycinetii로 동정을 하였고, 극지연구소 천연물 화학 연구실에 보존되었다.
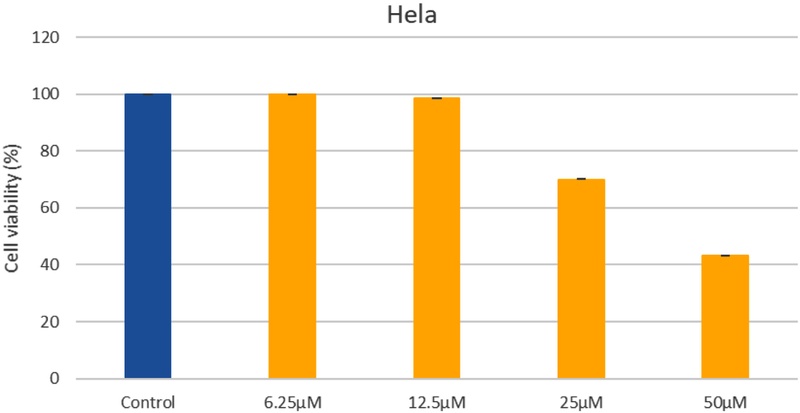
세포독성의 측정 – P. freycinetii의 메탄올 추출물을 DMSO에 용해 한 후 DMEM 배지 또는 RPMI 1640 배지에 6.25, 12.5, 25 그리고 50 µM의 농도로 처리하였다. Hela, B-16 melanoma, LLC cell (2×104 cells/well)를 96-well plate에 배양하였고, 이 후 P. freycinetii로부터 분리된 화합물들을 48시간 동안 50 µM 부터 6.25 µM농도까지 처리하였다. 배양액에 MTT를 처리하고 37°C에서 인큐베이션 하였다. 처리된 세포를 50% DMSO 와 20% SDS을 플레이트에 넣고 마이크로 플레이트 리더를 사용하여 570 nm에서 흡광도를 측정하였다. 생존 세포의 백분율을 다음 공식을 사용하여 계산하였다. 백분율 세포 생존력 = [광학 실험 샘플의 밀도(OD)/대조군의(OD)] × 100을 사용하여 백분율(%)을 계산하였다(Fig. 3).
시약 및 기기 – 1D 및 2D NMR은 Bruker AVANCE (600MHz) spectrometer를사용하였다. Mass spectra는 BioTOF II ESI mass spectrometer를 이용 하였다. TLC는 Merck precoated silica gel F254 plates를 사용 하였으며, 역상 TLC로는 RP-C18 F254s plates가 이용되었다. UV light를 이용하여 254 nm와 365 nm에서 1차적으로 확인하고, 10% sulfuric acid를 이용하여 발색을 확인하였다. Column chromatography에 이용한 충진제는 silica gel 60 (230-400 mesh, Merck, Germany), RP-C18 silica gel (YMC GEL ODS-A, 12 nm, S-75 μm, Japan)과 Sephadex LH-20 (Pharmacia Co. Japan)가 이용되었다. Semi-preparative HPLC는 YL9100 HPLC system (Young Lin, South Korea)을 이용하였고, column으로는 Alltech reversed-phase YMC-PakC-18 column (10 μm, 20 × 250 mm, Japan)을 사용하였다.
추출 및 분리 – 상온에서 음건한 P. freycinetii 100 g을 상온(25°C)에서 methanol (MeOH)을 1 L를 사용하여 1일, 3회 반복하여 저온 침출법으로 추출하였고, 감압농축기를 사용하여 15.2 g의 메탄올 추출물을 얻었다. 얻어진 추출물은 증류수(H2O, 1L)로 희석하였고 극성에 따라 hexane (Hex), ethyl acetate (EtOAc), butanol (BuOH) 순으로 각 1 L, 3회씩 순차적으로 분획하여 Hex (1.5 g), EtOAc (2.9 g), BuOH (3.1 g) 및 H2O 분획물(3.7 g)을 얻었다. 얻어진 분획물들 중 TLC 분석을 통하여 Hex 분획물에서 주요 화합물들이 포함된 것을 확인하였으며, Hex 분획물에 대하여 우선적으로 분리를 시도하였다. Hex 분획물(1.5 g)은 silica gel column을 사용하여 CHCl3:MeOH (99:1‒9:1)의 이동상 용매 조건으로 분리를 실시하였고, 총 12개의 분획물들을 얻었다(HS. 1‒HS. 12). 분획물들 중 HS. 6 (309 mg)을 다시 Sephadex-LH-20 gel column과 이동상 용매로 MeOH:H2O (70:30)를 이용하여 5개의 소분획(HS. 6.1‒HS. 6.5)들을 얻었으며, 그 중 분획물 HS. 6.4 (81 mg)을 semi-preparative HPLC와 60%MeOH의 이동상 용매를 사용하여 화합물 3 (5 mg)을 얻었다. 분석용 TLC에서 황산 발색 법에 의하여 두개의 주요 화합물이 관측된 분획물 HS. 8 (950 mg)을 silica gel column을 사용하여 Hex:EtOAc (9:1-7:3)의 이동상 용매로 분리를 실시하였다. 이로부터 하얀색의 무형 고체들이 관찰된 소분획물 HS. 8.2와 HS 8.4를 얻었으며, hexane:EtOAc (1:1)용매를 이용한 재결정법으로 화합물 1 (143 mg)과 2 (383 mg)를 각각 얻었다. 분획물 HS. 9 (40 mg)에 대하여 H2O:MeOH (50:50)의 용매 조건에서 Sepadex LH-20 gel column을 사용하여 5개의 소분획물(HS. 9.1‒HS. 9.5)들을 얻었고, 이들 중 HS. 9.3번은 semi-preparative HPLC (85% MeOH)를 사용하여 화합물 4 (5 mg)를 얻었다.
7β,22-Dihydroxyhopane (1) – 무형의 하얀색 고체; +25.2° (c 0.2, CHCl3); 1H-NMR (600 MHz, CDCl3): δ 3.88 (1H, m, H-7), 2.22 (1H, m, H-21), 2.23 (1H, m, H-6b), 1.78 (1H, m, H-20a), 1.71 (1H, m, H-15a), 1.65 (1H, m, H-1a), 1.65 (1H, m, H-3a), 1.63 (1H, m, H-6a), 1.55 (1H, m, H-5b), 1.54 (1H, m, H-16b), 1.52 (1H, m, H-11b), 1.52 (1H, m, H-20b), 1.51 (1H, m, H-2b), 1.51 (1H, m, H-3a), 1.51 (1H, m, H-15a), 1.46 (1H, s, H-17), 1.45 (1H, m, H-12a), 1.37 (1H, m, H-2a), 1.34 (1H, m, H-11a), 1.34 (1H, m, H-19b), 1.30 (1H, s, H-13), 1.29 (1H, m, H-16a), 1.21 (3H, s, CH3-30), 1.18 (3H, s, CH3-29), 1.13 (1H, m, H-19a), 1.05 (3H, s, CH3-27), 1.00 (3H, s, CH3-26), 0.84 (3H, s, CH3-23), 0.82 (3H, s, CH3-28), 0.79 (3H, s, CH3-24), 0.76 (3H, s, CH3-25), 0.72 (1H, H-1a), 0.72 (1H, s, H-5); 13C-NMR (150 MHz, CDCl3): δ 74.8 (C-7), 73.7 (C-22), 55.7 (C-5), 50.5 (C-9), 50.4 (C-21), 50.3 (C-17), 48.1 (C-13), 47.1 (C-8), 44.2 (C-18), 43.5 (C-14), 41.9 (C-19), 40.9 (C-3), 40.4 (C-1), 37.5 (C-10), 36.8 (C-15), 33.2 (C-23), 33.2 (C-4), 32.5 (C-6), 30.9 (C-30), 28.7 (C-29), 26.9 (C-20), 24.1 (C-12), 21.6 (C-24), 20.8 (C-16), 18.9 (C-11), 18.7 (C-2), 17.4 (C-27), 15.8 (C-28), 15.7 (C-25), 11.7 (C-26); (+)ESI-MS: m/z 445 [M+H]+.
7β-Acetoxy-22-hydroxyhopane (2) – 무형의 하얀색 고체; + 23.5° (c 0.2, CHCl3); 1H-NMR (600 MHz, CDCl3): δ 5.64 (1H, s, H-7), 2.22 (1H, s, H-21), 1.96 (3H, s, OCOCH3), 1.89 (1H, m, H-16b), 1.75 (1H, m, H-20b), 1.74 (1H, m, H-6b), 1.64 (1H, m, H-2b), 1.58 (1H, m, H-11b), 1.58 (1H, m, H-15b), 1.56 (1H, m, H-2b), 1.56 (1H, m, H-15a), 1.56 (1H, m, H-16b), 1.54 (1H, m, H-19b), 1.49 (1H, m, H-20a), 1.46 (1H, s, H-5), 1.44 (1H, s, H-17), 1.41 (1H, m, H-11a), 1.41 (2H, m, H-12), 1.39 (1H, m, H-2a), 1.39 (1H, m, H-6a), 1.38 (1H, s, H-9), 1.37 (1H, m, H-3b), 1.25 (1H, s, H-13), 1.20 (3H, s, CH3-30), 1.17 (3H, s, CH3-29), 1.12 (1H, m, H-3a), 1.08 (3H, s, CH3-26), 1.03 (3H, s, CH3-27), 0.94 (1H, m, H-19a), 0.86 (3H, s, CH3-23), 0.82 (3H, s, CH3-28), 0.75 (1H, m, H-1a), 0.75 (3H, s, CH3-25); 13C-NMR (150 MHz, CDCl3): δ 170.5 (OCOCH3), 75.9 (C-7), 73.9 (C-22), 53.3 (C-17), 52.7 (C-5), 51.5 (C-21), 50.5 (C-13), 49.9 (C-9), 46.4 (C-8), 44.1 (C-18), 43.2 (C-14), 41.7 (C-3), 41.5 (C-19), 40.1 (C-1), 37.3 (C-10), 36.6 (C-15), 33.1 (C-4), 33.0 (C-23), 30.9 (C-30), 28.8 (C-29), 25.5 (C-20), 25.7 (C-6), 23.9 (C-12), 22.3 (C-16), 21.9 (OCOCH3), 21.5 (C-24), 20.4 (C-11), 18.6 (C-2), 17.8 (C-27), 16.0 (C-28), 15.5 (C-25), 12.5 (C-26); (+)ESI-MS: m/z 487 [M+H]+.
3,6-Dimethyl-4-hydroxy-2-methoxybenzaldehyde (3) − 무형의 하얀색 고체; 1H-NMR (600 MHz, CD3OD): δ 10.5 (1-CHO), 6.99 (1H, s, H-5), 3.97 (3H, s, 2-OCH3), 2.55 (3H, s, 6-CH3), 2.16 (3H, s, 3-CH3); 13C-NMR (150 MHz, CD3OD): δ 188.1 (C-7), 166.0 (C-4), 163.1 (C-2), 147.8 (C-6), 122.6 (C-1), 114.0 (C-3), 111.8 (C-5), 54.9 (2-OCH3), 20.7 (6-CH3), 8.5 (3-CH3); (+)ESI-MS: m/z 182 [M+H]+.
2,4-Dihydroxy-6-methylbenzoate (4) − 무형의 하얀색 고체; 1H NMR (600 MHz, CD3OD): δ 6.18 (1H, d, J=2.4 Hz, H-5), 6.13 (1H, d, J=2.4 Hz, H-3), 3.89 (3H, s, 7-OCH3), 2.44 (3H, s, 6-CH3); 13C-NMR (150 MHz, CD3OD): δ 173.5 (C-7), 166.3 (C-2), 164.5 (C-4), 144.5 (C-6), 112.8 (C-5), 105.6 (C-1), 101.9 (C-3), 52.1 (7-OCH3), 24.4 (6-CH3); (+)ESI-MS: m/z 180 [M+H]+.
결과 및 고찰
P. freycinetii의 메탄올 추출물로부터 얻은 Hex 분획물에 대하여 open column chromatography로 분리한 후 semi-preparative HPLC를 실시하여 기존 보고된 화합물 1번 외에 3 종의 화합물들을 분리하였다(Fig. 1).
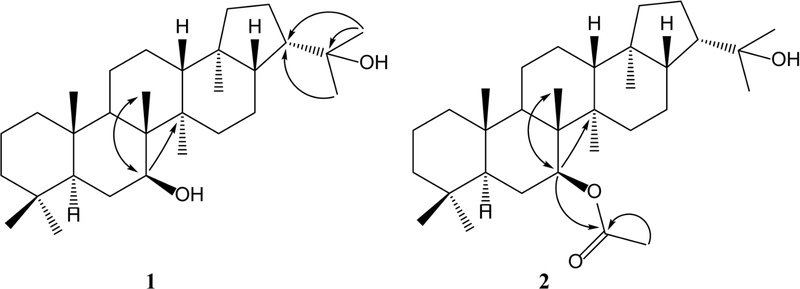
화합물 1은 ESI-MS 분석에서 m/z 445[M+H]+의 molecular ion 관측을 통하여 분자량 444를 유추할 수 있었다. 이 화합물의 1H-NMR spectrum 분석한 결과 hopane-type triterpenoid (C30-triterpenoid) 구조에서 보여지는 8개의 특징적인 singlet methyl기 [δH 1.18 (H-29), 1.21 H-30), 1.05 (H-27), 1.00 (H-26), 0.84 (H-23), 0.82 (H-28), 0.79 (H-24), 0.76 (H-25)]들과 δH 3.84 (H-7)에서 oxygenated methine proton을 확인하였다. 13C- 및 DEPT135 NMR, HSQC 분석을 통하여 δC 73.7 (C-22)에서 하나의 oxygenate quaternary carbon과 δC 74.8 (C-7)에서 1개의 oxygenated methine carbon들을 관측하였다. 또한, δC 33.2 (C-23), δC 21.6 (C-24), δC 15.7 (C-25), δC 11.7 (C-26), δC 17.4 (C-27), δC 15.8 (C-28), δC 28.7 (C-29), δC 30.9 (C-30)에서 8개의 methyl carbon들을 포함하여 총 30개의 탄소를 관측하였다. 이로부터 화합물 1은 hopane-type triterpenoid 화합물로 확인되었으며, zeorin의 구조와 매우 유사하였다.7) 1H-13C HMBC 실험에서 H-7 (δH 3.84)와 C-26 (δC 11.7)/C-14 (δC 43.5)들과의 상관관계를 확인 함으로써 OH group이 7번 위치의 탄소에 치환되어 있음을 확인하였다. 추가적으로 H-29 (δH 1.18)과 H-30 (δH 1.21)의 methyl proton들은 δC 50.4 (C-21)/73.7 (C-22)들과의 HMBC correlation을 확인함으로서 나머지 OH group이 치환된 2-hydroxypropyl group은 C-21번에 연결되어 있음을 확인하였다(Fig. 2). 화합물 1의 optical rotation 값(+ 25.2°)은 문헌 값( + 26.3°)과 비교하여 매우 유사함을 나타내었으며,12) 이로부터 7번 탄소에서 OH group은 β-form으로 결정되었다. 화합물 1은 1D와 2D NMR 분석 값 과 문헌 값과의 비교를 통하여 7β,22-dihydroxyhopane의 구조로 확인하였다.
화합물 2의 1H-NMR 및 13C-NMR 분석에서 화합물 1의 chemical shift들과 유사한 패턴을 보였다. 그러나, 화합물 1에서의 methine proton (δH 3.84, H-7)은 화합물 2에서는 δH 5.07까지 저자장 영역으로 이동한 것을 관측하였고, δH 1.96 (OCOCH3)에서 acetyl group에 치환된 methyl group proton의 특징적인 signal을 하나 더 나타내었다. 13C-NMR spectrum에서는 하나의 ester carbonyl carbon (δC 170.5)이 관측 되었으며, HMBC 분석을 통해 δH 5.07 (H-7)/δH 1.96 (-CH3)와 δC 170.5 (OCOCH3)에서의 carbonyl carbon과 상관관계를 확인함으로써 화합물 2은 화합물 1의 C-7번 위치에서 OH group 대신 acetyl group이 치환되어 있음을 확인 하였다(Fig. 3). 따라서, δH 5.07에서 관측된 methine proton은 acetyl group의 deshielding effect로 인하여 OH group이 치환되어 있을 때 보다 더 저자장 영역으로 이동된 것으로 보인다. 화합물 2의 optical rotation 값은( + 23.5°) 화합물 1의 값과 유사함을 나타내었으며, C-7에서의 acetyl group 또한 β-form으로 결정되었다. 따라서, 화합물 2번은 화합물 1과의 NMR data 비교, 2D-NMR 분석 및 문헌 값과의 비교에 의하여 7β-acetoxy-22-hydroxyhopane으로 동정하였다.13)
화합물 3의 1H-NMR spectrum 분석은 δH 6.99 영역에서 하나의 aromatic proton이 관측되었다. 고자장 영역에서 δH 2.16 (3H, s, H-3) 과 δH 2.55 (3H, s, H-6)의 관측은 2개의 methyl기의 존재를 유추하였고, δH 10.53 (H-1) 영역에서 하나의 aldehyde proton과 δH 3.97 (2-OCH3)의 영역에서 하나의 methoxy proton signal을 확인하였다. 화합물 3의 HSQC spectrum을 통해 1H- 및 13C-NMR 값들을 확인 하였다. 따라서, 화합물 3은 NMR 데이터 와 문헌 값을 비교하여 3,6-dimethyl-4-hydroxy-2-methoxybenzaldehyde로 확인하였다.14)
화합물 4의 1H-NMR spectrum은 화합물 3의 signal들과 매우 유사하였으나 AB type의 aromatic proton 두개가 관측되었고 이들의 coupling constant value (J = 2.4 Hz)로 두개의 proton들이 서로 meta 위치에 있음을 알 수 있었다. 또한 화합물 3에서 methyl group이 2개가 관측된 반면 화합물 4에서는 한 개만 관측하였다. HMBC 실험을 통해 δH 3.89 (7-OCH3)이 δC 173.5 (C-7) carbonyl carbon과 상관관계를 확인함으로써 화합물 4은 화합물 3의 7번 탄소(C-7) 위치에 aldehyde 대신 δH 3.89 (3H, s, 7-OCH3)에서 보여진 methoxy group이 치환된 구조임을 알 수 있었다. 화합물 4의 NMR결과들과 문헌의 데이터와 비교하여 2,4-dihydroxy-6-methylbenzoate로 확인하였다.15)
이전의 연구에서 교모 세포 종 줄기세포(Glioma Stem Cells)에 대한 강한 억제 작용이 보고된 화합물 1에 대한 자세한 구조 분석은 물리화학적 방법과 1D 및 2D NMR 분석법을 통하여 다시 한번 본 연구에 언급하였으며,11) 이번 연구에서 P. freycinetii의 메탄올 추출물로부터 화합물 1을 포함하여 처음으로 분리된 화합물들(2–4)에 대하여 여러 암세포 종에 대한 억제 실험을 진행하였다.
P. freycinetii로부터 분리된 화합물들은 B-16 melanoma, LLC, Hela cell들에 대하여 암세포 억제 실험을 실시하였고, 이들 중 화합물 1은 Hela cell에 대하여 6.25 µM ~ 50 µM까지 처리하였을 때 25 µM부터 농도 의존적으로 암세포 억제 활성을 보였다. 그러나, 나머지 암세포주들에서는 활성을 나타내지 않았다. 특히, 50 µM 처리된 농도에서 Hela 세포에 대하여 43%로 중간 정도의 억제 활성을 보였다(Fig. 3).
Hopane-type triterpene 화합물들의 암세포 억제에 대한 많은 연구가 이루어져 있지는 않지만 몇몇 연구들을 살펴보면, Sichaem 등(2019)의 연구에서 Parmotrema sancti-angelii로부터 여러 hopane-type triterpenoid들을 분리하였는데 이들 중 6α-acetoxyhopane-16β,22-diol 화합물이 HepG2, NCI-H400 그리고 MCF-7cell에서 IC50 값이 각각 52.67, 77.86, 47.08 µg/mL로 세포독성 효과를 보였고,16) 작은 땅 빈대 식물로 알려진 Euphorbia peplus에서 분리된 Friedo-hopane type triterpene에서는 C-22번위치의 OH group이 항암 활성에 중요한 역할을 하는 것으로 보고되었다.17) Wang 등(2009)의 연구에서는 내염성 균류, Aspergillus variecolor B-17로부터 hopane-type triterpenoid들을 분리하였고, 이들 중 C-2번 위치에 OH group이 치환된 형태의 2-hydroxydiplopterol 화합물이 K562 cell에 대해(IC50 22 µM)의 농도로 억제 활성이 보고되었다.18)
본 연구에서 화합물 1과 구조적으로 유사한 2번 화합물에서는 활성을 보이지 않았다. 이는 화합물 1과 비교하였을 때 7번 탄소 위치에서 acetyl group보다 OH group이 치환되어 있을 때 Hela cell에 대한 억제 활성이 강함을 유추할 수 있다.
결 론
P. freycinetii의 메탄올 추출물로부터 얻은 Hex 분획물에 대하여 open column chromatography등 여러 분리법을 사용하여 기존에 보고된 7β,22-dihydroxyhopane (1) 외에, 7β-acetoxy-22-hydroxyhopane (2), 3,6-dimethyl-4-hydroxy-2-methoxybenzaldehyde (3), 2,4-dihydroxy-6-methylbenzoate (4) 화합물들을 처음으로 분리하였다.
분리된 화합물들을 B16 melanoma, LLC 및 Hela cell에 대하여 cytotoxicity 실험을 실시한 결과 화합물 1번에만 Hela cell을 농도 의존적으로 억제하는 것을 발견하였다. 본 연구 결과 및 이전의 관련 유도체들의 연구들로부터 앞으로 다양한 hopane-type triterpene 화합물들에 대한 구조 활성 연구들이 필요해 보이며, 본 연구를 바탕으로 Hela cell을 포함한 다양한 암세포들에 대하여 이들의 성장을 억제하는 선도 화합물로서의 역할이 기대된다.
Acknowledgments
본 연구는 극지연구소의 KOPRI (PN25170) 과제의 지원을 받아 수행 되었다.
References
-
Kaasalainen, U., Kukwa, M., Rikkinen, J. and Schmidt, A. R. (2019) Crustose lichens with lichenicolous fungi from Paleogene amber. Sci. Rep. 9: 10360.
[https://doi.org/10.1038/s41598-019-46692-w]

-
Hidalgo, M. E., Fernández, E., Quilhot, W. and Lissi, E. A. (1994) Antioxidant capacity of depsides and depsidones. Phytochemistry 37: 1585-1587.
[https://doi.org/10.1016/S0031-9422(00)89571-0]

-
Kumar KC, S. and Müller, K. (1999) Lichen metabolites. 1. Inhibitory action against leukotriene B4 biosynthesis by a non-redox mechanism. J. Nat. Prod. 62: 817-820.
[https://doi.org/10.1021/np9803777]

-
Nguyen, T. T., Yoon, S., Yang, Y., Lee, H. B., Oh, S., Jeong, M. H. and Lee, K. Y. (2014) Lichen secondary metabolites in Flavocetraria cucullata exhibit anti-cancer effects on human cancer cells through the induction of apoptosis and suppression of tumorigenic potentials. PloS one 9: e111575.
[https://doi.org/10.1371/journal.pone.0111575]

- Kirk, P. M., Cannon, P. F., Minter, D. M. and Stalpers, J. A. (2008) Dictionary of the Fungi (10th ed), 568. Wallingford, CABI.
-
Brodo, I. M., Sharnoff, S. D. and Sharnoff, S. (2001) Lichens of North America, Yale University Press, New Haven.
[https://doi.org/10.29173/bluejay5827]

-
Piovano, M., Chamy, M. C. and Garbarino, J. A. (2001) Studies on Chilean lichens XXXI: Additions to the chemistry of Pseudocyphellaria. Bol. Soc. Chilena Quim. 46: 23-27.
[https://doi.org/10.4067/S0366-16442001000100005]

- Bjerke, J. W. and Elvebakk, A. (2004) Comparison of morphological, anatomical and chemical charcters in Pseudocyphellaria endochrysa and P. vaccina (Lobariaceae, lichenized Ascomycota). Ann. Bot. Fenn. 41: 27-35.
-
Fritis, M. C., Lagos, C. R., Sobarzo, N. Q., Venegas, I. M., Sánchez, C. S., Altamirano, H. C., Catalán, L. E. and Palma, W. Q. (2013) Depsides and triterpenes in Pseudocyphellaria coriifolia (lichens) and biological activity against Trypanosoma cruzi. Nat. Prod. Res. 27: 1607-1610.
[https://doi.org/10.1080/14786419.2012.740033]

-
Yang, Y., Nguyen, T. T., Pereira, I., Hur, J.-S. and Kim, H. (2019) Lichen secondary metabolite physciosporin decreases the stemness potential of colorectal cancer cells. Biomolecules 9: 797.
[https://doi.org/10.3390/biom9120797]

-
Kim, H.-J., Suh S.-S., Park, J., Shin, M.-J., Koo, M. H., Lee, S. J., Jeon, Y.-J., Lee, S., Youn, U.-J. and Kim, S.-H. (2022) 7β,22-Dihydroxyhopane, isolated from the sub-antarctic lichen, inhibits the viability and stemness in glioma stem like cells. Oncotargets Ther. 15: 1375-1383.
[https://doi.org/10.2147/OTT.S371042]

-
Cuellar, M., Quilhot, W., Rubio, C., Soto, C., Espinoza, L. and Carrasco, H. (2008) Phenolics, depsides and triterpenes from the Chilean lichen Pseudocyphellaria nudata (Zahlbr.) D.J. Galloway. J. Chil. Chem. Soc. 53: 1624-1625.
[https://doi.org/10.4067/S0717-97072008000300017]

-
Howarth, O. W., Rickard, T. M. A. and Sainsbury, M. (1983) The antarctic lichens: 1—The stereochemistry of 7β‐acetoxy‐22‐hydroxyhopane from Pseudocyphellaria freycinettii, indigenous to S. Georgia. Org. Magn. Reson. 21: 56-59.
[https://doi.org/10.1002/omr.1270210115]

-
Kawahara, N., Nozawa, K., Nakajima, S., Udagawa, S. I. and Kawai, K. I. (1988) Studies on fungal products. XVI.: New metabolites related to 3-methylorsellinate from Aspergillus silvaticus. Chem. Pharm. Bull. 36: 398-400.
[https://doi.org/10.1248/cpb.36.398]

-
Sakurai, A. and Goto, Y. (1987) Chemical studies on the lichen. I. The structure of isolecanoric acid, a new ortho-depside isolated from Parmelia tinctorum despr. Bull. Chem. Soc. Jpn. 60: 1917-1918.
[https://doi.org/10.1246/bcsj.60.1917]

-
Sichaem, J., Nguyen, H. H. and Duong, T. H. (2019) Hopane-6α, 16α, 22-triol: A new hopane triterpenoid from the lichen Parmotrema sancti-angelii. Nat. Prod. Commun. 14: 1934578X19858208.
[https://doi.org/10.1177/1934578X19858208]

-
Yu, J.-H., Wu, D.-X., Yu, Z.-P., Li, Y.-P., Wang, Y.-Y., Yu, S.-J. and Zhang, H. (2019) New e:b-friedo-hopane type triterpenoids from Euphorbia peplus with simiarendiol possessing significant cytostatic activity against Hela cells by induction of apoptosis and S/G2 cell cycle arrest. Molecules 24: 3106.
[https://doi.org/10.3390/molecules24173106]

-
Wang, W.-L., Liu, P.-P., Zhang, Y.-P., Li, J., Tao, H.-W., Gu, Q.-Q. and Zhu, W.-M. (2009) 2-Hydroxydiplopterol, A new cytotoxic pentacyclic triterpenoid from the halotolerant fungus Aspergillus variecolor B-17. Arch. Pharm. Res. 32: 1211-1214.
[https://doi.org/10.1007/s12272-009-1904-8]