
칠해목 메탄올 추출물의 항파킨슨 효과
Abstract
Parkinson's disease (PD) is a multifactorial neurodegenerative disorder driven by the complex interplay of oxidative stress, mitochondrial dysfunction, dysregulated dopamine metabolism, and α-synuclein aggregation. Despite extensive efforts, effective pharmacological interventions are still lacking that can target and regulate these pathological factors to cure PD. In this study, we investigated the neuroprotective potential of the Ribes fasciculatum methanolic extract (MRF) in Caenorhabditis elegans PD model. MRF treatment significantly attenuated dopaminergic neuronal loss and improved locomotor function in both wild-type worms exposed to MPP⁺ and cat-2-overexpressing mutants. In addition, MRF reduced intracellular ROS accumulation and enhanced survival under MPP⁺-induced oxidative stress condition. Furthermore, it reduced α-synuclein aggregation and oligomer formation in NL5901 transgenic worms, suggesting the inhibition of proteotoxicity. These findings indicate that MRF exerts multi-target protective effects by concurrently modulating redox balance, protein homeostasis, and mitochondrial function. The findings underscore the therapeutic promise of MRF as a multifaceted modulator that can address the intricate pathophysiology of PD.
Keywords:
Ribes fasciculatum, Parkinson's disease, Alpha-synuclein, Neurodegenerative disease, Dopaminergic neuron파킨슨병(Parkinson's disease, PD)은 중대뇌 흑질의 도파민 신경세포가 점진적으로 사멸하면서 운동 지연, 경련, 인지 장애 등을 초래하는 대표적인 신경퇴행성 질환이다.1) 특히, 도파민 신경세포 내에 알파-시누클레인(α-synuclein) 단백질이 비정상적으로 응집된 루이소체의 형성이 특징적으로 나타난다. 파킨슨병은 명확한 단일 원인보다는 여러 병인 인자가 복합적으로 작용하는 다요인성 질환으로 알려져 있다. 현재까지 알파-시누클레인 단백질의 응집, 도파민 대사 이상, 미토콘드리아 기능 저하 등 다양한 병리적 경로가 파킨슨병의 발병과 연관된 것으로 제시되어 왔으며, 이들 기전에서 산화 스트레스가 공통된 매개 요인으로 작용함이 밝혀지고 있다.2) 실제로 파킨슨병 환자의 뇌조직에서는 산화된 지질, 단백질 및 DNA의 축적이 관찰되는 등 만성적인 산화적 손상의 근거가 보고된 바 있다.3)
MPP⁺(1-methyl-4-phenylpyridinium)는 도파민 수송체를 통해 도파민 신경세포에 선택적으로 유입되는 신경독성 물질로, 파킨슨병의 병태생리를 모사하는 실험 모델로 널리 사용되고 있다. 세포 내로 유입된 MPP⁺는 미토콘드리아 전자 전달계 complex I의 활성을 저해하여 ATP 생성 저해와 함께 과도한 활성산소종(reactive oxygen species, ROS)의 생성을 유도함으로써, 도파민 신경세포의 기능 저하와 세포사멸을 초래한다.2) 도파민 대사 과정 또한 ROS의 주요 발생 경로로 작용하며, 알파-시누클레인의 기능이 손실될 경우 도파민 축적과 산화 스트레스의 악화로 이어진다.4,5) 이처럼 알파-시누클레인 응집, 도파민 산화, 미토콘드리아 기능 저하는 각각 독립적인 병인처럼 보이지만, 실제로는 ROS을 매개로 서로 긴밀히 연계되어 병리적 변화를 증폭시킨다. 따라서 산화 스트레스의 조절은 복합적인 병리 기전을 동시에 완화할 수 있는 효과적인 접근법으로 주목받고 있다.
파킨슨병 치료에 복합 병인 조절의 필요성이 부각되면서, 최근 천연물 유래 물질들이 다중표적 작용(multi-targeting)으로 신경보호 효과를 나타낼 수 있음에 관심이 증가하고 있다. 한 예로, 커큐민(curcumin)은 항산화 및 항염증 작용을 통해 파킨슨병 모델에서 알파-시누클레인 응집을 억제하고 도파민 신경세포의 사멸을 완화하는 효과가 보고된 바 있다.6)
칠해목(Ribes fasciculatum)은 우리나라에서 자생하는 다년생 관목으로, 전통적으로 옻나무 수액에 의한 피부 자극을 완화하는 데 사용되어 왔다. 현재까지 보고된 칠해목의 약리작용 및 구성 성분에 대한 연구는 매우 제한적이나, 선행 연구에 따르면 항노화, 항알레르기, 항염증, 진통 효과 등이 보고된 바 있다.7-11) 특히 과산화수소로 유도한 신경세포 독성 모델에서 칠해목 추출물이 신경세포 생존율을 높이고 산화 손상을 억제하는 효과가 보고된 바 있으며,12) catechin, gallocatechin, quercitrin 등 항산화 활성을 지닌 성분들이 칠해목으로부터 분리되었다고 알려져 있다.7) 선행 연구 결과를 종합해 볼 때, 칠해목 추출물이 도파민 신경보호 효능이 있을 것으로 추정되어 본 연구에서는 도파민 신경세포를 가지고 있고 신경 퇴행 매커니즘이 잘 보존되어 있는 예쁜꼬마선충(Caenorhabditis elegans) 모델을 이용해 칠해목 메탄올 추출물(methanolic extract of Ribes fasciculatum, MRF)의 항파킨슨 효과를 조사하였다.
재료 및 방법
실험재료 – 실험에 사용된 재료(칠해목, Ribes fasciculatum)는 전북특별자치도에 위치한 해인약업사에서 구입하였으며, 전용덕 교수(우석대학교 한약학과)의 감정을 거쳐 건조하여 (WH083) 우석대학교 약학대학 한약학과에 보관하였다. 건조된 줄기 및 가지 3 kg은 메탄올(12,000 mL)을 용매로 초음파 추출기에서 50℃로 2 시간 동안 추출하였으며, 이후 회전식 농축기를 이용해 100.64 g(수율 : 3.021%)으로 농축하였다. 최종 추출물은 동결 건조 후 –20℃에서 보관하였다.
실험동물 – 본 실험에 사용된 예쁜꼬마선충(Caenorhabditis elegans) Bristol N2 및 대장균(Escherichia coli) OP50 균주를 포함한 모든 선충 계통은 Caenorhabditis Genetic Center (CGC; University of Minnesota, Minneapolis, MN)로부터 분양받았다. 실험에 사용된 형질전환 선충은 NL5901 (pkIs2386, unc-54p::alphasynuclein::YFP), BZ555 (egIs1, Pdat-1::GFP), UA57 (baIs4, Pdat-1::GFP; Pdat-1::CAT-2), TK22 (kn1, mev-1)이 있다. 선충은 E. coli OP50를 도말한 nematode growth medium (NGM) 한천 배지에서 20℃로 배양하였으며,13) 칠해목 추출물은 D.W.에 적절한 농도로 용해한 후 멸균된 NGM 배지에 첨가하였다.
생존 실험 – 동일한 성장 단계(L1)의 선충을 0, 25, 50, 100 μg/mL 농도의 칠해목 추출물이 포함된 액체 배지에서 2시간 동안 전처리한 후, 1 mM MPP+를 처리하였다. 24시간 경과 후 선충의 생존 여부를 평가하였으며, 백금 와이어에 의한 물리적 자극에 반응하지 않는 개체는 사멸한 것으로 판정하였다.
도파민 신경퇴화 평가 – 성장 단계가 동일한(young adult) BZ555 선충을 칠해목 추출물이 첨가된 다양한 농도의 액체 배지에서 2시간 동안 전처리한 뒤, 4 mM MPP+를 처리하여 96시간 동안 배양하였다. UA57 선충은 칠해목 추출물이 포함된 NGM 배지에서 L4 단계부터 14일간 배양하였다. 도파민 신경세포의 형태학적 분석을 위해 선충을 20% sodium azide로 마취한 후 형광현미경(Nikon Eclipse Ni-u, Japan)을 이용하여 8개 도파민 신경(4 CEP, 2 ADE, 2 PDE)에 발현된 형광단백질(GFP)의 형광 신호를 관찰하였다.
먹이 탐지 능력검정 – 본 연구에서는 도파민 신경 기능 중 하나인 먹이 탐지 능력(basal slowing movement)을 평가하기 위해 Sawin의 방법을 일부 변형하여 적용하였다.14) 성장 단계가 동일한 성체 1일차 선충을 OP50가 없는 배지와 있는 배지에 옮긴 후, NIS program (Nikon Imaging Software, Japan)을 이용하여 이동 거리를 측정하였다. 이후 두 조건 간 이동 거리의 감소율을 산출하여 선충의 먹이 탐지 능력을 분석하였다.
선충 세포 내 활성산소종 측정 – 동일한 성장단계의 N2 선충을 칠해목 추출물이 농도별로 처리된 배지에서 배양한 후, 성체 1일차에 4 mM MPP+을 처리하여 1시간 동안 산화스트레스를 주었다. 이후 H2DCF-DA (25 μM)를 첨가한 후, microplate reader (Glomax-Multi+, Promega, USA)를 사용해 excitation 490 nm, emission 510-570 nm 조건에서 0, 30, 60, 90분 간격으로 형광 강도를 측정하였다.
운동성 및 몸체 요동 측정 – UA57 선충을 L4 단계부터 다양한 농도의 칠해목 추출물이 첨가된 NGM 배지에서 14일간 배양한 후, M9 buffer로 세 차례 세척하여 먹이가 없는 배지로 옮겼다. 이후 30초 동안의 이동 거리를 NIS program (Nikon Imaging Software, Japan)을 이용해 측정하였으며, 동일한 개체를 두 번 반복 관찰하여 평균값을 산출하였다. 선충의 몸체 요동은 M9 buffer 내에서 머리와 꼬리가 같은 방향으로 굽는 횟수를 기준으로 10초간 측정하였으며, 마찬가지로 동일 개체에 대해 두 차례 측정하여 평균값을 구하였다.
알파-시누클레인 응집 분석 – 알파-시누클레인 응집에 대한 약물의 효과를 평가하기 위해 인간 알파-시누클레인을 발현하는 형질전환 선충 NL5901 (α-synuclein::YFP)을 사용하여 실험을 수행하였다. 동일한 성장 단계의 선충을 NGM 배지에서 성체 4일까지 배양한 후, 알파-시누클레인에 결합한 YFP 형광 신호 관찰을 위해 10% sodium azide로 마취시켜 형광현미경(Nikon Eclipse Ni-u, Japan)으로 분석하였다. 알파-시누클레인의 발현 강도는 촬영된 형광 이미지를 ImageJ 소프트웨어로 정량 분석하여 평가하였다.
도트블롯분석 – 알파-시누클레인의 응집 정도를 평가하기 위해 NL5901 선충을 성체 4일차에 M9 buffer로 3회 세척한 후, 단백질을 추출하였다. 단백질 추출은 homogenization buffer (10 mM Tris-HCl, 150 mM NaCl, 0.1 mM EDTA, pH 7.5)를 사용하여 선충을 분쇄하는 방식으로 수행하였다. 정량한 단백질 시료 10 μL를 nitrocellulose membrane에 점적한 뒤, 5% skim milk로 처리하였다. 이후 membrane은 oligomer 및 fibril에 특이적인 1차 항체(1:3000, 5% skim milk 희석)에 1시간 반응시켰으며, 세척은 PBST로 3회 수행하였다. 이어서 HRP가 결합된 rabbit 2차 항체(1:5000, 1×PBS 희석)를 사용하여 oligomer는 1시간, fibril은 2시간 동안 면역 반응시킨 후, PBST로 5회 세척하였다. 표지 반응은 제조사 지침에 따라 ECL 키트(Bio-Rad, Berkeley, CA, USA)를 이용해 검출하였으며, 각 밴드의 강도는 ImageQuant 소프트웨어를 사용하여 densitometry로 정량 분석하였다.
통계 분석 – 통계 분석은 OriginPro 소프트웨어 2023 (10.0)을 이용하여 수행하였고, 모든 데이터는 평균 ± 표준편차(mean ± S.D.)로 표시하였다. 그룹 간 유의성 평가는 oneway ANOVA 후 Tukey 사후검정을 통해 실시하였고, 통계적 유의성은 각각 *p < 0.05, **p < 0.01, ***p < 0.001 수준에서 판정하였다.
결과 및 고찰
MPP+로 유도된 도파민 신경퇴화에 대한 칠해목 추출물의 보호 효과 – 본 연구에서는 파킨슨병 모델 선충을 이용하여 칠해목 추출물의 도파민 신경보호 효과를 평가하였다. 먼저 도파민 신경세포의 선택적 퇴화를 유도하는 MPP⁺ 독성에 대한 생존율을 분석한 결과, MPP⁺ 처리에 따라 선충의 생존율은 43.73%로 감소하였으나, 100 μg/mL의 칠해목 추출물을 병행 처리한 군에서는 77.49%로 유의한 증가를 보였다(Fig. 1A). 다음으로, 도파민수송체(dat-1p)에 형광단백질이 결합된 형질전환 선충(BZ555)을 이용하여 도파민 신경세포의 형태적 변화를 관찰하였다. MPP⁺를 처리한 대조군에서는 도파민 신경세포의 소실 또는 퇴화가 관찰되었으나(51.86%), 칠해목 추출물 처리군에서는 농도 의존적으로 신경세포 보존 효과가 나타났고(65.28%, 74.20%, 85.63%), 최고 농도에서는 대조군 대비 30.47% 높은 보존율을 보였다(Fig. 1B, 1C). 이에 따라 칠해목 추출물의 신경보호 효과가 도파민 신경 기능의 회복으로 이어지는지를 확인하고자 도파민 신경계에 의해 조절되는 먹이 탐지 능력(basal slowing response)을 분석하였다. 실험 결과, 정상 선충은 먹이 노출 시 이동 속도가 82.70% 감소했지만, MPP⁺ 처리군은 27.45% 감소에 그쳤다. 반면, 칠해목 추출물을 처리한 선충에서는 농도 의존적으로 먹이 탐지 능력이 회복되었으며, 최고 농도에서 64.93%의 감속 반응을 보였다(Fig. 1D). 이러한 결과는 칠해목 추출물이 도파민 신경세포의 형태적 손상뿐만 아니라 기능적 손상 또한 효과적으로 완화할 수 있음을 시사한다.
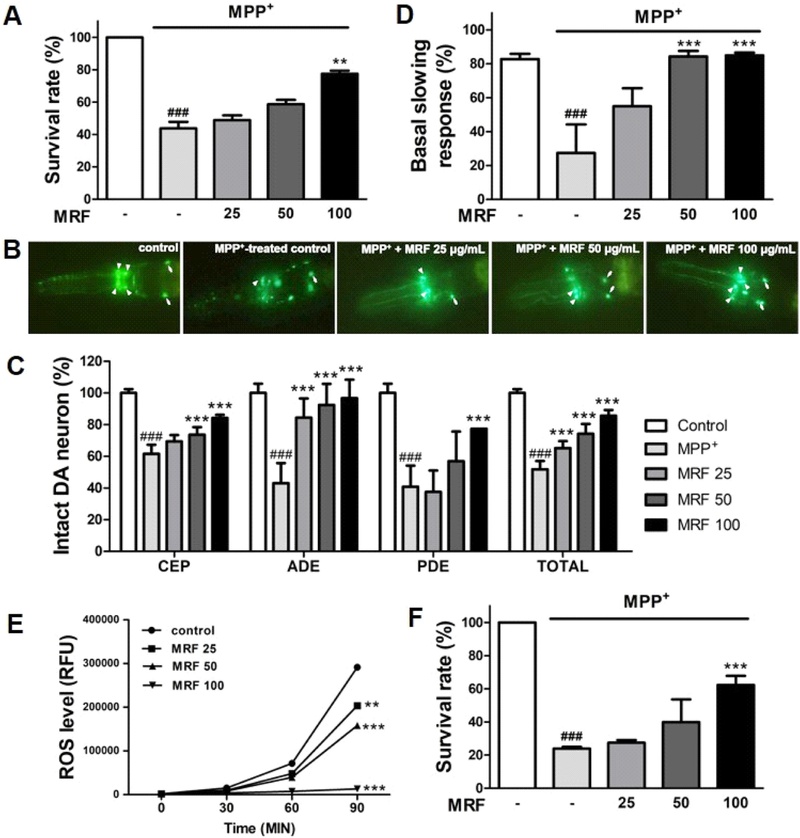
Effects of MRF on the chemically-induced DA neurodegeneration in C. elegans. (A) Survival rate of wild-type worms following 24 h exposure to 1 mM MPP⁺ from the L1 stage. (B) GFP expression in the dopaminergic neurons of 4mM MPP⁺-treated transgenic BZ555 worms (Pdat-1::GFP) was visualized under a fluorescence microscope at 400× magnification. The key features highlighted include the cell bodies of cephalic (arrowhead) and anterior deirid (arrow) neurons. (C) All eight DA neurons were manually assessed by analyzing GFP fluorescence of BZ555 worms. (D) The basal slowing response was calculated by measuring the velocity of 4mM MPP⁺-treated wild-type worms on both food-coated and non-coated plates. (E) Intracellular ROS levels measured spectrophotometrically at excitation 490 nm and emission 510–570 nm, recorded every 30 min for 90 min. (F) Survival rate of TK22(mev-1) worms following 24 h exposure to 1 mM MPP⁺ from the L1 stage. Data represent mean ± S.D. from three independent experiments. ###p < 0.001 vs. vehicle-treated control; **p < 0.01, ***p < 0.001 vs. MPP⁺-treated control.
도파민 신경세포의 보존 및 기능 회복 효과가 확인됨에 따라, 본 연구에서는 해당 효과가 산화 스트레스 경감과 관련이 있는지를 규명하고자 ROS 조절 능력을 분석하였다. ROS은 세포 신호전달과 항상성 유지에 필수적이나, 과도하게 축적될 경우 DNA, 지질, 단백질을 손상해 세포사멸을 유발할 수 있다.15) 특히 뇌는 높은 대사율과 풍부한 불포화지방산, 낮은 항산화 방어 능력으로 인해 산화 스트레스에 취약한 기관이다.16) 이에 본 연구에서는 산화 스트레스 조건에서 칠해목 추출물의 ROS 조절 효과를 분석하였으며, 칠해목 추출물 처리군에서 세포 내 ROS 생성이 농도 의존적으로 유의하게 감소함을 확인하였다(Fig. 2E). 이러한 선충 내 ROS 제거 효과는 mev-1 돌연변이 선충을 이용한 추가 실험에서도 확인되었다. mev-1 돌연변이는 미토콘드리아 전자전달계 복합체 II의 구성 요소인 succinate dehydrogenase cytochrome b의 기능 이상으로 인해 ROS 생성이 증가하며, 산화 스트레스에 민감한 것으로 알려져 있다.17) 해당 모델을 이용한 생존율 분석 결과, MPP⁺ 처리 시 칠해목 추출물 처리군은 대조군(23.85%) 대비 유의하게 높은 생존율(62.27%)을 보였다(Fig. 2F). 이러한 결과는 칠해목 추출물이 산화 스트레스에 취약한 조건에서도 도파민 신경세포를 효과적으로 보호하며, ROS 조절을 통해 미토콘드리아 기능과 에너지 대사의 회복에 관여했을 가능성을 보여준다.
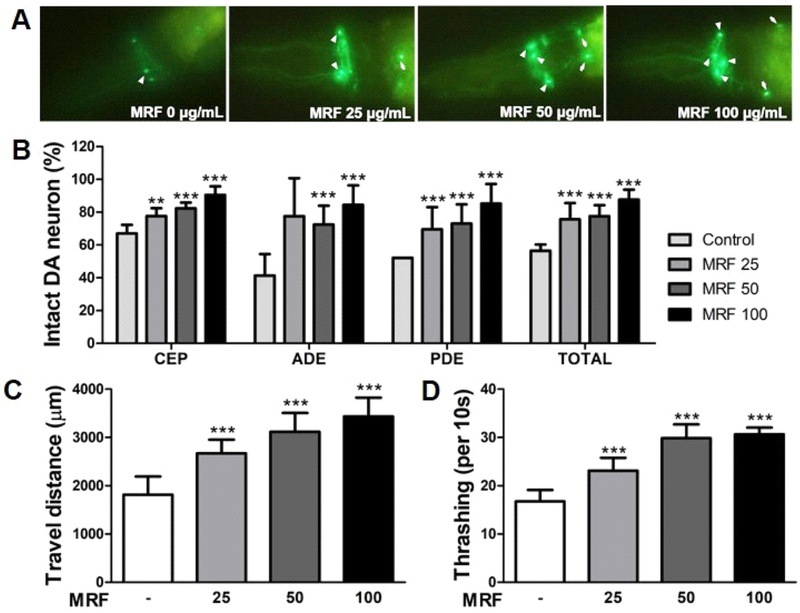
Effects of MRF on the genetically-induced DA neurodegeneration in C. elegans (A) Representative GFP fluorescence in dopaminergic neurons of aged UA57 worms (Pdat-1::GFP; Pdat-1::CAT-2), imaged at 400× magnification using a fluorescence microscope. The key features highlighted include the cell bodies of cephalic (arrowhead) and anterior deirid (arrow) neurons. (B) Quantification of intact DA neurons in UA57 worms based on manual analysis of GFP signals from all eight neurons. (C) The travel distance of aged UA57 worms was monitored and recorded using a behavioral tracking system. (D) Body thrashing behavior was observed for 10 seconds in the same group of worms. Data are presented as mean ± S.D. from three independent experiments. **p < 0.01 and ***p < 0.001 vs. vehicle-treated control.
유전적 요인에 대한 칠해목 추출물의 신경보호 효과 – 도파민 대사 이상이 유도하는 신경퇴행에 대한 칠해목 추출물의 신경보호 효과를 평가하기 위해, tyrosine hydroxylase(TH)의 선충 상동유전자인 cat-2를 과발현 하는 형질전환 선충(UA57)을 활용하였다. 도파민 생합성의 속도 제한 효소인 TH의 과발현은 도파민 산화를 증가시키며, 이 과정에서 생성되는 ROS과 3,4-dihydroxyphenylacetaldehyde(DOPAL)와 같은 반응성 대사산물은 신경세포 독성을 유발한다.18) 특히 DOPAL은 α-시누클레인의 구조를 변형시켜 응집을 유도하는 것으로 알려져 있으며, 이는 in vitro 및 in vivo 연구뿐 아니라 파킨슨병 환자의 뇌 조직에서도 관찰된 바 있다.19, 20) 이러한 병리적 기전을 바탕으로, 본 연구에서는 UA57 모델에서 칠해목 추출물의 신경보호 효과를 분석하였다. 그 결과, 대조군의 도파민 신경세포 보존율이 56.46%에 불과했던 반면, 추출물 처리군에서는 농도 의존적으로 보존율이 증가하였으며, 최고 농도에서는 87.66%에 도달하였다(Fig. 2A, 2B). 이러한 신경세포 보존은 기능적 회복으로도 이어져, 최고 농도 처리 시 선충의 이동 거리는 대조군 대비 89.47% 증가하였고, 몸체 요동(thrashing) 빈도 역시 82.99% 향상되었다(Fig. 2C, 2D). 이러한 결과는 칠해목 추출물이 도파민 대사 이상에 의해 유도된 신경 퇴행에 대해서도 유의한 보호 효과를 나타낼 수 있음을 시사한다.
알파-시누클레인 축적 및 응집에 대한 칠해목 추출물의 억제 효과 – 파킨슨병에서 알파-시누클레인의 비정상적인 축적은 주요 병리 특징으로, 루이소체(Lewy bodies)라 불리는 단백질 내포물 형성을 유도하며 도파민 신경세포 손상과 밀접하게 관련되어 있다.21) 특히, 응집된 알파-시누클레인은 ROS 및 도파민 대사 산물과 상호작용하여 다양한 세포 내 독성 반응을 유발하고 병태를 악화시킨다.22) 이러한 알파-시누클레인의 축적은 도파민 신경세포의 퇴행 및 기능 저하로 이어지며, 이는 선충 모델에서도 유사하게 관찰된다. 이에 따라 본 연구에서는 형질전환 돌연변이인 NL5901를 활용하여 알파-시누클레인 과형성 및 응집의 변화에 대한 칠해목 추출물의 효과를 분석하였다. 실험 결과, 칠해목 추출물의 투여에 따라 알파-시누클레인의 응집이 감소함을 확인하였으며, 최고 농도에서 대조군 대비 19.66%의 감소를 나타냈다(Fig. 3A, 3B). 알파-시누클레인은 루이소체 형성 과정에서 oligomer 및 fibril 형태로 응집되며, 최근 연구에서 루이소체 자체보다도 이전 단계의 oligomer 알파-시누클레인이 주요한 신경독성 원인임을 강조하고 있다.22) Oligomer보다 구조적으로 더 응축된 형태인 fibril은 추가적인 응집체 형성을 유도하지 않지만, oligomer는 알파-시누클레인 단량체 및 다른 oligomer와 결합해 응집을 촉진하며, 이로 인해 미토콘드리아 손상을 유도하고 도파민 신경세포에 독성을 유발하는 것으로 보고되어 있다.23) 이에 본 연구에서는 알파-시누클레인 응집 억제 효과를 보다 정밀하게 분석하기 위해 도트 블롯(dot blot) 분석으로 응집체의 형태 변화를 관찰하였다. 그 결과, 칠해목 추출물 처리군에서는 대조군 대비 oligomer가 39.95%, fibril은 39.76% 감소하였다(Fig. 3C, 3D). 이러한 응집 억제에는 알파-시누클레인 단백질의 발현 감소가 일부 기여했을 가능성이 있으며, 이는 나아가 응집체 형성을 저해함으로써 단백질 분해 시스템(프로테아좀 및 오토파지)의 부담을 줄이고, 단백질 항상성(proteostasis) 유지와 함께 시냅스 기능 저하, 축삭 수송 장애, 미토콘드리아 및 소포체 스트레스 등 병리적 변화의 완화를 통해 도파민 신경세포 기능 보전에 기여했을 것으로 판단된다.24) 알파-시누클레인의 병리적 축적은 이처럼 세포 내 항상성을 무너뜨릴 뿐만 아니라, 도파민 대사산물 및 ROS과의 상호작용을 통해 미토콘드리아 기능 저하 등 다른 주요 병리 기전과도 긴밀히 연결되어 있다. 이러한 연관성을 고려할 때, 본 연구에서 확인된 칠해목 추출물의 알파-시누클레인 응집 억제 효과는 MPP+ 유도 신경독성 및 도파민 대사 이상에 대한 보호 효과와 상호작용하며, 파킨슨병의 복합적인 병태생리를 조절할 수 있을 것으로 기대된다. 이러한 결과는 칠해목 추출물이 복합적인 발병기전에 대응할 수 있는 천연물 기반 후보물질로서의 가치를 지님을 시사하며, 이를 더욱 명확히 규명하기 위한 후속 연구가 필요할 것으로 판단된다.
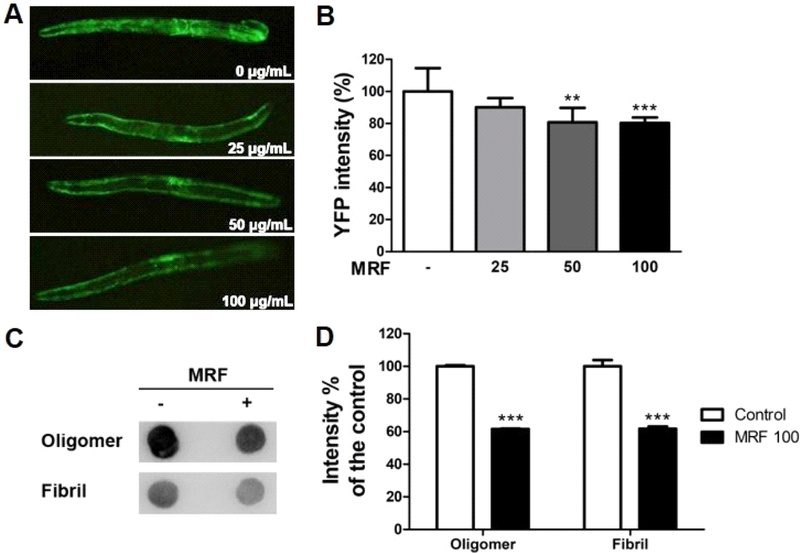
Effects of MRF on the α-synuclein aggregation in C. elegans (A) Representative YFP fluorescence images of NL5901 (unc-54p::α-synuclein::YFP). (B) Quantification of YFP fluorescence intensity, expressed as a percentage relative to the vehicle-treated control group. (C) α-synuclein aggregation assessed by immune dot-blot analysis using lysates from NL5901 worms. (D) Densitometric quantification of dot-blot signals, expressed as relative intensity compared to the control. Data are presented as mean ± S.D. from three independent experiments. **p <0.01 and ***p <0.001 vs. vehicle-treated group.
결 론
본 연구에서는 선충 모델에서 칠해목 메탄올 추출물이 도파민 신경보호에 미치는 효과를 평가하였다. 칠해목 추출물의 투여는 MPP+ 및 TH 과발현으로 유도된 도파민 신경퇴화에 대해 우수한 보호 효과를 나타냈으며, 이러한 신경보호 작용은 칠해목의 산화 스트레스 완화 효과와 밀접한 관련이 있는 것으로 확인되었다. 또한, 파킨슨병의 핵심 마커인 알파-시누클레인의 응집을 유의하게 감소시키는 효과도 관찰되었다. 이상의 결과는 칠해목 추출물이 다양한 기전을 통해 도파민 신경세포 보호 효능을 나타내며, 향후 파킨슨병 치료제 개발에 있어 천연물 기반 후보물질로 활용될 가능성을 시사한다.
References
-
Bernheimer, H., Birkmayer, W., Hornykiewicz, O., Jellinger, K. and Seitelberger, F. (1973) Brain dopamine and the syndromes of Parkinson and Huntington Clinical, morphological and neurochemical correlations. J. Neurol. Sci. 20: 415-455.
[https://doi.org/10.1016/0022-510X(73)90175-5]

-
Puspita, L., Chung, S. Y. and Shim, J. W. (2017) Oxidative stress and cellular pathologies in Parkinson’s disease. Mol. Brain 10: 53.
[https://doi.org/10.1186/s13041-017-0340-9]

-
Jenner, P. (2003) Oxidative stress in Parkinson’s disease. Ann. Neurol. 53(S3): S26-S36.
[https://doi.org/10.1002/ana.10483]

-
Burbulla, L. F., Song, P., Mazzulli, J. R., Zampese, E., Wong, Y. C., Jeon, S., Santos, D., Blanz, J., Obermaier, C. D., Strojny, C., Steger, J. and Krainc, D. (2017) Dopamine oxidation mediates mitochondrial and lysosomal dysfunction in Parkinson’s disease. Science 357: 1255-1261.
[https://doi.org/10.1126/science.aam9080]

- Wong, Y. C. and Krainc, D. (2018) Alpha-synuclein toxicity in neurodegeneration: mechanism and therapeutic strategies. Nat. Med. 24: 127-138.
-
Mythri, B. R. and Bharath, M. S. (2012) Curcumin: a potential neuroprotective agent in Parkinson's disease. Curr. Pharm. Des. 18: 91-99.
[https://doi.org/10.2174/138161212798918995]

-
Dat, N. T., Cai, X. F., Shen, Q., Lee, I. S. and Kim, Y. H. (2005) New inhibitor against nuclear factor of activated T cells transcription from Ribes fasciculatum var. chinense. Chem. Pharm. Bull. 53: 114-117.
[https://doi.org/10.1248/cpb.53.114]

- Jeon, H. (2013) Anti-nociceptive properties of Ribes fasciculatum. Nat. Prod. Sci. 19: 311-315.
- Jeon, H. and Cha, D. S. (2016) Anti-aging properties of Ribes fasciculatum in Caenorhabditis elegans. Chin. J. Nat. Med. 14: 335-377.
- Kim, J. K., Kim, H. N., Kang, C. S., Seo, J. H., Seo, H. W., Im, J. S., Kim, B. S., Cha, D. S., Kwon, J., Oh, C. H., Ma, S. Y., Nam, J. I. and Jeon, H. (2014) Anti-inflammatory effect of Ribes fasciculatum in IFN-γ/LPS-stimulated mouse peritoneal macrophage. Nat. Prod. Sci. 20: 113-118.
- Lee, J. Y., Jeong, J. A., Lee, H. J., Oh, S., Kim, S. and Jung, J. (2011) The anti-allergic effect of Ribes fasciculatum var. chinense MAX in vivo model. Yakhak Hoeji 55: 141-148.
- Park, J. W., Kim, J. H., Lee, Y. and Cha, D. S. (2018) Neuroprotective and antioxidant effects of Ribes fasciculatum extract against oxidative stress. Kor. J. Pharmacogn. 49: 287-293.
-
Brenner, S. (1974) The genetics of Caenorhabditis elegans. Genetics 77: 71-94.
[https://doi.org/10.1093/genetics/77.1.71]

-
Sawin, E. R., Ranganathan, R. and Horvitz, H. R. (2000) C. elegans locomotory rate is modulated by the environment through a dopaminergic pathway and by experience through a serotonergic pathway. Neuron 26: 619-631.
[https://doi.org/10.1016/S0896-6273(00)81199-X]

-
Halliwell, B. (2006) Oxidative stress and neurodegeneration: where are we now? J. Neurochem. 97: 1634-1658.
[https://doi.org/10.1111/j.1471-4159.2006.03907.x]

- Wakamatsu, M., Tabuchi, K., Ojika, M. and Nagatsu, T. (2019) Tyrosinase and DOPAL in the presence of ferric ions enhance alpha-synuclein oligomerization. Neurotox. Res. 35: 710-718.
-
Ishii, N., Fujii, M., Hartman, P. S., Tsuda, M., Yasuda, K., Senoo-Matsuda, N. and Suzuki, K. (1998) A mutation in succinate dehydrogenase cytochrome b causes oxidative stress and ageing in nematodes. Nature 394: 694-697.
[https://doi.org/10.1038/29331]

-
Daubner, S. C., Le, T. and Wang, S. (2011) Tyrosine hydroxylase and regulation of dopamine synthesis. Arch. Biochem. Biophys. 508: 1-12.
[https://doi.org/10.1016/j.abb.2010.12.017]

-
Burke, W. J., Kumar, V. B., Pandey, N., Panneton, W. M. and Gan, Q. (2008) Aggregation of α-synuclein by DOPAL, the monoamine oxidase metabolite of dopamine. Acta Neuropathol. 115: 193-203.
[https://doi.org/10.1007/s00401-007-0303-9]

- Faustini, G., Longhena, F., Bruno, A., Bono, F., Missale, C., Pizzi, M. and Bellucci, A. (2023) DOPAL-induced α-synuclein oligomers impair synaptic transmission and axonal transport in dopaminergic neurons. Neurobiol. Dis. 176: 105954.
-
Devine, M. J., Gwinn, K., Singleton, A. and Hardy, J. (2011) Parkinson’s disease and alpha-synuclein expression. Mov. Disord. 26: 2160-2168.
[https://doi.org/10.1002/mds.23948]

-
Marques, O. and Outeiro, T. F. (2012) Alpha-synuclein: from secretion to dysfunction and death. Cell Death Dis. 3: e350.
[https://doi.org/10.1038/cddis.2012.94]

-
Luth, E. S., Stavrovskaya, I. G., Bartels, T., Kristal, B. S. and Selkoe, D. J. (2014) Soluble, prefibrillar α-synuclein oligomers promote complex I-dependent, Ca2+-induced mitochondrial dysfunction. J. Biol. Chem. 289: 21490-21507.
[https://doi.org/10.1074/jbc.M113.545749]

-
Chinta, S. J., Mallajosyula, J. K., Rane, A. and Andersen, J. K. (2010) Mitochondrial alpha-synuclein accumulation impairs complex I function in dopaminergic neurons and results in increased mitophagy in vivo. Neurosci. Lett. 486: 235-239.
[https://doi.org/10.1016/j.neulet.2010.09.061]
