진피(Citrus reticulata)와 제주자생 진귤(Citrus sunki) 과피의 효능 및 지표성분 함량 비교연구
Abstract
The peel of Citrus has traditionally been used as a herbal medicine known as Chenpi, with Citrus reticulata officially listed in the Korean Pharmacopoeia for its antioxidant, anti-inflammatory, and digestive benefits. However, much of the Chenpi used in Korea is imported from China, and current pharmacopoeial standards include only C. reticulata and C. unshiu, limiting the use of native Korean citrus varieties. This study aimed to evaluate the potential of Citrus sunki, a native citrus species from Jeju Island, for inclusion in the Korean Pharmacopoeia, based on the Swingle and Tanaka classification systems. The Swingle system, which classifies C. sunki as C. reticulata, was used as a basis to provide scientific evidence for its inclusion through a comparison of their biological activities. DNA sequencing identified the Jeju-native variety Jingyul as C. sunki, while commercial Chenpi products and other Jeju citrus peels were identified as C. reticulata. HPLC analysis showed that C. sunki contained hesperidin levels comparable to or higher than those of C. reticulata. Furthermore, C. sunki demonstrated equivalent or superior antioxidant, skin-whitening, anti-wrinkle, and anti-inflammatory activities. These findings suggest that C. sunki has comparable therapeutic potential to Chenpi, supporting its inclusion in the Korean Pharmacopoeia. The study also underscores the importance of an integrative classification approach considering pharmacological efficacy in evaluating herbal medicines.
Keywords:
Citrus sunki, Citrus reticulata, Swingle system, Tanaka system, Hesperidin감귤은 중국 남부와 동남아시아를 원산지로 하며 현재는 전 세계적으로 재배된다.1,2) 특히 따뜻한 기후에서 잘 자라기 때문에 한국, 일본, 지중해 지역 등에서 재배되고 있다.3) 감귤류(Citrus)의 분류는 매우 복잡하며 다양한 품종이 존재한다. 감귤은 동남아시아의 열대 및 아열대 지역에서 유래한 것으로 추정되며 이후 다른 지역으로 퍼져 교배와 돌연변이 과정을 거치면서 지금의 다양성을 이루었다.4,5) 감귤은 수세기에 걸쳐 재배되어 왔으며 이러한 과정에서 자발적 체세포 돌연변이(somatic mutation)로부터 품종이 선택되는 경우가 많아 일부 감귤류 종들은 원래의 정체성을 잃거나 유전적으로 매우 복잡한 계통을 형성하게 되었다.6) 또한, 핵배아성(nucellar embryony)에 의한 무성 생식이 활발하게 일어나 모종의 특징이 그대로 자손에게 전달되므로 자연적인 품종 변이가 감소하는 결과를 초래하며7) 자연과 인공적인 교잡이 용이해 인공 잡종 뿐 아니라 자연 잡종이 활발히 형성된다.8)
감귤류의 다양한 변종을 구분하는데에는 Swingle과 Tanaka가 각각 제안한 두 가지 대표적인 분류 체계가 있으며, 이들은 분류 기준과 세분화 정도에서 상이한 접근 방식을 보인다. Swingle system은 1943년 미국의 식물학자인 Swingle에 의해 제안된 체계로, 감귤류를 Citrus 속과 Fortunella 속 두 개의 속으로 나누고 16가지 종으로 분류하는 방식이다.9) Swingle은 감귤류를 분류할 때 단순하고 통합적인 방식을 선호했으며 몇 개의 주요 종으로 구분하고 나머지 변종은 이들 종의 교배를 통해 발생했다고 설명하였다.9) 이 system은 형태적 차이보다는 진화적 계통과 유전적 연관성을 강조한 통합적 접근 방식으로, 감귤류의 복잡한 관계를 이해하는 데 유용한 체계이다.10) 반면 Tanaka system은 1954년 일본의 식물학자인 Tanaka에 의해 제안된 체계로, Swingle system보다 훨씬 세분화하여 감귤의 다양한 형태적 변이와 지역별 차이를 인정하면서 더 많은 종으로 분류하였으며 총 162종으로 나눈다.10,11) 이러한 방식은 지역별 품종 특성을 보다 구체적으로 설명하는 데 유용한 분류 방식이다.11)
C. reticulata는 감귤류 교잡 품종의 기초가 되는 핵심 종으로, 다양한 감귤 품종의 기원이 되지만 잡종과의 교잡 및 변이로 인해 분류가 어렵다. Scora (1975)는 생화학적 연구를 기반으로 감귤류 중 C. reticulata, C. medica, C. grandis 세 개의 종만을 독립적인 종으로 인정하였다.12)
감귤류의 과피를 말려 한약재로 사용하는 진피는 중국에서 수입되는 주요 한약재 중 하나로, 한국과 중국을 비롯해 동아시아 지역에서 전통적으로 소화 촉진, 기침 완화, 소화기 질환을 개선시키는 약재로 사용되어 왔다.13,14) 진피는 1953년 중국약전(Chinese Pharmacopoeia, CP)에 등록이 되었으며 C. chachi, C. dahongpao, C. wenzhou migan, C. unshiu, C. tangerina를 포함하며 폭넓은 품종 범위를 인정하고 있다.15) 반면, 대한약전(Korean Pharmacopoeia, KP)에는 C. unshiu Markovich와 C. reticulata Blanco (운향과 Rutaceae)만 등재되어 있으며 상대적으로 제한적인 품종 범위를 규정하고 있다. 한편, 진귤(Citrus sunki)은 제주 지역에서 자생하는 감귤류로서 산물 혹은 산귤로 불린다. 중국 남부 및 동아시아에서 기원하였으며 C. reticulata와 유전학적으로 밀접한 관련이 있다.16) Swingle system에서는 C. reticulata의 아종으로, Tanaka system에서는 별도의 종으로 분류된다.17)
제주도는 국내 감귤의 주요 생산지로, 2023년 기준 감귤 생산량은 약 60만톤에 달했다.18) 그러나 국내에서 사용되는 진피의 상당 부분은 여전히 중국에서 수입되고 있다. 식품의약품안전처(식약처)가 2018년 보고한 바에 따르면 우리나라의 진피 수입량은 약 150톤이었으며 2024년에는 약 260톤으로 1.7배 증가한 것으로 나타났다.19) 이는 한약재 및 건강기능식품 시장의 성장에 따라 진피 수요가 지속적으로 증가하고 있음을 보여준다. 그러나 이러한 수요 증가에도 불구하고 국내 감귤을 활용한 진피의 공급은 제한적이며 이에 따라 중국산 진피에 대한 의존도가 높아지고 있다. 이는 품질관리, 가격변동, 수입 제한 등의 문제를 초래할 수 있어 국내 진피의 안정적인 공급망 구축이 필요하다.
진귤은 대한약전에 등재되어 있지 않지만 전통적으로 한의학에서 중요한 한약재로 활용되어 왔다.20) 특히 진귤의 과피는 소화기능 증진과 기침 완화 등의 효능이 보고되어 있으며 최근 연구결과에서는 항산화 및 항염 효과가 입증되었다.20) 따라서 국내에서 생산되는 감귤류, 특히 진귤을 활용한다면 중국산 진피에 대한 의존도를 줄이고 국산 생약 자원의 활용 범위를 확대할 수 있을 것이다. 이에 본 연구에서는 제주에서 자생하는 진귤(C. sunki)의 효능과 유효 성분을 분석하고, 이를 진피 한약재 규격품(국산, 중국산), 제주자생 감귤의 과피(C. reticulata)와 비교하여 효능적 측면에서 활용 가능성을 평가하고자 하였다. 나아가, 진귤의 약전 등재 가능성을 검토하고 국산 생약 자원의 활용 범위를 확대할 근거를 마련하고자 하였다.
재료 및 방법
실험재료 – 진피 한약재 규격품은 2 02 4년 2월 조화제약(국산), 나음제약(중국산)에서 구입하였다. 제주자생 감귤의 과피는 2 02 3년 9월 제주특별자치도 서귀포시 예래동 및 하효동, 2024년 1월 제주특별자치도 제주시 애월읍 어음리에서 각각 채집되었다. 모든 실험재료는 국립생약자원관에 보관되어 있다.
Ascorbic acid, 1,1-diphenyl-2-picrylhydrazyl (DPPH), 2,2'-azino-bis-(3-ethylbenzothiazoline-6-sulfonic acid) (ABTS), dimethyl sulfoxide (DMSO), lipo-polysaccharide (LPS), 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide (MTT), griess reagent, sodium nitrite는 Sigma-Aldrich Co. (St. Louis, MO, USA)에서 구입하였다. Dulbeco's modified Eagle's medium (DMEM), penicillin-streptomycin (P/S), DEPC water는 welgene (Gyeongsan, Korea)에서, fetal bovine serum (FBS)는 Atlas Biologicals (Fort Collins, CO, USA)에서 각각 구입하였다. RNAiso Plus는 Takara Bio Inc. (Kusatsu, Japan)에서, chloroform은 Daejung (Seongnam, Korea)에서, 2-propanol은 Wako (Tokyo, Japan)에서 구입하였으며, tumor necrosis factor-α (TNF-α), interleukin-6 (IL-6), interleukin-1β (IL-1β), iNOS, β-actin은 Integrated DNA Technologies (Coralville, IA, USA)에서 구입하였다. TranScript® All-in-One Firest-Strand cDNA synthesis SuperMix for qPCR (One-Step DNA Removal), TransGen Biotech Co. (Beijing, China), Power SYBR® Green PCR Master Mix는 Thermo Fisher Scientific (Rockford, IL, USA)에서 구입하였다. 이 외 시약은 시중에서 구할 수 있는 최상급을 사용하였다.
DNA 분석 – DNA 추출을 위해 시료 약 0.01 g을 준비하고, CTAB buffer를 사용하여 DNA를 추출하였다.21) 시료에 CTAB buffer 900 μL와 β-mercaptoethanol 5 μL를 첨가한 뒤, 65°C에서 30분간 반응시켰다. 이후, CIA (chloroform : isoamyl alcohol, 24:1)로 2회 처리하고 원심분리하여 핵산이 포함된 상층액을 확보하였다. 이 상층액을 silica magnetic bead로 정제하고 70% EtOH 500 μL로 bead를 2회 세척하고 건조한 뒤, 50 μL의 TE buffer에 재현탁하여 핵산을 용출하였다. DNA polymerase chain reaction (PCR)을 위해 반응물의 조성을 주형 DNA 약 5 ng, 1 unit의 hot-start Taq polymerase, 2 μL의 10X PCR buffer, 2 mM MgCl2, 0.2 mM dNTP, 각 5 pM의 primer 쌍으로 구성하고, distilled water (D.W)를 첨가하여 총 반응 부피를 20 μL로 조절하였으며, 분석에 사용된 primer 염기서열은 Table I과 같다. ProFlex PCR 시스템을 사용하여 94°C에서 10분간 pre-denaturation을 진행한 후, 94°C에서 20초, 55°C에서 20초, 72°C에서 1분의 조건으로 30 cycles 반응을 수행하였다. 최종적으로 72°C에서 10분간 final extension을 실시하였다. 반응 산물은 1% 아가로스 젤 전기영동을 통해 PCR 증폭 여부를 확인하였다. 염기서열 해독은 3730xl DNA analyzer (ThermoFisher scientific, USA)를 활용하여 분석하였으며 모세관 전기영동 매질은 POP-7TM polymer를 사용하여 36 cm 모세관으로 분석하였다. 해독된 염기서열은 forward 방향과 reverse 방향 염기서열을 바탕으로 완성된 하나의 contiguous 염기서열을 만든 후 National Center for Biotechnology Information (NCBI) Blast 검색으로 이미 보고되어 있는 종들과 염기서열을 비교하여 분석하였다.
HPLC 성분분석 – High Performance Liquid Chromatography(HPLC)를 사용하여 C. reticulata와 C. sunki의 성분을 분석하였으며 실험에 사용된 장비는 Agilent 1260 Infinity II 고속액체크로마토그래프와 가변파장검출기(Variable Wavelength Detector)였다. 분석에 사용된 컬럼은 INNO C18 컬럼(4.6 × 250 mm, 5 μm)으로 설정하였고, 컬럼 오븐 온도는 35°C로 유지하였다.22) 각 시료 60 mg을 70% MeOH에 용해하여 30 mg/mL 농도로 제조하였다. 이 과정에서 초음파 진탕기를 사용하여 샘플을 완전히 녹인 후 5,000 rpm에서 10분간 원심분리하였다. 이후 0.22 μm PVDF membrane filter로 여과하여 최종 시험용액으로 사용하였다.23) Hesperidin의 농도는 피크면적(Y)과 농도(X, μg/10 μL) 간의 검량선(y = 13.817x + 3.0173, R2= 1)을 기반으로 산출되었으며 각 시료는 5회 반복 측정하여 평균 ± 표준편차(means ± deviation, S.D.)로 나타내었다. HPLC 분석 조건은 Table II에 제시하였다.
표준용액은 hesperidin 1.8 mg을 정밀하게 칭량하여 70% MeOH (10% DMSO)에 용해한 후 초음파 진탕기로 완전히 녹인 다음 0.22 μm PVDF membrane filter로 여과하여 사용하였다. Hesperidin의 함량은 시험용액의 농도와 샘플의 채취량을 기준으로 계산하였다. 결과는 mg/g으로 나타내었으며 계산방법은 아래와 같다.
표준품 함량(mg/g) = (C × V × D × P) / W
C : 시험용약 중의 표준품의 농도(mg/mL)
V : 시험용액의 전량(mL)
D : 희석배수
P : 표준품의 순도
W : 시료채취량(g)
추출물 제조 – 주정추출물은 건조된 각 진피와 제주자생 감귤의 과피 시료를 70% EtOH과 1:10 (w/v) 비율로 혼합한 후 초음파 추출기(sonicator)를 사용하여 70°C에서 2시간동안 추출하였다. 추출 후 여과지를 사용하여 여과하고 고형 잔여물을 제거하였다. 여과된 추출액은 50°C에서 감압농축하였고 농축된 추출액은 동결건조하여 분말형태로 확보한 후 -20°C에서 보관하였다.
열수 추출물은 건조된 진피와 제주자생 감귤의 과피 시료를 D.W와 1:10 (w/v) 비율로 혼합한 후 초음파 추출기(sonicator)를 사용하여 95°C에서 2시간동안 추출하였다. 추출된 혼합물은 여과한 후 70°C에서 감압 농축하였다. 이후 동결건조하여 분말형태로 확보하였고 -20°C에서 보관하여 실험에 사용하였다.
DPPH 자유 라디칼 소거 활성 측정을 통한 항산화능 평가 – DPPH (1,1-diphenyl-1-picrylhydrazyl) 라디칼 소거능 분석은 안정한 라디칼을 포함하는 보라색 용액인 DPPH를 이용하여 시료의 항산화 활성을 평가하였다.24) DPPH는 항산화 활성을 지닌 물질과 반응 시 노란색으로 탈색되는 특성을 가지며, 이를 통해 시료의 라디칼 소거 능력을 측정할 수 있다. 본 실험에서는 시료와 0.2 mM DPPH 용액을 각 100 μL씩 혼합하여 실온에서 30분 동안 반응시켰다. 반응 후, 흡광도는 517 nm에서 SpectraMax 190 Microplate Reader (Molecular Devices, San Jose, CA, USA)를 사용하여 측정하였다.
DPPH radical scavenging activity (%) = (1-B/A) × 100
A : 시료 무첨가 구의 흡광도
B : 시료 첨가 구의 흡광도
ABTS 자유 라디칼 소거 활성 측정을 통한 항산화능 평가 – ABTS (2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid) 소거 활성 분석은 potassium persulfate와 ABTS가 반응하여 생성되는 자유 라디칼 소거 활성을 측정하는 방법이다.24) 청록색 ABTS 용액은 항산화 활성을 지닌 물질과 반응 시 ABTS 라디칼이 환원되어 투명해진다. ABTS stock solution은 7 mM의 ABTS와 2.45 mM의 potassium persulfate를 5 mL D.W에 용해시킨 후 4°C에서 12시간 incubation 한 후 사용하였다. ABTS 용액은 stock solution에서 희석하여 사용하였으며 시료 50 μL과 ABTS 150 μL를 혼합한 후 실온에서 30분간 반응시킨 후 SpectraMax 190 Microplate reader를 사용하여 37°C에서 734 nm로 흡광도를 측정하였다. ABTS 라디칼 소거 활성 (%)은 아래 식에 따라 계산하여 비교하였다.
ABTS radical scavenging activity (%) = (1-B/A) × 100
A : 시료 무첨가 구의 흡광도
B : 시료 첨가 구의 흡광도
Tyrosinase 억제 활성을 통한 미백 개선 효능 평가 – 미백 개선 효능을 평가하기 위해 Yagi 등의 실험방법을 변형하여 tyrosinase 억제 활성을 확인하였다.25) 50 mM potassium phosphate buffer (pH 6.8) 90 μL와 0.2 kU/mL tyrosinase from mushroom 10 μL과 시료 50 μL를 혼합하여 37°C에서 90분간 안정화시켰다. 이후 2.5 mM tyrosine 100 μL를 첨가하여 37°C, 30분간 차광하여 반응시킨 이후 SpectraMax 190 Microplate reader를 사용하여 490 nm에서 흡광도를 측정하고 tyrosinase 억제 활성(%)는 아래 식에 따라 계산하여 비교하였다.
Tyrosinase inhibition activity (%) = (1-B/A) × 100
A : 시료 무첨가 구의 흡광도
B : 시료 첨가 구의 흡광도
Elastase 억제 활성을 통한 주름 개선 효능 평가 – 주름 개선 효능을 측정하기 위해 Cannell 등의 방법을 변형한 elastase 억제 활성 실험을 진행하였다.26) 0.2M Tris-HCl buffer 90 μL와 샘플 20 μL를 25°C에서 10분간 혼합하였다. 이후 4 U elastase from porcine pancreas를 5 μL 첨가하여 10분동안 재혼합하였다. 이후 N-Succinyl-(Ala)3-p-nitroanilide elastase를 20 μL 첨가하여 반응시킨 직후 SpectraMax 190 Microplate reader를 사용하여 37°C에서 410 nm로 흡광도를 측정하였다. Elastase 억제 활성(%) 계산식은 다음과 같다.
Elastase inhibition activity (%) = (1-B/A) × 100
A : 시료 무첨가 구의 흡광도
B : 시료 첨가 구의 흡광도
세포 배양 – 마우스 유래 대식세포인 RAW 264.7 세포와 인간 유래 각질 형성 세포인 HaCaT 세포는 한국세포주은행(Korean Cell Line Bank, KCLB)에서 구입하였다. 세포 배양 배지는 DMEM에 100 unit/mL의 P/S과 10% FBS를 넣어 사용하였다. 세포는 37°C, 5% CO2 조건의 인큐베이터에서 배양하였으며, 3일에 한 번씩 계대 배양하였다.
세포생존율 평가 – RAW 264.7 세포와 HaCaT 세포를 2 × 105 cells/well로 96 well cell culture plate에 분주하고, 37°C, 5% CO2 조건의 인큐베이터에서 24시간 배양하였다.27) 이후 배양액을 FBS가 없는 medium으로 교체하여 24시간 동안 추가 배양한 medium을 제거하고 추출물을 첨가한 100 μL의 medium을 각 well에 추가하였다. 추출물에 24시간동안 노출시킨 후 5 mg/mL MTT 시약을 serum free medium과 1:9로 혼합하고 4시간동안 배양하였다. 상층 medium을 제거 후 99.5% DMSO와 iso-propanol을 1:1 비율로 혼합하여 각 well에 100 μL씩 첨가하여 세포를 용해하였다. SpectraMax 190 Microplate reader를 사용하여 540 nm에서 흡광도를 측정하였다.
Nitric oxide (NO) 생성량 평가 –RAW 264.7 세포와 HaCaT 세포를 2×106 cells/well로 6 well cell culture plate에 분주하고, 37°C, 5% CO2 조건의 인큐베이터에서 24시간 배양하였다.27) 배양 후 FBS가 없는 배지로 교체하여 다시 24시간 배양하고 배양액에 추출물을 첨가하여 전처리하였다. 1시간 후 LPS (1 μg/mL)를 대조군을 제외한 모든 well에 첨가하여 24시간동안 자극하였다. 이후 세포 배양 상층액을 griess reagent와 1:1로 혼합하여 반응시킨 후 96 well plate에 200 μL씩 분주하고 microplate reader를 사용하여 540 nm에서 흡광도를 측정하였다. NO 농도는 sodium nitric oxide (NaNO2)로 표준 곡선을 작성하여 정량하였다.
사이토카인 발현량 확인 –RT-qPCR (Real time quantitative polymerase chain reaction)을 통해 IL-6, IL-1β, iNOS, COX-2, TNF-α 및 β-actin의 발현량을 분석하였다.28) 각 시료를 전처리한 세포에 RNAiso plus (Takara Bio, Otsu, Japan)를 사용하여 용해 후 RNA를 추출하였다. 추출한 RNA는 pure water에 용해하였고 TransGen Biotech (Beijing, China)의 All-in-One First-Strand cDNA Synthesis SuperMix를 사용하여 1 μg/mL의 RNA를 역전사하여 cDNA를 합성하였다. RT-qPCR 분석은 Applied Biosystems (Foster City, CA, USA)의 QuantStudio 3 시스템과 Thermo Fisher Scientific (Rockford, IL, USA)의 PowerSYBR® Green PCR Master Mix 및 유전자 특이적 primer (Table III)를 사용하여 증폭시켰다. 각 유전자의 발현은 β-actin을 기준으로 2-ΔΔCT 방법을 통해 정규화하여 계산하였으며 PCR cycle은 95°C에서 15초, 57°C에서 20초, 72°C에서 40초를 40회 반복하는 조건으로 설정되었다.29)
통계처리 – 모든 측정값은 평균 ± 표준오차(means ± Standard Error of the Mean, S.E.M.)로 나타내었으며, 대조군과 실험군 간의 통계적 유의성 검증은 GraphPad Prism (GraphPad Software Inc.)을 사용하여 one way analysis of variance (ANOVA)와 two-way ANOVA로 확인하였다. 사후 검증은 GraphPad Prism (GraphPad Software Inc.) Student-Newman-Keuls test를 통해 재검증 하였으며, 유의적인 차이는 P < 0.05 수준에서 판단하였다.
결 과
국산, 중국산 진피와 제주 자생 감귤류의 유전자 분석을 통한 종 판별 결과 – 진피 한약재 규격품 2종(국산, 중국산) 및 제주자생 감귤의 과피 3종(서귀포시 예래동(Yerae-dong), 하효동(Hahyo-dong), 제주시 애월읍 어음리(Eoeum-ri)에서 각각 채집)에 대한 DNA 유전자 염기서열 분석을 통해 종 판별을 진행하였다.
각 시료에 대한 DNA 분석을 통해 염기서열을 시퀀싱하고 이를 바탕으로 forward 방향과 reverse 방향의 염기서열을 토대로 하나의 완성된 contiguous 염기서열을 만들었다. 이 후 식물 종은 유전자 은행(National Center for Biotechnology Information; NCBI) blast 검색을 바탕으로 이미 보고된 생물 종과 염기서열 일치 정도를 비교 분석하여 결정하였다. 진피 규격품(국산, 중국산)과 예래동 및 하효동에서 채집한 감귤 과피의 ITS DNA 염기서열은 유전자 은행의 ON479693.1과 99% 이상 일치하여 C. reticulata로 확인되었다. 반면, 어음리에서 채집한 감귤 과피의 경우, ITS DNA 염기서열은 유전자 은행의 ON479690.1과 100% 일치하기 때문에 C. sunki로 결정지었고(Table IV), 다음의 연구결과부터 진귤 과피로 표기하였다.

Genetic identification and morphological comparison of C. reticulata (Yerae-dong, Hahyo-dong, Korea, China) and C. sunki (Eoeum-ri)
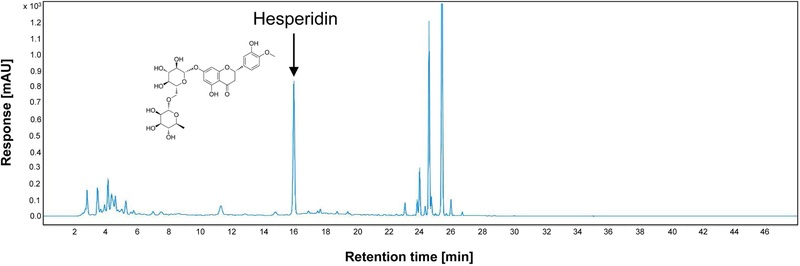
C. reticulata와 C. sunki의 hesperidin 함량 비교 – 진피(국산, 중국산), 감귤(예래동, 하효동)의 과피, 진귤 과피의 hesperidin 함량을 비교 분석하였다(Table V). Hesperidin은 항산화 및 항염증 효능이 잘 알려진 flavonoid 중 하나로, 진피의 품질 및 효능 평가의 핵심 지표로 활용된다. 열수추출물에서는 국산 진피의 hesperidin의 함량이 11.41 ± 0.06 mg/g으로 가장 높게 나타났으며 중국산 진피가 10.99 ± 0.07 mg/g으로 그 다음으로 높게 나타났다. 주정 추출물의 경우, 진귤 과피가 13.17 ± 0.01 mg/g으로 가장 높게 나타났으며 이는 규격품인 진피(국산, 중국산)보다 높은 hesperidin 함량을 함유하고 있는 것으로 나타났다(Fig. 1).

Hesperidin content comparison in C. reticulata (Yerae-dong, Hahyo-dong, Korea, China) and C. sunki (Eoeum-ri)
C. reticulata와 C. sunki의 항산화 효능 비교 – 감귤류 과피에는 60 여종 이상의 flavonoid가 함유되어 있어 항산화 효능이 있음이 알려져 있다. 진귤 과피가 진피 및 감귤(예래동, 하효동) 과피의 항산화 효능과 유사한지 비교하기 위해 DPPH 및 ABTS assay를 수행하였다. 항산화 활성은 자유라디칼 소거 효과(scavenging effects)가 50% 감소하는 데 필요한 샘플의 농도(scavenging concentration 50, SC50)으로 평가하였다(Table VI). DPPH assay를 통해 항산화 활성을 평가한 결과, 감귤(예래동) 과피의 열수 및 주정 추출물은 SC50= 1840.74 ± 132.49, 1828.47 ± 24.53 μg/mL로 가장 높은 값을 보여 항산화 활성이 가장 낮았다. 반면 감귤(하효동) 과피는 열수와 주정 추출물에서 각각 SC50= 1040.28 ± 17.29 μg/mL, 980.13 ± 49.60 μg/mL로 가장 낮은 값을 나타내어 항산화 활성이 가장 높았다. 한편, 진귤 과피의 SC50은 열수 추출물에서 1109.85 ± 27.75 μg/mL, 주정 추출물에서 1230.45 ± 59.47 μg/mL로, 진피(국산, 중국산)와 유사한 수준의 항산화 활성을 나타냈다.
ABTS assay에서도 DPPH assay 결과와 유사한 경향이 확인되었다. 감귤(하효동) 과피 주정 추출물(SC50= 378.22 ± 9.77 μg/mL), 진피(중국산) 주정 추출물(SC50= 395.46 ± 6.18 μg/mL)은 상대적으로 낮은 SC50 값을 보여 높은 항산화 활성을 나타냈다. 반면, 감귤(예래동) 과피 열수 추출물(SC50= 1362.34 ± 25.79 μg/mL) 및 주정 추출물(SC50= 986.27 ± 28.09 μg/mL)은 비교적 높은 SC50 값을 보여 항산화 효과가 가장 낮은 것으로 확인되었다. 진귤 과피 열수 및 주정 추출물의 SC50은 각각 966.22 ± 86.68 μg/mL, 899.95 ± 26.09 μg/mL로, 감귤(하효동) 과피 열수 추출물(SC50= 936.00 ± 31.40 μg/mL), 진피(국산, 중국산) 열수 추출물(801.63 ± 16.35 μg/mL, 829.90 ± 15.96 μg/mL)과 비슷한 수준의 항산화 활성을 나타냈다. 이러한 결과는 진귤 과피가 진피(국산, 중국산) 및 감귤(예래동 및 하효동) 과피와 항산화 효능 측면에서 유사한 효능을 보이므로 진귤(C. sunki)을 C. reticulata의 한 분류로 포함할 수 있는 가능성을 제시할 수 있다.
C. reticulata와 C. sunki의 미백 및 주름 개선 효능 비교 – Citrus 종은 비타민 C를 다량 함유하고 있으며 진귤 과피가 진피(국산, 중국산) 및 감귤(예래동, 하효동) 과피와 유사한 미백 및 주름 개선 효능을 나타내는지 확인하였다(Table VII). 진귤 과피 열수 추출물은 tyrosinase 억제 활성이 가장 낮게 나타났으나, 주정 추출물에서는 가장 우수한 억제 활성을 나타냈다. 또한, 진귤 과피 열수 추출물은 진피(국산, 중국산) 열수 추출물보다 높은 elastase 억제 활성을 보였다. 진피(중국산) 주정 추출물이 가장 우수한 elastase 억제 활성을 나타냈고, 진귤 과피 주정 추출물은 진피(중국산) 대비 5% 낮은 억제 활성을 보였다. 진귤 과피는 전반적으로 비교 생약 및 감귤의 억제 활성과 크게 다르지 않았으며, 이와 같은 결과는 진귤(C. sunki)이 C. reticulata 종과 비교했을 때 미백 및 주름 개선 효능 측면에서 유사함을 나타낸다.
C. reticulata와 C. sunki의 세포생존율 평가 및 비교 – 진피(국산, 중국산), 감귤(예래동, 하효동) 과피, 진귤 과피 추출물을 RAW 264.7 세포와 HaCaT 세포에서 다양한 농도로 처리하여 세포생존율을 평가하였다. Control의 세포생존율이 1일 때, 0.7보다 낮을 경우 세포 생존에 영향을 미치는 것으로 판단하였다. 진피(국산, 중국산), 감귤(예래동, 하효동) 과피, 진귤 과피 열수 및 주정 추출물은 세포생존율을 감소시키지 않았으며 대부분의 농도에서 80% 이상의 생존율을 유지하였다(Fig. 2). 따라서, 모든 추출물은 세포생존율을 저해하지 않으면서 효능을 발휘할 가능성이 있음을 시사한다.
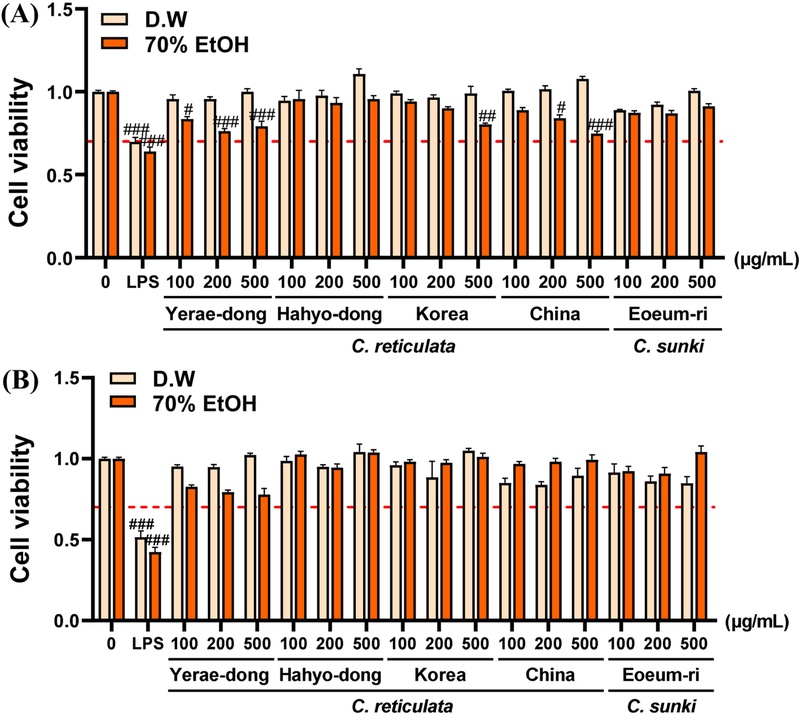
Effects of Citrus extracts on cell viability in RAW 264.7 and HaCaT cells. (A) RAW 264.7 cells and (B) HaCaT cells were treated with D.W and 70% EtOH extracts of Citrus reticulata (Yerae-dong, Hahyo-dong, Korea, China) and Citrus sunki (Eoeum-ri) at concentrations of 100, 200, and 500 μg/mL for 24 h. Data are presented as mean ± S.E.M. ###p < 0.001 vs. the control group (0 µg/mL). LPS, lipopolysaccharide.
C. reticulata와 C. sunki의 항염 효능 비교 – RAW 264.7 세포와 HaCaT 세포에 진피(국산, 중국산), 감귤(예래동, 하효동) 과피, 진귤 과피 열수 및 주정 추출물을 전처리 한 후 1시간 뒤에 LPS (1 μg/mL)으로 염증 반응을 유도하여 NO 생성량을 확인하였다(Fig. 3). RAW 264.7 세포와 HaCaT 세포에서 열수 추출물에 의해 NO 억제 효과가 나타나지 않았으나, 주정 추출물에서는 LPS 단독처리군 대비 NO 생성량이 유의적으로 감소하였다. 특히, RAW 264.7 세포에서는 감귤(예래동)과피가 NO 억제율이 가장 높았으며 감귤(하효동) 과피가 그 다음으로 높은 억제율을 보였다. 국산 진피는 진귤 과피와 비슷한 NO 억제율이 나타났고 중국산 진피가 가장 낮은 억제율을 나타냈다(Fig. 3A). 하지만, HaCaT 세포에서는 중국산 진피의 NO 억제 효능이 가장 높았으며 진귤 과피가 그 다음으로 우수한 NO 억제 효능이 나타나는 것을 확인하였다(Fig. 3B). 국산 진피와 감귤(예래동) 과피는 진귤 과피와 비슷한 수준으로 NO를 억제하였으며 감귤(하효동) 과피는 가장 낮은 NO 억제 활성을 보였다.
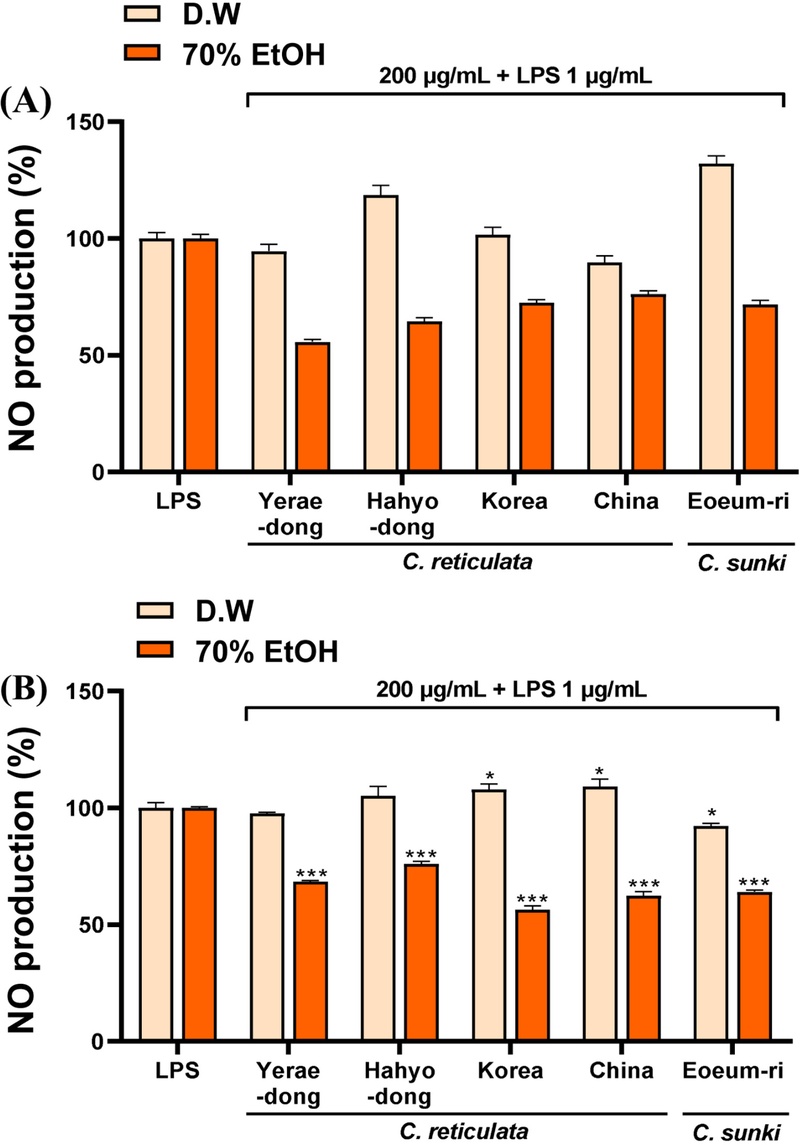
Effects of Citrus extracts on LPS-induced nitric oxide (NO) production in RAW 264.7 and HaCaT cells. (A) RAW 264.7 cells and (B) HaCaT cells were pre-treated with D.W and 70% EtOH extracts of Citrus reticulata (Yerae-dong, Hahyo-dong, Korea, China) and Citrus sunki (Eoeum-ri) at 200 μg/mL for 1 h, followed by stimulation with LPS (1 μg/mL) for 24 h. Data are presented as mean ± S.E.M. *p < 0.05, ***p < 0.001 vs. the LPS-stimulated group. LPS, lipopolysaccharide.
추가적으로 HaCaT 세포에서 진피(국산, 중국산)와 진귤 과피의 사이토카인의 발현 억제 정도를 평가하였다(Fig. 4). NO 생성량, IL-6과 TNF-α (Fig. 4A,C,D)의 발현량이 진피(국산, 중국산)와 진귤 과피 모두 농도 의존적으로 감소하였고, iNOS와 IL-1β (Fig. 4B,E)의 경우 진피(국산, 중국산)는 농도가 증가함에 따라 사이토카인의 발현량이 감소하였으나, 진귤 과피는 낮은 농도에서부터 유의미한 억제 효과를 보였다. 전반적으로 진귤 과피는 감귤 종과 비교하였을 때 동등 이상의 NO 억제 효능이 나타났다. 이와 같은 결과는 진귤(C. sunki)이 감귤(C. reticulata)과 유사한 항염 효능을 나타냈다는 점에서, 두 종을 동일 분류군으로 포함할 수 있는 근거를 제공한다.
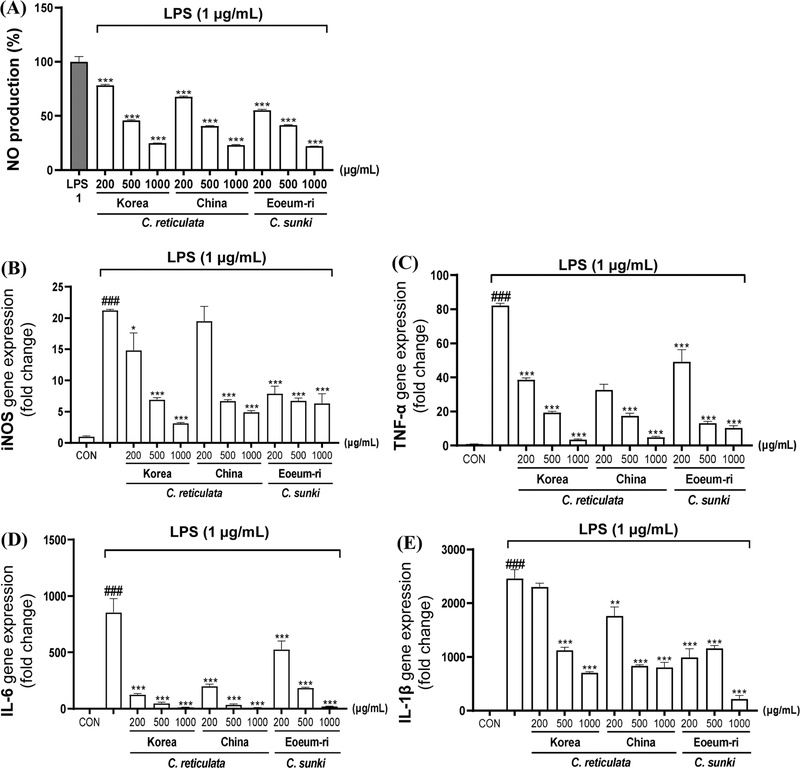
Effects of Citrus extracts on LPS-induced NO production and pro-inflammatory gene expression in HaCaT cells. (A) HaCaT cells were pre-treated with 70% EtOH extracts of Citrus reticulata (Korea, China) and Citrus sunki (Eoeum-ri) at concentrations of 200, 500, and 1000 μg/mL for 1 h, followed by stimulation with LPS (1 μg/mL) for 24 h. (B–E) Cells were pre-treated with 200 μg/mL of each extract for 1 h, followed by stimulation with LPS (1 μg/mL) for 24 h. mRNA expression levels of (B) iNOS, (C) TNF-α, (D) IL-6, and (E) IL-1β were then determined by RT-qPCR. Results are expressed as fold change relative to the control group (CON). Data are presented as mean ± S.E.M. ###p < 0.001 vs. CON, *p < 0.05, **p < 0.01, ***p < 0.001 vs. LPS-stimulated group. CON, control; LPS, lipopolysaccharide.
고 찰
본 연구에서는 진피 한약재 규격품(국산, 중국산), 감귤(예래동, 하효동) 과피, 진귤과피의 DNA 염기서열분석, hesperidin 함량분석, 항산화, 미백 및 주름 개선 효능 평가, 항염 효능을 비교분석하였다. DNA 분석결과, 어음리에서 채집한 진귤은 C. sunki, 나머지 시료는 C. reticulata로 동정되었다. 진귤(C. sunki) 과피의 hesperidin 함량은 진피(국산, 중국산) 및 감귤(예래동, 하효동) 과피와 유사하거나 높았다. 또한 진귤 과피는 항산화, 미백 및 주름 개선 효능 평가, 세포생존율, 항염 활성을 포함한 전반적인 생리활성 평가에서 진피(국산, 중국산) 및 감귤(예래동, 하효동) 과피와 유사하거나 높은 활성을 나타냈다. 특히 진귤 과피 주정 추출물은 항염 효능 측면에서 한약재 규격품으로 판매되고 있는 진피(국산, 중국산)와 비교했을 때 동등 이상의 수준으로 나타났다. 이러한 결과는 진귤(C. sunki)이 C. reticulata와 약리적 동등성을 가지며, C. reticulata의 생약 범주 내에 포함될 수 있음을 시사한다.
생약은 자연에서 얻어진 동물, 식물, 미생물 및 그 대사산물을 가공하여 의약품으로 사용하는 천연물로, 질병의 예방과 치료를 위해 오랜 기간 전통 의학에서 활용되어 왔다. 생약의 품질은 산지, 재배방식, 채집시기 등 다양한 환경적 요인을 크게 받기 때문에 그 특성을 규명하기 위한 분류 체계 역시 중요하다.30) Tanaka system은 이러한 형태학적 변이와 산지적 특성을 기반으로 감귤류를 세부적으로 분류하여 감귤(C. reticulata)과 진귤(C. sunki)을 독립된 종으로 구분하였으나11) 이러한 분류는 감귤류 간의 약리적 효과나 화학 성분의 유사성이 간과될 가능성이 있다. 반면, Swingle system은 유전적 유사성과 주요 화학적 특성을 기준으로 감귤류를 통합적으로 분류하며 C. sunki를 C. reticulata의 아종으로 간주한다. 이러한 접근은 실제 약효와 성분 유사성을 중시하는 관점으로, 약리적 효과를 기준으로 평가되는 생약 분류의 목적에 보다 부합하는 방식이라 판단된다.
진피는 감귤류의 과피를 건조하여 사용하는 대표적인 생약으로, 전통적으로 소화기능 개선, 기침완화, 항염증 효능 등으로 활용되어 왔으며 그 품질 기준 설정에 있어 flavonoid 성분인 hesperidin이 핵심 지표로 활용된다. 이는 진피의 품질과 약효를 평가하는 데 있어 중요한 기준이다. 본 연구 결과, 진귤 과피는 진피 규격품 및 감귤(예래동, 하효동) 과피와 유사하거나 더 높은 hesperidin 함량을 나타냈다. 또한 본 연구에서 진귤 과피는 항산화, 미백 및 주름 개선, 항염증 효과측면에서 진피(국산, 중국산), 감귤(예래동, 하효동) 과피와 유사한 효능을 보였다. 따라서 진귤 과피를 대체 생약 자원으로서 활용할 수 있는 가능성이 제시되며 이는 대한약전 내 C. reticulata의 생약 범주 안에서 C. sunki를 통합적으로 고려할 필요성을 시사한다. 이와 유사한 사례로 감초(Glycyrrhiza uralensis (licorice))가 있다. 감초는 콩과식물에 속하는 약용 식물로, 대표적으로 G. glabra, G. uralensis, G. inflata가 있으며,31) 각 종은 각각 지중해, 동아시아, 중앙아시아에 분포한다.32,33) 이들은 지리적 분포 차이로 인해 형태학적 특성에는 차이가 있으나, glycyrrhizin, glycyrrhetinic acid, flavonoid 등의 유효성분과 항염증, 항바이러스, 간 보호 등 약리 효과가 매우 유사하여 동일한 약재로 취급된다.33,34) 산지에 따라 성분 함량 차이가 다소 존재하나, 이 차이는 통계적으로 유의미하지 않은 것으로 보고되었으며33) 동양 전통 의학에서는 동일한 약재로 취급해왔다. 이에 따라 G. glabra와 G. uralensis는 중국약전(CP), 일본약전(JP), 대한약전(KP)에서 동일한 약재로 등재되어 있으며35) 이는 약리적 동등성과 화학적 유사성, 전통적 사례를 근거로 한 통합적 분류의 결과이다. 감초의 사례는 C. sunki와 C. reticulata 간의 관계를 해석하는 데 중요한 참고자료가 될 수 있으며 생약의 분류에 있어 형태학적 특성보다는 유효성분과 약리효과를 기준으로 접근하는 통합적 기준이 필요함을 시사한다.
결 론
본 연구에서는 진피 한약재 규격품(국산, 중국산), 감귤(예래동, 하효동) 과피, 진귤 과피를 대상으로 DNA 염기서열 분석, 항산화, 항염, 미백 및 주름 개선 효능, hesperidin 함량 분석을 수행하였다. DNA 분석 결과, 진귤 과피는 C. sunki, 나머지 시료는 C. reticulata로 동정되었으며, 생리활성 및 지표 성분 분석 결과 진귤 과피는 진피(국산, 중국산), 감귤(예래동, 하효동) 과피와 유사하거나 더 우수한 효능을 나타냈다. 특히 진귤 과피 주정 추출물은 항염 효능에서 가장 우수한 활성을 보였고, hesperidin 함량 또한 상대적으로 높은 수치를 나타내어 생약 자원으로서의 가능성을 보여주었다. 따라서 본 연구는 진귤(C. sunki)이 C. reticulata와 약리학적으로 동등한 효능을 가지기 때문에 통합적인 생약 분류 기준에서 진피의 대체 원료로서 활용될 수 있음을 시사한다. 또한, 감초처럼 형태와 분포는 다르지만 유효성분과 약효가 유사한 종들을 통합하여 하나의 약재로 인정한 사례를 참고할 때, 진귤(C. sunki) 역시 C. reticulata의 생약 범주 내에서 통합적으로 고려될 수 있는 근거가 충분하다. 본 연구는 국내 자생 자원을 활용한 진피의 대체 가능성을 제시함으로써, 국산 생약 자원의 활용 확대 및 약전 등재를 위한 과학적 근거를 제시하였다.
Acknowledgments
이 연구는 식품의약품안전평가원의 지원으로 수행되었으며 이에 감사드립니다(22204한약안142-2).
References
-
Zhong, G. and Nicolosi, E. (2020) Citrus origin, diffusion, and economic importance. The Citrus Genome. 5-21.
[https://doi.org/10.1007/978-3-030-15308-3_2]

-
Palangasinghe, P. C., Liyanage, W. K., Wickramasinghe, M. P., Palangasinghe, H. R., Shih, H.-C., Shiao, M.-S. and Chiang, Y.-C. (2024) Reviews on Asian citrus species: Exploring traditional uses, biochemistry, conservation, and disease resistance. Ecological Genetics and Genomics 100269.
[https://doi.org/10.1016/j.egg.2024.100269]

-
Xi, W., Zhang, Y., Sun, Y., Shen, Y., Ye, X. and Zhou, Z. (2014) Phenolic composition of Chinese wild mandarin (Citrus reticulata Balnco.) pulps and their antioxidant properties. Industrial Crops and Products 52: 466-474.
[https://doi.org/10.1016/j.indcrop.2013.11.016]

-
Yu, Y., Chen, C., Huang, M., Yu, Q., Du, D., Mattia, M. R. and Gmitter, F. G. (2018) Genetic diversity and population structure analysis of citrus germplasm with single nucleotide polymorphism markers. Journal of the American Society for Horticultural Science 143: 399-408.
[https://doi.org/10.21273/JASHS04394-18]

- Webber, H. J. (1967) History and development of the citrus industry. The Citrus Industry 1-37.
-
Nicolosi, E., Deng, Z., Gentile, A., La Malfa, S., Continella, G. and Tribulato, E. (2000) Citrus phylogeny and genetic origin of important species as investigated by molecular markers. Theoretical and Applied Genetics 100: 1155-1166.
[https://doi.org/10.1007/s001220051419]

-
Catalano, C., Las Casas, G., Giuffrida, A., Ferlito, F., Di Guardo, M., Continella, A., Bennici, S., La Malfa, S., Gentile, A. and Distefano, G. (2022) Reproductive biology factors hampering lemon [Citrus limon (L.) Burm. f.] genetic improvement. Agriculture 12: 2020.
[https://doi.org/10.3390/agriculture12122020]

-
Jin, S. B., Lee, W. J., Park, J. H., Park, S. M., Lee, D. H. and Yun, S. H. (2018) A phylogenic analysis of Citrus Cultivars native to Jeju using Chloroplast DNA trnL-trnF and internal transcribed spacer region sequences. Horticultural Science and Technology 36: 585-597.
[https://doi.org/10.12972/kjhst.20180059]

- Swingle, W. T. (1967) The botany of Citrus and its wild relatives. The Citrus Industry 1: 190-430.
- Kamatyanatt, M., Singh, S. K. and Sekhon, B. S. (2021) Mutation breeding in citrus—A review. Plant Cell Biotechnol. Mol. Biol. 22: 1-8.
-
Tanaka, K. and Sugeno, M. (1992) Stability analysis and design of fuzzy control systems. Fuzzy Sets and Systems 45: 135-156.
[https://doi.org/10.1016/0165-0114(92)90113-I]

-
Scora, R. W. (1975) On the history and origin of Citrus. Bulletin of the Torrey Botanical Club 369-375.
[https://doi.org/10.2307/2484763]

-
Lu, Y., Zhang, C., Bucheli, P. and Wei, D. (2006) Citrus flavonoids in fruit and traditional Chinese medicinal food ingredients in China. Plant Foods for Human Nutrition 61: 55-63.
[https://doi.org/10.1007/s11130-006-0014-8]

-
Liu, N., Li, X., Zhao, P., Zhang, X., Qiao, O., Huang, L., Guo, L. and Gao, W. (2021) A review of chemical constituents and health-promoting effects of citrus peels. Food Chemistry 365, 130585.
[https://doi.org/10.1016/j.foodchem.2021.130585]

-
Yu, X., Sun, S., Guo, Y., Liu, Y., Yang, D., Li, G. and Lü, S. (2018) Citri Reticulatae Pericarpium (Chenpi): Botany, ethnopharmacology, phytochemistry, and pharmacology of a frequently used traditional Chinese medicine. Journal of Ethnopharmacology 220: 265-282.
[https://doi.org/10.1016/j.jep.2018.03.031]

-
Yoo, Y.-H., Oh, C. J., Shin, S. C., Seo, S., Kim, M., Yun, S.-H., Song, K. J., Lee, H. and Kim, H. B. (2020) Complete chloroplast genome sequence of a medicinal landrace citrus Jinkyool (Citrus sunki Hort. ex Tanaka) in Jeju Island, Korea. Mitochondrial DNA Part B 5: 3701-3702.
[https://doi.org/10.1080/23802359.2020.1833771]

-
Froelicher, Y., Mouhaya, W., Bassene, J.-B., Costantino, G., Kamiri, M., Luro, F., Morillon, R. and Ollitrault, P. (2011) New universal mitochondrial PCR markers reveal new information on maternal citrus phylogeny. Tree Genetics & Genomes 7: 49-61.
[https://doi.org/10.1007/s11295-010-0314-x]

- 통계청(2023) 2023년 농작물생산통계.
- 식품의약품안전처(2023) Year book of imported food inspection.
-
Hyun, J. S., Kang, S.-M., Senevirathne, M., Koh, W.-J., Yang, T.-S., Oh, M.-C., Oh, C.-K., Jeon, Y.-J. and Kim, S.-H. (2010) Antioxidative activities of extracts from dried Citrus sunki and C. unshiu peels. Journal of the Korean Society of Food Science and Nutrition 39: 1-7.
[https://doi.org/10.3746/jkfn.2010.39.1.001]

- Doyle, J. J. and Doyle, J. L. (1987) A rapid DNA isolation procedure for small quantities of fresh leaf tissue. Phytochemical Bulletin 19: 11-15.
- Lee, H.-D., Lee, Y., Kim, H., Kim, H., Park, C.-G. and Lee, S. (2020) HPLC/UV quantification of (+)-catechin in Filipendula glaberrima from different regions and flowering stages. Korean Journal of Pharmacognosy 51: 291-296.
-
Sammani, M. S., Clavijo, S., Portugal, L., Suárez, R., Seddik, H. and Cerdà, V. (2017) Use of multiresponse statistical techniques to optimize the separation of diosmin, hesperidin, diosmetin and hesperitin in different pharmaceutical preparations by high performance liquid chromatography with UV-DAD. Talanta 167: 695-702.
[https://doi.org/10.1016/j.talanta.2017.02.069]

- Kim, S.-Y., Kim, S. M. and Park, S. J. (2019) Antioxidant activities of natural essential oils derived from Korean endemic plants. Journal of Agricultural, Life and Environmental Sciences 31: 17-25.
-
Yagi, A., Kanbara, T. and Morinobu, N. (1987) Inhibition of mushroom-tyrosinase by aloe extract. Planta Medica 53: 515-517.
[https://doi.org/10.1055/s-2006-962798]

-
Cannell, R. J., Kellam, S. J., Owsianka, A. M. and Walker, J. M. (1988) Results of a large scale screen of microalgae for the production of protease inhibitors. Planta Medica 54: 10-14.
[https://doi.org/10.1055/s-2006-962319]

- Kim, S.-Y., Kim, S.-H. and Park, S. J. (2024) Effects of Centaurea cyanus methanolic extract on antioxidant activity and anti-inflammatory effects in LPS-induced RAW 264.7 Macrophages. Journal of Agricultural, Life and Environmental Sciences 36: 362-374.
-
Kim, S.-Y., Yang, D. H., Kim, H. J. and Park, S. J. (2024) Anti-inflammatory effects of Tragopogon dubius methanolic extract on lipopolysaccharide-induced inflammatory responses in RAW 264.7 cells and ICR mice. Korean Journal of Pharmacognosy 55: 255-264.
[https://doi.org/10.22889/KJP.2024.55.4.255]

-
Kim, H.-J., Kim, S.-Y., Bae, H. J., Choi, Y.-Y., An, J.-Y., Cho, Y. E., Cho, S.-Y., Lee, S.-J., Lee, S., Sin, M., Yun, Y. M., Lee, J. R. and Park, S. J. (2023) Anti-inflammatory effects of the LK5 herbal complex on LPS-and IL-4/IL-13-stimulated HaCaT cells and a DNCB-induced animal model of atopic dermatitis in BALB/c mice. Pharmaceutics 16: 40.
[https://doi.org/10.3390/pharmaceutics16010040]

- 식품의약품안전처(2023) 한약(생약)제제 임상시험 가이드라인.
- Sung, K.-C. (2006) A study on the pharmacetical characteristics & analysis of glycyrrhizin extract. Journal of the Korean Applied Science and Technology 23: 215-222.
-
Wahab, S., Annadurai, S., Abullais, S. S., Das, G., Ahmad, W., Ahmad, M. F., Kandasamy, G., Vasudevan, R., Ali, M. S. and Amir, M. (2021) Glycyrrhiza glabra (Licorice): A comprehensive review on its phytochemistry, biological activities, clinical evidence and toxicology. Plants 10: 2751.
[https://doi.org/10.3390/plants10122751]

-
Cerulli, A., Masullo, M., Montoro, P. and Piacente, S. (2022) Licorice (Glycyrrhiza glabra, G. uralensis, and G. inflata) and their constituents as active cosmeceutical ingredients. Cosmetics 9: 7.
[https://doi.org/10.3390/cosmetics9010007]

-
Kondo, K., Shiba, M., Nakamura, R., Morota, T. and Shoyama, Y. (2007) Constituent properties of licorices derived from Glycyrrhiza uralensis, G. glabra, or G. inflata identified by genetic information. Biological and Pharmaceutical Bulletin 30: 1271-1277.
[https://doi.org/10.1248/bpb.30.1271]

- Choi, G. (2015) A comparative study on standards of Korean herbal medicines in the pharmacopoeias of Northeast-Asian countries (4) Liquorice. Korean Herbal Medicine Information 3: 17-26.