
Spicatoside A를 이용한 맥문동추출물의 정량분석법 개발
Abstract
In this study, we developed a reliable HPLC-UV (PDA) method for the quantification of spicatoside A in Liriope platyphylla extract. To overcome analytical interference, we introduced a solid-phase extraction (SPE) pretreatment using a C18 stationary phase to selectively remove hydrophilic components prior to analysis. Method validation was conducted in accordance with the guidelines of the Ministry of Food and Drug Safety (MFDS) of Korea, evaluating specificity, linearity, accuracy, precision (repeatability and reproducibility), and limit of quantitation. The developed method demonstrated high specificity, excellent linearity (R2 > 0.9998), acceptable accuracy (92.8–105.2%), and precision within the criteria defined by the MFDS. The limit of quantitation for spicatoside A was determined to be 1.24 μg/ml. Although the pretreatment process is relatively labor-intensive, the method does not require expensive instruments such as HPLC-MS, offering advantages in both practicality and economic feasibility for small-scale research settings.
Keywords:
Liriope platyphylla, Spicatoside A, Solid-phase extraction, HPLC-UV(PDA) method validation맥문동속(Liriope spp.) 식물은 백합과(Liliaceae)에 속하는 다년생 식물로 아열대 및 온대 지역에 주로 분포하고, 전 세계적으로 약 8종이 존재한다고 보고된다.1) 맥문동속 식물은 한국, 중국, 일본에서 이용되고 있는데, 한국은 맥문동(Liriope platyphylla F. T. Wang et T. Tang)과 소엽맥문동(Ophiopogon japonicus Ker-Gawer)을 사용하고 중국, 일본은 소엽맥문동을 주로 사용하며 대용으로 L. muscari, L. spicata, L. graminifolia 등의 식물도 사용한다.2,3) 동북아시아 지역에서는 전통적으로 위 식물들의 근경을 맥문동(麥門冬)의 이름으로 한방 처방에서는 천식, 가래 기침과 같은 기관지 질환 및 강장제로 이용된다.3) 현재 맥문동속 식물은 해열, 진해, 거담, 항염증, 혈당 강하, 뇌세포 보호, 신경세포 성장 촉진 작용 등 다양한 생물학적 활성이 있음이 알려져 있고, 여러 연구에서 플라보노이드, 식물성 스테롤, 스테로이드성 사포닌이 이러한 생리활성에 기인한다고 보고되고 있는데 특히 맥문동이 함유하는 대표적인 이차대사산물은 스테로이드성 사포닌으로 이는 맥문동속 식물이 가지는 가장 특징적인 성분이다.1,3) 잘 알려진 맥문동의 스테로이드성 사포닌은 spicatoside A–D, ophiopoginin A–D, prosapogenin II 및 III 등이 보고되며, 특히 spicatoside A는 맥문동을 대표하는 성분으로 HPLC를 이용한 맥문동의 정성 및 정량분석에 이용되고 있다.4–6) Spicatoside A는 항염증, 항천식, 파골세포 형성억제, 신경돌기 생장 유도, 기억력 강화, 항암 등의 여러 생리활성이 보고되었다.4) 한편, spicatoside A를 비롯한 스테로이드 사포닌은 맥문동속 식물을 대표하는 성분으로 간주되지만, 실제 가장 많이 함유한 성분군은 단당류 및 다당체로써 추출물의 50% 이상을 차지하지만 반면에 개별 사포닌의 함량은 추출물 대비 0.001-0.01%로 상대적으로 지극히 낮다.7–9) 따라서 맥문동 추출물의 대부분을 차지하고 있는 당류를 포함한 친수성 성분이 미량의 사포닌 성분의 함량을 상대적으로 낮추어 분석을 방해하는 요소로 작용하므로 분석의 영향을 주지 않는 범위에서 당류 성분을 제거하는 것이 바람직하다.
사포닌 성분은 페놀성 성분에 비하여 발색단이 부족하여 정성 및 정량분석이 까다로운데 이에 단파장을 이용한 HPLC-UV/PDA 방법, HPLC-ELSD 방법, HPLC-MS 방법이 주로 사용되고 있다.10,11) 세 방법 모두 장단점이 있으며, HPLC-ELSD의 경우 발색단이 없는 성분의 검출에 많이 사용되지만 미량의 성분을 정량분석하기 위해서 검출기의 감도를 높이면 정량분석시 정량곡선(calibration curve)의 직선성(linearity)에 대한 신뢰도를 확보하기 어려운 경향이 있다. HPLC-MS의 방법은 세 가지 방법 중 가장 감도가 좋지만 사용기기가 고가이며 또한 유지 및 보수 등의 비용이 매우 커 소규모의 시설에서는 운용하기 어려운 단점이 있다. 단파장을 이용한 HPLC-UV/PDA 방법은 다른 두 분석방법에 비하여 검출 감도는 떨어지지만 정량한계에서 정량곡선의 신뢰도가 보장되고 기기의 가격 및 운용비용이 가장 적어 특히 소규모의 연구시설에서 대중적으로 가장 많이 사용하는 검출방법이다. 이에 본 연구에서는 식품의약품안전처(이하 식약처)의 기준에12) 따라 HPLC-UV/PDA를 이용하여 맥문동추출물에 함유된 spicatoside A에 대한 정량분석법을 시료의 전처리 과정을 이용해 개발하고자 하였으며 이를 보고하고자 한다.
재료 및 방법
실험재료 – 실험에 사용된 맥문동추출분말은 ㈜성균바이오텍에서 제공받았으며 이는 동광한방몰에서 구입한 맥문동(Liriope platyphylla)을 30% 수성에탄올로 60℃ 온도에서 추출한 것이다.
시약 및 기기 – Spicatoside A 표준품(Cat.# SYC128397477-100MG, 분석보고서 순도: 99.25%)은 삼영이노베이션(경기, 평택)에서 구입하였고, HPLC용 메탄올, 아세토나이트릴은 J. T. baker (Center valley, PA, USA) 사의 제품을 사용하였고, 탈이온수는 Milli-Q water purification system (Millipore, Billerica, MA, USA)을 이용하여 생산하였다. 표준용액, 시험용액 조제에 사용된 메탄올은 부일화학(경기, 안산)에서 구입하였고 triflioroacetic acid는 Merck (Kenilworth, NJ, USA) 사의 제품을 사용하였다. 고체상추출(solid phase extraction)에 사용된 4 g용 카트리지는 인터테크놀로지스(서울) 사의 것을 사용하였으며 이용된 고체상은 ZEOCHEM (Uetikon, Switzerland) 사의 ZEOprep 90 C18 40–63 μm를 사용하였다. HPLC는 Agilent 1260 Infinity HPLC system (Agilent Technologies, Santa Clara, CA, USA)을 사용하였다. 분석용 HPLC 컬럼은 Luna C18(2) (4.6 × 250 mm I.D., 5 μm, Phenomenex, USA)를 사용하였다.
HPLC 분석조건 – 유기용매 이동상(A)은 아세토나이트릴(0.01% TFA)이고, 수성용매 이동상(B)은 탈이온수(0.01% TFA)를 사용하였다. 검출파장은 203 nm였고, 샘플의 온도는 20℃, 컬럼의 온도는 25℃로 유지하였으며 표준용액 및 시험용액은 20 μl를 주입하였다. 0–20분은 실제 분석시간으로 HPLC 크로마토그램이 기록되었으며, 20–27분은 컬럼의 세척, 27–35분은 초기 이동상 조건으로 컬럼이 포화되는 시간으로 설정하였다. 이동상의 유속 및 조성은 Table I과 같다.
표준용액의 조제 – Spicatoside A (순도 99.25%) 표준물질 약 10.08 mg을 정밀히 칭량하여 메탄올 10 ml에 녹여 농도가 1.0 mg/ml인 표준원액을 조제하였으며 밸리데이션 시험법 항목에 맞게 메탄올로 적절히 희석하여 표준용액을 조제하였다.
고체상추출(solid phase extraction, SPE) 카트리지 제작 – C18 고체상 2.0 g을 정밀히 칭량하여 플라스틱 공컬럼에 넣었으며 감압을 이용하여 균일하게 충진하였고, 폴리프로필렌 필터를 넣어 고체상을 밀봉하였다. SPE 카트리지는 시험에 사용되는 각 시료마다 새로 제작한 것을 전처리에 사용하였다.
시험용액의 조제 – 맥문동추출분말 약 10–20 g을 정밀히 칭량하여 100 ml 정용플라스크에 넣은 후, 탈이온수(0.1% TFA)을 정용 플라스크 부피의 80%를 넣어 30분간 초음파진탕기에서 추출한 후 탈이온수(0.1% TFA)로 정용플라스크의 100 ml 표선까지 정용하였으며 이 용액을 시험용액으로 하였다.
시험용액의 전처리 – SPE 카트리지에 메탄올 10 m1를 흘려주어 C18 고체상을 수화시킨 후 10% 메탄올 (0.1% TFA)을 10 ml를 첨가하여 전처리 초기 상태로 만들었다. 맥문동추출분말 시험용액 2 ml를 SPE 카트리지에 주입한 후 시험용액이 고체상 내로 모두 흡수되도록 하였고 시험용액이 모두 흡수된 SPE 카트리지에 10% 메탄올(0.1% TFA)를 6 ml를 넣어 용출시켜 친수성 성분들을 제거하였다. 이후 90% 메탄올 용액 3 ml를 넣어 흘려주었으며 이 때 용출되는 90% 메탄올 용액을 25 ml 용량의 농축 플라스크에 모두 받아 감압농축기를 이용하여 용매를 제거하였다. 이후 SPE 카트리지에 메탄올 6 ml를 넣어 다시 용출시켰고 이를 90% 메탄올 용출물이 있는 농축 플라스크에 다시 받아 감압농축기를 이용하여 용매를 제거하였다. 고형물이 있는 농축 플라스크에 메탄올 2 ml를 넣어 초음파 진탕기를 이용하여 고형물을 충분히 용해시켰고, 이 용액 1 ml를 취하여 0.45 μm 멤브레인필터를 이용하여 여과한 후 HPLC 분석에 사용하였다.
특이성 평가 – 표준용액(spicatoside A 12.5 μg/mL)과 전처리한 시험용액 [맥문동추출분말 100 mg/ml (spicatoside A로서 약 5 μg/ml)]의 HPLC 크로마토그램을 통해 spicatoside A 피크 및 인근 물질 피크의 머무름 시간 및 spicatoside A의 UV 스펙트럼 비교를 통해 시험법의 특이성을 측정하였다.
직선성 평가 – 5개의 농도(3.125, 6.25, 12.5, 25, 50 μg/ml)의 spicatoside A 표준용액을 HPLC를 이용하여 측정하였으며 농도별 면적을 구하여 검량선을 구하였다. 상기과정을 3회 반복하였으며 결정계수(r2)의 값이 0.990 이상인지 여부를 확인하였다.
정확도 평가 – 맥문동추출분말 10 g (spicatoside A로서 약 500 mg)을 정밀히 칭량하여 100 mL 정용플라스크에 탈이온수(0.1% TFA) 80 ml를 넣어 용해시켰다. 이 후 30분간 초음파 진탕기에서 충분히 용해시킨 후 탈이온수(0.1% TFA)을 넣어 정용플라스크의 표선까지 정용하여 맥문동추출분말 용액 100 mg/ml (spicatoside A로서 약 5 μg/ml)을 조제하였다. 이 용액 1900 ml에 각각 메탄올(0%) 및 100 μg/ml, 150 μg/ml, 200 μg/ml 농도에 해당하는 spicatoside A 표준용액 100 μl를 넣어 첨가한 spicatoside A의 최종농도가 각각 0 μg/ml (0%), 5 μg/ml (100%), 7.5 μg/ml (150%), 10 μg/ml (200%)이 되도록 하였으며 이를 시험용액의 전처리 방법을 통해 분석시료를 조제하였다. 전처리를 통한 시험용액의 경우 ① 메탄올(0%) ② 최종농도 5 μg/ml (100%) 첨가한 분석 시료 ③ 최종농도 7.5 μg/ml (100%) 첨가한 분석시료 ④ 최종농도 10 μg/mL (100%) 첨가한 분석시료를 각각 총 5회 반복 조제하였고 각각 분석시료의 측정은 다른 날에 수행하였으며, 측정된 spicatoside A 농도인 μg/mL 단위를 다시 μg/g의 단위로 환산하여 식약처의 기준과 비교하였다.
반복성 평가 – 맥문동추출분말 10, 15, 20 g을 정밀히 칭량하여 각각 100 ml 정용플라스크에 탈이온수(0.1% TFA) 80 ml를 넣어 충분히 용해시켰다. 이 용액을 30분간 초음파 진탕기에서 충분히 용해시킨 후 탈이온수(0.1% TFA)을 넣어 정용 플라스크의 표선까지 정용하여 맥문동추출분말 용액 100 mg/ml, 150 mg/ml, 200 mg/ml을 조제하였으며, 각각의 시험용액을 전처리하였다. 전처리한 시험용액은 각 농도당 5개씩 반복 조제하였고 조제된 총 15개의 시험용액은 같은 날 HPLC를 이용하여 분석하였으며 측정된 spicatoside A농도인 μg/mL 단위를 다시 μg/g의 단위로 환산하여 식약처의 기준과 비교하였다. 일내정밀도는 1회 실시하는 것이 원칙이나 신뢰성을 더 확보하기 위해 다른 날 2회 실시하였다.
재현성 평가 – 맥문동추출분말 10, 20 g을 정밀히 칭량하여 각각 100 ml의 탈이온수(0.1% TFA) 80 ml를 넣어 초음파 진탕기에서 충분히 용해시켜 맥문동추출분말 100 mg/ml, 200 mg/ml에 해당하는 시험용액을 조제하였으며, 각각의 용액을 상기한 전처리하였다. 전처리한 시험용액을 하루에 각 농도당 2개씩 총 4개 반복 조제하였으며, 조제된 시험용액은 같은 날 HPLC 분석하였다. 이를 6일 반복하여 총 24개의 시험용액을 조제하여 분석하였으며. Spicatoside A의 측정 농도인 μg/mL 단위를 다시 μg/g의 단위로 환산하여 식약처의 기준과 비교하였다.
정량한계 측정 – 7개의 농도(1.5625, 3.125, 6.25, 12.5, 25, 50, 100 μg/ml)의 spicatoside A 표준용액을 HPLC를 이용하여 측정하였으며 농도별 면적을 구하여 검량선을 구하였다. 상기과정을 3회 반복하였으며 정량한계는 검량선 기울기 평균(S) 및 y 절편의 표준편차(σ)를 이용하였고 계산식은 아래와 같다.
정량한계 = 10 × σ/S.
결과 및 고찰
본 연구는 HPLC-PDA를 이용하여 맥문동 추출물에 함유된 spicatoside A를 정량분석법을 개발하고자 하였는데, 추출물에 함유된 spicatoside A의 함량은 추출물의 건조무게 대비 0.001–0.01%이었다. 선행연구에서는 원추출물에서는 spicatoside A는 검출이 되지 않았으며 부탄올을 이용한 유기용매 분획법을 이용해서 당류 성분을 비롯한 친수성 성분을 제거한 시료를 분석했을 때에 검출되었다. Spicatoside A의 함량은 국내 다른 연구진에 의해 수행된 연구에 비하여 낮게 확인되었는데13,14) 이는 타 연구진은 맥문동을 추출하기 위해서 80% 수성메탄올을 이용한 열탕추출법을 사용한 반면, 본 연구에서는 60℃의 비교적 저온 조건에서 30% 수성에탄올을 이용해 추출하였기 때문에 spicatoside A의 추출 효율이 낮아졌다고 추정된다. 또한 Kim 등의 연구에서 가압 용매추출법을 이용하여 spicatoside A의 최적 추출온도(130℃) 및 최적 에탄올 농도(86%)를 산출하였는데,14)이는 본 연구에 사용된 맥문동추출물의 spicatoside A 함량이 낮은 이유를 간접적으로 뒷받침해준다.
따라서 HPLC-UV를 통해 미량 함유된 spicatoside A의 신뢰성 있는 분석법을 개발하기 위해서 친수성 성분 제거가 필수적이었으며 이를 위해 시험용액의 전처리 과정을 도입하였다. 시험용액의 전처리는 C18 고체상을 사용한 고체상추출(solid phase extraction)방법을 이용하였고, 개발된 정량분석법은 특이성, 직선성, 정확도, 재현성, 반복성, 정량한계의 6가지 항목의 측정을 통해 신뢰성을 평가하였으며(method validation), 모두 식약처에서 설정한 ‘한약(생약)제제의 성분 프로파일 설정 및 가이드라인’에서 제시한 기준과 비교하여 분석방법의 신뢰성을 입증하였다.
특이성 – HPLC 크로마토그램을 이용해 표준용액, 시험용액의 분석에 간섭현상이 없음을 확인하였다. 표준용액에서의 spicatoside A의 머무름 시간은 15.222 분이었고 시험용액에 함유된 spicatoside A의 머무름 시간은 15.381분이었다. 또한 HPLC 피크에 대한 UV 스펙트럼은 표준용액 및 시험용액이 일치함을 확인하였으며 시험용액의 HPLC 크로마토그램에서 spicatoside A의 주변에 성분 분석에 간섭하는 성분 피크가 검출되지 않아 특이성이 있음을 확인하였다(Fig. 1).
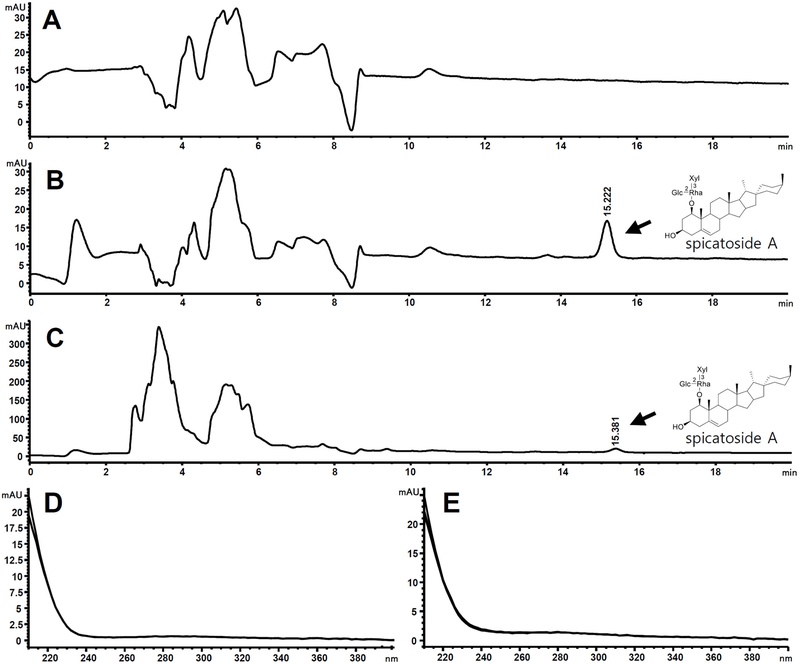
HPLC chromatogram of blank (methanol) (A), authentic spicatoside A (B), pretreated sample solution of Liriope platyphylla extract (C), UV spectrum of authentic spicatoside A (D), and UV spectrum of spicatoside A in the pretreated sample solution of Liriope platyphylla extract (E).
직선성 – 3.125–50 μg/ml 범위의 5개 농도범위에서의 검량선을 작성하였으며 검량선의 결정계수(R2) 값이 0.9998–0.9999 범위에 있어 직선성을 확인하였고 이는 식약처 기준 (R2 > 0.990)에 적합하였다(Table II).
정확도 – 회수율은 최종농도 5.0, 7.5, 10.0 μg/ml를 첨가한 시험용액들에서 측정한 각각의 spicatoside A 함량을 0% 첨가농도 시험용액 지표물질 함량 평균인 52.9029 μg/ml를 감하여 증가한 양을 계산하였고 이를 회수율(%)로 변환하였다. 회수율은 92.8–105.2% 범위로 측정되었으며 이는 식약처 기준(지표성분 10–100 ppm 구간일 때 80–110% 범위)에 적합함을 확인하였다(Table III).
반복성(일내정밀도) – 100 mg/ml, 150 mg/ml, 200 mg/ml의 세 가지 농도에 해당하는 맥문동추출물 시료 각 5개씩 조제하였으며(총 15개 시료) 이를 전처리한 후 분석하였다. 시료에 함유된 spicatoside A의 함량 평균은 μg/g으로 환산하였고 반복성은 다른 날 2회 실시하였다.
- 1차 반복성: 15개 시료에 함유된 spicatoside A의 평균함량은 59.3 μg/g이며, 상대표준편차(RSD%)는 3.9–5.4%로 식약처 기준(지표성분 10–100 ppm 구간일 때 7.3% 이내) 범위 이내에 있었다(Table IV).
- 2차 반복성: 15개 시료에 함유된 spicatoside A의 함량 평균은 58.8 μg/g이며, 상대표준편차(RSD%)는 2.0–5.0%로 식약처 기준(지표성분 10–100 ppm 구간일 때 7.3% 이내) 범위 이내에 있었다(Table IV).
재현성(일간정밀도) – 100 mg/ml, 200 mg/ml의 두 가지 농도에 해당하는 맥문동추출물 시료를 이용하여 하루에 각 2개씩 총 4개 시료를 조제하고 전처리하여 분석하였고 이를 1일 1회, 총 6일 반복하였다. 100 mg/ml와 200 mg/ml의 맥문동추출물에 함유된 spicatoside A의 함량 평균은 μg/g으로 환산하여 각각 54.9, 53.5 μg/g이었고, 전체 함량에 대한 상대표준편차(RSD%)는 5.7%로 측정되어 식품의약품안전처 기준(10–100 ppm의함량구간일때 11% 이내)에 부합하였다.
정량한계 – 1.5625–100 μg/ml 사이에 있는 7개 농도범위의 spicatoside A 표준용액을 HPLC를 이용하여 농도에 따른 피크면적을 측정하였으며 표준용액을 3회 분석하여 얻은 검량선의 기울기와 y 절편 값을 이용하여 정량한계를 구하였다. 기울기 평균은 15.05이며 y 절편의 표준편차는 1.87으로 계산식을 통해 정량한계는 1.24 μg/ml로 측정하였다.
결 론
맥문동의 주성분으로 스테로이드성 사포닌이 잘 알려져 있으나, 이 성분군은 극히 소량만 존재하며, 실제로는 다당체를 포함한 친수성 성분이 전체 추출물 중량의 50–70% 이상을 차지하는 것으로 보고되고 있다. 이러한 특성으로 인해, spicatoside A와 같이 상대적으로 미량 함유된 성분을 HPLC-UV(PDA)로 분석하기 위해서는 친수성 물질의 제거가 필요하다. 본 연구에서는 C18 고체상 추출(solid-phase extraction, SPE)을 이용하여 맥문동추출물 내 친수성 물질을 제거하는 전처리 과정을 도입하였으며, 이 방법을 기반으로 한 정량분석법의 신뢰성을 특이성, 직선성, 정확도, 재현성, 반복성, 검출한계의 측정을 통해 확인하였다. 시험용액의 전처리 과정은 다소 복잡하지만, 고가의 분석 장비(HPLC-MS 등)를 사용하지 않고도 분석이 가능하다는 점에서 본 분석법은 경제성과 실용성을 동시에 갖춘 방법으로 판단된다.
Acknowledgments
본 연구는 농림축산식품부 산하 한국식품연구원의 식품기능성 평가 지원 사업 및 한국연구재단의 대학중점연구소 지원사업(#2018R1A6A1A03025108)을 통하여 수행되었습니다.
Conflict of interest: The authors have no conflict of interest to declare.
References
-
Shang, Z. P., Wang, F., Zhang, J. Y., Wang, Z. J., Lu, J. Q., Wang, H. Y. and Li, N. (2017) The genus Liriope: Phytochemistry and pharmacology. Chin. J. Nat. Med. 15: 801-815.
[https://doi.org/10.1016/S1875-5364(18)30014-1]

-
Lei, F., Weckerle, C. S. and Heinrich, M. (2021) Liriopogons (Genera Ophiopogon and Liriope, Asparagaceae): A critical review of the phytochemical and pharmacological research. Front. Pharmacol. 12: 769929.
[https://doi.org/10.3389/fphar.2021.769929]

- 생약학교재 편찬위원회 (2018) 생약학. pp 255-257. 동명사, 경기.
-
Ramalingam, M. and Kim, S. J. (2016) Pharmacological activities and applications of Spicatoside A. Biomol. Ther. 24: 469-474.
[https://doi.org/10.4062/biomolther.2015.214]

- Shin, J. S. (2002) Saponin composition of Liriope platyphylla and Ophiopogon japonicus. Kor. J. Crop Sci. 47: 236-239.
- Yang, E. S., Cho, Y., Chin, Y. W., Lee, K. Y., Kim, S. H., Kim, H. K., Kim, Y. C. and Sung, S. H. (2008) Quantitative determination of spicatoside A using HPLC-CAD and opti- mized pressurized liquid extraction of spicatoside A from Liriope platyphylla. Korean Pharmaceutical Association Fall Symposium & Conference Abstracts 2008: 284.
-
Fang, J., Wang, X., Lu, M., He, X. and Yang, X. (2018) Recent advances in polysaccharides from Ophiopogon japonicus and Liriope spicata var. prolifera. Int. J. Biol. Macromol. 114: 1257-1266.
[https://doi.org/10.1016/j.ijbiomac.2018.04.022]

-
Kim, D. H., Oh, D. R., Baek, S. Y. and Kim, M. R. (2019) Quality characteristics and antioxidant activities of aged black Liriope platyphylla. Food Sci. Preserv. 26: 505-512.
[https://doi.org/10.11002/kjfp.2019.26.5.505]

-
Chen, M. H., Leong, F., Gao, S. J., Chen, X., Lu, J. J., Lin, L. G., Wang, Y. and Chen, X. J. (2023) Comparison of Ophiopogon japonicus and Liriope spicata var. prolifera from different origins based on multi-component quantification and anticancer activity. Molecules 28: 1045.
[https://doi.org/10.3390/molecules28031045]

-
Negi, J. S., Singh, P., Pant, G. J. and Rawat, M. S. (2011) High-performance liquid chromatography analysis of plant saponins: An update 2005–2010. Pharmacogn. Rev. 5: 155-158.
[https://doi.org/10.4103/0973-7847.91109]

-
Wang, Y., Ma, Y., Tao, L., Zhang, X., Hao, F., Zhao, S., Han, L. and Bai, C. (2022) Recent advances in separation and anal- ysis of saponins in natural products. Separations 9: 163.
[https://doi.org/10.3390/separations10010016]

- 건강기능식품 기능성 원료 인정을 위한 제출자료 작성 가이드 (2024) 식품의약품안전처 행정간행물 (등록번호: 안내서-0769-07).
-
Park, C. H., Morgan, A. M. A., Park, B. B., Lee, S. Y., Lee, S., Kim, J. K., Park, S. U. (2019) Metabolic analysis of four cultivars of Liriope platyphylla. Metabolites 9: 59.
[https://doi.org/10.3390/metabo9030059]

-
Lee, K. S., Kim, G. H., Kim, H. H., Choi, J. W., Lee, H. C., Song, M. R., Kim, M. R., Lee, G. H. (2009) Physicochemical characteristics of Liriope platyphylla tubers by ddrying pro- cess. J. Korean Soc. Food Sci. Nutr. 38: 1104-1110.
[https://doi.org/10.3746/jkfn.2009.38.8.1104]

-
Kim, S. H., Kim, H. K., Yang, E. S., Lee, K. Y., Kim, S. D., Kim, Y. C., Sung, S. H. (2010) Optimization of pressurized liquid extraction for spicatoside A in Liriope platyphylla. Sep. Purif. Technol. 71: 168-172.
[https://doi.org/10.1016/j.seppur.2009.11.016]

