개서어나무 잎의 항Helicobacter pylori 활성물질
Abstract
In our ongoing research for anti-Helicobacter pylori compounds from natural resources, the methanol extract of Carpinus tschonoskii Maxim. (Betulaceae), Asian hornbeam, distributed in eastern Asia showed significant anti-Helicobacter pylori activity. Five fractions of n-hexane, CH2Cl2, EtOAc, n-BuOH, and aqueous fractions were obtained from the MeOH extract of C. tschonoskii leaves, and tested against H. pylori strains 51 and 26695. The EtOAc fraction, demonstrating superior inhibitory activity, was subjected to further chromatography, leading to the isolation of four flavonols, namely isoquercetin (1), quercitrin (2), afzelin (3), and kaempferol (4), and a hydroquinone (5). The chemical structures of these compounds were elucidated using UV, 1H-NMR, 13C-NMR, and mass spectrometry. Among these isolates, compounds 4 and 5 displayed significant growth inhibition on H. pylori at a final concentration of 100 μM. While compound 4 showed anti-H. pylori activity against both the tested strains 51 and 26695 with MIC50 values of 63.6 µM and 55.1 µM, respectively, the values of compound 5 were more than 100 µM for the two strains. Structurally, compound 3, with a rhamnose moiety at the oxygen atom of the C-3 position of compound 4, failed to exhibit a significant inhibitory capability. Molecular docking studies predicted that compound 4 interactions occur at αTyr32, αVal33, βPhe441, and βLys445 of H. pylori urease 1E9Y. The five isolated compounds, except compound 3, are novel reports of isolation from this plant. Moreover, compound 1 is isolated first from the genus Carpinus. These findings suggest that the EtOAc fraction of C. tschonoskii leaves or kaempferol may be useful candidates for eradicating H. pylori infection. Further studies are required to elucidate the exact mechanism of action and their efficacy on the human body with safety issues.
Keywords:
Carpinus tschonoskii, Anti-Helicobacter pylori activity, Flavonols, Kaempferol, Hydroquinone위장관 질환은 전 세계적으로 심각한 건강 문제 중 하나이며, 그 중 소화성궤양은 빠르게 증가하고 있는 추세이다.1) 소화성궤양 질환은 위장관 내 점막에 대한 손상요인이 방어기전보다 강하게 작용할 때 발생한다. 위점막은 위산으로부터 손상을 방지하기 위하여 다양한 생리적 기전을 갖추고 있는데, 상피세포의 재생, 보호물질의 분비(점액, 중탄산염, 프로스타글란딘, NO 등), 점막혈류증가에 따른 장벽형성 등이 포함된다. 반면에, 손상요인에는 위산 분비를 유도하는 다양한 요인으로 펩신 및 담즙과 같은 소화액, 스트레스, 음주 및 흡연, 비스테로이드성 소염제(NSAIDs)의 장기복용이 있으며, Helicobacter pylori와 같은 균에 의한 감염 등이 있다.2) H. pylori는 나선형의 그람음성균이며 세계보건기구(World Health Organization, WHO)에서 지정한 1급 발암물질이다. 일반적으로 길이는 2.8–3.3 µm, 직경은 0.55–0.58 µm이며 대기보다 낮은 산소 농도에서 생존하는 미호기성(microaerophilic) 특성을 지닌다.3) H. pylori는 편모를 통해 장관 내강에서 점막으로 이동할 수 있으며,4) 다양한 병원인자를 통해 감염을 유발한다. 주요인자로는 urease, lipopolysaccharides, catalase, TNFα 유도 단백질(Tipα), cytotoxin-associated antigen A(CagA), mucinase, protease, lipase 등의 분비 효소 및 vacuolating cytotoxin autotransporter (VacA) 가 있다.5-10)
1983년 이전까지는 강한 산성환경인 위 내부에서는 세균이 생존할 수 없다는 것이 정설이었으나, Barry J. Marshall과 John R. Warren에 의해 H. pylori가 위 내부에서 생존하며 위장관 질환의 주요 원인이라는 사실이 밝혀졌다.11,12) 즉, H. pylori는 점막에 부착한 후 빠르게 증식하고 적응하며, 그 과정에서 urease를 생성하여 요소(urea)를 이산화탄소와 암모니아로 전환한다. 암모니아는 균 주변의 미세환경을 중성으로 유지하고, 수소이온의 역확산을 촉진하여 위산으로부터의 생존을 돕는다. 이와 동시에 이산화탄소는 물과 반응하여 탄산을 형성하며, 위점막에 대한 공격 요인으로 작용한다.13)
현재까지 가장 널리 사용되고 H. pylori 제균 치료법에는 일반적으로 프로톤 펌프 억제제(proton pump inhibitors, PPI)와 2–3종의 항생제를 병용하는 삼제 또는 사제요법(triple or quadruple therapy)이 있다.14) 치료 효과를 극대화하기 위해서는 환자의 상태, 증상의 중증도, 기저질환 등을 고려한 약제 선택이 필수적이다. 그러나 기존 치료법에 사용되는 약물로 인한 오심, 어지러움, 복부팽만감 등의 부작용과 내성발생률의 증가가 치료의 걸림돌이 되고 있다.15,16) 따라서, 기존 치료법의 보조제로서 내성발생률을 줄이고 부작용이 적은 천연물의약 소재의 발굴 및 천연성분의 도출연구가 진행되어 왔다.17)
개서어나무(Carpinus tschonoskii Maxim.)는 자작나무과(Betulaceae)에 속하는 동아시아 지역 자생의 낙엽성 다년생 식물로, 전초, 잎, 수피 등 여러 부위에 대하여 약리활성 연구가 진행되었으며, 주요한 약용자원으로 주목받고 있다. 현재까지 이 식물로부터 20여 종의 flavonoids, polyketide derivatives, tannins 계열 성분 등이 분리보고되었으며,18–23) 항노화 및 항여드름, 항멜라닌, 항증식 및 항세포사멸, 비만세포 탈과립 억제, 신경세포보호, 염증성 사이토카인 생성억제 등의 다양한 생리활성을 나타내는 것으로 보고되었다.19,22-28)
본 연구실에서는 그 동안 우리나라 생약자원에 함유되어 있는 항H. pylori 활성을 지닌 물질을 연구 해왔으며, 그 일환으로 개서어나무의 메탄올 추출물이 항H. pylori 활성을 보였기에, 본 연구에서는 개서어나무 잎의 메탄올 추출물로부터 항H. pylori 활성을 나타내는 생리활성 물질을 규명하고자 하였다.
재료 및 방법
식물재료 – 연구에 사용된 개서어나무(Carpinus tschonoskii Maxim.) 잎은 2023년 6월에 경상남도 진주시 월아산에서 채집하였으며, 채집한 시료는 경상국립대학교 약학대학 안미정 교수의 감정을 받은 뒤 사용하였다. 일부는 표본(PGSC-651, 652)으로 제작하여 경상국립대학교 표본실(Herbarium of the College of Pharmacy, Gyeongsang National University)에 보관 중이다.
시약 및 기기 – 추출 및 분획에 사용된 시약으로는 메탄올, n-hexane, CH2Cl2, EtOAc, n-BuOH을 Daejung Chemicals & Metals (Siheung, South Korea)에서 구입하여 사용하였으며, DMSO는 Junsei (Tokyo, Japan) 제품을 사용하였다. 아니스알데하이드 시약은 Sigma-Aldrich (St. Louis, MO, USA)에서 구입하여 사용하였다. HPLC 분석용 물과 아세토나이트릴(ACN)은 Fisher Scientific (Hampton, NH, USA)에서 구입하였고, NMR 분석용 용매인 CD3OD 및 CDCl3는 Eurisotop (Tewksbury, MA, USA) 제품을 사용하였다. H. pylori 배양 및 활성측정에는 Brucella Broth (BD Co., MD, USA)와 말 혈청(Horse serum, Gibco, NY, USA)을 사용하였고, 양성대조군으로는 quercetin (Sigma-Aldrich)과 metronidazole (Sigma-Aldrich)을 사용하였다. 컬럼크로마토그래피(CC)의 충진재로는 silica gel 60 (0.040-0.063 mm, Merck, Darmstadt, Germany)와 RP silica gel (C18, 0.040-0.063 mm, Merck), Sephadex LH-20 (Cytiva, Uppsala, Sweden)을 사용하였으며, 박층크로마토그래피(TLC)용 plate는 silica gel 60 F254 (Merck)를 사용하였다. MPLC에는 Biotage Isolera Flash Chromatography System (Charlotte, NC, USA)을 사용하였다. HPLC는 Agilent 1260 Infinity binary HPLC system (Santa Clara, CA, USA)을 사용하였으며, ChemStation 소프트웨어(Agilent Technologies, Germany)로 데이터 분석을 수행하였다. 이때 사용된 컬럼은 Gemini C18 column (110 Å, 4.6 × 250 mm, 5 μm) (Phenomenex, Torrance, CA, USA)이며, 흡광도 측정에는 Optizen POP (Mecasys, Daejeon, South Korea) 분광기를 사용하였다. MS 스펙트럼은 Xevo G2-XS TOF (Waters, MA, USA) 및 X500R (AB SCIEX, MA, USA)을 사용하여 얻었고, NMR 스펙트럼은 DRX-300 (Bruker, MA, USA)나 AvanceNeo400 nanobay (Bruker), AvanceNeo600 (Bruker)를 사용하여 얻었다.
추출 및 분획 – 건조한 개서어나무 잎(2.7 kg)을 메탄올로 초음파 추출하여 얻은 추출액을 감압농축하여 메탄올 총 추출물(579.4 g)을 얻었다. 여기에 증류수를 가하여 현탁시킨 후 용매극성을 점차 올려가며 n-hexane (19.2 g), CH2Cl2 (21.0 g), EtOAc (181.2), n-BuOH (221.0 g), 물 분획물(84. 3g)을 얻었다. 이 중 EtOAc 분획물에 대하여 Gemini C18 column (110 Å, 4.6 × 250 mm, 5 μm)을 사용하여 semi-preparative HPLC를 실시하였다. 물(A)과 ACN (B) 혼합용액을 전개용매로 0 min, 10% B; 0–50 min, 10% B; 50–51 min, 100% B; 51–55 min, 100%로 설정하였으며, 유속은 1 mL/min으로 유지하였다. 그 결과, 210 nm에서 화합물 1 (1.1 mg, tR 31 min), 2 (0.9 mg, tR 36 min), 3 (2.2 mg, tR 43 min)을 얻었다. 이후 동일한 EtOAc 분획물에 대하여 CH2Cl2와 메탄올의 혼합용액(100:0 → 0:100)을 전개용매로 하여 open silica gel CC을 실시하여 총 8개의 소분획물(fr. 1–fr. 8)을 얻었다. 그다음, 소분획물 fr. 2 (1.036 g)에 대하여 물과 메탄올의 혼합용액(100:0 → 0:100)을 전개용매로 open RP silica gel CC를 실시하여 33개의 소분획물(fr. 2.1–fr. 2.33)을 얻었다. 소분획물 fr. 2.1 (229 mg)으로부터 재결정과정을 통하여 화합물 5 (15.7 mg)를 얻었다. 소분획물 fr. 2.26 (53. 3mg)에 대해서 메탄올을 전개용매로 Sephadex LH-20 CC를 실시하여 화합물 4 (46.3 mg)를 얻었다.
Isoquercetin (1) – Yellow amorphous powder; C21H20O12, ESI-QTOF-MS (m/z): 465.1019 [M+H]+ (calcd. C21H21O12, 465.1033); 1H-NMR (300 MHz, CD3OD): δ 7.73 (1H, d, J=2.2 Hz, H-2ʹ), 7.61 (1H, dd, J=8.5, 2.2 Hz, H-6ʹ), 6.88 (1H, d, J=8.5 Hz, H-5ʹ), 6.42 (1H, d, J=2.1 Hz, H-8), 6.23 (1H, d, J=2.1 Hz, H-6), 5.28 (1H, d, J=7.5 Hz, H-1ʹʹ), 3.72 (1H, dd, J=11.8, 2.3 Hz, H-6ʹʹa), 3.59 (1H, dd, J=11.8, 5.2, H-6ʹʹb), 3.50 (1H, t, J=8.9 Hz, H-2ʹʹ), 3.47 (1H, J=8.9 Hz, H-3ʹʹ), 3.44 (1H, t, J=8.0 Hz, H-4ʹʹ) 3.24 (1H, m, H-5ʹʹ); 13C-NMR (150 MHz, CD3OD): δ 178.1 (C-4), 165.0 (C-7), 161.6 (C-5), 157.6 (C-2), 157.1 (C-8a), 148.5 (C-4ʹ), 144.5 (C-3ʹ), 134.2 (C-3), 121.8 (C-6ʹ), 121.7 (C-1ʹ), 116.1 (C-5ʹ), 114.6 (C-2ʹ), 104.2 (C-4a), 102.9 (C-1ʹʹ), 98.6 (C-6), 93.4 (C-8), 77.0 (C-5ʹʹ), 76.7 (C-3ʹʹ), 74.3 (C-2ʹʹ), 69.8 (C-4ʹʹ), 61.1 (C-6ʹʹ).
Quercitrin (2) – Yellow amorphous powder; C21H20O11, ESI-QTOF-MS (m/z): 449.1073 [M+H]+ (calcd. C21H21O11, 449.1084); 1H-NMR (300 MHz, CD3OD): δ 7.34 (1H, d, J=2.1 Hz, H-2ʹ), 7.32 (1H, dd, J=8.2, 2.1 Hz, H-6ʹ), 6.93 (1H, d, J=8.2 Hz, H-5ʹ), 6.39 (1H, d, J=2.1 Hz, H-8), 6.22 (1H, d, J=2.1 Hz, H-6), 5.36 (1H, d, J=1.6 Hz, H-1ʹʹ), 4.24 (1H, dd, J=3.3, 1.6 Hz, H-2ʹʹ), 3.76 (1H, dd, J=9.5, 3.3 Hz, H-3ʹʹ), 3.44 (1H, dd, J=9.5, 6.0 Hz, H-5ʹʹ), 3.35 (1H, d, J=9.5 Hz, H-4ʹʹ), 0.96 (3H, d, J=6.0 Hz, 6ʹʹ-CH3); 13C-NMR (100 MHz, CD3OD): δ 178.3 (C-4), 164.5 (C-7), 161.8 (C-5), 157.9 (C-2), 157.1 (C-8a), 148.4 (C-4ʹ), 145.0 (C-3ʹ), 134.8 (C-3), 121.6 (C-1ʹ), 121.5 (C-6ʹ), 115.5 (C-2ʹ), 115.0 (C-5ʹ), 104.5 (C-4a), 102.1 (C-1ʹʹ), 98.4 (C-6), 93.3 (C-8), 71.9 (C-4ʹʹ), 70.7 (C-3ʹʹ), 70.6 (C-2ʹʹ), 70.5 (C-5ʹʹ), 16.2 (C-6ʹʹ).
Afzelin (3) – Orange amorphous powder; C21H20O10, ESI-QTOF-MS (m/z): 433.1126 [M+H]+ (calcd. C21H21O10, 433.1135); 1H-NMR (300 MHz, CD3OD): δ 7.79 (2H, d, J=8.8 Hz, H-2ʹ and H-6ʹ), 6.95 (2H, d, J=8.8 Hz, H-3ʹ and H-5ʹ), 6.40 (1H, d, J=2.1 Hz, H-8), 6.23 (1H, d, J=2.1 Hz, H-6), 5.40 (1H, d, J=1.7 Hz, H-1ʹʹ), 4.24 (1H, dd, J=3.4, 1.7 Hz, H-2ʹʹ), 3.73 (1H, dd, J=5.8, 3.4, H-3ʹʹ), 3.36 (1H, m, H-4ʹʹ), 3.35 (1H, m, H-5ʹʹ), 0.94 (3H, d, J=5.8 Hz, H-6''); 13C-NMR (100 MHz, CD3OD): δ 178.2 (C-4), 164.5 (C-7), 161.8 (C-5), 160.2 (C-4ʹ), 157.9 (C-8a), 157.2 (C-2), 134.8 (C-3), 130.5 (C-2ʹ and C-6ʹ), 121.2 (C-1ʹ), 115.1 (C-3ʹ and C-5ʹ), 104.5 (C-4a), 102.1 (C-1ʹʹ), 98.4 (C-6), 93.3 (C-8), 71.8 (C-4ʹʹ), 70.7 (C-2ʹʹ), 70.6 (C-3ʹʹ), 70.5 (C-5ʹʹ), 16.2 (C-6ʹʹ).
Kaempferol (4) – Yellow amorphous powder; C15H10O6, API-QTOF-MS (m/z): 286.0489 [M]+ (calcd. C15H11O6, 286.0477); 1H-NMR (300 MHz, CD3OD): δ 8.11 (2H, d, J=9.1 Hz, H-2ʹ and H-6ʹ), 6.93 (2H, d, J=9.1 Hz, H-3ʹ and H-5ʹ), 6.41 (1H, d, J=2.1 Hz, H-8), 6.20 (1H, d, J=2.1 Hz, H-6); 13C-NMR (100 MHz, CD3OD): δ 176.0 (C-4), 164.4 (C-7), 161.1 (C-5), 159.2 (C-4ʹ), 156.9 (C-8a), 146.6 (C-2), 135.7 (C-3), 129.3 (C-2ʹ and H-6ʹ), 122.3 (C-1ʹ), 114.9 (C-3ʹ and H-5ʹ), 103.1 (C-4a), 97.9 (C-6), 93.1 (C-8).
Hydroquinone (5) – Brown crystalline powder; C6H6O2, API-QTOF-MS (m/z): 110.0377 [M]+ (calcd. C6H7O2, 110.0368); 1H-NMR (300 MHz, CD3OD): δ 6.56 (4H, s, H-2, H-3, H-5 and H-6); 13C-NMR (100 MHz, CD3OD): δ 150.2 (C-1 and C-4), 116.1 (C-2, C-3, C-5 and C-6).
균배양 – 실험에 사용한 H. pylori 51, 26695 균주는 Helicobacter pylori 분리균주은행[Helicobacter pylori Korean Type Culture Collection (HKTCC), 경상국립대학교 의학대학 미생물학교실]에서 분양받아 실험에 사용하였다. 균주 51은 2005년 우리나라 위암 환자로부터 분리된 임상균주이며,29) 균주 26695는 1997년 영국인 환자로부터 분리된 ATCC 표준균주이다.30) 각 균주를 말혈청(Gibco, NY, USA)이 10% 첨가된 Brucella Broth (BD, MD, USA) 액체배지를 사용하여 37℃, 10% CO2 조건에서 배양하였으며, 24시간마다 계대배양하였다.
항H. pylori 활성측정 – 최소억제농도(Minimum Inhibitory Concentration, MIC)를 측정하기 위해 액체배지희석법을 진행하였다. MIC는 해당 화합물이 H. pylori의 생장을 억제하는데 필요한 최소농도를 의미하며, MIC50은 H. pylori의 생장을 50% 억제하는데 필요한 최소농도를 의미한다.31) 각 균주를 6 well plate에 8시간 동안 배양하여 얻은 각 균주의 균액을 최종농도가 2–3 × 108 cfu/mL가 되게끔 Brucella Broth 액체배지에 현탁하여 사용하였다. 시료는 DMSO로 녹여 최종농도가 100 μg/mL이 되도록 맞추었다. 그 다음 37℃, 10% CO2 조건에서 24시간동안 배양한 후 흡광도를 600 nm에서 측정하였다. 음성대조군으로는 DMSO를 사용하였고 양성 대조군으로는 quercetin과 metronidazole을 사용하였다. MIC와 MIC50 값은 GraphPad Version 5.01 (GraphPad Software, Inc., San Diego, CA, USA)을 이용하여 계산하였다. H. pylori에 대한 억제율은 다음과 같은 식을 사용하였다.
억제율(%) = [(음성대조군 흡광도 – 시료 흡광도) / 음성 대조군 흡광도] × 100
통계처리 – 모든 실험은 3회 반복으로 실시하였으며, 그 결과를 평균 ± 표준편차(mean ± SD)로나타내었다. 통계학적 비교분석은 SPSS statistics 24.0 (IBM, Armonk, NY, USA)을 이용하여 일원분산분석(One-way ANOVA)으로 실시하였으며, p값이 0.05 미만인 경우를 통계적으로 유의한 것으로 판단하였다.
분자도킹시뮬레이션(Molecular docking simulation) – 항H. pylori 활성을 나타낸 화합물들에 대해 분자도킹시뮬레이션을 수행하였다. 이를 위해 H. pylori가 보유한 urease 효소의 결정 구조를 기반으로 분석을 진행하였으며, 단백질 구조정보는 RCSB Protein Data Bank에서 확보하였다. 사용된 구조는 ID: 1E9Y와 ID: 1E9Z로, 각각 acetohydroxamic acid가 결합된 H. pylori urease 복합체구조와 urease의 단독결정구조이다. 분자도킹분석은 분리된 화합물의 화학구조를 리간드로 설정한 후 수행하였으며, 해당 화합물은 효소의 기질결합 부위에 작용하는 리간드로 작용하였다. 도킹 과정에는 AutoDockTools 1.5.6와 AutoDock Vina, Discovery Studio Visualizer의 소프트웨어를 사용하였다. AutoDockTools 1.5.6은 단백질과 리간드의 구조를 준비하고 최적화하며, 활성부위를 예측하는데 사용하였다. AutoDock Vina는 결합친화도(binding affinity)를 계산하는데 사용하였고, Discovery Studio Visualizer는 최소결합에너지 상태에서의 도킹구조 등 3차원 공간에서의 결합위치 및 방향, 그리고 상호작용하는 원자들을 시각화하는 데 사용하였다.32)
결과 및 고찰
개서어나무(C. tschonoskii) 잎의 메탄올 추출물은 H. pylori 51, 26695 두 균주에 대하여 최종농도 100 μg/mL에서 유의미한 항H. pylori 활성을 보였다. 이러한 결과를 바탕으로 메탄올 총추출물을 물에 현탁한 후 n-hexane, CH2Cl2, EtOAc, n-BuOH으로 극성을 높여 가며 분획하여 각각의 분획물과 물분획물을 얻었다. 이들 분획물의 항H. pylori 활성을 평가한 결과, EtOAc 분획물이 100 μg/mL의 농도에서 51, 26695 균주에 대해 각각 92.6%와 84.5%의 억제율을 보여 다른 분획물들에 비해 높은 항H. pylori 활성을 보였다(Table I). EtOAc 분획물의 억제활성은 양성대조군으로 사용한 metronidazole의 억제활성과 유사하였으며, 다른 양성대조군인 quercetin보다 높은 억제활성을 보였다.
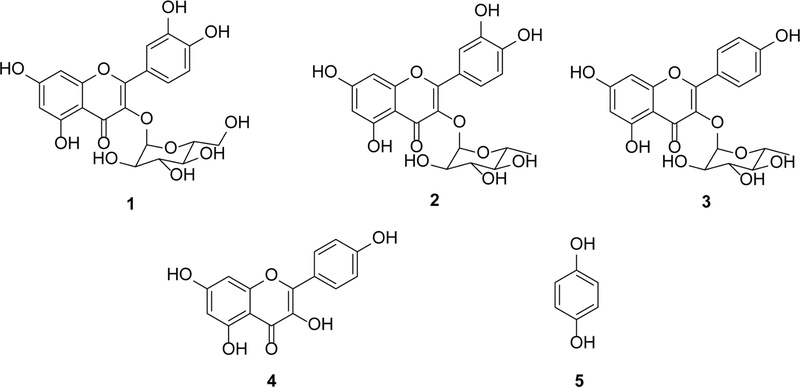
해당 결과를 바탕으로, 가장 높은 항H. pylori활성을 보인 EtOAc 분획물로부터 silica gel, RP silica gel, Sephadex LH-20을 이용한 컬럼크로마토그래피와 semi-preparative HPLC를 실시하여 5개(1–5)의 주요성분을 분리하였다. 분리한 화합물의 NMR, MS spectrum과 같은 분광학적 데이터를 기존에 보고된 데이터와 대조한 결과, 각 화합물의 화학구조를 isoquercetin (1), quercitrin (2), afzelin (3), kaempferol (4)의 4가지 flavonol 화합물과 phenol 화합물인 hydroquinone (5)으로 동정하였다(Fig. 1).33-37) 화합물 3을 제외한 나머지 화합물들은 C. tschonoskii로부터의 처음으로 분리보고되는 물질이며, 화합물 1은 Carpinus 속에서 처음으로 분리보고되는 물질이다.
다음으로 분리한 화합물(1–5)의 51과 26695 두 균주에 대한 항H. pylori 활성을 최종농도 100 μM에서 측정하였다. 화합물 4의 H. pylori에 대한 억제활성은 각 균주에 대하여 각각 91.5%와 91.9%로 양성대조군으로 사용한 metronidazole과 유사하게 높은 억제활성을 보였다(Table II). 화합물 5의 억제활성은 각각 28.9%와 15.8%로 화합물 4보다는 낮은 활성을 보였다. 다른 화합물에서는 유의미한 억제활성이 관찰되지 않았다. 따라서 항H. pylori 활성을 보인 화합물 4와 5에 대한 MIC와 MIC50 값을 측정하였다. 그 결과, 화합물 4의 MIC 값은 51과 26695 균주에 대하여 25 μM이었으며, 화합물 5의 MIC 값은 각각 50 μM과 100 μM이었다. 화합물 4의 MIC50 값은 51과 26695 균주에 대하여 각각 63 .57 μM와 55.07 μM이었고, 화합물 5의 MIC50 값은 100 μM 이상이었다. 화합물 4의 항H. pylori 활성이 화합물 5보다 유의적으로 높았다(Table III). 화합물 4의 MIC와 MIC50 값은 양성대조군으로 사용한 metronidazole의 MIC와 MIC50 값보다는 높았으며, quercetin의 MIC와 MIC50 값보다는 낮았다.
화합물 1의 경우, 본 연구에서 사용한 51과 26695 균주에 대하여 유의미한 활성이 나타나지 않았지만, H. pylori 43504 균주에 대해서는 약한 항균활성을 나타내었다는 보고가 있다.38) 화합물 4와 5의 H. pylori 타 균주(NCTC11637, NCTC11916, ATCC43504, 193, P12, ATCC49503 등)에 대한 항균활성은 알려져 있으며,39) 본 연구에서 가장 높은 억제활성을 보인 kaempferol (4)의 경우에는 본 연구에서 사용한 균주들에 대해서도 항H. pylori 활성이 알려져 있다.40)
본 연구에서 분리된 4종의 flavonol계 성분(1–4) 중에서는 화합물 4만이 항H. pylori 활성을 보였다. 화합물 1과 2는 quercetin의 C-3 위치의 hydroxyl group에 각각 glucose와 rhamnose가 결합하고 있는 배당체이다. 비당체인 quercetin은 본 연구에서 positive control로 사용될만큼 천연성분 중에서 유의미한 항H. pylori 활성이 알려져 있는 것에 반해, 배당체인 1과 2는 유의미한 억제활성을 보이지 않았다. 분리한 5종의 화합물 중 가장 높은 억제활성을 보인 kaempferol (4)은 afzelin (3)의 aglycone이며, 화합물 3은 4의 C-3 위치의 hydroxyl group에 rhamnose moiety가 결합되어 있는 구조로 유의미한 억제활성을 보이지 않았다. 따라서, flavonol계열 성분의 항H. pylori 활성에 있어서는 C-3 위치의 hydroxyl group이 필수적인 것으로 추정된다. 또한, kaempferol (4)의 항H. pylori 활성이 quercetin보다 높은 것으로 보아 flavonol 구조의 B-ring의 3′,4′-catechol group보다 4′-hydroxyl group을 가진 flavonol의 항H. pylori 활성이 높은 것으로 추정할 수 있다. 페놀성 화합물인 화합물 5는 tyrosinase 저해제로 tyrosine의 melanin으로 전환을 억제하여 피부미백작용을 나타내는 것으로 잘 알려진 물질이다.41) 따라서, 기존에 보고된 개서어 나무잎 추출물의 피부미백작용은 hydroquinone 성분에 기인한다고 볼 수 있다.
한편, H. pylori의 생장억제활성을 보인 kaempferol (4)과 hydroquinone (5)의 H. pylori에 또한 억제활성기전을 알아보기 위하여 분자도킹시뮬레이션을 통하여 H. pylori urease(PDB ID: 1E9Y 및 1E9Z)에 대한 결합친화도(binding affinity)와 상호작용 유형을 분석하였다(Table IV). 그 결과, 두 화합물 모두 상대적으로 낮은 결합에너지를 보였으며, 화합물 4의 urease 1E9Y와 1E9Z에 대한 결합에너지가 각각 −8.7과 −8.5 kcal/mol로 화합물 5의 결합에너지(−5.0와 −5.0 kcal/mol)보다 더 낮아 urease에 대한 결합친화도가 더 높다는 것을 알 수 있었다. 이는 화합물 4의 항H. pylori 활성이 화합물 5의 억제활성보다 높은 앞의 결과와 일치하며, 화합물 4와 5의 항H. pylori 활성이 H. pylori urease에 대한 억제로 인한 것으로 추정할 수 있다. 두 화합물 모두 urease 1E9Y에 대해서는 공통적으로 α32와 β445에 존재하는 tyrosine과 lysine과는 친수성 상호작용(hydrophilic interaction)을, β441 위치의 phenylalanine과는 소수성 상호작용(hydrophobic interaction)을 하는 것으로 관찰되었다. 화합물 4의 경우에는 1E9Y와 1E9Z 모두에서 β471 위치의 glutamine과 친수성 상호작용을, α33의 valine과는 소수성 상호작용을 하며, 화합물 5의 경우에는 1E9Y와 1E9Z 두 효소에 대하여 β445 위치의 lysine과의 친수성 상호작용을 제외한 나머지 상호작용의 유형이 일치하였다(Fig. 2, Table IV).
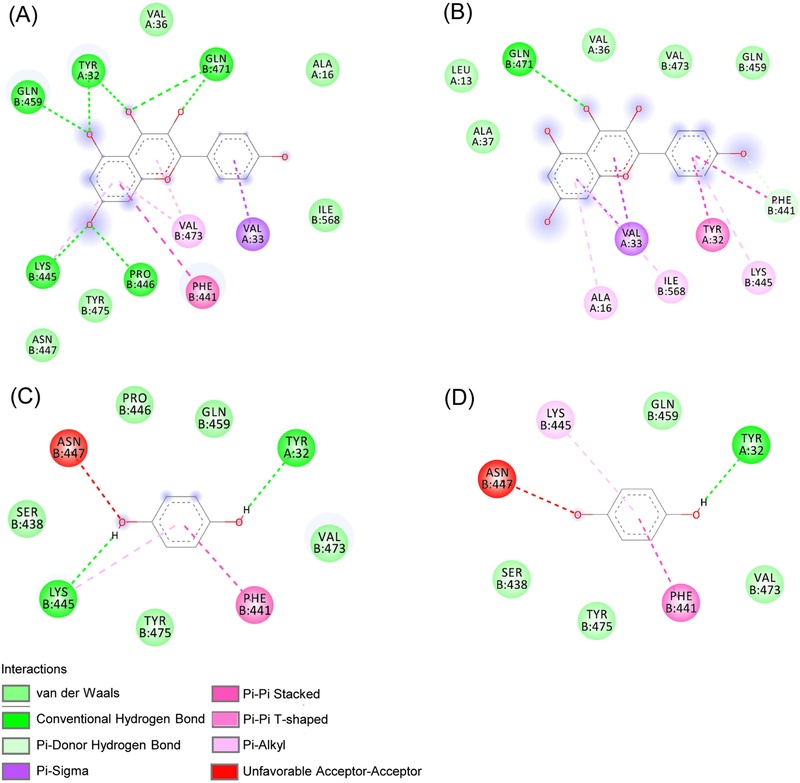
Molecular docking simulation of compounds 4 and 5 with H. pylori urease 1E9Y and 1E9Z. (A) and (B), Interactions of compound 4 with H. pylori urease 1E9Y and 1E9Z, respectively. (C) and (D), Interactions of compound 5 with H. pylori urease 1E9Y and 1E9Z, respectively.
결 론
개서어나무(Carpinus tschonoskii) 잎 추출물로부터 얻은 분획물 중에서 가장 높은 항H. pylori 활성을 보인 EtOAc 분획에 대하여 주요물질분리를 실시하여 4종의 flavonol 화합물인 isoquercetin (1), quercitrin (2), afzelin (3), kaempferol (4)과 페놀성 화합물인 hydroquinone (5)의 총 5개의 화합물을 분리하였다. 이 중 afzelin (3)을 제외한 나머지 화합물들은 C. tschonoskii로부터 처음으로 분리보고되는 물질이고, isoquercetin (1)은 Carpinus 속에서 처음으로 분리 보고되는 물질이다. 분리한 5종의 화합물 중에서 kaempferol (4)와 hydroquinone (5)의 두 화합물이 유의미한 항H. pylori 활성을 나타내었으며, kaempferol의 H. pylori 생장억제활성이 hydroquinone보다 높았다. 또한, 구조-활성상관관계를 분석한 결과 flavonol의 C-3 위치의 free hydroxyl group의 존재가 항H. pylori 활성에 필수적이라는 것을 알 수 있었다. 이상으로 개서어나무 잎의 항H. pylori 활성은 kaempferol과 hydroquinone에 기인한다는 것을 알 수 있었다. 또한, 분자 도킹시뮬레이션을 통하여 이 두 화합물의 항H. pylori활성이 urease에 대한 억제활성에 의한 것이라고 추정할 수 있었다. 개서어나무 잎 추출물의 항H. pylori 활성을 처음으로 보고되는 것이며, 그 유효성분이 kaempferol과 hydroquinone이라는 것을 본 연구에서 처음으로 밝혔다. 이상의 연구결과는 향후 개서어나무의 추출물과 kaempferol 유도체에 대한 심층연구를 통하여 이들 물질들의 항H. pylori 활성을 가진 위장관질환 치료제로서의 개발가능성을 제시한다.
Acknowledgments
본 연구는 농촌진흥청의 지역특화작목기술개발사업의 일환인 경남지역 도라지 거점 생산단지 구축 및 고기능성 제품화기술 개발(RS-2025-14383142) 과제와, 교육부와 경상남도의 재원으로 지원을 받아 수행된 경상남도 지역혁신중심 대학지원체계(RISE) (2025-RISE-16-001), 국립산림과학원 산림바이오소재연구소 연구(FE0100-2023-02-2025)의 지원에 의해 이루어진 결과로 이에 감사드립니다.
References
- WHO Mortality database: Interactive platform for mortality data, global report of peptic ulcer disease by Map. 2024. (https://platform.who.int/mortality/themes/theme-details/topics/indicator-groups/indicator-group-details/MDB/peptic-ulcer-disease, )
-
Lemos, M., Santin, J. R., Júnior, L. C. K., Niero, R. and Andrade, S. F. D. (2011) Gastroprotective activity of hydroalcoholic extract obtained from the leaves of Brassica oleracea var. acephala DC in different animal models. J. Ethnopharmacol. 138: 503-507.
[https://doi.org/10.1016/j.jep.2011.09.046]

-
Goodwin, C. S., Armstrong, J. A., Chilvers, T., Peters, M., Collins, M. D., Sly, L., McConnell, W. and Harper, W. E. S. (1989) Transfer of Campylobacter pylori and Campylobacter mustelae to Helicobacter gen. nov. as Helicobacter pylori comb. nov. and Helicobacter mustelae comb. nov., respectively. Int. J. Syst. Bacteriol. 39: 397-405.
[https://doi.org/10.1099/00207713-39-4-397]

-
Duan, Q., Zhou, M., Zhu, L. and Zhu, G. (2013) Flagella and bacterial pathogenicity. J. Basic Microbiol. 53: 1-8.
[https://doi.org/10.1002/jobm.201100335]

-
Lin, Q., Lin, S., Fan, Z., Liu, J., Ye, D. and Guo, P. (2024) A review of the mechanisms of bacterial colonization of the mammal gut. Microorganisms 12: 1026.
[https://doi.org/10.3390/microorganisms12051026]

-
Testerman, T. L. and Morris, J. (2014) Beyond the stomach: An updated view of Helicobacter pylori pathogenesis, diagnosis, and treatment. World J. Gastroenterol. 20: 12781.
[https://doi.org/10.3748/wjg.v20.i36.12781]

-
Ramarao, N., Gray‐Owen, S. D. and Meyer, T. F. (2000) Helicobacter pylori induces but survives the extracellular release of oxygen radicals from professional phagocytes using its catalase activity. Mol. Microbiol. 38: 103-113.
[https://doi.org/10.1046/j.1365-2958.2000.02114.x]

-
Watanabe, T., Takahashi, A., Suzuki, K., Kurusu-Kanno, M., Yamaguchi, K., Fujiki, H. and Suganuma, M. (2014) Epithelial-mesenchymal transition in human gastric cancer cell lines induced by TNF-α-inducing protein of Helicobacter pylori: Cell migration induced by Tipα of H. pylori. Int. J. Cancer 134: 2373-2382.
[https://doi.org/10.1002/ijc.28582]

-
Broutet, N., Marais, A., Lamouliatte, H., De Mascarel, A., Samoyeau, R., Salamon, R. and Mégraud, F. (2001) cagA status and eradication treatment outcome of anti-Helicobacter pylori triple therapies in patients with non-ulcer dyspepsia. J. Clin. Microbiol. 39: 1319-1322.
[https://doi.org/10.1128/JCM.39.4.1319-1322.2001]

-
Hisatsune, J., Yamasaki, E., Nakayama, M., Shirasaka, D., Kurazono, H., Katagata, Y., Inoue, H., Han. J., Sap, J., Yahiro, K., Moss, J. and Hirayama, T. (2007) Helicobacter pylori VacA enhances prostaglandin E2 production through induction of cyclooxygenase 2 expression via a p38 mitogen-activated protein kinase/activating transcription factor 2 cascade in AZ-521 cells. Infect. Immun. 75: 4472-4481.
[https://doi.org/10.1128/IAI.00500-07]

- Marshall, B. J., Royce, H., Annear, D. I., Goodwin, C. S., Pearman, J. W., Warren, J. R. and Armstrong, J. A. (1984) Original isolation of Campylobacter pyloridis from human gastric mucosa. Micobios Lett. 25: 83-88.
-
FitzGerald R. and Smith, S. M. (2021) An overview of Helicobacter pylori infection. Methods Mol. Biol. 2283: 1-14.
[https://doi.org/10.1007/978-1-0716-1302-3_1]

-
Ha, N. C., Oh, S. T., Sung, J. Y., Cha, K. A., Lee, M. H. and Oh, B. H. (2001) Supramolecular assembly and acid resistance of Helicobacter pylori urease. Nat. Struct. Biol. 8: 505-509.
[https://doi.org/10.1038/88563]

-
Gené, E., Calvet, X., Azagra, R. and Gisbert, J. P. (2003) Triple vs. quadruple therapy for treating Helicobacter pylori infection: a meta‐analysis. Aliment. Pharmacol. Ther. 17: 1137-1143.
[https://doi.org/10.1046/j.1365-2036.2003.01566.x]

-
Graham, D. Y., Lee, Y. C. and Wu, M. S. (2014) Rational Helicobacter pylori therapy: Evidence-based medicine rather than medicine-based evidence. Clin. Gastroenterol. Hepatol. 12: 177-186.
[https://doi.org/10.1016/j.cgh.2013.05.028]

-
Bell, G. D., Powell, K., Burridge, S. M., Pallecaros, A., Jones, P. H., Gant, P. W., Harrison, G. and Trowell, J. E. (1992) Experience with‘triple’ anti-Helicobacter pylori eradication therapy: side effects and the importance of testing the pretreatment bacterial isolate for metronidazole resistance. Aliment. Pharmacol. Ther. 6: 427-435.
[https://doi.org/10.1111/j.1365-2036.1992.tb00556.x]

-
Osato, M. S., Reddy, R. and Graham, D. Y. (1999) Metronidazole and Clarithromycin resistance amongst Helicobacter pylori isolates from a large metropolitan hospital in the United States. Int. J. Antimicrob. Agents 12: 341-347.
[https://doi.org/10.1016/S0924-8579(99)00079-5]

-
Yin, J., Ahn, H. S., Ha, S. Y., Hwang, I. H., Yoon, K. D., Chin, Y. W. and Lee, M. W. (2019) Anti-skin ageing effects of phenolic compounds from Carpinus tschonoskii. Nat. Prod. Res. 33: 3317-3320.
[https://doi.org/10.1080/14786419.2018.1497026]

- Hwang, J. W. (2020) Neuroprotective effects of Carpinus tschonoskii leaves extract against glutamate-induced oxidative stress in HT22 Hippocampal cells. Jeju National University. Master Thesis.
-
Yamada, P., Ono, T., Shigemori, H., Han, J. and Isoda, H. (2012) Inhibitory effect of tannins from galls of Carpinus tschonoskii on the degranulation of RBL-2H3 cells. Cytotechnology 64: 349-356.
[https://doi.org/10.1007/s10616-012-9457-y]

-
Shigemori, H. and Ono, T. (2009) Two new hydrolyzable tannins, Carpinerins A and B, from galls of Carpinus tschonoskii. Heterocycles 78: 1993.
[https://doi.org/10.3987/COM-09-11683]

-
Yin, J., Hwang, I. H. and Lee, M. W. (2019) Anti-acne vulgaris effect including skin barrier improvement and 5α-reductase inhibition by Tellimagrandin I from Carpinus tschonoskii. BMC Complement. Altern. Med. 19: 323.
[https://doi.org/10.1186/s12906-019-2734-y]

-
Goenka, S., Ceccoli, J. and Simon, S. R. (2021) Anti-melanogenic activity of ellagitannin casuarictin in B16F10 mouse melanoma cells. Nat. Prod. Res. 35: 1830-1835.
[https://doi.org/10.1080/14786419.2019.1636242]

- Kim, H. H., Park, K. H., Kim, M. H., Oh, M. H., Kim, S. R., Park, K. J., Heo, J. H. and Lee, M. W. (2013) Antiproliferative effects of native plants on prostate cancer cells. Nat. Prod. Sci. 19: 192-200.
-
Kim, M.-K., Kim, S.-C., Kang, J.-I., Boo, H.-J., Hyun, J.-W., Koh, Y.-S., Park, D.-B., Yoo, E.-S., Kang, J.-H. and Kang, H.-K. (2010) Neuroprotective effects of Carpinus tschonoskii MAX on 6-hydroxydopamine-induced death of PC12 cells. Biomol. Ther. 18: 454-462.
[https://doi.org/10.4062/biomolther.2010.18.4.454]

-
Koo, J.-E., Hong, H.-J., Mathema, V. B., Kang, H.-K., Hyun, J.-W., Kim, G.-Y., Kim, Y.-R., Maeng, Y.-H., Hyun, C.-L., Chang, W.-Y. and Koh, Y.-S. (2012) Inhibitory effects of Carpinus tschonoskii leaves extract on CpG-stimulated pro-inflammatory cytokine production in murine bone marrow-derived macrophages and dendritic cells. In Vitro Cell. Dev. Biol. Anim. 48: 197-202.
[https://doi.org/10.1007/s11626-012-9495-y]

-
Kang, S.-H., Koo, J.-E., Hong, H.-J., Mathema, V. B. and Koh, Y.-S. (2012) Anti-inflammatory activity of Carpinus tschonoskii leaves extract in R848-stimulated bone marrow-derived macrophages and dendritic cells. J. Bacteriol. Virol. 42: 77.
[https://doi.org/10.4167/jbv.2012.42.1.77]

-
Kang, G.-J., Kang, N.-J., Han, S.-C., Koo, D.-H., Kang, H.-K., Yoo, B.-S. and Yoo, E.-S. (2012) The chloroform fraction of Carpinus tschonoskii leaves inhibits the production of inflammatory mediators in HaCaT keratinocytes and RAW 264.7 macrophages. Toxicol. Res. 28: 255-262.
[https://doi.org/10.5487/TR.2012.28.4.255]

- Kang, H.-L., Lee, W.-K., Song, J.-Y., Choi, S.-H., Park, S.-G., Ryu, B.-D., Lee, E.-J., Kim, J.-S., Park, J.-U., Baik, S.-C., Choi, M.-B., Youn, H.-S., Ko, G.-H., Bae, D.-W., Kim, Y.-S., Cho, M.-J., and Rhee, K.-H. (2005) Helicobacter pylori strain 51 (Korean isolate): Ordered overlapping BAC library, Combined physical and genetic map, and comparative analysis with H. pylori strain 26695 and strain J99. J. Microbiol. Biotechnol. 15: 844-854.
-
Tomb, J. F., White, O., Kerlavage, A. R., Clayton, R. A., Sutton, G. G., Fleischmann, R. D., Ketchum, K. A., Klenk, H. P., Gill, S., Dougherty, B. A., Nelson, K., Quackenbush, J., Zhou, L., Kirkness, E. F., Peterson, S., Loftus, B., Richardson, D., Dodson, R., Khalak, H. G., Glodek, A., McKenny, K., Fitzegerald, L. M., Lee, N., Adams, M. D., Hickey, E. K., Berg, D. E., Gocyane, J. D., Utterback, T. R., Peterson, J. D., Kelly, J. M., Cotton, M. D., Weidman, J. M., Fujii, C., Bowman, C., Watthey, L., Wallin, E., Hayes, W. S., Borodovsky, M., Karp, P. D., Smith, H. O., Fraser, C. M. and Venter J. C. (1997) The complete genome sequence of the gastric pathogen Helicobacter pylori. Nature 388: 539-547.
[https://doi.org/10.1038/41483]

-
Kadeřábková, N., Mahmood, A. J. S. and Mavridou, D. A. I. (2024) Antibiotic susceptibility testing using minimum inhibitory concentration (MIC) assays. npj Antimicrob. Resist. 2: 37.
[https://doi.org/10.1038/s44259-024-00051-6]

-
Trott, O. and Olson, A. J. (2010) AutoDock Vina: Improving the speed and accuracy of docking with a new scoring function, efficient optimization, and multithreading. J. Comput. Chem. 31: 455-461.
[https://doi.org/10.1002/jcc.21334]

-
Huang, H.-M., Ho, C.-Y., Chang, G.-R., Shia, W.-Y., Lai, C.-H., Chao, C.-H., and Wang, C.-M. (2021) HPLC/ESI-MS and NMR analysis of chemical constitutes in bioactive extract from the root nodule of Vaccinium emarginatum. Pharmaceuticals 14: 1098.
[https://doi.org/10.3390/ph14111098]

-
Napolitano, J. G., Lankin, D. C., Chen, S.-N., and Pauli, G. F. (2012) Complete 1H NMR spectral analysis of ten chemical markers of Ginkgo biloba. Magn. Reson. Chem. 50: 569-575.
[https://doi.org/10.1002/mrc.3829]

-
Oliveira, E. S. C., Pontes, F. L. D., Acho, L. D. R., Rosário, A. S., Silva, B. J. P., Bezerra, J. A., Campos, F. R., Lima, E. S. and Machado, M. B. (2021) qNMR quantification of phenolic compounds in dry extract of Myrcia multiflora leaves and its antioxidant, anti-AGE, and enzymatic inhibition activities. J. Pharm. Biomed. Anal. 201: 114109.
[https://doi.org/10.1016/j.jpba.2021.114109]

-
Tenkeu, A. C., Mabou, F. D., Botezatu, A. V. D., Tamokou, J. D. D., Takongmo, G. M., Tomasi, S., Voutquenne-Nazabadioko, L., Dinica, R. M., Tsopmo, A., and Ngnokam, D. (2025) 15-Methylhexadecanoic acid and other chemical constituents from Calliandra calothyrsus (Meisn) (Fabaceae) with their antibacterial activities. Nat. Prod. Sci. 31: 24-31.
[https://doi.org/10.20307/nps.2025.31.1.24]

-
Crecely, R. W., Butler, R. S. and Goldstein, J. H. (1968) The 13C-H satellite NMR spectra of para-benzoquinone, hydroquinone and para-dimethoxybenzene. J. Mol. Spectrosc. 26: 489-495.
[https://doi.org/10.1016/S0022-2852(68)80064-5]

-
Konstantinopoulou, M., Karioti, A., Skaltsas, S. and Skaltsa, H. (2003) Sesquiterpene lactones from Anthemis altissima and their anti-Helicobacter pylori Activity. J. Nat. Prod. 66: 699-702.
[https://doi.org/10.1021/np020472m]

-
Termentzi, A., Fokialakis, N. and Skaltsounis, A. L. (2011) Natural resins and bioactive natural products thereof as potential antimicrobial agents. Curr. Pharm. Des. 17: 1267-1290.
[https://doi.org/10.2174/138161211795703807]

-
Moon, S. H., Lee, J. H., Kim, K.-T., Park, Y.-S., Nah, S.-Y., Ahn, D. U. and Paik, H.-D. (2013) Antimicrobial effect of 7-O-butylnaringenin, a novel flavonoid, and various natural flavonoids against Helicobacter pylori strains. Int. J. Environ. Res. Public Health 10: 5459-5469.
[https://doi.org/10.3390/ijerph10115459]

-
Gold, M. H. and Biron, J. (2011) Efficacy of a novel hydroquinone‐free skin‐brightening cream in patients with melasma. J. Cosmet. Dermatol. 10: 189-196.
[https://doi.org/10.1111/j.1473-2165.2011.00573.x]