
삼중 음성 유방암 줄기세포에서 Wnt/β-Catenin 경로 억제를 통한 알파-망고스틴의 세포독성 효과
Abstract
Triple-negative breast cancer stem cells (TNBCSCs) play a critical role in the high aggressiveness, metastatic potential, and therapeutic resistance of triple-negative breast cancer (TNBC). Consequently, targeting TNBCSCs represents a promising strategy to improve clinical outcomes in TNBC patients. α-Mangostin, a natural xanthone compound isolated from the tropical fruit Garcinia mangostana (mangosteen), has attracted attention for its potential anticancer properties. In this study, we investigated the inhibitory effects of α-mangostin on the growth of TNBCSCs derived from MDA-MB-231 and HCC1937 cell lines. Our results demonstrated that α-mangostin significantly inhibited both the proliferation and tumorsphere-forming capacity of TNBCSCs. Importantly, this antiproliferative effect was closely associated with the induction of apoptosis. Further mechanistic analysis revealed that α-mangostin suppressed the Wnt/β-Catenin signaling pathway and reduced the expression of key stemness-related markers. Collectively, these findings suggest that α-mangostin may serve as a promising natural therapeutic agent for the prevention and treatment of TNBC by targeting its cancer stem cell population.
Keywords:
α-Mangostin, Triple-negative breast cancer stem cells, Apoptosis, β-Catenin유방암은 전 세계 여성에게 가장 흔하게 진단되는 암으로, 2022년에는 약 230만 건의 신규 발병과 67만 건의 사망 사례가 보고되었다.1) 이 중 삼중 음성 유방암(triple-negative breast cancer, TNBC)은 전체 유방암의 약 15~20%를 차지하며, 에스트로겐 수용체, 프로게스테론 수용체, HER2 발현이 모두 결여된 아형이다.2) 이러한 분자적 특징으로 인해 표적 치료제가 부재하고, 화학요법에 대한 의존도가 높지만, 약물 저항성과 높은 재발률, 전이 가능성 때문에 환자의 생존율은 여전히 낮은 실정이다.3,4) 따라서 새로운 치료 전략의 개발은 TNBC 극복을 위한 중요한 과제로 남아 있다.
TNBC의 공격성과 치료 저항성에는 암줄기세포(cancer stem cells, CSCs)가 핵심적인 역할을 한다. CSCs는 자가재생 및 종양 개시 능력을 보유한 세포 아형으로, CD133, CD44, Nanog, Oct4, Sox2 등의 줄기세포 마커를 과발현하며, Wnt/β-Catenin, Notch, Hedgehog, JAK/STAT 등의 신호전달 경로를 통해 줄기세포성을 유지한다.5,6) 이러한 CSCs는 화학요법과 방사선치료에도 살아남아 종양의 재발과 전이를 유발하는 주요 원인으로 알려져 있다. 따라서 CSCs를 직접적으로 표적화하는 전략은 TNBC 치료 성과를 개선할 수 있는 유망한 접근법으로 주목받고 있다.
최근 천연물 유래 화합물들이 다양한 암종에서 CSCs의 줄기세포성을 억제하는 활성을 보인다는 연구가 다수 보고되었다. 예를 들어, 로즈마린산(rosmarinic acid)은 비소세포폐암 CSCs의 증식을 억제하였고, 쇠비름 추출물과 꽃송이버섯 유래 분획 역시 뇌종양 및 자궁경부암 CSCs에 대해 억제 활성을 나타냈다.7-9) 이러한 결과는 천연물 기반 화합물이 CSCs를 표적으로 하는 새로운 치료제 개발에 중요한 잠재력을 가진다는 점을 시사한다.
알파-망고스틴(α-mangostin)은 망고스틴(Garcinia mangostana) 열매 껍질에서 추출된 잔톤(xanthone) 계열의 화합물로, 항산화, 항염증, 항바이러스, 항암 효과 등 폭넓은 생리활성을 보여 왔다.10) 특히 간암, 폐암, 전립선암 등 다양한 암세포에서 세포자멸사(apoptosis)와 자가포식(autophagy)을 유도하고, 종양 성장과 전이를 억제한다는 연구들이 보고되었다.11) 더 나아가, 일부 연구에서는 α-mangostin이 CSCs의 종양구체 형성 및 줄기세포 마커 발현을 억제할 수 있음이 밝혀졌다.12,13) 그러나 TNBC 줄기세포(TNBCSCs)를 대상으로 한 α-mangostin의 효과와 그 분자적 기전은 아직 충분히 규명되지 않았다.
따라서 본 연구에서는 α-mangostin이 TNBC 유래 CSCs의 증식, 종양구체 형성, 줄기세포성 유지에 미치는 영향을 규명하고, 그 작용 기전을 분자 수준에서 평가하고자 한다. 이를 통해 α-mangostin의 항CSC 활성을 새롭게 제시하고, TNBC 치료 전략 개발에 있어 천연물 기반 후보물질로서의 가능성을 검증하고자 한다.
재료 및 방법
실험재료 − 알파-망고스틴은 Sigma-Aldrich (St. Louis, MO, USA)에서 구매하였으며, dimethyl sulfoxide (DMSO)에 100 mM 농도로 용해한 후 −20℃에서 보관하며 실험에 사용하였다. 세포배양에 사용된 DME/F-12 배지는 HyClone (Marlborough, MA, USA)에서, epidermal growth factor (EGF) 및 basic fibroblast growth factor (bFGF)는 Prospecbio (East Brunswick, NJ, USA)에서 구매하였다. B-27 supplement, penicillin/streptomycin은 Gibco (Grand Island, NY, USA)에서, Accutase는 EMD Millipore (Temecula, CA, USA)에서 확보하였으며, heparin은 Sigma-Aldrich (St. Louis, MO, USA)에서 구매하였다. 세포 생존율 평가는 CellTiter-Glo® luminescent assay kit (Promega, Madison, WI, USA)를 사용하였으며, 세포 주기 및 세포 사멸 분석은 각각 Muse® Cell Cycle kit와 Muse® Annexin V and Dead Cell kit (Luminex, Austin, TX, USA)를 이용하여 수행하였다. 세포 염색 및 기능 분석을 위한 시약으로는 4′,6-diamidino-2-phenylindole dihydrochloride (DAPI)와 tetramethylrhodamine ethyl ester perchlorate (TMRE)를 Sigma-Aldrich (St. Louis, MO, USA) 및 Invitrogen (Carlsbad, CA, USA)에서 각각 구매하였다. 단백질 발현 분석에 사용된 1차 및 2차 항체는 Cell Signaling Technology (Danvers, MA, USA), Santa Cruz Biotechnology (Dallas, TX, USA), 및 Bioss (Woburn, MA, USA)에서 구매하였다.
세포배양 − 인간 삼중 음성 유방암 세포주인 MDA-MB-231 (KCLB No. 30026)과 HCC1937 (KCLB No. 9S1937) 세포는 한국세포주은행(Seoul, Korea)에서 분양 받았다. 삼중 음성 유방암 세포주로부터 암줄기세포를 선택적으로 배양하기 위하여, EGF (20 ng/mL), bFGF (20 ng/mL), B-27 supplement (1X), heparin (5 μg/mL), 및 penicillin/streptomycin (1%)이 포함된 DME/F-12 기반 무혈청 배지를 사용하였다. 세포는 37℃, 5% CO2 조건의 이산화탄소 배양기(Thermo Scientific, Vantaa, Finland)에서 부유배양(suspension culture) 방식으로 배양하였다. 배양 3~4일 후 형성된 종양구체(tumorspheres)를 회수한 뒤, Accutase 처리하여 단일세포로 분리(dissociation)하였다. 이후 동일 조건의 무혈청 배지에서 재부유배양을 수행하였으며, 이와 같은 종양구체의 형성과 단일세포 분리 과정을 2~3회 반복함으로써 암줄기세포 특성이 강화된 세포 집단을 확보하였다. 최종적으로 확보된 세포들의 줄기세포 특성은 핵심적인 줄기세포 마커의 발현 분석을 통해 검증하였다.14)
세포 증식도 분석 − MDA-MB-231 및 HCC1937 유래 삼중 음성 유방암 줄기세포(TNBCSCs)를 각각 5×103 cells/well의 밀도로 96-well white plate에 분주한 후, 알파-망고스틴을 최종 농도 1.25, 2.5, 5, 10 μM로 처리하였다. 세포는 37℃, 5% CO2 조건의 인큐베이터에서 72시간 동안 배양하였다. 배양 후 각 well에 CellTiter-Glo® luminescent assay 기질용액 20 μL를 첨가한 뒤, 2분간 진탕 교반하고 상온에서 10분간 반응시켰다. 이후 생성된 발광 신호는 microplate reader (BioTek, Inc., Winooski, VT, USA)를 사용하여 측정하였다. 세포 증식 억제 농도의 50% (IC50) 값은 GraphPad Prism 6 (GraphPad Software, La Jolla, CA, USA)를 사용하여 분석하였다.
종양구체 형성 분석 − MDA-MB-231 및 HCC1937 유래 삼중 음성 유방암 줄기세포(TNBCSCs)를 5×103 cells/well의 밀도로 96-well plate에 분주한 후, 알파-망고스틴을 최종 농도 0.625, 1.25, 2.5, 5 μM로 처리하였다. 세포는 37℃, 5% CO2 조건의 인큐베이터에서 72시간 동안 배양하였다. 배양 후, 형성된 종양구체는 위상차 현미경(Olympus, Tokyo, Japan)을 사용하여 200배 배율에서 관찰하였으며, 직경이 100 μm를 초과하는 종양구체의 수를 계수하여 분석에 사용하였다.
세포주기 분석 − MDA-MB-231 및 HCC1937 유래 삼중 음성 유방암 줄기세포(TNBCSCs)를 2×105 cells/well의 밀도로 60-mm 배양접시에 분주한 후, 알파-망고스틴을 최종 농도 2 및 4 μM로 24시간 동안 처리하였다. 이후 세포를 회수하여 1× PBS로 세척한 뒤, 70% 에탄올을 사용하여 −20℃에서 최소 3시간 이상 고정하였다. 고정된 세포는 다시 1× PBS로 세척한 후, Muse® Cell Cycle 시약 200 μL로 염색하여 상온에서 30분간 반응시켰다. 세포주기 분포는 Guava® Muse® Cell Analyzer 및 MuseSoft_V1.8.0.3 소프트웨어(Luminex, Austin, TX, USA)를 이용하여 분석하였다.
세포자멸사 분석 − MDA-MB-231 및 HCC1937 유래 삼중 음성 유방암 줄기세포(TNBCSCs)를 2×105 cells/well의 밀도로 60-mm 배양접시에 분주하고, 알파-망고스틴을 최종 농도 2 및 4 μM로 24시간 동안 처리하였다. 처리 후 세포를 회수하여 1× PBS로 세척한 다음, Muse® Annexin V & Dead Cell 시약 100 μL로 염색하여 상온에서 20분간 반응시켰다. 세포자멸사 단계별 세포 분포는 Guava® Muse® Cell Analyzer 및 MuseSoft_V1.8.0.3 소프트웨어(Luminex, Austin, TX, USA)를 이용하여 분석하였다.
핵 형태 분석 − MDA-MB-231 및 HCC1937 유래 삼중음성 유방암 줄기세포(TNBCSCs)를 1×105 cells/well의 밀도로 24-well plate에 분주한 후, 알파-망고스틴을 최종 농도 2 및 4 μM로 처리하여 24시간 동안 배양하였다. 이후 각 well에 DAPI를 최종 농도 20 μg/mL로 처리하고, 암실에서 1시간 동안 염색하였다. 염색 후 세포는 형광현미경(Optinity KI-2000F, Korea Lab Tech, Seong Nam, Korea)을 이용하여 400배 배율에서 관찰하였으며, 핵의 형태 변화를 분석하였다.
미토콘드리아 막 전위 측정 − MDA-MB-231 및 HCC1937 유래 삼중 음성 유방암 줄기세포(TNBCSCs)를 1×105 cells/well의 밀도로 24-well plate에 분주한 후, 알파-망고스틴을 최종 농도 2 및 4 μM로 처리하여 24시간 동안 배양하였다. 이후 각 well에 TMRE를 최종 농도 50 nM로 처리하고, 암실에서 20분간 반응시켰다. 염색된 세포는 형광현미경을 이용하여 100배 배율에서 관찰하였으며, 미토콘드리아 막 전위(mitochondrial membrane potential, MMP)는 TMRE 형광 강도를 기반으로 ImageJ 소프트웨어(version 1.5; NIH, Bethesda, MD, USA)를 사용하여 정량 분석하였다.
단백질 발현 분석 − 알파-망고스틴이 단백질 발현에 미치는 영향은 western blot 분석을 통해 평가하였다. MDA-MB-231 및 HCC1937 유래 삼중 음성 유방암 줄기세포(TNBCSCs)를 5×105 cells/well의 밀도로 60-mm 배양접시에 분주한 후, 알파-망고스틴을 최종 농도 2 및 4 μM로 처리하여 24시간 동안 배양하였다. 이후 세포를 회수하여 RIPA buffer (ATTO, Tokyo, Japan)를 사용하여 용해하였으며, 획득한 세포 용해액의 단백질 농도를 정량한 후 균등하게 조절하였다. 단백질은 7.5–15% SDS-PAGE를 통해 분리한 뒤, PVDF membrane (Cytiva, Marlborough, MA, USA)으로 전이시켰다. 막은 4℃에서 표적 단백질에 대한 1차 항체로 하룻밤 동안 면역 반응시킨 후, 상온에서 horseradish peroxidase (HRP)-conjugated 2차 항체로 1시간 동안 반응시켰다. 단백질 신호는 제조사의 지침에 따라 enhanced chemiluminescence (ECL) detection kit (Dogenbio, Seoul, Republic of Korea)를 이용하여 검출하였다. 밴드의 강도는 ImageJ 소프트웨어(version 1.5; NIH, Bethesda, MD, USA)를 사용하여 정량하였으며, 표적 단백질의 발현량은 β-actin 또는 lamin A/C를 내부 대조군으로 하여 비교 분석하였다.
세포질/핵 단백질 분리 분석 − MDA-MB-231 및 HCC1937 유래 삼중 음성 유방암 줄기세포(TNBCSCs)를 5×105 cells/well의 밀도로 60-mm 배양접시에 분주한 후, 알파-망고스틴을 최종 농도 2 및 4 μM로 처리하여 24시간 동안 배양하였다. 이후 세포를 수거하여 RIPA buffer를 사용해 용해한 후, 14,000 rpm, 4℃에서 10분간 원심 분리하여 세포질 단백질(supernatant)과 핵 단백질(pellet)을 분리·회수하였다. 분리된 단백질 시료는 western blot 분석을 통해 표적 단백질의 세포 내 분획별 발현 수준을 평가하였다. 세포질 및 핵 단백질 분리의 정확성은 각각 β-actin (세포질 마커)과 lamin A/C (핵 마커)의 발현을 통해 확인하였다.
통계 처리 − 실험 결과는 최소 3번의 독립 실험에서 얻은 평균값 ± 표준편차(SD)로 표시되었다. 통계 분석은 SPSS 9.0 (SPSS Inc., Chicago, IL, USA)의 ANOVA를 사용하여 분석한 후 Tukey의 사후 검정을 통해 수행하였다. p<0.05일 경우 통계적으로 유의한 것으로 간주하였다.
결과 및 고찰
알파-망고스틴의 삼중 음성 유방암 줄기세포 증식 및 종양구체 형성 저해 효과 − 삼중 음성 유방암(TNBC) 세포주인 MDA-MB-231 및 HCC1937로부터 암줄기세포를 선택적으로 배양하기 위해, 무혈청 조건하에서의 3차원 스페로이드 배양(tumorsphere culture)을 수행하였다. 이를 통해 줄기세포 유사 특성(stem-like properties)을 갖는 종양구체(tumorspheres)를 확보하였으며, 이들을 후속 실험에 활용하였다.14,15) 우선, 알파-망고스틴이 TNBC 유래 암줄기세포의 증식(proliferation)에 미치는 영향을 분석하였다. MDA-MB-231 및 HCC1937 유래 암줄기세포에 대해 각각 1.25, 2.5, 5, 10 μM 농도의 알파-망고스틴을 72시간 동안 처리한 후, ATP 기반 발광 분석법을 통해 세포 증식 억제 활성을 평가하였다. 그 결과, 두 세포주 모두에서 알파-망고스틴의 농도 증가에 따라 세포 증식이 유의미하게 감소하였으며, IC50 값은 MDA-MB-231의 경우 2.00 μM, HCC1937의 경우 2.25 μM로 확인되었다(Fig. 1). 다음으로, 암줄기세포의 주요 기능적 지표 중 하나인 종양구체 형성 능력에 대한 알파-망고스틴의 효과를 평가하였다. TNBC 유래 암줄기세포에 0.625, 1.25, 2.5, 5 μM의 알파-망고스틴을 72시간 처리한 결과, 두 세포주 모두에서 종양구체의 크기 및 수가 농도 의존적으로 유의하게 감소하였다(Fig. 1). 이러한 결과는 알파-망고스틴이 TNBC 유래 암줄기세포의 증식 및 종양구체 형성 능력을 효과적으로 억제함을 시사하며, 향후 TNBC 치료 전략 개발을 위한 유망한 후보 물질로서의 가능성을 제시한다.
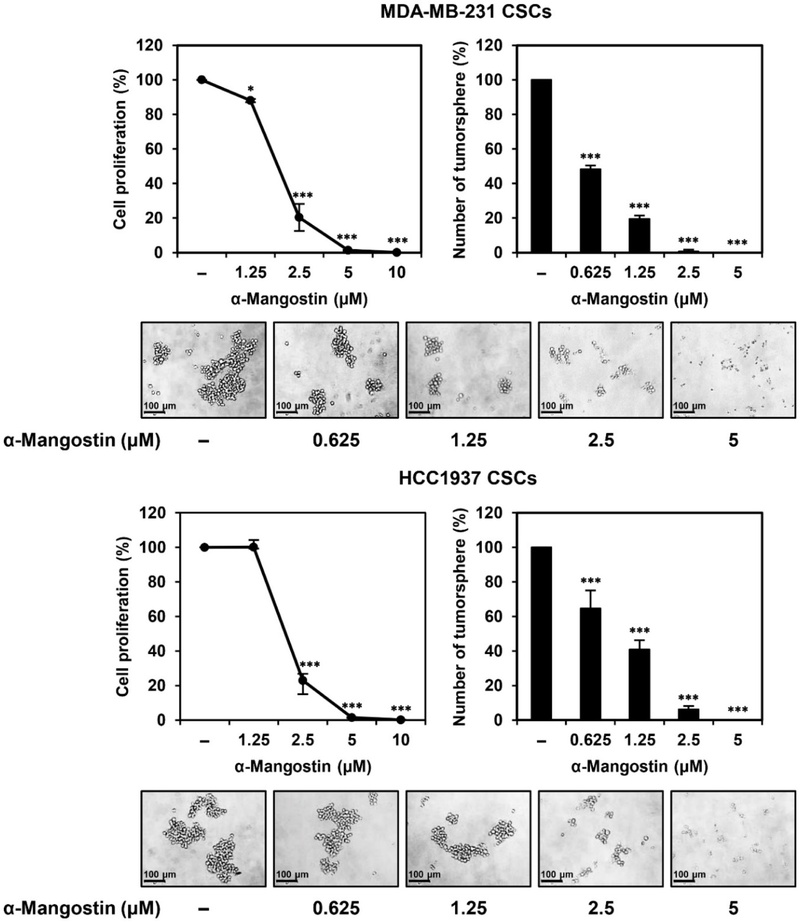
α-Mangostin inhibits the proliferation and tumorsphere formation of TNBCSCs. The effects of α-mangostin on the proliferation and tumorsphere-forming ability of TNBC stem cells (TNBCSCs) derived from MDA-MB-231 and HCC1937 cell lines were evaluated. For the proliferation assay, cells were treated with α-mangostin at concentrations of 1.25, 2.5, 5, and 10 μM and incubated for 72 h. Cell proliferation was assessed using the CellTiter-Glo® luminescent assay. For the tumorsphere formation assay, cells were treated with α-mangostin at concentrations of 0.625, 1.25, 2.5, and 5 μM and cultured for 72 h. The number and size of tumorspheres in each well were observed under an optical microscope. Data are presented as the mean ± SD (n=3). Statistical analysis was performed using one-way ANOVA with Tukey’s post hoc test. *p < 0.05, ***p < 0.001 vs. the control.
알파-망고스틴의 삼중 음성 유방암 줄기세포에 대한 세포주기 정지 및 세포자멸사 유도 효과 − 알파-망고스틴이 세포주기(cell cycle) 조절 및 세포자멸사(apoptosis)를 통해 TNBC 유래 암줄기세포의 증식을 억제하는지를 규명하기 위하여, 유세포 분석법(flow cytometry)을 이용한 정량적 분석을 수행하였다. MDA-MB-231 및 HCC1937 유래 암줄기세포에 알파-망고스틴을 2 및 4 μM 농도로 24시간 동안 처리한 후, 세포 주기 분포 변화를 분석한 결과, 두 세포주 모두에서 처리 농도 증가에 따라 sub-G1기 세포의 비율이 유의하게 증가하였다(Fig. 2A). 이어 동일한 조건에서 세포자멸사 유도 여부를 분석한 결과, 알파-망고스틴 처리군에서는 초기 및 후기 자멸사 세포를 포함한 total apoptotic cell의 비율이 대조군 대비 유의하게 증가하였다(Fig. 2B). 이와 같은 결과는 알파-망고스틴이 TNBC 유래 암줄기세포에서 세포자멸사를 유도함과 동시에 세포 주기 진행을 방해하여 sub-G1기에 세포가 축적되도록 한다는 것을 시사한다. 따라서 알파-망고스틴은 세포 주기 조절과 자멸사 유도를 병행하여 TNBC 줄기세포의 증식을 효과적으로 억제하는 기전을 가지는 것으로 판단된다.
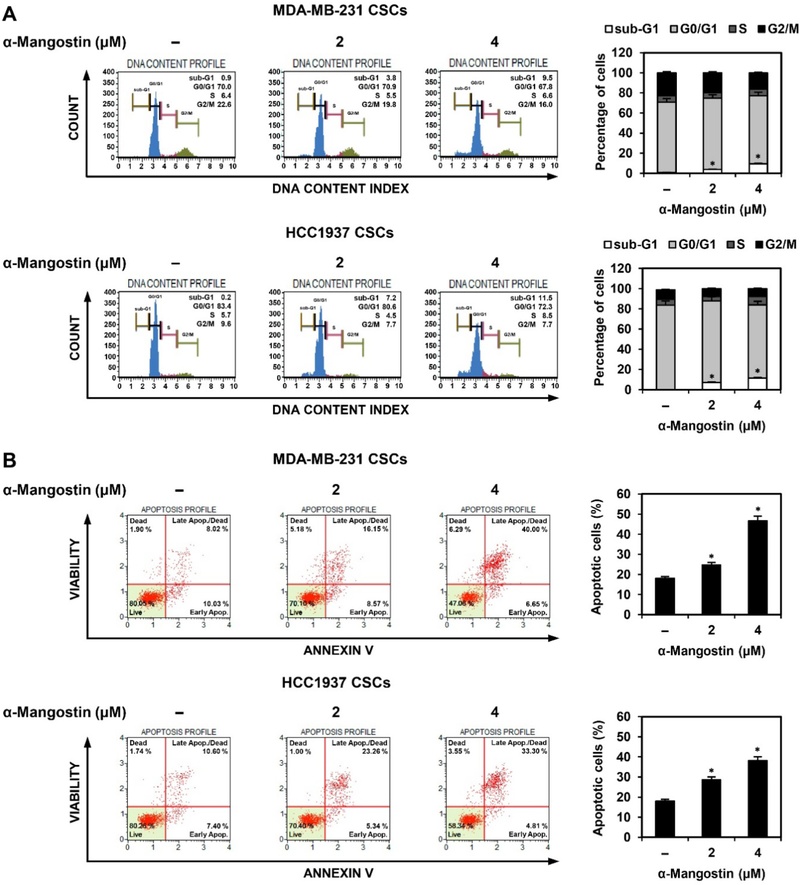
α-Mangostin induces cell cycle arrest and apoptosis in TNBCSCs. TNBC stem cells (TNBCSCs) derived from MDA-MB-231 and HCC1937 cell lines were treated with α-mangostin at concentrations of 2 and 4 μM for 24 h. (A) Cell cycle distribution was analyzed using a Muse® Cell Analyzer with the Muse® Cell Cycle Kit. (B) Apoptotic cell death was assessed using the Muse® Annexin V & Dead Cell Kit. Data are presented as the mean ± SD (n=3). Statistical analysis was performed using one-way ANOVA with Tukey’s post hoc test. *p < 0.05 vs. the control.
알파-망고스틴에 의한 삼중 음성 유방암 줄기세포의 내인성 세포자멸사 경로 활성화 효과 − 알파-망고스틴에 의해 유도된 세포자멸사의 특성을 보다 정밀하게 규명하고자, 내인성 세포자멸사 경로(intrinsic apoptosis pathway)의 주요 지표인 핵 형태학적 변화와 미토콘드리아 막 전위(MMP)를 분석하였다.16) MDA-MB-231 및 HCC1937 유래 TNBC 줄기세포에 알파-망고스틴을 2 및 4 μM 농도로 24시간 처리한 후, DAPI 염색을 통해 핵 형태 변화를 관찰한 결과, 처리 농도 증가에 따라 대조군 대비 명확한 핵의 응축과 단편화가 확인되었다(Fig. 3A). 또한, 동일한 조건에서 TMRE 염색을 통해 MMP를 측정한 결과, 알파-망고스틴 처리군에서 두 세포주 모두 미토콘드리아 막 전위의 유의한 감소가 관찰되었다(Fig. 3B). 이는 알파-망고스틴이 미토콘드리아 기능 저해를 유도함으로써 내인성 세포자멸사 경로를 활성화함을 시사한다. 더불어, 알파-망고스틴에 의해 유도된 세포자멸사의 분자적 기전을 규명하기 위해, 세포자멸사 관련 단백질의 발현을 western blot 분석을 통해 확인하였다. 세포 내 미토콘드리아 경로에 따라 활성화되는 caspase-9는 하위 효소인 caspase-3의 절단 및 활성을 유도하며, 활성화된 caspase-3는 DNA 복구 단백질인 PARP (poly(ADP-ribose) polymerase)의 절단을 통해 세포자멸사를 진행시킨다.17) 실험 결과, 알파-망고스틴 처리 후 MDA-MB-231 및 HCC1937 유래 암줄기세포 모두에서 cleaved caspase-9, cleaved caspase-3, cleaved PARP의 발현이 농도 의존적으로 증가하였다(Fig. 3C). 이와 같은 결과는 알파-망고스틴이 TNBC 유래 암줄기세포에서 미토콘드리아 매개 내인성 세포자멸사 경로를 효과적으로 활성화시킴으로써 세포자멸사를 유도하고, 결과적으로 종양 줄기세포의 증식을 억제함을 강하게 시사한다.
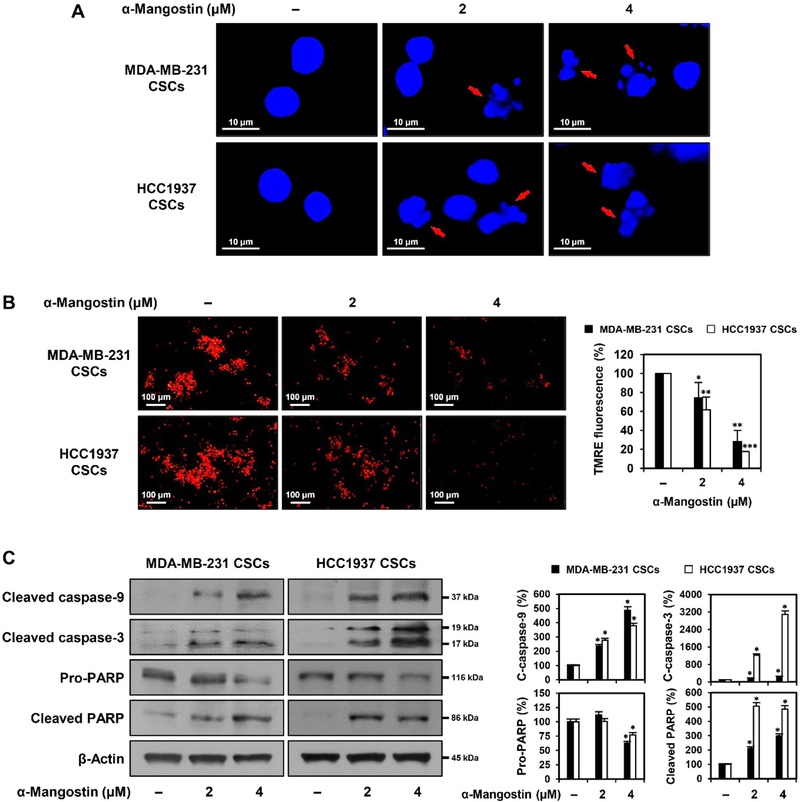
α-Mangostin induces apoptotic characteristics in TNBCSCs. TNBC stem cells (TNBCSCs) derived from MDA-MB-231 and HCC1937 cell lines were treated with α-mangostin (2 and 4 μM) and cultured for 24 h. (A) Nuclear morphology was assessed by DAPI fluorescence staining. Condensed and fragmented nuclei, indicative of apoptosis, are marked with red arrows. (B) Mitochondrial membrane potential (MMP) was evaluated using TMRE fluorescence staining. (C) Protein expression levels of apoptosis-related regulators were examined by Western blot analysis. β-Actin was used as a loading control, and band intensities were quantified by densitometry. Data are presented as the mean ± SD (n=3). Statistical analysis was performed using one-way ANOVA with Tukey’s post hoc test. *p < 0.05, **p < 0.01, ***p < 0.001 vs. the control.
알파-망고스틴의 삼중 음성 유방암 줄기세포 억제에 관한 분자적 기전 규명 − 알파-망고스틴이 TNBC 유래암줄기세포의 줄기세포 특성에 미치는 영향을 분석하고자, 주요 줄기세포 마커의 발현을 대상으로 western blot 분석을 수행하였다. 암줄기세포의 대표적인 세포 표면 마커인 CD133과 CD44는 종양 개시 능력, 자가 재생(self-renewal), 침습성 및 전이에 핵심적인 역할을 수행하며,18,19) 핵심 전사 인자인 Nanog와 Oct4는 줄기세포성 유지, 분화 조절 및 약물 내성과 밀접하게 연관되어 있다.20) MDA-MB-231 및 HCC1937 유래 암줄기세포에 알파-망고스틴을 2 및 4 μM 농도로 24시간 처리한 결과, CD133, CD44, Nanog, Oct4 단백질의 발현이 농도 의존적으로 유의하게 감소하였다(Fig. 4A). 이는 알파-망고스틴이 줄기세포 마커 발현을 저해함으로써 TNBC 암줄기세포의 줄기세포성을 억제함을 시사한다.
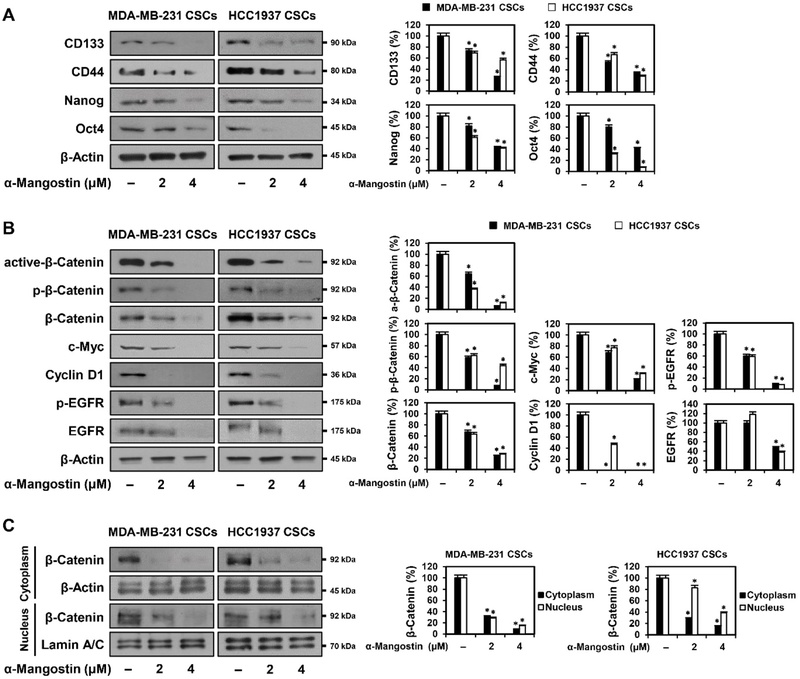
α-Mangostin downregulates stemness markers and inhibits the Wnt/β-Catenin signaling pathway in TNBCSCs. TNBC stem cells (TNBCSCs) derived from MDA-MB-231 and HCC1937 cell lines were treated with α-mangostin (2 and 4 μM) and cultured for 24 h. (A,B) The protein expression levels of stemness markers and components of the Wnt/β-Catenin signaling pathway were analyzed by Western blotting. β-Actin was used as a loading control, and band intensities were quantified by densitometry. (C) Cytoplasmic and nuclear fractions were isolated after α-mangostin treatment, and the expression levels of β-Catenin were analyzed by Western blotting. β-Actin and Lamin A/C served as loading controls for the cytoplasmic and nuclear fractions, respectively. Band intensities were quantified by densitometry. Data are presented as the mean ± SD (n=3). Statistical analysis was performed using one-way ANOVA with Tukey’s post hoc test. *p < 0.05 vs. the control.
나아가, 알파-망고스틴이 줄기세포 유지 및 증식에 핵심적인 Wnt/β-Catenin 신호전달 경로에 미치는 영향을 분석하였다.21) β-Catenin은 Wnt 신호 활성 여부에 따라 비인산화 상태(active form)로 존재하거나, Ser33/37 및 Thr41에서 인산화(phosphorylation)되어 GSK3β에 의해 분해되는 비활성 형으로 존재한다.22,23) Wnt 신호가 활성화되면 active β-Catenin은 핵 내로 이동하여 TCF/LEF 전사인자와 상호작용하며, c-Myc, cyclin D1, EGFR과 같은 하위 표적 유전자의 발현을 유도한다.22) 알파-망고스틴을 24시간 처리한 결과, 총 β-Catenin을포함하여 c-Myc 및 cyclin D1 단백질의 발현이 유의하게 감소하였고, EGFR의 경우 총 단백질 발현은 4 μM에서 유의하게 억제되었으며, 특히 인산화된 EGFR의 발현은 농도 증가에 따라 현저하게 감소하였다(Fig. 4B). 세포질 및 핵 분획 분석에서도 β-Catenin의 세포질 및 핵 내 발현 수준이 모두 저해됨을 확인하였다(Fig. 4C). 종합하면, 알파-망고스틴은 β-Catenin의 전체 발현 및 핵 내 이동을 저해함으로써 Wnt/β-Catenin 신호전달 경로의 활성을 억제하며, 동시에 주요 줄기세포 마커의 발현을 낮춤으로써 TNBC 유래 암줄기세포의 줄기세포성 유지 및 증식을 효과적으로 차단하는 항암 활성을 나타내는 것으로 판단된다.
결 론
본 연구는 알파-망고스틴(α-mangostin)이 삼중 음성 유방암 줄기세포(TNBCSCs)의 성장과 종양구체 형성을 농도 의존적으로 억제하며, 이 과정이 세포자멸사(apoptosis) 유도를 통해 매개됨을 확인하였다. 또한, α-mangostin은 Wnt/β-Catenin 신호전달 경로의 활성을 억제하고, CD133, CD44, Nanog, Oct4 등 핵심 줄기세포 마커의 발현을 감소시켜 TNBCSCs의 줄기세포성 유지 능력을 저해하였다. 이는 α-mangostin이 단순히 암세포 증식을 억제하는 수준을 넘어, TNBCSCs라는 특정 세포 아형을 직접적으로 표적화할 수 있는 독창적인 항암 기전을 보유하고 있음을 의미한다. 더 나아가 본 연구는 기존에 보고된 α-mangostin의 항암 활성을 TNBCSCs로 확장시킨 최초의 보고라는 점에서 의의가 있다. 이러한 결과는 α-mangostin이 TNBC 환자의 약물 저항성과 재발을 극복하는 새로운 치료 옵션으로 발전할 수 있는 가능성을 보여주며, 향후 임상 적용을 위한 기반 자료로 활용될 수 있을 것이다.
다만, α-mangostin의 실제 임상 적용에는 몇 가지 한계가 존재한다. α-mangostin은 낮은 수용성과 빠른 대사로 인해 생체이용률이 낮고, 체내 약물 전달 효율에도 제한이 있다. 또한, 고농도 투여 시 독성 가능성에 대한 우려가 제기되고 있다. 최근 나노입자 기반 제형, 지질 나노입자, 구조적 유도체 개발 등을 통해 이러한 한계를 극복하려는 시도가 이루어지고 있으며,11,24) 향후 연구에서는 약물 전달 효율 개선과 안전성 검증이 병행되어야 한다. 특히 본 연구는 세포 수준에서의 결과를 제시하였기 때문에, 향후 in vivo 동물모델을 통한 검증이 필수적이며, α-mangostin의 약물동태학적 특성 및 생체 이용률 향상 전략에 대한 심층적인 논의가 필요하다. 이러한 추가적 연구가 수행된다면, α-mangostin의 임상적 활용 가능성은 한층 더 강화될 것이다.
Acknowledgments
이 논문은 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구임(RS-2024-00343772).
References
-
Bray, F., Laversanne, M., Sung, H., Ferlay, J., Siegel, R. L., Soerjomataram, I. and Jemal, A. (2024) Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J. Clin. 74: 229-263.
[https://doi.org/10.3322/caac.21834]

-
Obidiro, O., Battogtokh, G. and Akala, E. O. (2023) Triple negative breast cancer treatment options and limitations: future outlook. Pharmaceutics 15: 1796.
[https://doi.org/10.3390/pharmaceutics15071796]

-
Shen, M., Pan, H., Chen, Y., Xu, Y. H., Yang, W. and Wu, Z. (2020) A review of current progress in triple-negative breast cancer therapy. Open Med. 15: 1143-1149.
[https://doi.org/10.1515/med-2020-0138]

-
Bianchini, G., Balko, J. M., Mayer, I. A., Sanders, M. E. and Gianni, L. (2016) Triple-negative breast cancer: challenges and opportunities of a heterogeneous disease. Nat. Rev. Clin. Oncol. 13: 674-690.
[https://doi.org/10.1038/nrclinonc.2016.66]

-
Fultang, N., Chakraborty, M. and Peethambaran, B. (2021) Regulation of cancer stem cells in triple negative breast cancer. Cancer Drug Resist. 4: 321-342.
[https://doi.org/10.20517/cdr.2020.106]

-
Manni, W. and Min, W. (2022) Signaling pathways in the regulation of cancer stem cells and associated targeted therapy. MedComm. 3: e176.
[https://doi.org/10.1002/mco2.176]

-
Kwon, M. K., Park, S. J., Cho, H. J., and Jung, H. J. (2024) Antiproliferative effect of rosmarinic acid in non-small cell lung cancer stem cells. Kor. J. Pharmacogn. 55: 134-141.
[https://doi.org/10.22889/KJP.2024.55.3.134]

-
Kim, H. L. and Jung, H. J. (2023) Cytotoxic effect of chloroform extract of Portulaca oleracea by inducing apoptosis and suppressing expression of stemness regulators in human glioblastoma stem cells. Kor. J. Pharmacogn. 54: 102-111.
[https://doi.org/10.22889/KJP.2023.54.3.102]

- Han, J. M., Kim, S. M., Kim, H. Y., Baek, S. B., and Jung, H. J. (2022) Anticancer activity of chloroform fraction of methanol extract of Sparassis crispa in human cervical cancer stem cells. Kor. J. Pharmacogn. 53: 21-28.
-
Alam, M., Rashid, S., Fatima, K., Adnan, M., Shafie, A., Akhtar, M. S., Ganie, A. H., Eldin, S. M., Islam, A., Khan, I. and Hassan, M. I. (2023) Biochemical features and therapeutic potential of α-mangostin: mechanism of action, medicinal values, and health benefits. Biomed. Pharmacother. 163: 114710.
[https://doi.org/10.1016/j.biopha.2023.114710]

-
Kim, S. M., Han, J. M., Le, T. T., Sohng, J. K. and Jung, H. J. (2020) Anticancer and antiangiogenic activities of novel α-mangostin glycosides in human hepatocellular carcinoma cells via downregulation of c-Met and HIF-1α. Int. J. Mol. Sci. 21: 4043.
[https://doi.org/10.3390/ijms21114043]

-
Jo, M. K., Moon, C. M., Kim, E. J., Kwon, J. H., Fei, X., Kim, S. E., Jung, S. A., Kim, M., Mun, Y. C., Ahn, Y. H., Seo, S. Y. and Kim, T. I. (2022) Suppressive effect of α-mangostin for cancer stem cells in colorectal cancer via the Notch pathway. BMC Cancer 22: 341.
[https://doi.org/10.1186/s12885-022-09414-6]

-
Chien, H. J., Ying, T. H., Hsieh, S. C., Lin, C. L., Yu, Y. L., Kao, S. H. and Hsieh, Y. H. (2020) α-Mangostin attenuates stemness and enhances cisplatin-induced cell death in cervical cancer stem-like cells through induction of mitochondrial-mediated apoptosis. J. Cell Physiol. 235: 5590-5601.
[https://doi.org/10.1002/jcp.29489]

-
Park, S. J. and Jung, H. J. (2025) Bufalin suppresses triple-negative breast cancer stem cell growth by inhibiting the Wnt/β-catenin signaling pathway. J. Microbiol. Biotechnol. 35: e2503002.
[https://doi.org/10.4014/jmb.2503.03002]

-
Thoma, C. R., Zimmermann, M., Agarkova, I., Kelm, J. M. and Krek, W. (2014) 3D cell culture systems modeling tumor growth determinants in cancer target discovery. Adv. Drug Deliv. Rev. 69-70: 29-41.
[https://doi.org/10.1016/j.addr.2014.03.001]

-
Elmore, S. (2007) Apoptosis: a review of programmed cell death. Toxicol. Pathol. 35: 495-516.
[https://doi.org/10.1080/01926230701320337]

-
Los, M., Mozoluk, M., Ferrari, D., Stepczynska, A., Stroh, C., Renz, A., Herceg, Z., Wang, Z. and Schulze-Osthoff, K. (2002) Activation and caspase-mediated inhibition of PARP: a molecular switch between fibroblast necrosis and apoptosis in death receptor signaling. Mol. Biol. Cell 13: 978-988.
[https://doi.org/10.1091/mbc.01-05-0272]

-
Grover, R., Drall, S., Poonia, N., Kumar Jain, G., Aggarwal, G., Lather, V., Kesharwani, P., Pandita, D. and Goyal, R. K. (2023) CD44 and CD133 aptamer directed nanocarriers for cancer stem cells targeting. Eur. Polym. J. 183: 111770.
[https://doi.org/10.1016/j.eurpolymj.2022.111770]

-
Kagara, N., Huynh, K. T., Kuo, C., Okano, H., Sim, M. S., Elashoff, D., Chong, K., Giuliano, A. E. and Hoon, D. S. B. (2012) Epigenetic regulation of cancer stem cell genes in triple-negative breast cancer. Am. J. Pathol. 181: 257-267.
[https://doi.org/10.1016/j.ajpath.2012.03.019]

-
Wang, D., Lu, P., Zhang, H., Luo, M., Zhang, X., Wei, X., Gao, J., Zhao, Z. and Liu, C. (2014) Oct-4 and Nanog promote the epithelial-mesenchymal transition of breast cancer stem cells and are associated with poor prognosis in breast cancer patients. Oncotarget 5: 10803-10815.
[https://doi.org/10.18632/oncotarget.2506]

-
Yang, X., Cao, D., Ma, W., Gao, S., Wen, G. and Zhong, J. (2022) Wnt signaling in triple-negative breast cancers: its roles in molecular subtyping and cancer cell stemness and its crosstalk with non-coding RNAs. Life Sci. 300: 120565.
[https://doi.org/10.1016/j.lfs.2022.120565]

-
Liu, J., Xiao, Q., Xiao, J., Niu, C., Li, Y., Zhang, X., Zhou, Z., Shu, G. and Yin, G. (2022) Wnt/β-catenin signalling: function, biological mechanisms, and therapeutic opportunities. Signal Transduct. Target Ther. 7: 3-23.
[https://doi.org/10.1038/s41392-021-00762-6]

-
Shah, K. and Kazi, J. U. (2022) Phosphorylation-dependent regulation of Wnt/β-catenin signaling. Front. Oncol. 12: 858782.
[https://doi.org/10.3389/fonc.2022.858782]

-
Verma, R. K., Yu, W., Shrivastava, A., Shankar, S. and Srivastava, R. K. (2016) α-Mangostin-encapsulated PLGA nanoparticles inhibit pancreatic carcinogenesis by targeting cancer stem cells in human, and transgenic (Kras(G12D), and Kras(G12D)/ tp53R270H) mice. Sci. Rep. 6: 32743.
[https://doi.org/10.1038/srep32743]
