귀전우로부터 분리한 betulin의 인지기능 개선활성
Abstract
This study evaluated the cognitive-enhancing effects of betulin, a triterpenoid compound isolated from Euonymus alatus, in a mouse model of scopolamine-induced amnesia. Behavioral assessments were conducted using the Morris water maze and passive avoidance tests. In the Morris water maze, betulin significantly attenuated scopolamine-induced impairments in spatial reference memory, as indicated by decreased escape latency and path length, along with improved swimming trajectories. In the passive avoidance test, betulin markedly improved memory retention, restoring performance to approximately 70% of that observed in the normal control group. Betulin markedly suppressed acetylcholinesterase activity in both the cortex and hippocampus, demonstrating a level of inhibition comparable to that observed with oral administration of donepezil at a dose of 1 mg/kg. These findings suggest that betulin may have therapeutic potential for the management of memory deficits associated with cholinergic dysfunction.
Keywords:
Betulin, Euonymus alatus, Alzheimer’s disease, Cognitive enhancing activity, Acetylcholinesterase알츠하이머병은 고령 인구에서 흔히 발생하는 신경퇴행성 질환으로, 아밀로이드 플라크와 신경섬유 엉킴의 축적, 염증, 그리고 신경세포 손실이 주요 병리기전이다. 주 증상은 점진적인 기억력 감퇴이며, 이후 다양한 인지 기능의 저하로 이어진다.1) 알츠하이머병에서는 여러 신경전달물질 시스템이 영향을 받지만, 그 중에서도 콜린성 시스템의 퇴행과 기능 저하는 질환 초기부터 나타나는 중요한 병리적 특징 중 하나이다. 아세틸콜린을 포함한 신경전달물질이 작용하는 콜린성 시스템은 기억과 학습 등 인지 기능에 필수적인 역할을 한다. 알츠하이머병 환자에서는 콜린성 신경세포의 소실과 아세틸콜린 농도의 감소가 기억력 저하와 전반적인 인지 기능 장애에 직접적인 영향을 미친다. 이러한 조기 변화는 콜린성 시스템이 알츠하이머병의 발병 기전에서 중심적인 위치를 차지하고 있음을 보여주며, 이에 따라 신약 개발에 있어서 콜린성 경로를 주요 표적으로 삼는 근거가 될 수 있다.2) 알츠하이머병의 대표적인 병리적 특징 중 하나는 기저 전뇌, 특히 중격-해마 콜린성 경로에서의 신경세포 소실이다. 현재 사용되는 치료제들은 시냅스 내 아세틸콜린의 농도를 증가시키기 위해 아세틸콜린에스터라제 억제제를 활용하고 있다. 피소스티그민, 타크린, 도네페질 등은 행동 실험에서 스코폴라민으로 유도된 공간 기억 손상을 효과적으로 완화하는 것으로 보고되었다.3-5) 스코폴라민은 중추 콜린성 기능을 차단하는 무스카린 수용체 길항제로, 가역적인 인지 장애를 유발하며 주의력 유지, 정보 처리, 새로운 학습 능력에 부정적인 영향을 미친다.6-9) 이러한 장애는 알츠하이머병의 기억 이상과 유사한 양상을 나타낸다. 이에 따라 스코폴라민 유도 기억상실 마우스 모델은 알츠하이머병의 병태 생리와 치료 가능성을 탐색하는 데 널리 활용되는 주요 실험 모델이다.10,11) 이전 연구에서 우리는 화살나무(Euonymus alatus)에 함유된 주요 생리활성 성분인 betulin의 신경보호 효과를 조사하였다. Betulin은 HT-22 신경세포에서 글루탐산에 의해 유도된 신경독성을 억제하는 능력을 보였으며, 항산화 효과를 통해 세포 내 과잉 칼슘(Ca²⁺)과 과산화물의 생성을 감소시켰다. 또한 글루타티온(GSH) 감소를 증가시켰고, 배양된 대뇌 피질 신경세포에서도 유사한 보호 효과를 나타내었다.12) 자작나무에서 분리한 betulin의 인지기능 개선활성을 보고한 논문도 있었다.13) Betulin이 스코폴라민으로 유도된 기억 장애를 완화하는 효과가 있는지를 평가하기 위해 행동실험을 실시하였다. 수동회피시험과 모리스 수중미로시험을 통해 학습과 기억 능력을 확인했으며, 동시에 뇌의 아세틸콜린에스터라제 활성을 측정하여 그 작용 기전을 조사하였다. 이러한 연구를 통하여 betulin이 인지 기능을 향상시키고 기억 장애 개선에 도움이 될 가능성이 있는지 평가하고자 하였다.
재료 및 방법
실험 동물 − 본 연구에서는 인지 기능 향상 효과를 평가하기 위해 ICR 생쥐를 사용하였다. 체중 약 25 g의 4주령 수컷 ICR 생쥐는 강원라이프사이언스(강원도, 대한민국)로부터 공급받았다. 생쥐는 도착 후 강원대학교 동물실험센터에 입주시켜 1주일간의 순화 기간을 거쳤다. 순화 기간 동안 사육실은 일정하게 조절된 조건에서 유지되었으며, 온도는 23 ± 1℃, 습도는 60%로 유지되었고, 12시간의 명암 주기(12-hour light-dark cycle)가 적용되었다. 생쥐는 순화 기간 동안 먹이와 물을 자유롭게 섭취할 수 있었다. 생쥐의 사육, 관리 및 실험 절차는 모두 강원대학교 동물실험윤리위원회 지침(IACUC, KIACUC, 07/2024)에 따라 수행되었으며, 실험 프로토콜은 동물실험 보고의 국제 가이드라인인 ARRIVE 지침을 준수하여 윤리적이고 신뢰할 수 있는 연구 수행 기준을 충족하였다.
시약 및 재료 − Betulin은 화살나무(Euonymus alatus) 전초로부터 분리한 것을 사용하였다.14) 순도 98% 이상인 스코폴라민(scopolamine), 인산완충생리식염수(PBS), 카복시메틸셀룰로오스(CMC)는 모두 Sigma(St. Louis, MO, USA)에서 구입하였다. 스코폴라민은 아세틸콜린에스터라제(acetylcholinesterase) 활성을 증가시켜 알츠하이머형 치매를 유도하기 위해 사용되었다. 순도 95% 이상의 도네페질(donepezil)은 삼진제약(주)(서울, 대한민국) 제품을 구입하여 사용하였다. 도네페질은 아세틸콜린에스터라제를 억제함으로써 아세틸콜린의 분해를 막아, 신경세포 내 아세틸콜린 농도를 높게 유지시킨다. 이러한 작용을 통해 도네페질은 일반적으로 기억력과 인지기능을 향상시키는 데 사용된다. 스코폴라민은 알츠하이머병에서 관찰되는 인지 결손을 유도하는 기전이 잘 알려져 있기 때문에 본 연구에 사용되었다. 스코폴라민은 아세틸콜린에스터라제 활성을 증가시킴으로써 뇌 내 아세틸콜린 농도를 감소시키고, 그 결과 기억력 및 인지기능이 저하된다. 도네페질은 양성 대조군(positive control)으로 본 연구에 포함되었다. 도네페질은 알츠하이머병 치료에 널리 사용되는 아세틸콜린에스터라제 억제제로, 아세틸콜린의 분해를 방지함으로써 뇌 내에서 이 신경전달물질의 농도를 높게 유지시킨다. 이와 같은 도네페질의 작용은 알츠하이머 환자의 기억력과 인지기능 향상에 효과적인 치료 기전으로 작용한다15)
약물 투여 − 생쥐는 총 여섯 그룹(n=6)으로 나뉘었다: 대조군, 스코폴라민 투여군, 양성 대조군(도네페질 1 mg/kg), 그리고 세 개의 botulin 투여군(1, 5, 10 mg/kg). betulin의 용량은 시험관 내(in vitro) 실험 데이터와 향후 임상시험 가능성을 고려하여 설정되었다. 약물 투여로 인한 독성 사망 사례는 없었으며, 실험 종료 후 장기 검사에서도 대조군과 비교하여 이상 소견 또한 관찰되지 않았다. betulin과 도네페질은 스코폴라민 처리 90분 전에 경구 투여되었으며, 대조군은 0.5% 카복시메틸셀룰로오스(CMC) 용액을 투여받았다. 스코폴라민(1 mg/kg)은 행동 실험 30분 전에 피하 주사로 투여되었다. 생쥐는 Morris 수중 미로 실험 전에 4일간 연속 투여되었고, 수동회피 실험에서는 훈련 당일에 1회 투여되었다.
Morris 수중 미로 실험 − 수중 미로 실험은 Morris의 방법을 일부 수정하여 수행되었다. 지름 90 cm, 높이 40 cm의 원형 수조에 따뜻한 물(20 ± 1℃)과 흰 우유 500 ml를 채웠다. 수조는 네 개의 사분면으로 나뉘었으며, 탈출용 플랫폼은 한 사분면의 중앙에 설치되었고, 수면에서 1 cm 아래에 위치하도록 배치되었다. 플랫폼은 원기둥 형태로, 지름 10 cm, 높이 26 cm였다. 마우스의 수영 정보(시간, 거리, 속도 등)은 비디오 카메라와 연결된 스마트 비디오 추적 시스템(Smart ver. 2.5.21)을 이용하여 관찰 및 기록되었다. 마우스가 플랫폼을 찾고 그 위에 머무르는 데 걸린 시간은 탈출 시간(escape latency)으로 기록되었다. 첫날에는 마우스가 학습할 수 있도록 플랫폼이 없는 상태에서 60초 동안 연습 세션(acquisition trial)을 진행하였다. 이후 4일간 하루에 한 번씩 실험을 수행하였다. 만약 마우스가 120초 이내에 플랫폼을 찾지 못한 경우, 실험은 종료되며 해당 시도의 탈출 시간은 120초로 기록되었다. 모든 실험 종료 후, 마우스는 경추 탈골법(cervical dislocation)을 통해 안락사시켰다.
수동회피 실험 − 수동회피 실험은 이전 연구를 기반으로 일부 수정하여 수행되었다. 실험 장치는 전기 격자 바닥이 설치된 동일한 크기의 두 구획(각각 17 cm × 12 cm × 10 cm)으로 구성되어 있으며, 이 두 구획은 guilotine 문으로 연결되어 있다. 실험은 Acquisition trial, Training trial, Testing trial의 세 단계로 이루어졌다. Acquisition trial 에서는 생쥐를 밝은 방에 넣고 자유롭게 탐색하도록 하였으며, 40초 후 자동으로 문이 열렸다. 그러다가 생쥐가 어두운 방으로 들어가면 문이 자동으로 닫혔다. 24시간 후 training trial이 진행되었으며, 생쥐를 다시 밝은 방에 넣고 30초 후 문을 열었다. 생쥐가 어두운 방으로 들어가면 문이 닫히고, 발바닥에 짧은 전기 자극(0.1 mA/10g 체중당, 2초간)이 가해졌다. Training trial이 있은 24시간 후에는 test trial이 이루어졌으며, 생쥐를 다시 밝은 방에 넣고 어두운 방으로 들어가기까지의 걸린 시간(latency time)을 최대 180초까지 측정하였다. 실험이 종료된 후, 생쥐는 경추 탈골법(cervical dislocation)을 통해 안락사시켰다.
아세틸콜린에스터라제 저해 활성 평가 − 아세틸콜린에스터라제(AChE) 저해 활성은 Ellman의 고전적인 방법을 일부 수정하여 분석하였다. 모리스 수중 미로 시험 또는 수동 회피 시험 종료 후 30분 이내에 마우스의 뇌를 신속하게 적출하였으며, 이 중 해마(hippocampus)를 정밀하게 분리하였다. 분리된 해마 조직은 sodium phosphate buffer를 이용하여 Tissue Stick (Bioneer Inc., Alameda, CA, USA)으로 균질화하였고, 이후 원심분리를 통해 상층액을 확보하였다. 효소 활성 측정은 해마 상층액 33 μl, pH 8.0의 phosphate buffer 470 μl, 3 mM 5,5’-dithio-bis(2-nitrobenzoic acid, DTNB) 167 μl, 그리고 1 mM acetylcholine iodide 280 μl를 혼합하여 반응을 유도하였다. AChE 효소 활성에 대한 S. maxima 추출물의 억제 효과는 412 nm에서 흡광도를 측정함으로써 평가하였으며, 측정에는 분광광도계(BioTek EL808, BioTek Instruments, Winooski, VT, USA)를 사용하였다.
통계 − 모리스 수중 미로 시험, 수동 회피 시험, 그리고 아세틸콜린에스터라제 저해 활성 측정 결과는 각각 평균 ± 표준오차(Mean ± S.E.M.)로 나타내었다. 실험에서 얻은 모든 데이터는 IBM SPSS Statistics V26 (IBM, Armonk, NY, USA) 소프트웨어를 활용하여 분석하였으며, 통계적 유의성 검정을 위해 일원분산분석(one-way ANOVA)을 실시하였다. 유의한 차이가 확인된 경우, 사후 검증으로 Tukey의 다중 비교 검정을 적용하였다. 각 실험군 간의 차이는 p<0.05, p<0.01, p<0.001일 때 통계적으로 유의한 것으로 판단하였다.
결과 및 고찰
모리스 수중 미로 시험을 통하여 E. alatus에서 분리한 betulin이 스코폴라민으로 유도된 기억 손상에 대해 인지 개선 효과를 나타내는지를 평가하였다(Fig. 1). 대조군 생쥐의 escape latency는 실험 4일 동안 유의미하게 지속적으로 감소하여, 4일째에는 54.1초에 도달하였다. 반면, 스코폴라민 처리군은 첫날 이후에도 escape latency가 훨씬 더 길었고 4일 동안 큰 변화가 없었으며, 4일째에는 115.2초에 이르렀다. 이러한 결과는 스코폴라민에 의해 기억 장애가 효과적으로 유도되었음을 확인할 수 있었다. betulin의 기억 개선 효과는 4일 동안 평가되었으며, 각 농도군에서 3일째 이후부터 유의미한 개선이 관찰되었다. 도네페질 처리군은 3일째에 도피 시간이 65.3초였으며, 4일째에는 약 47.2초로 더욱 감소하였다. Betulin 처리군은 스코폴라민 처리군에 비해 용량 의존적으로 escape latency가 감소하였다. 10 mg/kg의 betulin 처리군에서는 도피 시간이 64.1초였고, 5 mg/kg 및 1 mg/kg 처리군은 각각 84.5초, 95.6초였다(Fig. 2).
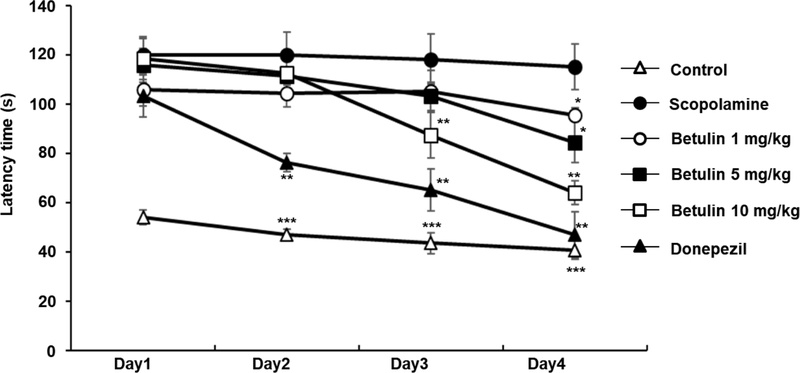
The effect of betulin on the spatial memory enhancement. Data are mean escape latencies ± SD (n=6). (*p < 0.05, **p < 0.01 and ***p < 0.001 versus scopolamine-treated mice).
대조군의 수영 거리는 스코폴라민 처리군보다 유의성 있게 짧았다. 대조군은 398 cm를 수영한 반면, 스코폴라민 처리군은 754 cm를 수영하여 스코폴라민에 의한 기억 손상이 뚜렷하게 나타났음을 보여준다. 4일에 걸친 실험 기간 동안, betulin 투여는 스코폴라민에 의해 증가한 수영 거리를 현저히 감소시켰으며, 이러한 감소는 용량 의존적으로 나타났다. 1 mg/kg, 5 mg/kg, 10 mg/kg의 betulin을 투여한 군의 수영 거리는 각각 673 cm, 576 cm, 511 cm로, 높은 용량일수록 점진적인 개선 효과를 보였다(Fig. 3).
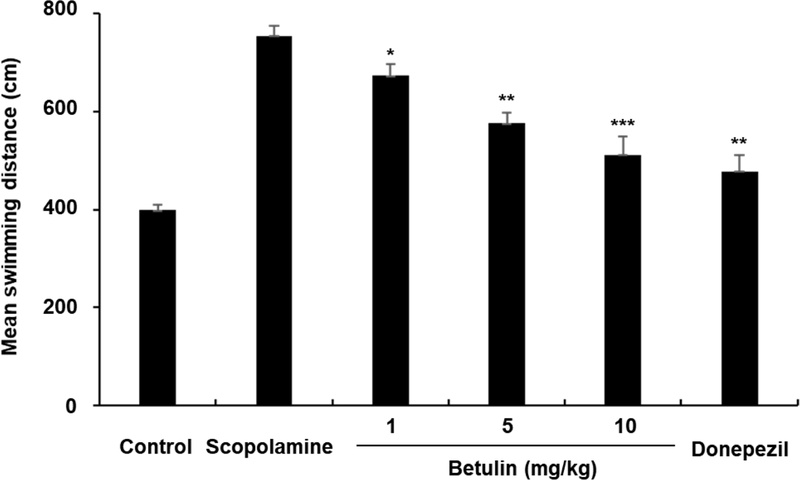
The effect of betulin on mean swimming distance to find the platform over 4 days of scopolamine-treated mice in the Morris water maze test. Data are mean escape latencies ± SD (n=6). (*p < 0.05, **p < 0.01 and ***p < 0.001 versus scopolaminetreated mice).
프로브 테스트를 통해 기억 유지 능력을 평가한 결과, 대조군은 목표 사분면에서 유의하게 더 오랜 시간을 머문 반면, 스코폴라민 처리군은 현저히 짧은 시간을 기록하였다. 대조군은 평균 35.7초 동안 목표 사분면에 머물렀으나, 스코폴라민 처리군은 9.5초에 불과하였다. 이는 스코폴라민이 공간 기억을 현저히 저하시켰음을 시사한다. 반면, betulin을 투여한 실험군에서는 용량 의존적으로 목표 사분면 체류 시간이 증가하는 양상을 보였다. 구체적으로, 1 mg/kg, 5 mg/kg, 10 mg/kg의 betulin을 투여한 군은 각각 16.9초, 26.3초, 28.9초 동안 목표 사분면에 머물렀다. 이러한 결과는 betulin이 스코폴라민으로 유도된 기억 손상을 완화하고, 고용량일수록 그 효과가 뚜렷하다는 것을 보여준다(Fig. 4).
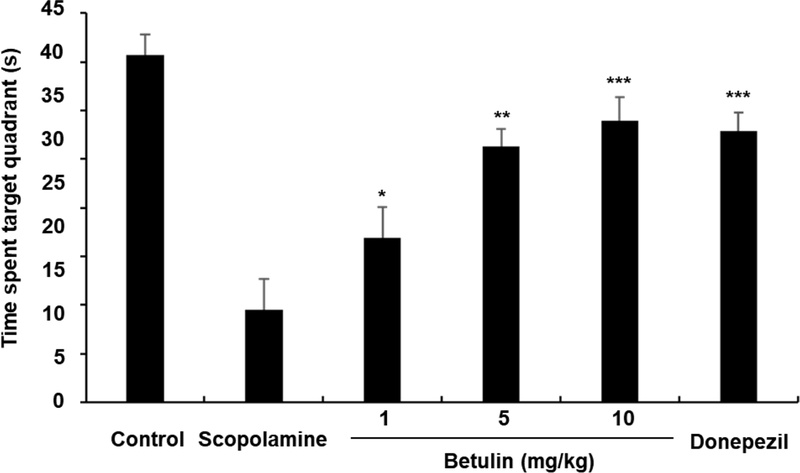
The effect of betulin in the probe trial. The time spent in the target quadrant during the probe trial was presented. Data are mean escape latencies ± SD (n=6). (*p < 0.05, **p < 0.01 and ***p < 0.001 versus scopolamine-treated mice).
Betulin 처리군에서 목표로 하는 플랫폼을 찾는데 걸린 시간이 단축된 것이 생쥐의 운동 능력 향상에 의한 것이 아님을 평가하기 위해 생쥐의 수영 속도를 측정하였다. 실험한 결과, 대조군, 스코폴라민 처리군, botulin 처리군, 도네페질 처리군 간 평균 수영 속도에는 유의미한 차이는 보이지 않았다 (Fig. 5). 수영 속도에서의 차이가 없다는 점은 betulin의 기억력 향상 효과에 의하여 나타난 결과이지 마우스의 신체 운동 능력 변화와는 무관함을 뒷받침하는 결과로 볼 수 있다. Morris water maze 시험은 betulin이 스코폴라민으로 유도한 마우스의 인지장애에 대해 치료 효과를 나타내는지를 평가하기 위해 사용되었다.16) 스코폴라민은 콜린성 신호 전달을 방해하여 학습 및 기억력 저하를 유발하며, 해마에서 아세틸콜린에스터라제(AChE) 활성을 증가시키는 것으로 알려져 있다.17) Betulin은 마우스의 공간 기억 및 학습 능력을 효과적으로 개선하였으며, 이는 escape latency의 감소와 목표 사분면에서 머무는 시간의 증가로 확인되었고, 수영 속도에는 영향을 미치지 않았다. 이러한 결과를 정리하면, betulin은 E. alatus로부터 분리된 화합물로서 강력한 인지 기능 향상 활성을 나타내었다.
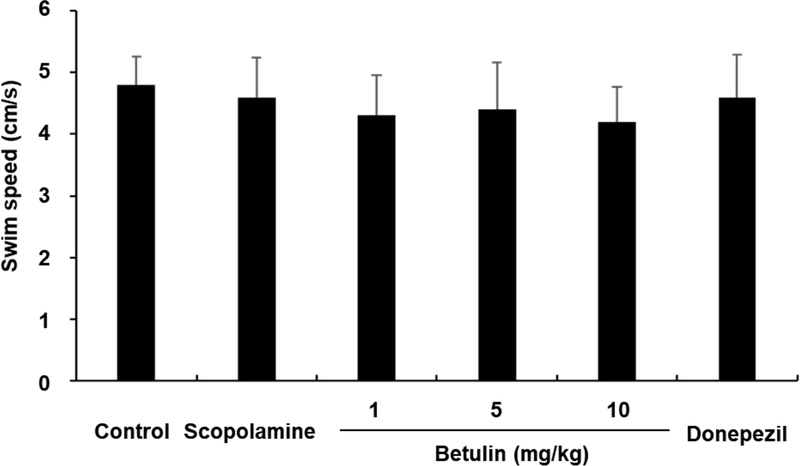
The effect of betulin on swim speed to find the platform over 4 days of scopolamine-treated mice in the Morris water maze test. Data are mean escape latencies ± SD (n=6). (*p < 0.05, **p < 0.01 and ***p < 0.001 versus scopolamine-treated mice).
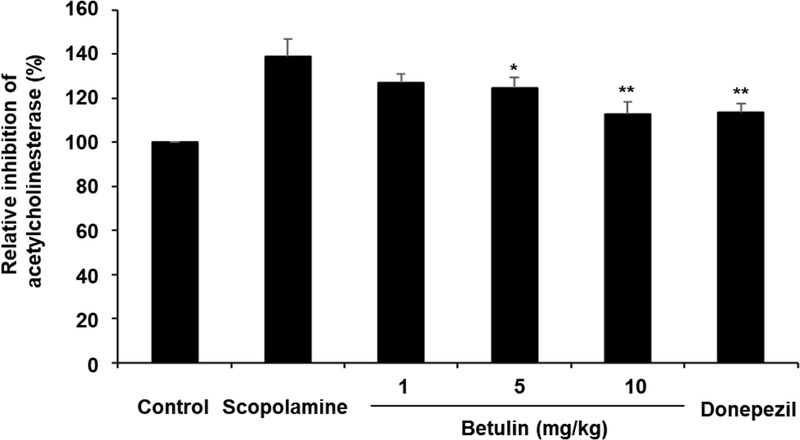
수동 회피(passive avoidance) 시험은 장기 기억을 평가하고 기억력 향상 효과를 확인하는 데 일반적으로 사용된다.18) Betulin 처리에 따른 지속적인 기억력 향상 효과를 조사하기 위해, 스코폴라민으로 유도된 기억 손상 마우스 모델을 이용한 수동 회피 실험이 수행되었다. Acquisition trial 동안에 마우스가 소리나 빛 자극을 회피하는 데 걸린 latency time을 측정하였다. 그 결과, 각 그룹 간 지연 시간에 유의미한 차이가 없어, 모든 조건에서 초기 학습 능력이 유사함을 확인할 수 있었다. 대조군, 스코폴라민 처리군, 도네페질 처리군의 평균 지연 시간은 각각 3.55초, 3.21초, 2.78초였다. Betulin 처리군의 경우, 1 mg/kg 농도에서 3.19초, 5 mg/kg 농도에서 3.05초, 10 mg/kg 농도에서 3.42초로 측정되었다(Fig. 6). 이러한 결과는 acquisition trial 과정에서 그룹 간 지연 시간에 유의한 차이가 없음을 확인해주며, 실험이 기억력 성능에 있어 동일한 기준선에서 시작되었음을 보여준다. 이와 같은 결과는 이후에 test trial에서 관찰된 기억력 향상 또는 손상이 초기 학습 능력의 차이가 아닌, 시험 약물의 처리에 따른 효과임을 뒷받침해 줄 수 있다. Test trial에서 스코폴라민 처리군의 latency time은 대조군에 비해 유의하게 짧았으며, 이는 스코폴라민이 기억 손상을 효과적으로 유도했음을 보여준다. 대조군의 평균 latency time은 48.93초였던 반면, 스코폴라민 처리군은 약 15.32초로 감소하였다. 이에 반해, betulin 처리군은 농도 의존적으로 latency time이 증가하였으며, 1 mg/kg, 5 mg/kg, 10 mg/kg 농도에서 각각 28.93초, 29.33초, 35.32초의 평균 latency time을 나타내었다(Fig. 6). 수동 회피 시험을 통하여 betulin이 스코폴라민에 의하여 유도된 기억 손상을 완화시키고 장기 강화(long-term potentiation, LTP)를 개선할 수 있는지를 평가하고자 하였다. Acquisition trial단계에서는 모든 군에서 지연 시간에 유의성 있는 차이가 없어 초기 학습 조건이 유사함을 나타냈다. 그러나 test trail단계에서는 botulin 처리를 통하여 스코폴라민 처리군에 비해 평균 latency time 이 농도 의존적으로 증가시켰다. 이러한 결과는 betulin이 학습 능력을 효과적으로 향상시키고 스코폴라민에 의해 유도된 기억 손상을 회복시키는 데 기여함을 시사한다. Betulin이 해마에서의 AChE(아세틸콜린에스터라제) 활성에 미치는 영향을 평가하였다. 스코폴라민은 대조군에 비해 AChE 활성을 138.8% 증가시켰으며, betulin은 용량 의존적으로 AChE 활성을 유의하게 감소시켰다(p<0.05). 구체적으로, betulin을 1 mg/kg, 5 mg/kg, 10 mg/kg 농도로 투여했을 때 AChE 활성은 각각 126.9%, 124.5%, 112.6%로 감소하였다(Fig. 7). Betulin이 인지 기능을 어떻게 향상시키는지 알아내기 위해, 효소의 활성 변화를 분석하였다. 아세틸콜린은 학습과 기억을 포함한 인지 기능에 중요한 역할을 하며, 작업 기억과 공간 기억 모두에 영향을 미친다. 알츠하이머병과 같은 질환에서는 아세틸콜린 수치가 감소하는 경향이 있으며, 이는 인지 기능 저하의 주요 원인 중 하나이다. 이러한 아세틸콜린 감소는 아세틸콜린을 분해하는 효소인 아세틸콜린에스터라제(AChE)의 활성이 증가하는 것과 관련이 있다. 따라서 AChE는 알츠하이머 치료의 주요한 표적으로 간주되고 있다.19,20) 도네페질, 갈란타민, 타크린과 같은 여러 아세틸콜린에스터라제(AChE) 저해제가 아세틸콜린의 분해를 억제함으로써 그 농도와 기능을 향상시켜 기억력 저하를 개선하기 위해 개발되었다.20,21) 본 연구에서 betulin이 농도 의존적으로 AChE 활성을 유의성 있게 억제하는 효과를 확인하였다. 이러한 결과는 betulin이 AChE 활성을 억제함으로써 스코폴라민에 의해 유도된 기억 손상을 완화시킨다는 것을 알 수 있다. AChE 활성을 감소시킴으로써 betulin은 아세틸콜린의 농도를 더 높게 유지하도록 도와주며, 이는 기억력 향상에 필수적으로 작용할 수 있다. 따라서 betulin은 아세틸콜린의 가용성을 증가시켜 인지 기능을 개선하고, 스코폴라민으로 인한 기억 장애를 완화하는 데 기여할 수 있다고 생각할 수 있을 것이다.
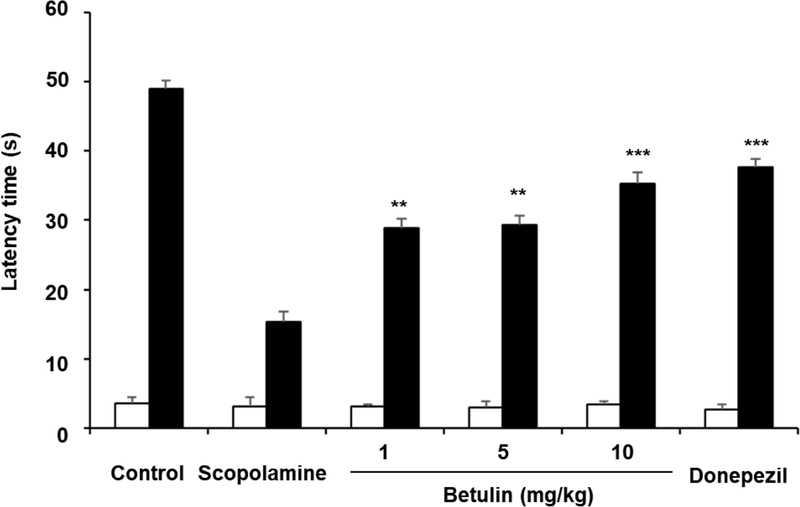
The effect of betulin on scopolamine-induced memory impairment in the passive avoidance test. The latency prior to entry to the dark compartment was recorded. Data are mean latency times (s) ± SD (n=6). (*p < 0.05, **p < 0.01 and ***p < 0.001 versus scopolamine-treated mice).
결 론
결론적으로, 본 연구는 E. alatus 추출물에서 분리된 화합물인 betulin이 스코폴라민에 의해 유도된 기억 손상을 용량의존적으로 효과적으로 완화시킨다는 것을 보여준다. 이러한 유익한 효과는 학습과 기억 같은 인지 기능에 필수적인 신경전달물질인 아세틸콜린을 분해하는 효소인 아세틸콜린에스터라제(AChE)의 억제를 통해 매개되는 것으로 보인다. Betulin이 AChE를 억제함으로써 아세틸콜린의 농도를 더 높게 유지하도록 도와주며, 이는 기억력 및 인지 능력 향상에 중요한 역할을 한다. 이러한 결과는 betulin이 알츠하이머병을 포함한 신경퇴행성 질환의 예방 및 치료를 위한 천연 유래 의약품으로 개발될 수 있는 가능성을 보여준다. 작용 기전과 기억력 저하 완화 효과를 고려할 때, betulin이 이러한 질환과 관련된 인지 장애를 해결하기 위한 새로운 치료 전략을 제공할 수 있을 것이다.
Acknowledgments
본 연구는 2023년도 교육부의 재원으로 한국기초과학지원연구원 국가연구시설장비진흥센터의 지원을 받아 수행된 연구임(과제번호 2022R1A6C101A739).
References
-
Lane, C. A., Hardy, J. and Schott, J. M. (2018) Alzheimer’s disease. Eur. J. Neurol. 25: 59-70.
[https://doi.org/10.1111/ene.13439]

-
Ferreira-Vieira, T. H., Guimaraes, I. M., Silva, F. R. and Ribeiro, F. M. (2016) Alzheimer’s disease: Targeting the cholinergic system. Curr. Neuropharmacol. 14: 101-115.
[https://doi.org/10.2174/1570159X13666150716165726]

-
Kim, Y. H., Lee, Y., Kim, D., Jung, M. W. and Lee, C. J. (2010) Scopolamine-induced learning impairment reversed by physostigmine in zebrafish. Neurosci. Res. 67: 156-161.
[https://doi.org/10.1016/j.neures.2010.03.003]

-
Chvojkova, M., Kolar, D., Kovacova, K., Cejkova, L., Misiachna, A., Hakenova, K., Gorecki, L., Horak, M., Korabecny, J., Soukup, O. and Vales, K. (2024) Pro-cognitive effects of dual tacrine derivatives acting as cholinesterase inhibitors and NMDA receptor antagonists. Biomed. Pharmacother. 176: 116821.
[https://doi.org/10.1016/j.biopha.2024.116821]

- Ayobami, F. G., Ogundipe, O. J., Emmanuel, A. A. and Kolawole, I. O. (2025) Effects of lauric acid on cognitive impairment in a scopolamine-induced Alzheimer’s disease-like rat model. Nutr. Neurosci. 26: 1-11.
-
Chen, W.N. and Yeong, K. Y. (2020) Scopolamine, a toxin-induced experimental model, used for research in Alzheimer's disease. CNS Neurol. Disord. Drug Targets 19: 85-93.
[https://doi.org/10.2174/1871527319666200214104331]

-
Tang, K. S. (2019) The cellular and molecular processes associated with scopolamine-induced memory deficit: A model of Alzheimer's biomarkers. Life Sci. 15: 116695.
[https://doi.org/10.1016/j.lfs.2019.116695]

-
Sunderland, T., Tariot, P., Murphy, D. L., Weingartner, H., Mueller, E. A. and Cohen, R. M. (1985) Scopolamine challenges in Alzheimer's disease. Psychopharmacology 87: 247-249.
[https://doi.org/10.1007/BF00431817]

-
Sandeep Ganesh, G., Konduri, P., Kolusu, A. S., Namburi, S. V., Chunduru, B. T. C, Nemmani, K. V. S. and Samudrala, P. K. (2023) Neuroprotective effect of saroglitazar on scopolamine-induced Alzheimer's in rats: Insights into the underlying mechanisms. ACS Chem. Neurosci. 14: 3444-3459.
[https://doi.org/10.1021/acschemneuro.3c00320]

-
Bajo, R., Pusil, S., López, M. E., Canuet, L., Pereda, E., Osipova, D., Maestú, F. and Pekkonen, E. (2015) Scopolamine effects on functional brain connectivity: a pharmacological model of Alzheimer's disease. Sci. Rep. 5: 9748.
[https://doi.org/10.1038/srep09748]

-
Abdelghany, A. K., El-Nahass, E. S., Ibrahim, M. A., El-Kashlan, A. M., Emeash, H. H. and Khalil, F. (2022) Neuroprotective role of medicinal plant extracts evaluated in a scopolamine-induced rat model of Alzheimer's disease. Biomarkers 27: 773-783.
[https://doi.org/10.1080/1354750X.2022.2112975]

-
Jung, Y. S. and Ma, C. J. (2025) Therapeutic potential of methanol extract of Euonymus alatus in HT22 cells through neuroprotective mechanisms. Nat. Prod. Sci. 29: 49-54.
[https://doi.org/10.20307/nps.2025.31.1.49]

-
Cho, N., Kim, H. W., Lee, H. K., Jeon, B. J. and Sung, S. H. (2016) Ameliorative effect of betulin from Betula platyphylla bark on scopolamine-induced amnesic mice. Biosci. Biotech. Biochem. 80: 166-171.
[https://doi.org/10.1080/09168451.2015.1072460]

-
Jung, Y. S., Lee, H. W. and Ma, C. J. (2020) Neuroprotective effect of compounds isolated from Euonymus alatus on glutamate-induced oxidative stress in HT22 hippocampal cells. Pharmacogn. Mag. 16: S308-S314.
[https://doi.org/10.4103/pm.pm_450_19]

-
Birks, J. S and Harvey, R. J. (2018) Donepezil for dementia due to Alzheimer’s disease. Cochrane Database Syst. Rev. 6: CD001190.
[https://doi.org/10.1002/14651858.CD001190.pub3]

-
Bromley-Brits, K., Deng, Y. and Song, W. (2011) Morris water maze test for learning and memory deficits in Alzheimer's disease model mice. J. Vis. Exp. 20: 2920.
[https://doi.org/10.3791/2920]

-
Ghasemi, S., Moradzadeh, M., Hosseini, M., Beheshti, F. and Sadeghnia, H. R. (2019) Beneficial effects of Urtica dioica on scopolamine-induced memory impairment in rats: protection against acetylcholinesterase activity and neuronal oxidative damage. Drug Chem. Toxicol. 42: 167-175.
[https://doi.org/10.1080/01480545.2018.1463238]

-
Ahmadalipour, A., Sadeghzadeh, J., Samaei, S. A. and Rashidy-Pour, A. (2017) Protective effects of enriched environment against transient cerebral ischemia-induced impairment of passive avoidance memory and long-term potentiation in rats. Basic Clin. Neurosci. 8: 443-452.
[https://doi.org/10.29252/nirp.bcn.8.6.443]

-
Li, X. T. (2022) Alzheimer's disease therapy based on acetylcholinesterase inhibitor/blocker effects on voltage-gated potassium channels. Metab. Brain Dis. 37: 581-587.
[https://doi.org/10.1007/s11011-022-00921-w]

-
Diez-Ariza, M., Redondo, C., García-Alloza, M., Lasheras, B., Del Río, J. and Ramírez, M. J. (2003) Flumazenil and tacrine increase the effectiveness of ondansetron on scopolamine-induced impairment of spatial learning in rats. Psychopharmacology 169: 35-41.
[https://doi.org/10.1007/s00213-003-1467-1]

-
Snyder, P. J., Bednar, M. M., Cromer, J. R. and Maruff, P. (2005) Reversal of scopolamine-induced deficits with a single dose of donepezil, an acetylcholinesterase inhibitor. Alzheimer’s Dement. 1: 126-135.
[https://doi.org/10.1016/j.jalz.2005.09.004]