사람 혈소판의 인산화단백질 및 과립분비 조절을 통한 apigenin의 항혈전효과
Abstract
Cardiovascular disease is a major health problem worldwide, and excessive platelet activation and aggregation are identified as the main causes of cardiovascular disease. Therefore, controlling platelet activation is a key strategy in the prevention and treatment of cardiovascular disease. Apigenin is a major flavonoid compound abundantly contained in the flowers of the chamomile plant, and previous studies have reported that it has anti-inflammatory, antiviral, and anticancer effects. However, the efficacy and mechanism of apigenin in inhibiting platelet activation and aggregation have not been clearly elucidated. This study confirmed the effect of apigenin on collagen-induced human platelets and clarified its mechanism of action. Apigenin inhibited the phosphorylation of phosphoproteins PI3K/Akt and MAPK during platelet activation, and also inhibited the phosphorylation of cPLA2. In addition, apigenin reduced the production of TXA2 and the release of intraplatelet granules such as ATP and serotonin. As a result, apigenin potently inhibited platelet aggregation induced by collagen, and ultimately affected the inhibition of thrombus formation. Through these results, this study shows that apigenin can be an effective antithrombotic substance that inhibits the activation and aggregation of human platelets by preventing granule release through the regulation of phosphorylated proteins.
Keywords:
Apigenin, Mitogen-activated protein kinases, PI3K/Akt, Granule secretion, Platelet aggregation전 세계적으로 주요한 건강 문제로 대두되고 있는 심혈관 질환은 미국 워싱턴대학교 의과대학의 연구팀에서 1990년부터 2019년까지 자료 분석한 결과를 볼 때, 2019년 전 세계 심혈관 질환자의 수는 약 5억 2,300만 명으로, 2억 7,100만 명이었던 1990년에 비해 두 배 가까이 증가한 것으로 확인되었다.1) 이 기간 동안 심혈관 질환으로 사망한 사람의 수가 1,210만 명에서 1,860만 명까지 크게 증가하였으며, 이는 전체 사망자의 사망 원인에서 3분의 1을 차지할 정도이고, 심혈관 질환으로 인한 사망이 세계 사망 원인 1위임을 보여주었다.1) 혈전은 혈관 내에서 혈액이 응고되며 덩어리가 형성되는 것으로 심혈관 질환의 주요 원인 중 하나로 꼽히며, 과도한 혈소판 활성화와 혈전생성에 의해서 발생된다.2) 혈관이 손상받았을 경우, 혈소판이 손상 부위에 점착하여 응집이 일어남으로써 1차 혈전이 만들어지고, 이후 응고 인자들이 활성화되어 섬유소가 형성되면서 혈전의 안정화가 일어난다.2) 이 과정에서 만들어지게 된 혈전은 심장이나 뇌로 가는 혈관을 막으면서 허혈성 뇌졸증이나 심근경색 등의 심각한 심혈관 질환을 유발시키는데, 혈관이 좁아진 상태에서는 작은 혈전에 의해서도 혈류가 차단됨으로써 돌연사로 이어질 가능성이 있다.3,4) 따라서, 혈소판 활성화를 조절하는 것이 심혈관 질환 예방과 치료를 위한 핵심 전략이 될 수 있다.
혈소판 응집 될 때, MAPK(Mitogen-Activated Protein Kinase)와 phosphatidylinositol 3-kinase (PI3K)/protein kinase B (Akt) 신호전달 경로가 혈소판 활성화에서 중요한 역할을 하는 것으로 알려져 있다.5) MAPK는 ERK, JNK, p38로 구성된 kinase 효소 그룹이다.6) MAPK 신호는 ATP, serotonin 등 혈소판 내 과립 내 물질의 분비를 촉진하고, αIIb/β3의 활성화를 일으켜 혈소판 응집으로 이어진다.7-12) 또한 세포막에 존재하는 cytosolic phospholipase A2 (cPLA2)의 인산화를 촉진함으로써 thromboxane A2 (TXA2) 생성이 증거되는데, 이는 혈소판의 활성화 및 응집을 더 강력하게 촉진하는 작용을 한다.12,13) 이와 함께, PI3K/Akt 경로는 혈소판 내 Ca2+ 농도를 높여주고, αIIb/β3 수용체의 친화력을 높임으로 fibrinogen과의 결합을 강화시키는데, 이들에 의해 혈소판 응집이 촉발된다.14) 정상적인 혈액순환 가운데 있을 때, 생체 내에서는 이들을 통해 혈소판 응집을 억제하는 기전과 촉진하는 기전이 상호보완 작용 하면서, 지혈 반응을 조절한다.
Apigenin은 캐모마일 식물의 꽃에 많이 들어있는 주요 플라보노이드 화합물로 알려져 있다.15) 이전 연구들은 apigenin이 항염증, 항바이러스, 항암 효과를 가지고 있음을 보고하였으며, 당귀수산에 함유된 apigenin이 혈소판 응집을 억제할 가능성과 함께 심혈관 질환 예방에 관여할 수 있는 잠재력이 있음이 보고된 바 있다.16-19) 그러나, 현재까지 apigenin의 혈소판 활성화 및 응집억제에 관한 구체적인 기전이 밝혀진 바 없다. 따라서, 본 연구는 apigenin이 혈소판 응집을 억제하는 확실한 기전을 규명하고, 항혈전제로서의 가능성을 탐색하여 새로운 혈전증 치료 전략을 찾는데 기여하고자 한다.
재료 및 방법
시약 − Avention Corporation (Incheon, Korea)로부터 apigenin을 구입하여 사용하였다. Chrono-Log Corporation (PA, Havertown, USA)에서 collagen을 구입하였다. ATP, serotonin 및 TXB2 측정을 위한 assay kit는 Cayman Chemical Co. (Ann Arbor, MI, USA)에서 구입하였다. Western blot 분석에 사용된 항체와 lysis buffer는 Cell Signaling Technology (Beverly, MA, USA)로부터 제공받았으며, polyvinylidene difluoride (PVDF) membrane과 enhanced chemiluminescence (ECL) 용액은 Thermo Fisher Scientific Korea (Seoul, Korea)에서 공급되었다.
사람 혈소판 부유액 제작 − 사람에서 얻은 혈소판 풍부혈장(PRP)은 1,650 × g에서 5분 동안 원심분리한 후, 현탁완충액으로 세척하였다. 사용된 buffer의 조성은 138 mM NaCl, 2.7 mM KCl, 12 mM NaHCO3, 0.36 mM NaH2PO4, 0.49 mM MgCl2 및 5.5 mM glucose였으며, pH는 7.4로 유지하였다. 이후 혈소판은 동일한 완충액에 재현탁하였고, 최종 농도가 1×108 cells/mL가 되도록 조절하였다. 모든 실험 과정은 이전 보고된 방법을 참고하여 25℃ 조건에서 수행되었다. 본 연구에 사용된 PRP는 대한적십자 혈액원(KRBC, 수원)으로부터 공급받았으며, 인체 유래 물질의 활용은 남서울대학교 생명윤리위원회(IRB)의 승인을 거쳐 진행되었다(승인번호: 1041479-HR-201803-003).
혈소판 응집능 측정 − 다양한 농도의 apigenin을 준비하여 인간 혈소판 현탁액(108 cells/mL)과 혼합하였다(Fig. 1). 이후, 2 mM CaCl2를 첨가한 후 37℃에서 3분간 배양하였다. 혈소판 응집 반응의 유도를 위해 U46619 (0.5 μM)을 첨가한 뒤, 1,000 rpm에서 5분간 교반하며 응집 반응을 측정하였다. 혈소판 응집률은 혈소판 응집계(Chrono-Log Co., Havertown, PA, USA)에서 측정하였고, 광 투과도에 의해 산출된 최대 진폭(Max amplitude, %)을 기준으로 하였다. Apigenin은 dimethyl sulfoxide (DMSO)에 용해하여 최종 농도가 0.1%가 되도록 하였고, 이는 DMSO의 영향을 최소화하면서도 apigenin을 충분히 용해할 수 있는 농도임을 확인하였다. 대조군은 동일한 농도의 DMSO만 처리한 것으로 하여 DMSO가 주는 자체적인 영향을 고려하였다.
세포 독성 분석 − Apigenin의 세포 독성은 혈소판 세포질에서 방출되어 나오는 젖산탈수소효소(lactate dehydrogenase, LDH)를 통해 평가하였다. 먼저, 사람 혈소판 현탁액(108 cells/mL)을 준비한 후, 다양한 농도의 apigenin을 첨가하여 1시간 동안 배양하였다. 이후, 10,000 × g에서 2분간 원심분리한 뒤, 상층액을 회수하여 LDH Cytotoxicity Assay Kit (Cayman Chemical, Ann Arbor, MI, USA)를 사용하여 ELISA 기기(TECAN, Salzburg, Austria)에서 490 nm에서 측정함으로써 세포 독성을 평가하였다.
TXB2의 확인 − 세척된 사람 혈소판(108 cells/mL)에 다양한 농도의 apigenin을 처리하여 3분 간 37℃에서 배양한 후, 2 mM의 CaCl2를 첨가하여 collagen (2.5 μg/mL)으로 5분 간 자극하였다. TXA2의 안정적인 대사물질로 알려진 TXB2을 확인함으로써 TXA2의 생성정도를 확인할 수 있기에, TXB2 assay kit를 사용하여 synergy HT multi-reader (BioTek Instruments, Winooski, VT, USA)에서 측정하여 정량하였다.
ATP 및 serotonin 방출량 측정 − ATP와 serotonin의 측정을 위해 얼음 위에서 유지된 2 mM EDTA를 첨가하는 것으로 반을을 중지시켰다. 이 후, 10,000×g에서 10분 간 원심분리한 상층액을 수집하였고, ATP Detection Assay Kit (Cayman Chemical, Ann Arbor, MI, USA)를 사용하여 발광 신호를 측정함으로써 ATP 방출량을 정량하였다. Serotonin 방출량은 동일한 방법으로 Serotonin ELISA Kit (Abcam, Cambridge, UK)를 사용하여 410 nm에서 ELISA reader (TECAN, Salzburg, Austria)를 통해 측정 및 정량하였다.
Western Immunoblotting − 5분 동안 혈소판 응집반응을 일으킨 후, 1× Cell Lysis Buffer를 처리하여 반응이 중단되며 세포가 용해되게 하였다. 이 안의 단백질 농도를 BCA Protein Kit (Pierce Biotechnology, IL, USA)로 정량하여, 단백질 15 µg로 동일하게 희석한 후, 8% SDS-PAGE에서 단백질을 분리하였고 이를 PVDF 막으로 전이하였다. 3% BSA Blocking Solution으로 blocking을 수행하고, 1차 항체(1:1,000 희석) 및 2차 항체(1:2,000 희석) 처리함으로써 면역 반응을 일으켰다. Western Bright ECL Kit (Advansta, Menlo Park, CA, USA)를 사하여 단백질 신호를 확인하였고, Quantity One Version 4.5(Bio-Rad, Hercules, CA, USA) 소프트웨어를 이용하여 특정 단백질의 차이를 분석하였다.
혈소판 매개의 fibrin clot 생성량 측정 − 혈소판 세포가 비특이적으로 시험관 벽에 점착되어 활성화 되는 일을 막기 위하여 polyethylene 재질의 시험관으로 옮기고, 2 mM CaCl2 및 thrombin (0.05U/mL)을 첨가해 주어 37℃에서 20분 동안 반응이 일어나게 하였다. 형성된 fibrin clot의 모습을 디지털 카메라로 사진 촬영하였고, ImageJ (v1.46, National Institutes of Health, Bethesda, MD, USA)를 통해 응고된 영역을 계산하였고 혈전 형성 정도를 정량하여 비교하였다.
통계 분석 − 실험 자료는 평균(mean) ± 표준편차(SD)로 제시하였다. 집단 간 차이 검정을 위해 일원분산분석(ANOVA)을 실시하였고, 유의성이 확인된 경우 사후분석은 Tukey-Kramer 방법을 적용하였다. 모든 통계 처리는 SPSS software ver. 21.0.0.0 (SPSS Inc., Chicago, IL, USA)을 이용하였으며, p값이 0.05 미만일 때 통계적으로 유의한 것으로 간주하였다.
결과 및 고찰
Apigenin의 혈소판 응집 및 세포 독성에 대한 영향 − 본 연구에서는 우선적으로 apigenin이 collagen 유도에 의한 사람 혈소판의 응집이 억제되는 확인하고, apigenin이 이 과정에서 어떤 기전에 관여하는지를 규명하고자 하였다(Fig. 1). 혈소판 응집의 유도를 위해서 강력한 응집유도 물질로 알려진 collagen (2.5 μg/mL)을 사용하여 사람 혈소판을 자극하였다. 그 결과, collagen에 의한 혈소판 응집률이 83.0%로 나타났고 apigenin을 첨가함에 따라 혈소판 응집이 농도의존적으로 억제되었다(Fig. 2A). 응집 억제율은 16 µM에서 30.1%, 24 µM에서 80.7%, 32 µM에서 94.3%로 확인되었고, apigenin의 half-maximal inhibitory concentration (IC50)가 18.01 µM로 측정되었으며(Fig. 2B), 이는 해당 물질이 뛰어난 효능을 가지며 적은 농도에서도 효과적으로 작용할 수 있음을 시사한다. 기존에 항혈소판 효과가 있다고 확인된 물질들과 비교해보더라도, cordycepin, esculeitin 및 isoscopoletin의 IC50이 261.10, 135.85 및 240.93 µM인 것에 비하여 더 강한 효과를 갖는다는 것을 알 수 있으며, 항혈소판 효과가 우수한 것으로 유용한 홍삼의 G-Rk3보다더 효과가 강하였음을 알 수 있었다.21-24) 또한, 세포 생존율에 의해 확인되는 세포 독성 유무 평가를 통해, apigenin이 혈소판에 유해한 영향을 주지 않았음을 확인하였다(Fig. 2C). 이 결과들을 통해, apigenin이 세포 독성을 보이지 않으면서 뛰어난 혈소판 응집 억제 효과를 나타내는 유효한 성분인 것을 확인하였다.
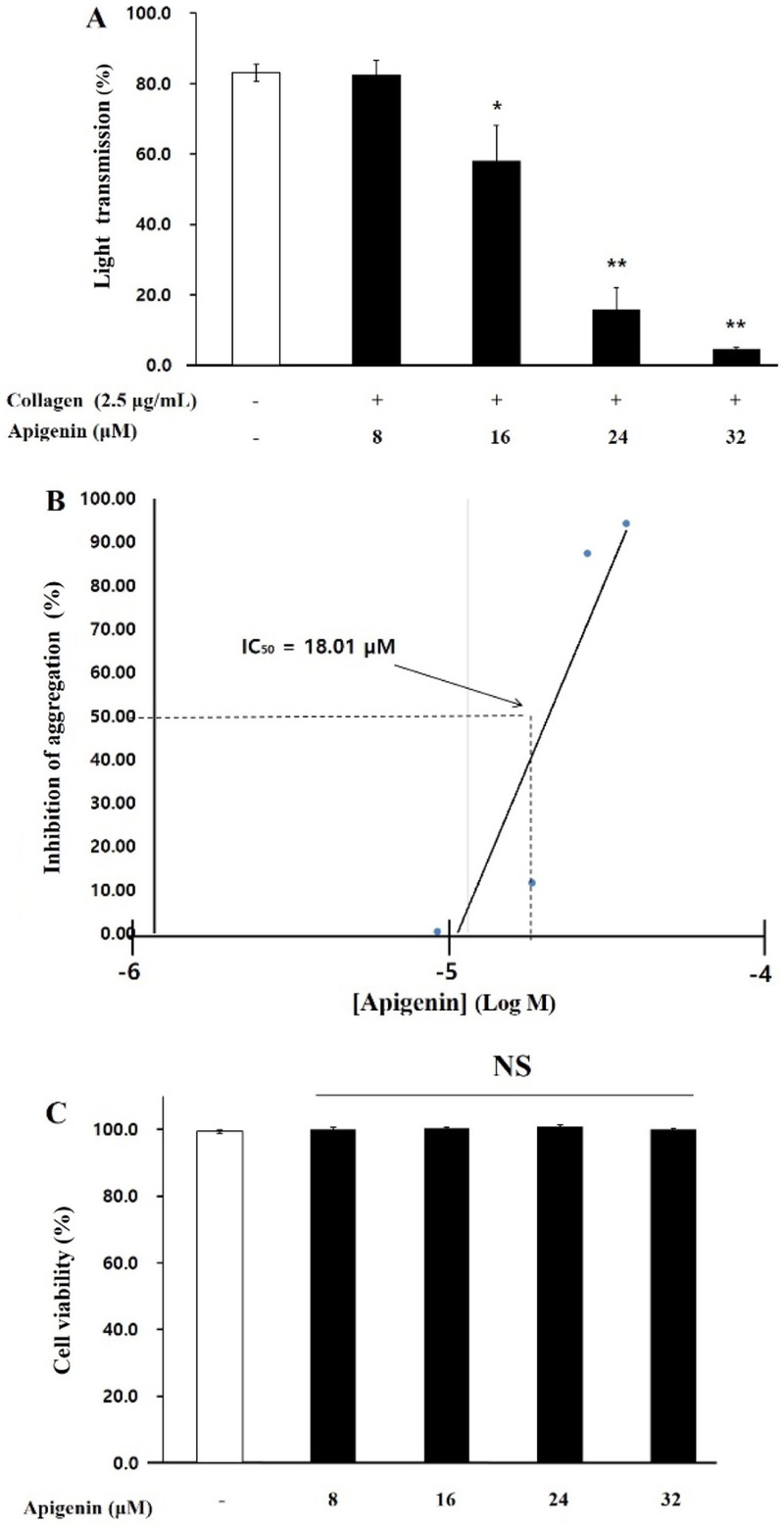
Apigenin’s effect on human platelet aggregation. (A) Apigenin’s effect on collagen-induced human platelet aggregation. (B) The IC50 of apigenin on platelet aggregation. (C) The cytotoxicity of apigenin on human platelets. The results are shown as mean ± SD (n=4). *p < 0.05, **p < 0.001 in comparison to the collagen-induced platelets.
Apigenin이 PI3K/Akt 인산화에 미치는 영향 − 본 연구를 통해, apigenin이 혈소판 내 과립 방출 및 활성화와 관여하는 PI3K/Akt의 인산화에 미치는지 확인하였다. Fig. 3에서 보여주는 바와 같이, collagen으로 자극이 유도된 혈소판에서 PI3K와 Akt의 인산화 강도가 현저히 증가하였으나, apigenin을 처리하였을 경우, 이들의 인산화 정도가 확연히 줄어드는 것을 볼 수 있었다. PI3K 및 Akt 경로가 세포 내 신호전달 과정에서 혈소판을 활성화시키며 이들의 인산화를 통해 혈소판 응집과 혈소판 내 dense 과립 분비가 일어난다는 것이 잘 알려져 있다.25-26) 본 연구에서 확인한 결과에서도, apigenin이 PI3K/Akt 인산화를 억제하였기에 이 경로를 조절함으로써 혈소판의 과립분비 및 응집을 감소시켰을 것이라 짐작된다.
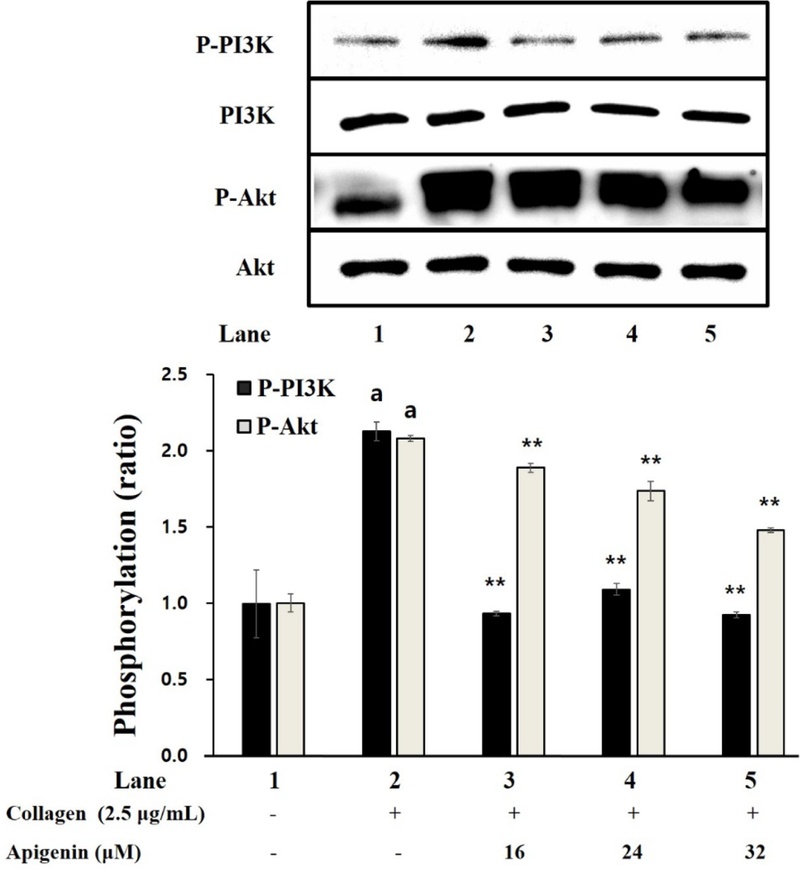
Apigenin’s effect on the phosphorylation of PI3K/Akt. The results are shown as mean±SD (n=4). ap < 0.05 in comparison to no-stimulated platelets, **p < 0.001 in comparison to collagen-induced platelets.
Apigenin이 MAPK 인산화에 미치는 영향 − MAPK 경로의 단백질들 역시 세포 내 신호 전달을 통해 세포 내 반응을 조절하는 것으로 알려져 있고, 혈소판의 과립 방출에 관여하는 것으로 보고 되고 있다. 본 연구에서는 MAPK 경로에 있는 ERK, JNK 및 p38의 인산화에 미치는 apigenin의 영향을 확인하였고, Fig. 4를 보여지는 바와 같이, collagen은 intact 혈소판에서 JNK/p38의 인산화 강도를 현저히 높였지만, ERK의 인산화에는 유의한 영향을 주지 못하였다. 또한, collagen호 유발된 JNK/p38의 인산화가 apigenin을 처리하였을 때 유의하게 억제되었는데(Fig. 4), 이는 apigenin이 JNK/p38의 인산화를 감소시킴으로써 혈소판 응집의 신호 전달 과정을 조절하고 있다는 것을 보여준다. 다른 연구에서도 혈소판 응집을 억제하는 물질들이 JNK/p38보다 ERK의 인산화에 덜 관여한다는 보고가 있으며, 또한 사람 혈소판에서 응집유도제가 ERK의 인산화 자체에 영향을 미치지 않는다는 연구들도 있다.27,28) 이와 관련하여 이들 MAPK 단백질들의 인산화와 사람 혈소판의 신호전달 및 응집억제에 어떻게 관여하는지에 관한 추가적인 연구가 필요하다고 판단된다.
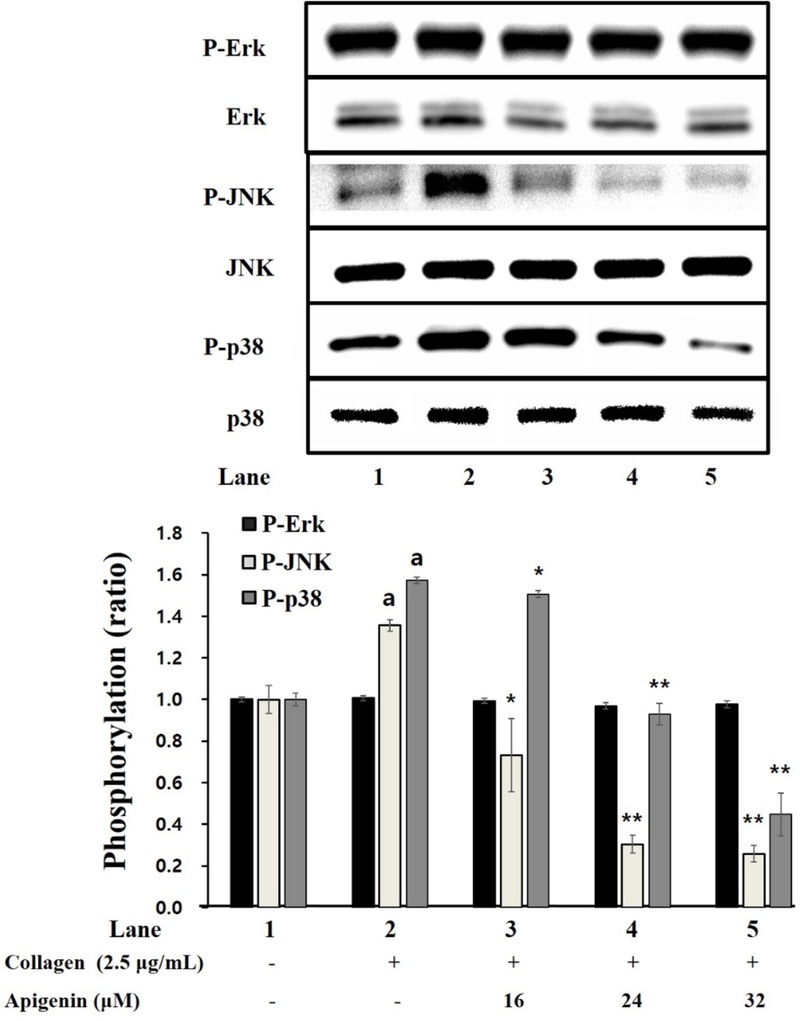
Apigenin’s effect on the phosphorylation of MAPK. The results are shown as mean±SD (n=4). ap < 0.05 in comparison to no-stimulated platelets, *p < 0.05, **p < 0.001 in comparison to collagen-induced platelets.
이전 연구들을 통해 MAPK 경로에 관여하는 단백질들이 사람의 혈소판에 상당하게 존재하고 있음이 확인되었고, 응집유도제들이 혈소판을 자극하여 MAPK 경로의 단백질들의 인산화를 일으킴으로써 기능한다고 알려져 있다.29-31) 본 연구의 결과를 통해서도, collagen 유도의 사람 혈소판에서 JNK/p38의 인산화가 강하게 일어나며 혈소판 활성화를 일으키는 것을 알 수 있었고, apigenin의 처리가 JNK/p38의 인산화를 강하게 감소시키면서 혈소판 활성화를 저해한다는 것을 확인하였다.
Apigenin이 cPLA2 인산화에 미치는 영향 − 앞선 연구들에 따르면, MAPK 경로의 활성화가 세포질 내 phospholipase A2 (cPLA2)의 인산화를 유도하면서 혈소판 막 인지질을 가수분해를 일으키고, arachidonic acid의 생성 및 혈소판 활성화를 증폭시키는 thromboxane A2 (TXA2) 생성을 증가시킨다고 알려져 있다.32,33) 따라서, apigenin이 cPLA2의 인산화 및 TXA2 생성에도 관여하였는지 확인할 필요가 있다.
cPLA2의 인산화에 미치는 apigenin의 효과를 확인하였고, Fig. 5A에서 볼 수 있는 바와 같이, collagen의 유도에 의해 혈소판 내 cPLA2가 강하게 인산화되었고, 이를 apigenin가 농도의존적으로 크게 감소시킨다는 것을 알 수 있었다. 뿐만 아니라, apigenin에 의해 TXA2 생성도 농도의존적으로 감소되는 것을 확인하였다(Fig. 5B). 이는 apigenin이 cPLA2의 인산화를 강하게 억제하면서 TXA2 생성을 억제함으로써 혈소판 응집을 저해하는 역할을 하고 있는 것을 의미한다.
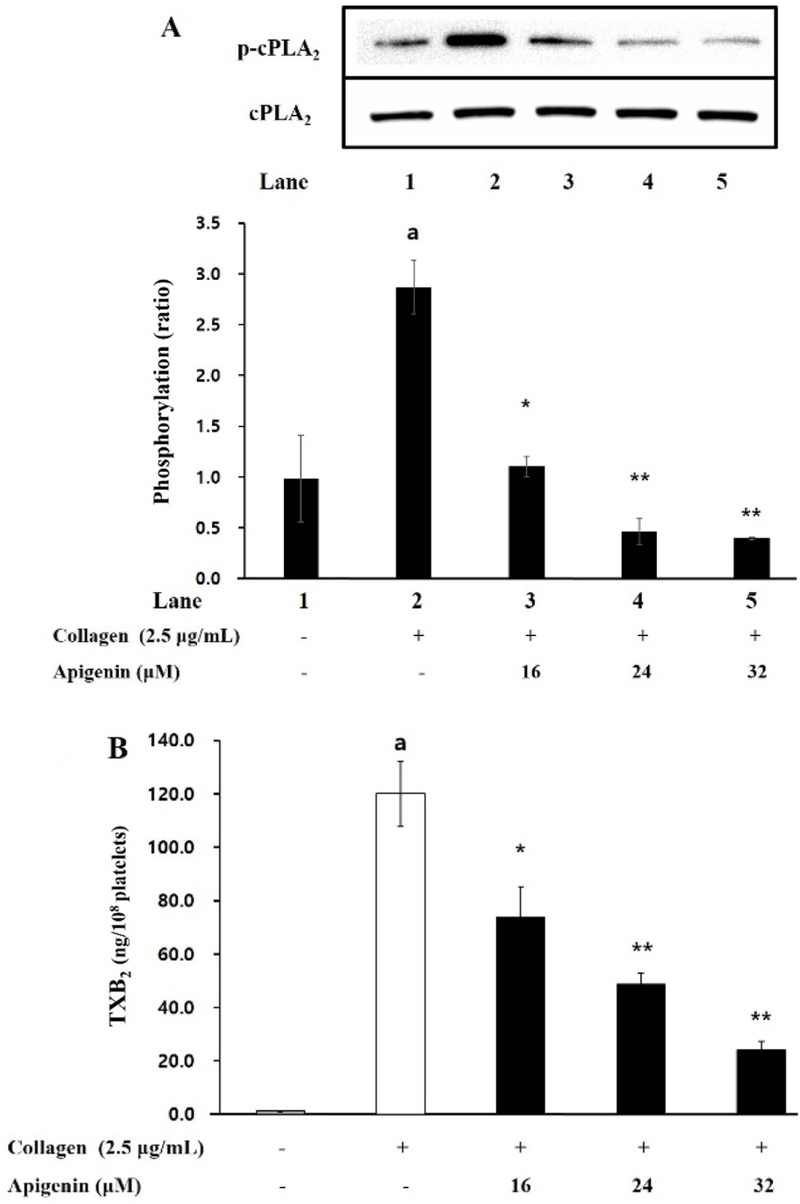
Apigenin’s effect on the phosphorylation of cPLA2 and TXA2 production. (A) Apigenin’s effect on the phosphorylation of cPLA2. (B) Apigenin’s effect on TXA2 production. The results are shown as mean ± SD (n=4). ap < 0.05 in comparison to nostimulated platelets, *p < 0.05, **p < 0.001 in comparison to collagen-induced platelets.
Apigenin이 혈소판 과립 분비에 미치는 영향 − 혈소판 내의 과립에 존재하는 물질들이 방출될 때, 혈소판 응집이 증폭되어 더 강력하게 일어나고 유지되기에 apigenin이 과립 내 물질인 ATP 및 serotonin의 방출에 관여하는지 확인하였다. 그 결과, 손상되지 않은 세포에서 0.24 ± 0.03 mM의 ATP 방출량이 collagen에 의해 10.13 ± 0.62 mM로 강하게 증가하였다. 그러나, 증가된 ATP 방출량이 apigenin (16, 24 및 32 µM)에 의해 농도의존적으로 억제되었다(Fig. 6A). 또한, serotonin 방출량에 있어서도 14.27 ± 0.16 ng/108 cells였던 것을 collagen가 130.45 ± 3.20 ng/108 cells까지 증가시켰고. 증가된 serotonin 방출량을 apigenin (16, 24 및 32 µM)가 89.22 ± 12.63, 52.06 ± 3.31 및 22.80 ± 0.84 ng/108 cells로 농도의존적으로 감소시키는 것을 볼 수 있다(Fig. 6B). 이 결과들을 통해 보면, apigenin이 혈소판 내 과립의 물질 분비를 강하게 억제함으로써 추가적인 혈소판 응집을 저해시킨다는 것을 알 수 있다.
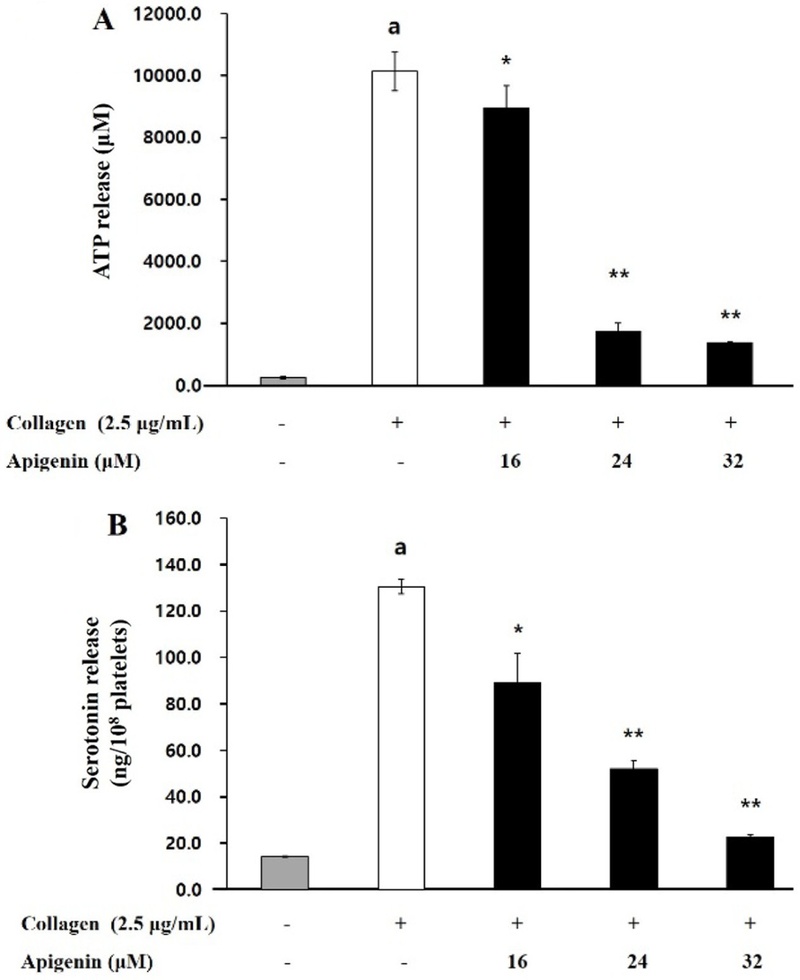
Apigenin’s effect on granule secretion. (A) Apigenin’s effect on ATP release. (B) Apigenin’s effect on serotonin release. The results are shown as mean ± SD (n=4). ap < 0.05 in comparison to no-stimulated platelets, *p < 0.05, **p < 0.001 in comparison to collagen-induced platelets.
혈소판 내 과립 물질의 분비는 혈소판의 활성화를 촉진하고 손상된 혈관으로 순환하는 혈소판의 점착 및 응집을 유도함으로써 혈전을 일으키는 것으로 알려져 있다.34) 본 연구의 결과들은 apigenin이 collagen에 의해 유도된 PI3K/Akt 및 MAPK 경로의 활성화를 강력하게 억제함으로써 혈소판 내 과립으로부터의 ATP 및 serototnin 방출을 농도의존적으로 감소시키고, 결과적으로 혈소판 활성화 및 혈소판 응집을 억제하는 물질임을 규명하였다.
Apigenin이 혈소판 매개의 fibrin clot 생성량에 미치는 효과 − 본 연구에서는 thrombin로 유도한 fibrin 응고 형성에 미치는 apigenin의 효과를 평가하였고, Fig. 7A에 제시한 바와 같이, thrombin (0.05 U/mL)은 fibrin 응고 형성을 강하게 유발하였다. 그러나, 다양한 용량(16, 24 및 32 µM)의 apigenin을 처리하였을 때, fibrin 응고 형성의 정도가 농도의존적으로 감소되는 것을 확인하였고, apigenin의 억제율은 각각 5.6%, 55.2% 및 71.4%인 것을 볼 수 있었다(Fig. 7B). 이러한 결과들로 볼 때, apigenin가 혈전 형성을 조절하여 심혈관 질환을 억제할 수 있는 효과적인 물질임을 시사한다.
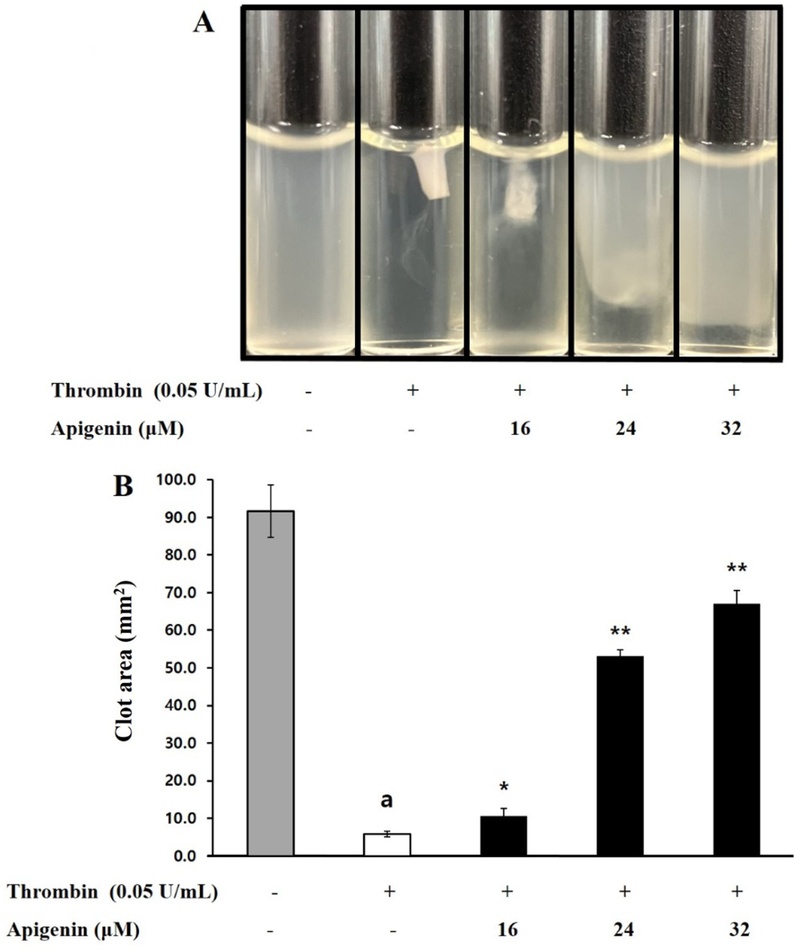
Apigenin’s effect on thrombin-retracted fibrin clot. (A) Apigenin’s effect on thrombin-retracted fibrin clot photographs (B) Apigenin’s effect on thrombin-retracted fibrin clot area. The results are shown as mean ± SD (n=4). ap < 0.05 compared with no-stimulated platelets, *p < 0.05, **p < 0.001 compared with the thrombin-stimulated platelets.
Conflict of interest: The authors declare no conflict of interest.
References
-
Schwartz, S. M., Heimark, R. L. and Majesky, M. W. (1990) Developmental mechanisms underlying pathology of arteries. Physiol. Rev. 70: 1177-1209.
[https://doi.org/10.1152/physrev.1990.70.4.1177]

-
Wonerow, P., Obergfell, A., Wilde, J. I., Bobe, R., Asazuma, N., Brdicka, T., Leo, A., Schraven, B., Horejsí, V., Shattil, S. J. and Watson, S. P. (2002) Differential role of glycolipid-enriched membrane domains in glycoprotein VI- and integrin-mediated phospholipase Cgamma2 regulation in platelets. Biochem. J. 364: 755-765.
[https://doi.org/10.1042/bj20020128]

-
Jennings, L. K. (2009) Role of platelets in atherothrombosis. Am. J. Cardiol. 103: 4A-10A.
[https://doi.org/10.1016/j.amjcard.2008.11.017]

-
Sabatine, M. S. and Jang, I. K. (2000) The use of IIb/IIIa inhibitors in patients with coronary artery disease. Am. J. Med. 109: 224-237.
[https://doi.org/10.1016/S0002-9343(00)00474-5]

-
Irfan, M., Jeong, D., Kwon, H. W., Shin, J. H., Park, S. J., Kwak, D., Kim, T. H., Lee, D. H., Park, H. J. and Rhee, M. H. (2018) Ginsenoside-Rp3 inhibits platelet activation and thrombus formation by regulating MAPK and cyclic nucleotide signaling. Vascul. Pharmacol. 109: 45-55.
[https://doi.org/10.1016/j.vph.2018.06.002]

-
Adam, F., Kauskot, A., Rosa, J. P. and Bryckaert, M. (2008) Mitogen-activated protein kinases in hemostasis and thrombosis. J. Thromb. Haemost. 6: 2007-2016.
[https://doi.org/10.1111/j.1538-7836.2008.03169.x]

-
Bugaud, F., Nadal-Wollbold, F., Lévy-Toledano, S., Rosa, J. P. and Bryckaert, M. (1999) Regulation of c-jun-NH2 terminal kinase and extracellular-signal regulated kinase in human platelets. Blood 94: 3800-3805.
[https://doi.org/10.1182/blood.V94.11.3800]

-
Kramer, R. M., Roberts, E. F., Strifler, B. A. and Johnstone, E. M. (1995) Thrombin induces activation of p38 MAP kinase in human platelets. J. Biol. Chem. 270: 27395-27398.
[https://doi.org/10.1074/jbc.270.46.27395]

-
Nadal-Wollbold, F., Pawlowski, M., Lévy-Toledano, S., Berrou, E., Rosa, J. P. and Bryckaert, M. (2002) Platelet ERK2 activation by thrombin is dependent on calcium and conventional protein kinases C but not Raf-1 or B-Raf. FEBS Lett. 531: 475-482.
[https://doi.org/10.1016/S0014-5793(02)03587-1]

-
Michelson, A. D. (2010) Antiplatelet therapies for the treatment of cardiovascular disease. Nat. Rev. Drug Discov. 9: 154-169.
[https://doi.org/10.1038/nrd2957]

-
Flevaris, P., Li, Z., Zhang, G., Zheng, Y., Liu, J. and Du, X. (2009) Two distinct roles of mitogen-activated protein kinases in platelets and a novel Rac1-MAPK-dependent integrin outside-in retractile signaling pathway. Blood 113: 893-901.
[https://doi.org/10.1182/blood-2008-05-155978]

-
Kramer, R. M., Roberts, E. F., Um, S. L., Börsch-Haubold, A. G., Watson, S. P., Fisher, M. J. and Jakubowski, J. A. (1996) p38 mitogen-activated protein kinase phosphorylates cytosolic phospholipase A2 (cPLA2) in thrombin-stimulated platelets. Evidence that proline-directed phosphorylation is not required for mobilization of arachidonic acid by cPLA2. J. Biol. Chem. 271: 27723-27729.
[https://doi.org/10.1074/jbc.271.44.27723]

-
McNicol, A. and Shibou, T. S. (1998) Translocation and phosphorylation of cytosolic phospholipase A2 in activated platelets. Thromb. Res. 92: 19-26.
[https://doi.org/10.1016/S0049-3848(98)00097-8]

-
Chuang, W. Y., Kung, P. H., Kuo, C. Y. and Wu, C. C. (2013) Sulforaphane prevents human platelet aggregation through inhibiting the phosphatidylinositol 3-kinase/Akt pathway. Thromb. Haemost. 109: 1120-1130.
[https://doi.org/10.1160/TH12-09-0636]

-
Venigalla, M., Gyengesi, E. and Münch, G. (2015) Curcumin and apigenin – novel and promising therapeutics against chronic neuroinflammation in Alzheimer’s disease. Neural. Regen. Res. 10: 1181-1185.
[https://doi.org/10.4103/1673-5374.162686]

-
Yoon, J. H., Kim, M. Y. and Cho, J. Y. (2023) Apigenin: A therapeutic agent for treatment of skin inflammatory diseases and cancer. Int. J. Mol. Sci. 24: 1498.
[https://doi.org/10.3390/ijms24021498]

-
Lee, I. G., Lee, J., Hong, S. H. and Seo, Y. J. (2023) Apigenin’s therapeutic potential against viral infection. Front. Biosci. 28: 237.
[https://doi.org/10.31083/j.fbl2810237]

-
Imran, M., Gondal, T. A., Atif, M., Shahbaz, M., Qaisarani, T. B., Mughal M. H., Salehi, B., Martorell, M. and Sharifi-Rad, J. (2020) Apigenin as an anticancer agent. Phytother. Res. 34: 1812-1828.
[https://doi.org/10.1002/ptr.6647]

- Kim, S. O., Jeong, J. S. and Choi, Y. H. (2019). Antioxidant and anti-inflammatory effects of ethanol extract of Aster yomena in RAW 264.7 macrophages. J. Life Sci. 29: 977-985.
-
Ko, S. N., Son, J. W., Kim, G. R., Kim, M. S., Lee, Y. J., Kim, S. J., Shin, J. H., Jo, D. I., Bok, W. Y., Oh, H. G. and Kwon, H. W. (2023) The inhibitory effects of Glycyrrhiza uralensis on human platelet aggregation and thrombus formation. Biomed. Sci. Lett. 29: 242-248.
[https://doi.org/10.15616/BSL.2023.29.4.242]

-
Kwon, H. W. and Lee, D. H. (2017) The inhibitory effects of cordycepin on phosphoproteins including PI3K, Akt, and p38. Korean. J. Clin. Lab. Sci. 49: 99-107.
[https://doi.org/10.15324/kjcls.2017.49.2.99]

-
Lee, D. H. (2020) Anti-platelet effects of isoscopoletin through regulation of PI3K/Akt and MAPK on collagen-induced human platelets. Kor. J. Pharmacogn. 51: 151-157.
[https://doi.org/10.3839/jabc.2020.018]

-
Lee, D. H. (2021) Thrombus Formation Inhibition of Esculetin through Regulation of Cyclic Nucleotides on Collagen-Induced Platelets. Biomed. Sci. Letters 27: 270-276.
[https://doi.org/10.15616/BSL.2021.27.4.270]

-
Kwon, H. W., Shin, J. H., Rhee, M. H., Park, C. E. and Lee, D. H. (2023) Anti-thrombotic effects of ginsenoside Rk3 by regulating cAMP and PI3K/MAPK pathway on human platelets. J. Ginseng Res. 47: 706-713.
[https://doi.org/10.1016/j.jgr.2023.04.006]

-
Chuang, W. Y., Kung, P. H., Kuo, C. Y. amd Wu, C. C. (2013) Sulforaphane prevents human platelet aggregation through inhibiting the phosphatidylinositol 3-kinase/Akt pathway. Thromb. Haemost. 109: 1120-1130.
[https://doi.org/10.1160/TH12-09-0636]

- Thanaketpaisarn, O., Waiwut, P., Sakurai, H. and Saiki, I. (2011) Artesunate enhances TRAIL-induced apoptosis in human cervical carcinoma cells through inhibition of the NF-κB and PI3K/Akt signaling pathways. Int. J. Oncol. 39: 279–285.
-
Irfan, M., Jeong, D., Saba, E., Kwon, H. W., Shin, J. H., Jeon, B. R., Kim, S., Kim, S. D., Lee, D. H., Nah, S. Y. and Rhee, M. H. (2019) Gintonin modulates platelet function and inhibits thrombus formation via impaired glycoprotein VI signaling. Platelets 30: 589-598.
[https://doi.org/10.1080/09537104.2018.1479033]

-
McNicol, A. and Jackson, E. C. (2003) Inhibition of the MEK/ERK pathway has no effect on agonist-induced aggre-gation of human platelets. Biochem. Pharmacol. 65: 1243-1250.
[https://doi.org/10.1016/S0006-2952(03)00069-8]

-
Adam, F., Kauskot, A., Nurden, P., Sulpice, E., Hoylaerts, M. F. and Davis, R. J. (2010) Platelet JNK1 is involved in secretion and thrombus formation. Blood 115: 4083-4092.
[https://doi.org/10.1182/blood-2009-07-233932]

-
Bugaud, F., Nadal-Wollbold, F., Lévy-Toledano, S., Rosa, J. P. and Bryckaert, M. (1999) Regulation of c-jun-NH2 terminal kinase and extracellular-signal regulated kinase in human platelets. Blood 94: 3800-3805.
[https://doi.org/10.1182/blood.V94.11.3800]

-
Kramer, R. M., Roberts, E. F., Strifler, B. A. and Johnstone, E. M. (1995) Thrombin induces activation of p38 MAP kinase in human platelets. J. Biol. Chem. 270: 27395-27398.
[https://doi.org/10.1074/jbc.270.46.27395]

-
Kramer, R. M., Roberts, E. F., Um, S. L., Börsch-Haubold, A. G., Watson, S. P. and Fisher, M. J. (1996) p38 mitogen-activated protein kinase phosphorylates cytosolic phospholipase A2 (cPLA2) in thrombin-stimulated platelets. Evidence that proline-directed phosphorylation is not required for mobilization of arachidonic acid by cPLA2. J. Biol. Chem. 271: 27723-27729.
[https://doi.org/10.1074/jbc.271.44.27723]

-
McNicol, A. and Shibou, T. S. (1998) Translocation and phosphorylation of cytosolic phospholipase A2 in activated platelets. Thromb. Res. 92: 19-26.
[https://doi.org/10.1016/S0049-3848(98)00097-8]

-
Calderwood, D. A. (2004) Integrin activation. J. Cell Sci. 117: 657-666.
[https://doi.org/10.1242/jcs.01014]