강활(Ostercum koreanum) 잎의 극성 용매 분획의 성분
Abstract
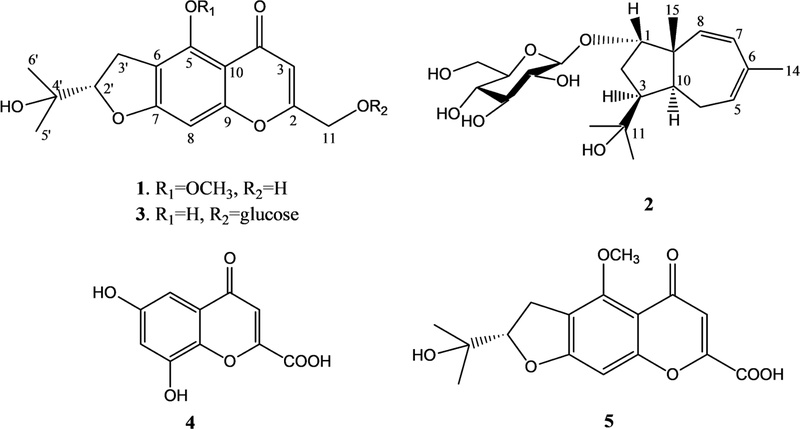
Four chromone derivatives and one sesquiterpene glycoside were isolated from the n-BuOH fraction of the leaves of Ostericum koreanum. Based on spectral data analysis, the isolated compounds were identified as cimifugin (1), polymorpholide-1-O-β-D-glucoside (2), prim-glucosylangelicin (3), 5,7-dihydroxy-4-oxo-4H-chromene-2-carboxylic acid (4), and dviaricatiacid (5). We revised several carbon chemical shifts for compound 3. Among these, compound 4 was isolated from a plant source for the first time, and compounds 2, 3, and 5 were also isolated from O. koreanum for the first time.
Keywords:
Ostericum koreanum, Leaves, Chromones, Sesquiterpene glycoside한방에서 뿌리를 해열, 진통작용을 목표로 감기나 근육통의 치료에 중요하게 사용되고 있는 강활(Ostericum koreanum)은 산형과(Umbelliferae)에 속하는 다년초로 우리나라, 만주, 우수리 등의 지역에 분포한다.1,2) 강활의 뿌리에 대한 연구는 매우 다양하게 이루어져 있으나, 줄기나 잎 등의 부위에 대한 연구는 거의 이루어지지 않고 있다. 또한 강활은 그 학명이 Angelica koreana, Ostericum koreanum 및 O. praeteritum 등3)으로 명명되어 사용되었으나, 최근 Angelica reflexa로 변경되는 등4) 매우 복잡한 분류학적 특징을 가지고 있는 식물이기도 하다. 그럼에도 불구하고 본 논문에서는 강활의 학명을 대한민국 약전에 수재되어 있는 O. koreanum으로 사용하였다. 저자 등은 우리나라에 자생하고 있는 산형과 식물에 대한 모든 부위의 함유 성분을 밝혀 약용으로 사용하는 부위를 제외한 부위도 자원으로 사용할 수 있는지의 여부를 알아보기 위하여 계속적인 연구를 수행해 오던 중 강활(O. koreanum)의 줄기와 잎으로부터 수종의 coumarin과 chromone 계열의 화합물을 분리하고 구조를 밝혀 보고한 바 있다.5-7) 이 연구는 강활 잎의 성분에 대한 계속적인 연구로 잎의 methanol 추출물 중 n-BuOH 가용성 분획에 함유되어 있는 성분을 밝혀 자원 성분으로서의 가치 뿐 아니라 성분 분류학적 지표로 사용할 수 있는 표준품으로의 이용가치 등을 알아보고자 하였으며, 약간의 결과를 얻었기에 이를 보고하고자 한다.
재료 및 방법
실험재료 − 실험에 사용한 강활(O. koreanum)의 잎은 2016년 8월 태기산의 7부 능선 계곡에서 채집하여 강원대학교 약학대학 권용수 교수가 정확하게 감정한 후 음건하였다. 확증표본(KNUH-L-1608-1)은 강원대학교 약학대학 생약학 연구실에 보관 중이다.
기기 및 시약 − Mass spectra는 Waters사의 Micromass Quattro micro API를 이용하여 측정하였다. NMR spectra는 JEOL사의 JNM-ECZ500R을 이용하여 측정하였다. 선광도는 Jasco사의 DIP-1000 digital polarimeter를 이용하여 측정하였다. 화합물의 분리는 Merck 사의 silica gel (63~200 μm)을 이용한 open column chromatography와 Teledyne Isoco사의 CombiFlash® Flash chromatography system을 이용하여 RediSep® column으로 수행하였다. TLC 분석은 Merck사의 Kieselgel 60 F254와 RP F254s plates를 사용하였다. Chromatography에 사용한 유기 용매는 따로 언급이 없는 한 대정화금의 extra pure grade를 한번 증류한 것을 사용하였다. 기타 시약은 analytical grade를 사용하였다.
추출 및 분리 − 음건하여 잘게 자른 강활(O. koreanum)의 잎 1.5 kg에 MeOH 20 L를 가하고 실온에서 1주일간 3회 추출한 후 여과하고 여액을 40℃에서 감압농축하여 MeOH 분획 178 g을 얻었다. 얻어진 MeOH 분획(175 g)을 증류수에 현탁시키고 n-hexane, CHCl3 및 n-BuOH의 순으로 분획하고 감압 농축하고 n-hexane 분획 32 g, CHCl3 분획 13 g 및 n-BuOH 분획 80 g을 얻었다. n-BuOH 분획 60 g을 silica gel (63~200 μm, 1 kg) column (9.5×50 cm)에 걸고 CHCl3:MeOH(5:1)을 용매로 용출시킨 후 MeOH 100%로 세척하였으며, 이를 TLC 분석을 통하여 일곱 개의 분획(OLB-1~OLB-7)으로 나누었다. 분획 OLB-3 (2.3 g)에 대하여 RediSep® silica gel column (24 g)을 사용하여 CHCl3:MeOH (29:1)을 용매로 flash chromatography를 실시하고 화합물 1 (840 mg)을 얻었다. 분획 OLB-5 (4.5 g)를 RediSep® silica gel column (80 g)을 이용하여 benzene-EtOAc-MeOH (6:3:1)을 용매로 용출시켜 다섯 개의 분획(OLB-5-1 ~ OLB-5-5)으로 나누었다. 이중 분획 OLB-5-1 (1.4 g)을 RediSep® C18 column (43 g)을 이용하여 MeOH-H2O (40:60)으로 용출시켜 화합물 2 (90 mg)을 얻었다. 분획 OLB-5-2 (3.7 g)을 RediSep® C18 column (130 g)을 이용하여 MeOH-H2O (40:60)으로 용출시켜 화합물 3 (980 mg)을 얻었다. 분획 OLB-8 (15 g)을 silica gel (63~200 μm, 600 g) column (6.5 × 50 cm)에 걸고 CHCl3-MeOH-H2O (3:1:0.1)을 용매로 용출시켜 네 개의 분획(OLB-8-1 ~ OLB-8-4)으로 나누었다. 이들 분획 중 분획 OLB-8-3 (2.7 g)에 대하여 RediSep® silica gel column (80 g)을 이용하여 EtOAc-MeOH-H2O (8:1:0.5)을 용매로 용출시켜 네 개의 분획(OLB-8-3-1~OLB-8-3-4)으로 다시 나누었다. 분획 OLB-8-3-2 (1.7 g)를 MeOH로 반복 정제하여 화합물 4 (340 mg)를 얻었다. 분획 OLB-8-3-3 (0.3 g)에 대하여 RediSep® silica gel column (24 g)을 이용하여 water saturated EtOAc-MeOH (5:1)을 용매로 용출시켜 화합물 5 (70 mg)을 얻었다.
Cimifugin (1) − White powder; [α]D27 +42.9° (c 0.12, MeOH); 1H-NMR (CD3OD, 500 MHz) δ: 6.46 (1H, s, H-8), 6.15 (1H, s, H-3), 4.69 (1H, t, J=8.5 Hz, H-2′), 4.38 (2H, s, 11-CH2), 3.88 (3H, s, OCH3), 3.28 (2H, overlapped with CD3OD, m, H-3′), 1.26 (3H, s, CH3-5′), 1.20 (3H, s, CH3-6′); 13C-NMR (CD3OD, 125 MHz): See Table I; ESI-MS m/z 305 [M-H]-.
Polymorpholide-1-O-glucoside (2) − White powder; [α]D27 –33.1° (c 0.12, MeOH); 1H-NMR (CD3OD, 500 MHz) δ: 6.56 (1H, d, J=11.5 Hz, H-8), 5.84 (2H, br d, J=11.0 Hz, H-5, H-7), 4.69 (1H, d, J=8.0 Hz, H-1'), 4.16 (1H, d, J=2.0 Hz, H-1), 4.14 (1H, dd, J=12.0, 1.5 Hz, H-6'a), 4.00 (1H, dd, J=12.0, 5.0 Hz, H-6'b), 3.70~3.58 (3H, m, H-3', 4', 5'), 3.51 (1H, dd, J=9.0, 7.5 Hz, H-2'), 3.32 (1H, m, H-4a), 2.86 (3H, m, H-3, 4b, 10), 2.45 (1H, dd, J=13.5, 7.5 Hz, H-2a), 2.09 (3H, s, CH3-14), 2.05 (1H, m, H-2b), 1.55 (6H, s, CH3-12, 13), 1.19 (3H, s, CH3-15); 13C-NMR (CD3OD, 125 MHz) δ: 139.88 (C-8), 130.51 (C-6), 128.43 (C-5), 126.82 (C-7), 105.66 (C-1'), 91.45 (C-1), 78.20 (C-3'), 77.66 (C-5'), 75.43 (C-2'), 74.12 (C-11), 71.49 (C-4'), 62.73 (C-6'), 52.53 (C-9), 50.42 (C-3), 44.12 (C-10), 35.63 (C-2), 31.94 (CH3-12), 30.67 (C-4), 28.40 (CH3-13), 27.62 (CH3-14), 19.66 (CH3-15); ESI-MS m/z 397 [M-H]-.
Prim-O-glucosylangelicain (3) − Pale yellow powder; 1H-NMR (CD3OD, 500 MHz) δ: 6.36 (1H, s, H-3), 6.25 (1H, s, H-8), 4.70 (1H, br t, J=9.0 Hz, H-2΄), 4.71 (1H, d, J=15.0 Hz, H-11a), 4.55 (1H, d, J=15.0 Hz, H-11b), 4.38 (1H, d, J=8.0 Hz, H-1″), 3.83 (1H, br d, J=11.5 Hz, H-6″a), 3.63 (1H, dd, J=11.5, 4.5 Hz, H-6″b), 3.35~3.23 (4H, m, H-2″, 3″, 4″, 5″), 3.03 (2H, br d, J=9.0 Hz, H-3′), 1.23 (3H, s, CH3-5′), 1.17 (3H, s, CH3-6′); 13C-NMR (CD3OD, 125 MHz): See Table I; ESI-MS m/z 455 [M + H]+, 477 [M+ Na]+.
5,7-Dihydroxy-4-oxo-4H-chromene-3-carboxylic acid (4) − White powder; 1H-NMR (DMSO-d6, 500 MHz) δ: 12.85 (1H, s, 5-OH), 6.56 (1H, s, H-3), 6.48 (1H, d, J=2.5 Hz, H-8), 6.17 (1H, d, J=2.5 Hz, H-6); 13C-NMR (DMSO-d6, 125 MHz): See Table I; ESI-MS m/z 221 [M-H]-, 176 [M-H-COOH]-.
Divaricatacid (5) − White powder; [α]D27 +13.5° (c 0.1, MeOH); 1H-NMR (CD3OD, 500 MHz) δ: 6.72 (1H, s, H-3), 6.63 (1H, s, H-8), 4.69 (1H, t, J=8.0 Hz, H-2′), 3.86 (3H, s, OCH3), 3.27 (2H, d, J=8.0 Hz, H-3′), 1.22 (3H, s, 6′-CH3), 1.16 (3H, s, 5′-CH3); 13C-NMR (CD3OD, 125 MHz): See Table I; ESI-MS m/z 319 [M-H]-, 275 [M-H-COOH]-.
Polymorpholide-1-O-glucoside (2)와 prim-O-glucosylangelicain (3)의 구성 당 확인 − 양 등8)의 방법에 따랐으며, 화합물 2와 3을 각각 2 mg씩 취하여 2 M HCl (H2O/1,4-dioxane, 1:1) 1 ml에 녹이고 90℃에서 4시간 가열한 후 냉각 시켜 질소 가스로 반응액을 농축시켰다. 농축물을 물에 현탁시키고 EtOAc로 3회 분획하여 버린 후 남은 물 층을 다시 질소 가스로 농축시켜 잔류물을 얻었다. 이 잔류물을 L-cysteine methyl ester hydrochloride 1 mg을 함유하는 pyridine 300 μl에 녹이고 60℃로 1시간 가열한 후 여기에 o-tolyisothiocyanate 10 μl를 가하고 60℃에서 1시간 반응시킨다. 이 반응물을 YMC-Triart C-18 column (YMC Co. Ltd., Japan, 250×4.6 mm, 5 μm)을 이용하여 MeCN-0.1% H3PO3 (25:75)을 용매로 0.8 ml/min 속도로 용출시키고 250 nm로 측정하여 Aglient 1260 infinity HPLC system으로 분석을 수행하였으며, 표준품과 결과를 비교하여 구성 당은 두 화합물 모두 D-glucose 임을 확인하였다(tR: D-glucose 23.16 min).
Prim-O-glucosylangelicain (3)의 효소 가수분해 − Zhao 등9)의 방법에 따라 아래와 같이 실시하였다. 화합물 3 (90 mg)을 물 10 ml에 현탁시키고, 여기에 cellulase (Sigma #22178, cellulase from Aspergilus niger, 200 mg)를 넣고 magnetic stirrer를 이용하여 교반하면서 35℃에서 72시간 반응시켰다. 반응액에 EtOAc 20 ml를 넣고 3회 분획한 후 EtOAc 분획을 농축시키고 RediSep® silica gel column (24 g)을 이용하여 CHCl3-MeOH (29:1)을 용매로 Teledyne Isco사의 ComFlash®에 걸어 flash chromatography를 실시하고 가수분해물 3a (13 mg)를 얻었다.
Norcimifugin (angelicain)5) (3a) − White needle; [α]D27 +4.4° (c 0.11, MeOH); 1H-NMR (CD3OD, 500 MHz) δ: 6.36 (1H, s, H-8), 6.27 (1H, s, H-3), 4.76 (1H, t, J=8.5 Hz, H-2′), 4.45 (2H, s, 11-CH2), 3.11 (1H, d, J=9.5 Hz, H-3′a), 3.10 (1H, d, J=8.5 Hz, H-3′b), 1.27 (3H, s, 5′-CH3), 1.22 (3H, s, 6′-CH3); 13C-NMR (CD3OD, 125 MHz) δ: 184.28 (C-4), 171.50 (C-2), 168.17 (C-5), 159.64 (C-7), 157.46 (C-9), 110.62 (C-6), 106.73 (C-3), 106.41 (C-10), 93.06 (C-2′), 90.03 (C-8), 72.32 (C-4′), 61.38 (C-11), 27.31 (C-3′), 25.31 (C-5′), 25.25 (C-6′).
결과 및 고찰
화합물 1은 NMR, MS 및 선광도 등을 문헌치7)와 비교하여 cimifugin으로 동정하였으며, 화합물 2는 1H- 과 13C-NMR의 chemical shifts와 선광도 값의 비교 및 가수분해에 의한 구성 당의 확인 등의 실험 결과들을 문헌10)과 대조하여 polymorpholide-1-O-glucoside로 동정하였다. 화합물 3은 1H-NMR spectrum의 δH 6.36과 6.25에서 각각의 singlet이 나타나는 것으로부터 이 화합물이 chromone계열의 화합물임을 알 수 있었으며, δH 4.70에서 J=9.0 Hz의 broad triplet, 3.03에서 J=9.0 Hz의 broad doublet 및 δH 1.23과 1.27에서 나타나는 methyl기에 의한 각각의 singlet들과 더불어 δH 4.71과 4.55에서 J=15.0 Hz의 doublet이 각각 나타나며, 13C-NMR spectrum의 δC 93.03과 27.20에서 나타나는 signal들이 HSQC spectrum을 이용하여 확인한 결과 1H-NMR spectrum의 δH 4.70에서 나타나는 J=9.0 Hz의 broad triplet 및 δH 3.03에서 나타나는 J=9.0 Hz의 broad doublet과 각각 correlation하므로 이 화합물은 dihydrofuran ring이 존재하는 chromone계열의 화합물인 norcimifugin을 모핵으로 가지고 있음을 알 수 있었다.5) 또한 NMR의 δH 4.38에서 나타나는 J=8.0 Hz의 doublet과 δC 104.07에서 나타나는 signla로부터 화합물 3은 한 개의 당이 결합되어 있으며 당이 결합된 위치는 HMBC spectrum 분석을 이용하여 확인할 수 있었다. 즉 δH 4.38에서 나타나는 당의 anomeric proton이 δC 65.66에서 나타나는 CH2O의 탄소와 correlation 하므로 당은 11번 위치에 결합되어 있음을 알 수 있었다. 한편, 문헌11)에 기재된 각 탄소의 chemical shifts 값이 본 연구자 등이 실험하여 얻은 값과 조금 다르다는 것을 확인하고 정확한 assignment를 위해 DQF-COSY, HSQC 및 HMBC 분석을 통하여 모든 탄소의 chemical shifts를 결정할 수 있었다. Table I에서 보는 것처럼 Kozawa 등11)이 보고한 carbon chemical shifts 중 2, 3, 6, 10번 탄소의 chemical shifts가 δC 104.88, 107.04 및 155.69에서 각각 나타나지만 저자 등은 HSQC와 HMBC spectra를 분석하여 이들 탄소의 chemical shifts를 δC 167.72, 108.27, 110.61 및 106.45로 결정할 수 있었다. 이상의 결과를 종합하여 화합물 3을 prim-O-glucosylangelicain으로 동정하였다. 화합물 4의 1H-NMR spectrum을 보면 δH 12.85에서 나타나는 singlet, 6.56에서 나타나는 singlet, 그리고 δH 6.48과 6.17에서 J=2.5 Hz의 doublet이 각각 나타나는 것 외에 다른 peak은 확인할 수 없었는데 이는 2, 5 및 7번에 치환기가 존재하는 chromone 계열의 화합물로 추정되었다. 또한 1H-NMR spectrum에서 methoxyl group, methylene group, methyl group 등의 관능기를 확인할 수 없었으므로 2번 위치에는 이들과는 다른 관능기가 치환되어 있을 것으로 추정되었다.12) 13C-NMR spectrum에서도 methoxyl, methylene 및 methyl group 등에 의한 signal은 확인할 수 없었다. 분자량을 확인하기 위하여 negative mode로 측정한 ESI-MS spectrum의 m/z 221 [M-H]-에서 quassi molecular ion peak를 확인할 수 있었으며, 또한 m/z 176에서 나타나는 fragment ion은 COOH가 떨어지면서 만들어진 것으로 추정되며 이는 13C-NMR spectrum의 δC 162.96에서 나타나는 carbonyl에 의한 signal로도 확인할 수 있었고 이는 2번 위치에 carboxylic acid가 치환되어 있음을 알 수 있었다. 이 결과를 문헌13)과 비교하여 화합물 4는 5,7-dihydroxy-4-oxo-4H-chromene-3-carboxylic acid로 동정하였다. 화합물 5도 1H-NMR spectrum을 보면 δH 6.36과 6.27에서 각각의 singlet이 나타나고, δH 4.69에서 J=8.0 Hz로 나타나는 triplet과 3.27에서 나타나는 J=8.0 Hz의 doublet, δH 1.22와 1.16에서 나타나는 각각의 singlet 그리고 δH 3.86에서 나타나는 methoyl기에 의한 singlet 등의 signal 들을 확인할 수 있었으며, 이들 외에 다른 1H-NMR signal은 찾아 볼 수 없었다. 이는 δH 4.50 부근에서 나타나는 CH2O에서 유래하는 signal이 없다는 것을 제외하면 cimifugin의 1H-NMR spectrum과 매우 유사함을 알 수 있었으며14), 13C-NMR spectrum의 δC 50에서 70사이에서도 OCH3나 CH2O에 의한 탄소 signal들이 나타나지 않고 δC 25 부근에도 두 개의 methyl기를 제외하고 다른 methyl기에 의한 탄소 signal은 찾아 볼 수 없었다. 한편 ESI-MS spectrum의 m/z 319 [M-H]-에서 quassi molecular ion peak을 확인할 수 있었고, 여기에서 COOH가 탈리되면서 생성된 fragment ion이 m/z 275에서 나타므로 이 화합물에도 하나의 COOH가 존재하며, HMBC spectrum의 δH 6.36에서 나타나는 3번의 proton이 δC 113.07 (C-3), 156.93 (C-2) 및 164.18 (COOH)와 correlation하는 것을 확인할 수 있었으므로 COOH의 치환위치는 2번 임을 알 수 있었다. 이러한 사실과 문헌15),16)을 비교하여 화합물 5는 divaricatacid로 동정하였다. 본 연구에서 분리하고 구조를 동정한 화합물들의 활성에 관한 연구는 cimifugin (1)에 대해서는 활성연구가 활발하게 이루어져 인슐린 저항성억제작용,17) 아토피성 가려움증의 억제,18) 신경성 통증의 억제,19) 등 다양한 활성이 보고되었고, 5,7-Dihydroxy-4-oxo-4H-chromene-3-carboxylic acid (4)는 Liu 등13)이 이 화합물을 합성한 후 NO 생성 억제 활성에 관하여 보고하였다. Polymorpholide-1-O-glucoside (2), prim-O-glucosylangelicain (3) 및 divaricatacid (5)의 활성에 관한 연구는 보고되지 않은 것으로 확인하였다.
결 론
국내에 자생하고 있는 강활(Ostericum koreanum)의 모든 부위에 관한 성분을 밝히기 위한 계속되는 연구의 일부로 잎 추출물 중 n-BuOH 가용성 분획의 성분상을 알아 보기 위하여 연구에 착수하였으며, 각 종 chromatography를 실시하고 5종의 화합물을 분리하였으며, 이들에 대하여 NMR, MS 등의 분석법을 이용하여 그 구조를 cimifugin (1), polymorpholide-1-O-glucoside (2), prim-O-glucosylangelicain (3), 5,7-dihydroxy-4-oxo-4H-chromene-3-carboxylic acid (4) 및 divaricatacid (5)로 동정하였다. 이들 화합물 중 cimifugin (1)을 제외한 모든 화합물은 이 식물에서는 처음으로 분리된 것이었으며, 5,7-dihydroxy-4-oxo-4H-chromene-3-carboxylic acid (4)은 식물의 함유 성분으로는 처음으로 발견되는 것이었다. 특히 prim-O-glucosylangelicain (3)은 구조를 해석하는 과정 중에 선행 연구자들의 13C-NMR chemical shfts와 일치하지 않는 부분이 있어 이들을 수정하였다. 분리된 화합물들 중 cimifugin (1)을 제외한 화합물들은 활성에 관한 연구가 없는 실정이므로 이들의 활성 연구가 필요할 것으로 생각되며, carotane계 sesquiterpenoid인 polymorpholide-1-O-glucoside (2), chromone 모핵의 2번 위치에 carboxylic acid가 치환되어 있는 5,7-dihydroxy-4-oxo-4H-chromene-3-carboxylic acid (4)와 divaricatacid (5)도 식물에서 드물게 발견되는 성분으로 산형과(Umbelliferae)의 성분분류학을 위한 표준품으로도 사용할 수 있을 것으로 생각된다.
Acknowledgments
이 연구는 강원대학교 약학대학 전공심화연구 프로그램에 의해 수행되었으며, 핵자기공명분광기는 강원대학교 항암혁신신약개발 핵심연구지원센터(CFICDD, 과제번호: 2022R1A6C101A739)의 기술적 지원으로 수행되었으며 이에 감사드린다.
References
- 배기환 (2019) 천연약물도감, 886, 교학사, 서울.
- 이우철 (1996) 원색 한국기준식물도감, 260, 아카데미서적, 서울.
- Suk, K. D. (1976) Studies on the umbelliferous rhizoma and root(Ⅲ) The original plant of Korean qianghuo (Gangwhal), Kor. J. Pharmacogn. 7: 25-33.
-
Lee, B. Y., Kwak, M., Han, J.E., Jung, E.-H. and Nam, G.-H. (2013) Ganghwal is a new species, Angelica reflexa. J. Species Res. 2: 245–248.
[https://doi.org/10.12651/JSR.2013.2.2.245]

- Ko, J. H., Keum, J. H., Jung, J. W., Jhee, H. K., Hong, S. P., Kim, M. J., Chun, W. and Kwon, Y. (2020) Chemical constituents of Ostericum koreanum stem. Kor. J. Pharmacogn. 51: 158-162.
-
Lee, H. J., Lee, Y. J., Choi, S. G., Jang, H. S., Choi, S. Y., Kim, M. J., Chun, W., Yang, H. and Kwon, Y. (2023) A new chromone from Ostericum koreanum. Chem. Nat. Compd. 59: 259-261.
[https://doi.org/10.1007/s10600-023-03970-4]

-
Byeon, W. B., Kim, Y. J., Lim, H. J., Lee, S., Hwang, J. S., Kim, M. J. and Kwon, Y. (2024) Chemical constituents of Ostericum koreanum Maximowicz leaves, Kor. J. Pharmacogn. 55: 67-71.
[https://doi.org/10.22889/KJP.2024.55.2.67]

-
Ko, K., Wahyudi, L. D., Kwon, Y., Kim, J. H. and Yang, H. (2018) Nuclear factor erythroid 2-related factor 2 activating triterpenoid saponins from Camellia japonica roots. J. Nat. Prod. 81: 2399-2409.
[https://doi.org/10.1021/acs.jnatprod.8b00374]

-
Ye, Q., Qin, G. and Zhao, W. (1986) Immunomodulatory sesquiterpene glycosides from Dendrobium nobile. Phytochemistry 61: 885-890.
[https://doi.org/10.1016/S0031-9422(02)00484-3]

-
Choi, S. Y., Kim, M. J., Kim, S. H., Chun, W., Oh, K. and Kwon, Y. (2025) A new carotane sesquiterpene glycoside from the leaves of Angelica polymorpha. Chem. Nat. Compd. 61: 483-486.
[https://doi.org/10.1007/s10600-025-04683-6]

-
Kozawa, M., Matsuyama, Y., Fukumoto, M. and Baba, K. (1983) Chemical studies of Coelopleurum gmelinii (D. C.) LEDER. Ⅰ. Constituents of the root. Chem. Pharm. Bull. 31: 64-69.
[https://doi.org/10.1248/cpb.31.64]

-
Kobayashi, M., Tawara, T., Tsuchida, T. and Mitsuhashi, H. (1990) Studies on the constituents of Umbelliferae plants. ⅩⅧ. Minor constituents of Bupleuri Radix: occurrence of saikosaponis, polyhydrosterols, a trihydroxy C18 fatty acid, a lignan and a new chromone. Chem. Pharm. Bull. 38: 3169-3171.
[https://doi.org/10.1248/cpb.38.3169]

-
Liu, G. B., Xu, J. L., Geng, M., Xu, R., Hui, R. R., Zhao, J. W., Xu, Q., Xu, H. X. and Li, J. X. (2010) Synthesis of a novel series of diphenolic chromone derivatives as inhibitors of NO production in LPS-activated RAW264.7 macrophages. Bioorg. Med. Chem. 18: 2864-2871.
[https://doi.org/10.1016/j.bmc.2010.03.020]

-
Baba, K., Hata, K., Kimura, Y., Matsuyama, Y. and Kozawa, M. (1981) Chemical studies of Angelica japonica A. GRAY. Ⅰ. On the constituents of the ethyl acetate extract of the root. Chem. Pharm. Bull. 29: 2565-2570.
[https://doi.org/10.1248/cpb.29.2565]

-
Kang, J., Zhou, L., Sun, J. H., Ye, M., Han, J., Wang, B. R. and Guo, A. D. (2008) Three new compounds from the roots of Saposhnikovia divaricata. J. Asian Nat. Prod. Res. 10: 971-976.
[https://doi.org/10.1080/10286020802217556]

-
Kang, J., Sun, J. H., Zhou, L., Ye, M. Han, J., Wang, B. R. and Guo, A. D. (2008) Characterization of compounds from the roots of Saposhnikovia divaricata by high-perfromance liquid chromatography coupled with electrospray ionization tandem mass spectrometry. Rapid Commun. Mass Spectrom. 22: 1899-1911.
[https://doi.org/10.1002/rcm.3559]

-
Deng, X., Liu, Z. and Han, S. (2023) Cimifugin inhibits adipogenesis and TNF-α-induced insulin resistance in 3T3-L1 cells. Open Med. 18: 20230855.
[https://doi.org/10.1515/med-2023-0855]

-
Zheng, J., Gu, A., Kong, L., Lu, W., Xia, J., Hu, H. and Hong, M. (2024) Cimifugin relieves histamine-independent itch in atopic dermatitis via targeting the CQ receptor MrgprA3. ACS Omega 9: 7239-7248.
[https://doi.org/10.1021/acsomega.3c09697]