돌피 부탄올 분획물의 예쁜꼬마선충 내의 항산화 효과
Abstract
In the search for antioxidants among native plants in Korea, it was observed that n-butanol fraction of Echinochloa crus-galli (L.) Beauv. (Gramineae) methanol extract had a strong scavenging effect on DPPH radicals. In the expreiments using Caenorhabditis elegans model system, the n-butanol fraction of Echinochloa crus-gali (BEC) decreased reactive oxygen species (ROS) levels, increased the activity of superoxide dismutase (SOD), catalase, and increased oxidative stress resistance. In addition, we confirmed SOD-3 expression using the transgenic strain CF1553 to determine whether BEC-treated C. elegans produced resistant proteins against oxidative stress. As a result, BEC-treated CF1553 nematodes had higher SOD-3:GFP intensity than controls.
Keywords:
Echinochloa crus-galli, Caenorhabditis elegans, Antioxidant activity, SOD, Catalase ROS, SOD-3::GFP생체 내의 여러 대사과정 중 에너지 이용과 관련된 adenosine triphosphate (ATP)를 생성하는 대사경로는 미토콘드리아와 연결되어 있으며 활성산소종(reactive oxygen species, ROS)과 자유 라디칼이 생성된다.1-3) 일정량의 자유 라디칼이나 ROS는 세포의 생리적 환경을 보호하고 적절한 기능을 유지하는데 필요하나, 과도한 자유 라디칼이나 ROS의 축적은 산화 스트레스(oxidative stress)를 유발시켜 세포의 생존율을 떨어뜨리고 노화를 촉진하거나 장애, 다양한 질병을 초래할 수 있다.3,4) 산화 스트레스로 인해 나타나는 질병과 장애에는 심혈관 질환, 폐쇄성 폐질환, 만성 신장 질환, 퇴행성 신경 질환이나 암 등이 있고, 이들과 관련된 노화는 인체 조직과 장기의 기능이 점차 상실되는 것으로 ROS의 축적과 이로 인한 조직과 장기의 손상이나 변형이 초래됨으로 촉진될 수 있다.1,5) 인체는 이러한 다양한 내인성 및 외인성 과정을 통해 생성되는 자유 라디칼이나 ROS에 의해 유도된 산화 스트레스를 서로 다른 효소적 및 비효소적 항산화제(antioxidants)로 제거하여 세포, 조직 및 장기의 손상을 방지한다. 그러나 산화 스트레스가 오래 지속되면 인체 내의 항산화 효소의 활성이 감소하게 되고 이는 세포의 스트레스를 일으키고 다양한 병리학적 변화를 초래한다.1,5) 따라서 인체는 이러한 항산화 효소의 활성을 강화하고 ROS나 자유 라디칼을 효율적으로 제거할 수 있는 항산화제가 필요하게 되어 비타민 C나 E를 비롯하여 색소 성분이며 항산화 효능이 우수한 것으로 알려진 β-carotene 등을 이용하고 있으며, 그 외에 비교적 안전한 것으로 생각되는 천연물에서 공급되는 polyphenol성 항산화 물질들을 대상으로 임상에 적용하기 위한 연구가 꾸준히 이어지고 있는 실정이다.6,7)
돌피(Echinochloa crus-galli (L.) Beauv.는 벼과(Gramineae) 식물로 벼농사를 짓는 각 나라에서 쌀 생산을 위협하는 가장 심각한 잡초로 취급되고 있으며 한국에서도 전국에서 자생하며 약용식물로서의 효능은 보고되어 있지 않는 식물이다.8) 돌피 관련 연구는 주로 잡초로서 제거하여야 할 대상이므로 이와 관련된 연구들이 다수 보고되어 있다.9,10)
본 연구는 한국 내에 자생하는 식물에서 항노화와 관련된 항산화 활성 물질을 찾는 과정 중에 돌피의 돌피의 methanol 추출물을 극성에 따라 계통적 용매 분획물을 제조하였다. 분획물 중 DPPH radical 소거 활성이 가장 강한 n-butanol 분획을 예쁜꼬마선충(Caenorhabditis elegans) 내에 존재하는 항산화 효소인 catalase, SOD 활성 변화와 산화 스트레스에 대한 저항 능력을 측정하고 ROS 축적에 미치는 영향을 실험하였다.11) 또한, 산화 스트레스를 견디는 C. elegans 내의 저항단백질의 생성 여부를 측정할 수 있는 C. elegans mutant인 CF1553을 이용하여 활성을 측정하였으며 이를 통하여 몇 가지 지견을 얻었기에 이를 보고하고자 한다.
재료 및 방법
실험재료 − 실험에 사용한 돌피는 전북 완주군에서 채집하여 김대근 교수(우석대학교)가 검증한 후에 실험에 사용하였으며, 표준품은 우석대학교 약학과 생약표본실에 보관하고 있다(WS-24-005).
추출 및 분획 − 음건한 돌피 500 g을 methanol로 50℃에서 5시간씩 2회 추출하였다. 이 추출액을 50℃ 수욕상에서 감압농축하여 methanol 엑스를 얻었다(24.5 g). 이 methanol 추출물을 증류수로 현탁하여 n-hexane (7.0 g), methylene chloride (3.6 g), ethyl acetate (1.3 g) 및 n-butanol (1.5 g)로 분획하여 각각의 분획물을 확보하였다.
DPPH free radical 소거능 측정 − 농도별로 조제된 각 시료를 96 well plate에 분주한 후, 0.2 mM의 1,1-diphenyl-2-picrylhydrazyl (DPPH) ethanol 용액을 일정량씩 가하고 10초간 진탕한 후 25℃에서 30분간 반응시킨 다음 517 nm에서 microplate reader를 이용하여 흡광도를 측정하였으며, control로는 vitamin C를 사용하였다.12)
예쁜꼬마선충(Caenorhabditis elegans) 배양 − C. elagans는 20℃에서 E. coli OP50을도말한 Nematode Growth Medium (NGM) agar plate상에서 배양하였으며, 돌피 시료는 0.1% (v/v)의 DMSO에 용해한 후 NGM plate에서 배양하였다.13)
선충 체내의 SOD, catalase 효소 활성 측정 − 돌피 시료를 농도별로 조제한 plate에 선충을 배양하였으며, 성체가 된 2일째에 M9 buffer로 세척한 후 선충을 분쇄하고 각 효소의 활성을 측정하였다(buffer: 10 mM Tris-HCl, 150 mM NaCl, 0.1 mM EDTA, pH 7.5). SOD 활성은 pH 8.0의 10 mM phosphate buffer를 용매로 반응 혼합물(1.6 mM xanthine과 0.48 mM NBT 0.49 mL)을 제조한 후 시료 10 μL를 가한 뒤 37℃에서 5분간 pre-incubation시켰다. Xanthine oxidase 100 μL (0.05 U/mL)를 첨가한 후 37℃에서 20분 동안 incubation시키고 69 mM SDS로 반응을 멈춘 후 570 nm에서 흡광도를 측정하였다.14) Catalase 활성은 25 mM H2O2에 농도별로 제조된 돌피의 시료 50 μL씩을 3분 동안 반응시킨 후 240 nm에서 흡광도를 측정하였다.15)
선충 세포 내 활성 산소종(ROS) 분석 − 선충 세포 내의 ROS의양은 2',7'-dichlorodihydro fluorescein diacetate (H2DCF-DA)를 사용하여 측정하였고, 돌피 시료를 농도별로 첨가한 plate에 성장 단계가 같은 성체가 된 후 4일째되는 선충을 50 μM juglone을 함유한 M9 buffer에 넣은 후 2시간 동안 노출하고 M9 buffer가 50 μL씩 담긴 96 well plate에 3마리씩 옮겼다. 100 μM의 H2DCF-DA 50 μL를 첨가하고 여기 485 nm, 방출 535 nm에서 각각 흡광도를 측정하였다.16)
산화적 스트레스 저항성 측정 − 성체가 된 후 7일째인 선충을 산화적 스트레스를 유발제로 1 mM juglone이 함유된 M9 buffer 넣은 96 well plate에 분주하고 시간 별로 생존율을 확인하였다.17)
형질 전환 선충 내 SOD-3::GFP 형광 측정 − 형질 전환시킨 SOD-3::GFP 유전자를 가지고 있는 선충 CF1553을돌피 시료를 농도별로 투여된 배지에서 배양하였다. 성체가 된 후 3일째인 선충을 sodium azide (4%)로 마취시키고 발현된 GFP를 형광 실체 현미경(Olympus, Japan)을 이용하여 관찰하였으며, 발현강도의 정량분석은 현미경을 통한 사진과 ImageJ 소프트웨어를 사용하여 분석하였다.18)
통계 분석 − 통계 자료의 값은 평균값±표준오차(mean ± S.E.M.)로 나타냈으며, 그룹 간의 통계적 유의성은 Student's t-test를 통해서 분석하였고, 선충의 생존도는 Log-rank test 분석 방법을 이용하였다. p값은 *p<0.05, **p<0.01, ***p<0.001로 유의성을 나타내었다.
결 과
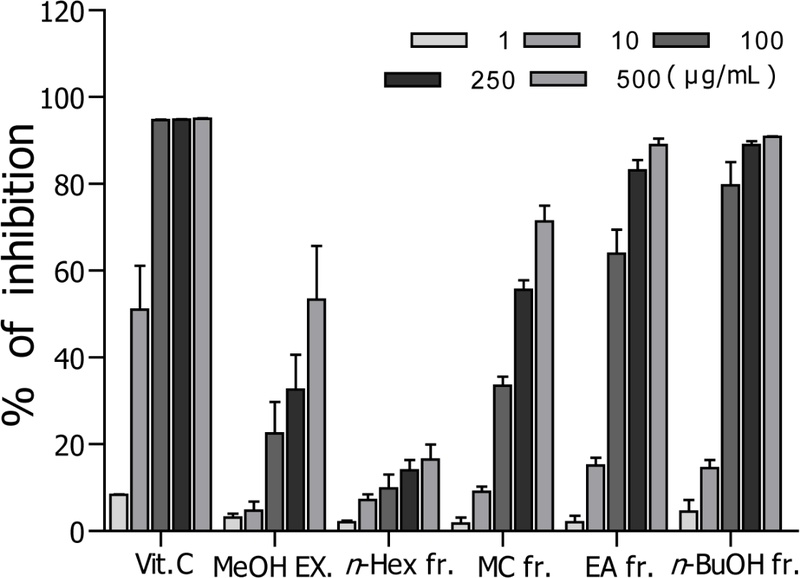
DPPH radical 소거 효과 − 돌피의 methanol 엑스와 이의 계통분획물의 DPPH radical 소거능은 Fig. 1에 나타난 바와 같이 n-butanol 분획물(BEC, IC50 value, 38.0 μg/mL)이 가장 좋은 radical 소거 효과를 보여 주었다(vitamin C, IC50 value, 9.5 μg/mL) (Fig. 1).
SOD, Catalase 효소 활성 증가 효과 – 돌피 BEC 분획물의 xanthine oxidase의 반응을 이용한 SOD의 활성을 측정한 결과 농도의존적으로 증가시켰다. 돌피 BEC 250 μg/mL, EACS 500 μg/mL 투여군은 대조군에 비해 SOD 활성을 각각 12.0% (**p<0.01), 24.2% (***p<0.001)를 증가시켰다. 활성산소종인 hydrogen peroxide를 대사와 관련된 catalase의 활성은 돌피 BEC 250 μg/mL, BEC 500 μg/mL 농도에서 대조군에 비해 각각 16.2% (**p<0.01), 58.4% (**p<0.01)를 증가시켰다(Fig. 2).
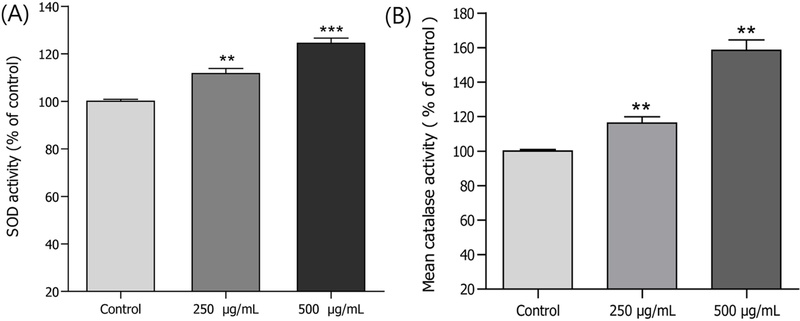
Effects of n-butanol fraction of the E. crus-galli on the antioxidant enzyme activity of wild-type N2 nematode. (A) The enzymatic reaction of xanthine with xanthine oxidase was used to generate •O2- and the SOD activity was estimated spectrophotometrically through formazan formation by NBT reduction. The SOD activity was showed as a percentage of superoxide-scavenged amount per control. (B) Catalase activity was calculated from the concentration of residual H2O2, as determined by a spectrophotometric method. The catalase activity was expressed in U/mg protein. Data are expressed as the mean ± S.E.M. of three independent experiments. Differences compared to the control were considered significant at **p<0.01 and ***p<0.001 by one-way ANOVA.
ROS 축적 감소 효과 – 돌피 BEC의 세포 내 ROS 축적 감소 효능은 H2DCF-DA와 선충 내의 ROS를 반응시켜 형성되는 형광을 관찰하며, 형광의 감소 효능은 대조군과 비교하여 돌피 BEC 250 μg/mL, 500 μg/mL 투여군에서 각각 14.2% (***p<0.001), 18.3% (***p<0.001)를 감소시키는 것으로 나타났다(Fig. 3).
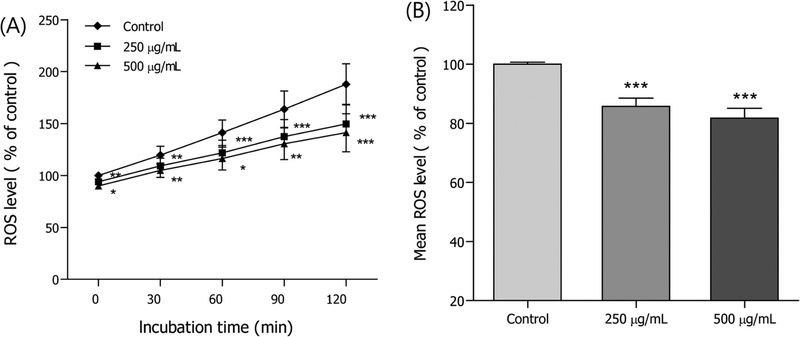
Effects of n-butanol fraction of the E. crus-galli on the intracellular ROS levels of wild-type N2 nematodes. Intracellular ROS accumulation was examined in a microplate fluorescence reader at 535 nm (emission) and 485 nm (excitation). (A) Plates were read for 120 min. (B) The average percentages of intracellular ROS accumulation were presented. Differences compared with the control were considered significant at *p<0.05, **p<0.01 and ***p<0.001 by the one-way ANOVA.
산화적 스트레스 저항성 증가 효능 – 돌피 BEC의 산화 스트레스에 미치는 효능 평가는 BEC를 처리하지 않은 대조군의 최고 생존시간은 28시간이었고, 돌피 BEC 250 μg/mL, 500 μg/mL 농도에서의 생존시간은 각각 36시간 및 43시간으로 증가시키는 것으로 관찰되었다. 대조군의 평균 생존 시간은 19.7±1.0시간인 반면, 250 μg/mL, 500 μg/mL 투여군은 각각 28.4±1.2시간(28.4%, ***p<0.001), 33.0±1.1시간(55.6%)의 생존시간의 향상을 보여주었다(*p<0.05)(Fig. 4, Table I).
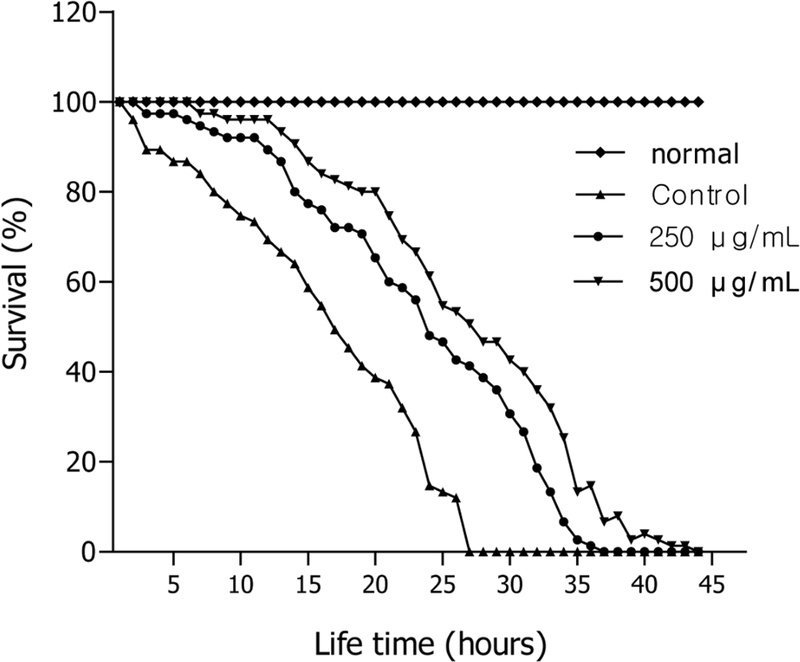
Effects of n-butanol fraction of the E. crus-galli on the stress tolerance of wild-type N2 nematodes. For the oxidative stress assays, worms were transferred to 96-well plate containing 1 mM of juglone liquid culture, and then their viability was scored. Statistical difference between the curves was analyzed by log-rank test.
형질 전환 선충 내 SOD-3의 발현 증가 효과 − 돌피BEC의 선충 내의 산화 스트레스에 대하여 이를 극복하기 위한 저항 백질의 생성 여부를 판별하기 위해 SOD-3을 포함한 C. elegans의 mutant인 CF1553을 사용하였다. CF1553에 돌피 BEC 250 μg/mL, 500 μg/mL 처리군이 대조군에 비해 각각 27.3% (**p<0.01), 42.5% (*p<0.05)로 SOD-3::GFP의 발현 증가효과를 보여 주었다(Fig. 5A, 5B).
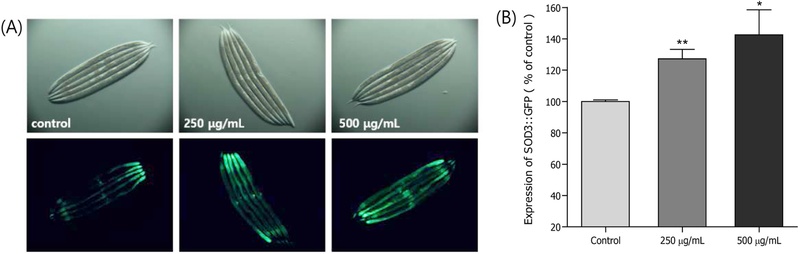
Effect of n-butanol fraction of the E. crus-galli on the expression of SOD-3 was determined using transgenic nematodes. (A) Images of SOD-3::GFP expression of CF1553 worm in the presence or absence of ethyl acetate fraction. (B) The mean GFP intensity of mutant was represented as mean ± S.E.M. of values from 19 to 25 animals per each experiment. The GFP intensity was quantified using Image software by determining average pixel intensity. Data are expressed as the mean ± standard deviation of three independent experiments. Differences compared with the control were considered significant at *p<0.05 and **p<0.01 by one-way ANOVA.
고 찰
예쁜꼬마선충(Caenorhabditis elegans)은 크기가 작고 투명한 몸체를 가지고 있으며 수명이 짧으면서도 생식능이 왕성하여 자손 생산량이 많고 배양조건이 비교적 간단하여 질병연구, 유전공학, 신경과학 등에 실험모델로 많이 활용되고 있다. 또한, C. elegans는 사람의 노화 관련 유전자와 유사한 부분이 많아 사람의 노화와 관련된 기초적인 연구를 시행하는데 도움이 되고 있으며, 천연물에서 항산화제, 항노화제 도출 연구에서 C. elegans의 mutant들을 이용하여 효능 확인 및 기전을 연구하는데 이용되고 있다.19) 본 연구는 C. elegans를 이용하여 국내 자생하는 돌피의 methanol 추출물의 분획물들 중 가장 강한 DPPH radical 소거활성을 나타낸 n-butanol 분획물(BEC)을 대상으로 C. elegans 내의 항산화 실험을 실시하였다. BEC는 선충 내의 SOD, catalase의 항산화 효소의 활성을 유의하게 높여주었고, 반면에 C. elegans 체내의 ROS 축적양을 농도 의존적으로 유의성 있게 억제하는 결과를 보여 주었다. 또한, juglone으로 유도한 산화 스트레스 연구에서는 BEC를 처리한 실험군에서 처리하지 않은 대조군에 비해 농도 의존적으로 생존율을 크게 증가시켜 산화 스트레스를 크게 억제하는 효능을 보여주었다. 산화 스트레스에 저항하는 저항 단백질 발현여부를 확인하는 연구에서는 C. elegans mutant인 CF1553 (GFP-fused transgenic strain CF1553)을 이용하였는데, 산화 스트레스를 주고 형광현미경으로 관찰하였을 때 mutant 내의 형광이 크게 증가되어 산화 스트레스에 저항하기 위한 저항 단백질이 상당량 생성되었음을 확인할 수 있었다.20)
세포 에너지인 ATP를 생성하기 위해 미토콘드리아 내에서 진행되는 산소의 산화 및 환원 과정에서 불완전한 부산물로 축적될 수 있는 것이 ROS이다. 낮은 수준의 ROS는 세포 생리학에서 중요한 조절 역할을 하나, 과도한 수준이나 부적절하게 국소적으로 축적된 ROS는 세포 성장을 억제하고 세포 분화나 신호 전달 등에 영향을 미치는 비정상적인 생리 상태를 초래하여 암, 당뇨병, 심장병, 신경 퇴행성 질환 등 노화와 관련된 각종 질병의 원인이 될 수 있기 때문에 미토콘드리아 내에서 생성되는 ROS는 신속히 제거할 필요가 있다.21,22)
BEC는 C. elegans 내의 catalase나 SOD의 효소활성을 유의성 있게 높여 주었고, 세포의 노화나 소멸의 원인이 되는 ROS의 농도를 낮추어 주었으며, 산화 스트레스에 대한 저항할 수 있는 단백질을 생산하여 C. elegans의 체내 항산화 능력을 향상시켜 수명연장에도 영향을 미칠 것으로 판단된다. 이러한 결과는 벼과 식물에 다량 존재하는 polyphenol 성분들이 돌피 BEC에도 함유되어 있을 것으로 생각되며 이러한 phenol성 화합물들이 선충의 항산화 및 항노화 활성에 영향을 미칠 것으로 판단된다.23,24) 추후에 돌피 BEC에서의 항산화나 항노화 활성을 나타내는 단일 물질을 확보하고 이들 물질에서의 항산화 기전에 대한 연구가 필요할 것으로 사료된다.
결 론
돌피의 n-butanol 분획물은 높은 DPPH free radical 소거 활성을 나타냈으며, C. elagans 내의 SOD 및 catalase를 농도 의존적으로 활성도를 높였다. ROS를 농도 의존적으로 감소시켰고, 산화 스트레스 조건에서도 C. elagans의 생존율을 증가시켰다. C. elagans의 mutant인 CF1553에 산화 스트레스를 가한 후 돌피의 n-butanol 분획물을 처리한 선충의 형광 발현율이 크게 상승되어 산화 스트레스에 저항할 수 있는 단백질의 증가가 확인되었다. 이러한 결과는 돌피의 n-butanol 분획물이 항산화 및 이와 관련된 수명연장 등과 관련된 질병의 예방 및 치료에 도움이 되는 자원이 될 수 있음을 의미한다.
References
-
Hajam, Y. A., Rani, R., Ganie, S. Y., Sheikh, T. A., Javaid, D., Qadri, S. S., Pramodh, S., Alsulimani, A., Alkhanani, M. F., Harakeh, S., Hussain, A., Haque, S. and Reshi, M. S. (2022) Oxidative stress in human pathology and aging: Molecular mechanisms and perspectives. Cells 11: 552.
[https://doi.org/10.3390/cells11030552]

-
Al-Suhaimi, E., AlQuwaie, R., AlSaqabi, R., Winarni, D., Dewi, F. R. P., AlRubaish, A. A., Shehzad, A. and Elaissari, A. (2024) Hormonal orchestra: mastering mitochondria's role in health and disease. Endocrine 86: 903-929.
[https://doi.org/10.1007/s12020-024-03967-1]

-
Halliwell, B. (2024) Understanding mechanisms of antioxidant action in health and disease. Nat. Rev. Mol. Cell Biol. 25: 13-33.
[https://doi.org/10.1038/s41580-023-00645-4]

-
Sahoo, B. M., Banik, B. K., Borah, P. and Jain, A. (2022) Reactive oxygen species (ROS): Key components in cancer therapies. Anticancer Agents Med. Chem. 22: 215-222.
[https://doi.org/10.2174/1871520621666210608095512]

-
Almalki, W. H. and Almujri, S. S. (2024) Aging, ROS, and cellular senescence: a trilogy in the progression of liver fibrosis. Biogerontology 26: 10.
[https://doi.org/10.1007/s10522-024-10153-3]

-
Liu, Z. Q. (2022) Why natural antioxidants are readily recognized by biological systems? 3D architecture plays a role! Food Chem. 380: 132143.
[https://doi.org/10.1016/j.foodchem.2022.132143]

-
Lourenço, S. C., Moldão-Martins, M. and Alves, V. D. (2019) Antioxidants of natural plant origins: from sources to food industry applications. Molecules 24: 4132.
[https://doi.org/10.3390/molecules24224132]

-
Wu, L., Wu, C., Yang, H., Yang, J., Wang, L. and Zhou, S. (2023) Proteomic analysis comparison on the ecological adaptability of quinclorac-resistant Echinochloa crus-galli. Plants (Basel)12: 696.
[https://doi.org/10.3390/plants12040696]

-
Cai, X., Chen, J., Wang, X., Gao, H., Xiang, B. and Dong, L. (2022) Mefenacet resistance in multiple herbicide-resistant Echinochloa crus-galli L. populations. Pestic. Biochem. Physiol. 182: 105038.
[https://doi.org/10.1016/j.pestbp.2022.105038]

-
Rigon, C. A. G., Cutti, L., Turra, G. M., Ferreira, E. Z., Menegaz, C., Schaidhauer, W., Dayan, F. E., Gaines, T. A. and Merotto, A. Jr. (2023) Recurrent selection of Echinochloa crus-galli with a herbicide mixture reduces progeny sensitivity. J. Agric. Food Chem. 71: 6871-6881.
[https://doi.org/10.1021/acs.jafc.3c00920]

-
Durán, B., A., Manzano, S., G., Sánchez, I., G.,Arribas, M., V., M., Bartolomé, B., Buenhombre, M., S.,Guadarrama, A., Buelga, C., S. and Paramás, A., M., G. (2019) Antioxidant characterization and biological effects of grape pomace extracts supplementation in Caenorhabditis elegans. Foods 75: 1-14.
[https://doi.org/10.3390/foods8020075]

-
Baliyan, S., Mukherjee, R., Priyadarshini, A., Vibhuti, A., Gupta, A., Pandey, R. P. and Chang, C. M. (2022) Determination of antioxidants by DPPH radical scavenging activity and quantitative phytochemical analysis of Ficus religiosa. Molecules 27: 1326.
[https://doi.org/10.3390/molecules27041326]

-
Roux, A. E., Langhans, K., Huynh, W. and Kenyon, C. (2016) Reversible age-related phenotypes induced during larval quiescence in C. elegans. Cell Metab. 23: 1113-1126.
[https://doi.org/10.1016/j.cmet.2016.05.024]

-
Mekheimer, R. A., Sayed, A. A. and Ahmed, E. A. (2012) Novel 1,2,4-triazolo[1,5-a]pyridines and their fused ring systems attenuate oxidative stress and prolong lifespan of Caenorhabditis elegans. J. Med. Chem. 55: 4169-4177.
[https://doi.org/10.1021/jm2014315]

-
Zhang, J., Chen, R., Yu, Z. and Xue, L. (2017) Superoxide dismutase (SOD) and catalase (CAT) activity assay protocols for Caenorhabditis elegans. Bio. Protoc. 7: e2505.
[https://doi.org/10.21769/BioProtoc.2505]

- Kim, H. N., Seo, H. W., Kim, B. S., Lim H. J., Lee, H, N., Park, J. S., Yoon, Y. J., Oh, J. W., Oh, M. J., Kwon, J., Oh, C. H., Cha, D. S. and Jeon, H. (2015) Lindera obtusiloba extends lifespan of Caenorhabditis elegans. Nat. Prod. Sci. 21: 128-133.
-
Hernández-Cruz, E. Y., Eugenio-Pérez, D., Ramírez-Magaña, K. J. and Pedraza-Chaverri, J. (2023) Effects of vegetal extracts and metabolites against oxidative stress and associated diseases: Studies in Caenorhabditis elegans. ACS Omega 8: 8936-8959.
[https://doi.org/10.1021/acsomega.2c07025]

-
Ahmad, T. and Suzuki, Y. J. (2019) Juglone in oxidative stress and cell signaling. Antioxidants (Basel)8: 91.
[https://doi.org/10.3390/antiox8040091]

-
Motta, H. S., Roos, D., Tabarelli, G., Rodrigues, O. E. D., Ávila, D. and Quines, C. B. (2020) Activation of SOD-3 is involved in the antioxidant effect of a new class of beta-arylchalcogenium azide compounds in Caenorhabditis elegans. An. Acad. Bras. Cienc. 92(suppl 2): e20181147.
[https://doi.org/10.1590/0001-3765202020181147]

-
Lin, Y., Lin, C., Cao, Y. and Chen, Y. (2023) Caenorhabditis elegans as an in vivo model for the identification of natural antioxidants with anti-aging actions. Biomed. Pharmacother. 167: 115594.
[https://doi.org/10.1016/j.biopha.2023.115594]

-
Waters, J. C. (2009) Accuracy and precision in quantitative fluorescence microscopy. J. Cell Biol. 185: 1135-1148.
[https://doi.org/10.1083/jcb.200903097]

-
Okoye, C. N., MacDonald-Jay, N. and Kamunde, C. (2019) Effects of bioenergetics, temperature and cadmium on livermitochondriareactive oxygen species production and consumption. Aquat. Toxicol. 214: 105264.
[https://doi.org/10.1016/j.aquatox.2019.105264]

-
Dilberger, B., Baumanns, S., Schmitt, F., Schmiedl, T., Hardt, M., Wenzel, U. and Eckert, G. P. (2019) Mitochondrial oxidative stress impairs energy metabolism and reduces stress resistance and longevity of C. elegans. Oxid. Med. Cell Longev. 2019: 6840540.
[https://doi.org/10.1155/2019/6840540]

-
Jin, H. M., Dang, B., Zhang, W. G., Zheng, W., C. and Yang, X. J. (2022) Polyphenoland anthocyanin composition and activity of hghland barley with different colors. Molecule 27: 3411.
[https://doi.org/10.3390/molecules27113411]

-
Zhang, W., Lan, Y., Dang, B., Zhang, J., Zheng, W., Du, Y., Yang, X. and Li, Z. (2023) Polyphenol profile and in vitro antioxidant and enzyme inhibitory activities of different solvent extracts of highland barley ban. Molecules 28: 1665.
[https://doi.org/10.3390/molecules28041665]