대추의 면역조절 효과: 분자적 기전 및 사이토카인 조절에 관한 종설
Abstract
Ziziphus jujuba (Z. jujuba) Mill. (Rhamnaceae), commonly known as jujube, has been used in traditional medicine systems including Traditional Chinese Medicine, Ayurveda, and Unani medicine for thousands of years. The fruit contains various bioactive compounds such as polysaccharides, triterpenoids, flavonoids, and saponins, which contribute to its diverse pharmacological activities. This review comprehensively summarizes the immunomodulatory effects of Z. jujuba and its bioactive constituents, with particular focus on molecular mechanisms and cytokine regulation. Z. jujuba exhibits bidirectional immunomodulatory properties: enhancing immune function in normal or immunosuppressed states while suppressing excessive inflammatory responses in pathological conditions. In macrophages, Z. jujuba extracts increase pro-inflammatory cytokine expression under normal conditions but inhibit lipopolysaccharide-induced inflammatory mediators. Polysaccharides from Z. jujuba promote splenocyte and lymphocyte proliferation and enhance spleen and thymus indices in vivo. The anti-inflammatory effects are mediated through suppression of NF-κB and MAPK pathways, accompanied by Nrf2/HO-1 pathway activation. Polysaccharides also modulate gut microbiota composition, influencing systemic immunity through the gut-immune axis. Z. jujuba regulates the expression of inflammatory cytokines including tumor necrosis factor (TNF)-α, interleukin (IL)-1β, and IL-6 across various disease models affecting the gastrointestinal, hepatic, nervous, musculoskeletal, and respiratory systems. These findings suggest that Z. jujuba and its constituents represent promising candidates for the development of immunomodulatory agents with therapeutic potential in inflammatory and immune-related disorders.
Keywords:
Ziziphus jujuba, Immunomodulation, Cytokine, NF-κB, Polysaccharide면역계는 외부 병원체로부터 생체를 방어하고 내부 항상성을 유지하는 데 핵심적인 역할을 수행한다. 면역 기능의 불균형은 자가면역질환, 만성 염증성 질환, 감염 및 종양 등 다양한 병리적 상태와 연관되어 있으며, 이에 따라 부작용이 적고 효능이 우수한 천연물 유래 면역조절제에 대한 연구가 활발히 진행되고 있다.
대추(Ziziphus jujuba (Z. jujuba) Mill.)는 갈매나무과(Rhamnaceae)에 속하는 식물로서, 그 식품적 가치와 약용적 중요성으로 널리 알려져 있다.1) 본 식물은 아시아, 아메리카의 열대 및 아열대 기후 지역과 지중해 연안에 분포하며,2) 중국에서는 수천 년의 재배 역사와 함께 약 700여 품종이 존재한다.3) Z. jujuba의 전통적 사용은 약 2,500년 전 중국 본초서(Materia Medica)에 기록된 이래 오랜 역사를 가지고 있으며,1) 아유르베다(Ayurveda), 중의학, 유나니 의학(Unani medicine) 등 다양한 전통의학 체계에서 활용되어 왔다.4) 전통의학에서 Z. jujuba는 당뇨, 설사, 피부 감염, 간 질환, 비뇨기 장애, 비만, 발열, 인후염, 기관지염, 빈혈, 불면증 등 다양한 질환의 치료에 사용되었다.2) 또한 Z. jujuba의 과실, 잎, 수피 등 다양한 부위가 수천 년간 전통의학에서 사용되어 왔으며, 면역자극, 항암, 항염증, 간보호, 항비만, 항궤양 등의 약리활성이 보고되어 있다.5)
Z. jujuba의 주요 재배 품종으로는 가장 오래된 재배 역사와 최대 재배 면적을 가진 회조(Z. jujuba cv. Huizao),6) 신장 지역의 대표적 건조용 품종인 Z. jujuba cv. Junzao,7) 황하 유역에서 재배되는 무조(Z. jujuba cv. Muzao),8) 그리고 다당류 연구에 활용되는 금사소조(Z. jujuba cv. Jinsixiaozao) 9) 및 참조 게놈 품종인 Z. jujuba cv. Dongzao 10) 등이 있다(Table I). 한편, Z. jujuba의 야생종인 산조인(Z. jujuba Mill. var. spinosa (Bunge) Hu ex H. F. Chou)은 중국 북부 지역에 주로 분포하며,11) 그 종자는 동아시아 전통의학에서 진정 및 수면 작용을 목적으로 사용되어 왔다.12) 본 종설에서는 재배종 대추(Z. jujuba Mill.) 및 그 품종을 대상으로 한 연구에 초점을 맞추며, 산조인에 관한 연구는 범위에서 제외하였다.
Z. jujuba 과실은 영양학적으로 풍부한 식품으로서, 탄수화물이 55-85%로 주요 구성 성분을 이루며, 수분 25-30%, 조단백질 2.9-6.6%, 조섬유 2.4-8.4%, 조지방 0.4-1.0%를 함유하고 있다.8) 주요 생리활성 성분으로는 비타민 C (vitamin C), 페놀산(phenolic acid), 플라보노이드(flavonoid), 트리테르펜산(triterpenic acid), 다당류(polysaccharide), 사포닌(saponin), 환상 뉴클레오티드(cyclic nucleotide) 등이 보고되어 있다.8,13) 중국 황토고원 지역에서 재배된 5개 품종의 Z. jujuba를 분석한 연구에서, 총 폴리페놀(polyphenol) 함량은 428.5-600.4 mg 갈릭산 등가량(gallic acid equivalents; GAE)/100 g 신선중량(fresh weight; FW), 총 플라보노이드 함량은 159.3-230.3 mg/100 g FW로 보고되었다.14) 품종 및 숙성 단계에 따른 생리활성 성분 함량의 변이가 크며, Cosmulescu 등은 숙성 단계에 따라 총 폴리페놀 함량이 472.38-1634.44 mg GAE/100 g 범위로 나타남을 보고하였다.15)
Z. jujuba의 약리학적 효과에 관한 현대 연구에서는 항산화, 항염증, 간보호, 신경보호, 항불안, 혈당강하, 면역조절, 창상치유 및 항균 효과 등이 보고되어 있다.16) 특히 Z. jujuba 다당류의 수용성 분획 중 펙틴(pectin) 함량이 높은 ZSP3 분획은 49%의 에스테르화도(degree of esterification)를 나타내며 잠재적 면역반응 유도 효과가 보고되었다.17)
본 종설에서는 Z. jujuba의 면역조절 효과에 관한 국내외 연구를 종합적으로 고찰하고, 특히 분자적 기전 및 사이토카인(cytokine) 조절 작용에 초점을 맞추어 최신 연구 동향을 정리하고자 한다.
대추의 주요 면역활성 성분
다당류 – 다당류는 여러 개의 단당류가 글리코시드(glycoside) 결합으로 연결된 고분자 화합물로, Z. jujuba 과실의 주요 생리활성 성분 중 하나이다. Z. jujuba 과실 내 다당류 함량은 약 7.9%로 보고되어 있으며, 산지에 따라 1.31%에서 2.22% 범위의 차이를 보인다.18)
Z. jujuba 다당류의 분자량은 분획 및 정제 조건에 따라 넓은 범위를 나타낸다. 무조(Z. jujuba cv. Muzao) 품종에서 분리된 산성 다당류 분획인 PZMP4는 27.90 kDa의 분자량을 나타내었으며, 람노스(rhamnose), 아라비노스(arabinose), 만노스(mannose), 글루코스(glucose), 갈락토스(galactose), 갈락투론산(galacturonic acid)이 2.32:2.21:0.22:0.88:2.08:8.83의 몰비로 구성되어 있다.8) 동일 품종에서 분리된 고분자량 분획 PZMP3-1은 241 kDa의 평균 분자량을 나타내었다.8) Z. jujuba cv. Jinsixiaozao에서 분리된 Ju-B-7 분획은 2000 kDa 이상의 분자량을 보였으며, 갈락투론산과 람노스가 8.1:1의 몰비로 확인되었다.19) 8개 산지의 Z. jujuba 과실 다당류를 분석한 연구에서는 분자량 분포가 1.14×105 에서 1.73×106 Da 범위로 확인되었으며, 갈락투론산, 글루코스, 아라비노스가 주요 단당류로 나타났다.18)
Z. jujuba 다당류는 다양한 단당류로 구성된 이종다당류이다. Z. jujuba cv. Jinsixiaozao 품종에서 추출한 다당류는 람노스, 아라비노스, 자일로스(xylose), 만노스, 글루코스, 갈락토스로 구성된 전형적인 이종다당류로 보고되었다.9) Z. jujuba 다당류의 기본 골격은 주로 (1→4)-연결된 갈락투론산(galactopyranosyluronic acid; GalpA)으로 구성되며, O-3 위치에서 (1→3)-연결된 아라비노푸라노스(arabinofuranose; Araf), (1→2)-연결된 람노피라노스(rhamnopyranose; Rhap) 분지가 결합하고 갈락투론산으로 말단이 종결되는 구조를 나타낸다.8)Z. jujuba cv. Muzao 다당류의 다양한 분획을 체계적으로 비교 분석한 연구에서, 대부분의 분획이 펙틴 다당류(pectic polysaccharide) 특성을 나타내는 것으로 확인되었다.20) ZJP-I 분획의 경우 T-d-Galp(1→, →4)-d-Glcp(1→, →3,6)-d-Glcp(1→, →6)-d-Galp(1→, →6)-d-Manp(1→의 당 잔기로 구성되어 있으며, 분자량은 2.01×104 Da로 보고되었다.21)
트리테르페노이드 – 트리테르페노이드는 Z. jujuba의 주요 기능성 성분 중 하나로, 유리 산 형태 또는 트리테르페노이드 사포닌의 비당체(aglycone) 형태로 존재한다.14) Z. jujuba 과실에서 총 트리테르페노이드 함량은 최적 추출 조건에서 19.21 ± 0.25 mg/g으로 보고되었다.22)
Z. jujuba에서 현재까지 120종 이상의 트리테르페노이드가 동정되었으며, 이들은 비당체, 에스테르(ester), 에테르(ether), 배당체(glycoside) 형태로 존재한다.23) Z. jujuba 과실에서 베툴린산(betulinic acid), 알피톨산(alphitolic acid), 마슬린산(maslinic acid), 올레아놀산(oleanolic acid), 우르솔산(ursolic acid)이 주요 트리테르페노이드산으로 확인되었다.22) Guo 등은 건조 Z. jujuba 과실에서 세아노트산(ceanothic acid), 알피톨산, 지지베라날산(zizyberanal acid), 지지베라날산(zizyberanalic acid), 에피세아노트산(epiceanothic acid), 세아노텐산(ceanothenic acid), 베툴린산, 올레아놀산, 우르손산(ursonic acid), 지지베레날산(zizyberenalic acid) 등 10종의 트리테르페노이드산을 동시 정량하였다.14) Bai 등은 Z. jujuba 과실에서 3-O-(trans-p-coumaroyl)-alphitolic acid, 3-O-(cis-p-coumaroyl)-alphitolic acid, 3β-O-(trans-p-coumaroyl)-maslinic acid, 포모닉산(pomonic acid), 벤타믹산(benthamic acid), 터미닉산(terminic acid), 베툴린산 등 9종의 트리테르페노이드를 분리하였다.24)
Z. jujuba 트리테르페노이드는 골격 구조에 따라 루판형(lupane-type), 올레아난형(oleanane-type), 우르산형(ursane-type), 세아노탄형(ceanothane-type)으로 분류된다.25) 트리테르페노이드의 측쇄 구조는 산화, 환원, 수산화 반응을 받기 쉬워 구조적 다양성을 나타내며, 이러한 구조적 다양성은 다양한 약리활성과 연관된다.26) 루판형 트리테르페노이드 중 베툴린산은 식물계에서 가장 풍부한 루판형 트리테르페노이드 중 하나로, 항염증, 항바이러스, 항종양 활성 등 다양한 생물학적 활성이 보고되어 있다.27)
플라보노이드 – 플라보노이드는 페놀산과 함께 Z. jujuba 과실의 주요 2차 대사산물로서, 항산화, 항노화, 진정 및 수면 유도, 혈압 강하, 간 및 심혈관계 보호 등 다양한 생리활성에 기여하는 것으로 보고되어 있다.28) Xue 등은 20개 우수 Z. jujuba 품종을 대상으로 초고성능 액체크로마토그래피(ultra-high-performance liquid chromatography; UHPLC)를 이용한 체계적 분석을 수행하여 과실에서 12종의 페놀산 및 플라보노이드를 검출하였으며, (+)-카테킨(catechin), 에피카테킨(epicatechin), 루틴(rutin)이 과실의 주요 조성으로 확인되었고, 20개 품종 전체에서 (+)-카테킨이 가장 풍부하며 에피카테킨, 루틴, 퀘르세틴(quercetin) 순으로 함유되어 있었다.28) Shi 등은 고성능 액체크로마토그래피(high-performance liquid chromatography; HPLC)를 이용하여 Z. jujuba 과실에서 19종의 페놀 화합물을 정량하였으며, 플라바놀(flavanol)류로 프로시아니딘(procyanidin) B1, B2, B3, (-)-에피카테킨, (+)-카테킨의 5종을, 플라보놀(flavonol)류로 퀘르세틴-3-갈락토시드(quercetin-3-galactoside), 퀘르세틴-3-글루코시드(quercitrin-3-glucoside), 퀘르세틴-3-루티노시드(quercetin-3-rutinoside), 퀘르세틴-3-람노시드(quercetin-3-rhamnoside), 퀘르세틴의 5종을 동정하였다.29)
총 플라보노이드 함량은 품종에 따라 변이가 크다. Cosmulescu 등은 두 Z. jujuba 품종의 4단계 숙성 과정에서 총 플라보노이드 함량이 19.9-48.5 mg quercetin equivalents (QE)/100 g 범위임을 보고하였다.15) 과실의 성숙 과정에서 플라보노이드 함량은 감소하는 경향을 보이며, Yan 등은 8개 Z. jujuba 품종의 발달 단계에 따른 성분 변화를 분석한 결과, 카테킨, 에피카테킨, 프로안토시아니딘(proanthocyanidin), 루틴 함량이 성숙 과정에서 감소함을 확인하였다.30) Cosmulescu 등도 숙성 단계가 Z. jujuba 과실의 생리활성 화합물 및 항산화 활성에 유의한 영향을 미치며, 백숙기(white maturity)에서 가장 높은 항산화 활성이 나타남을 보고하였다.15)
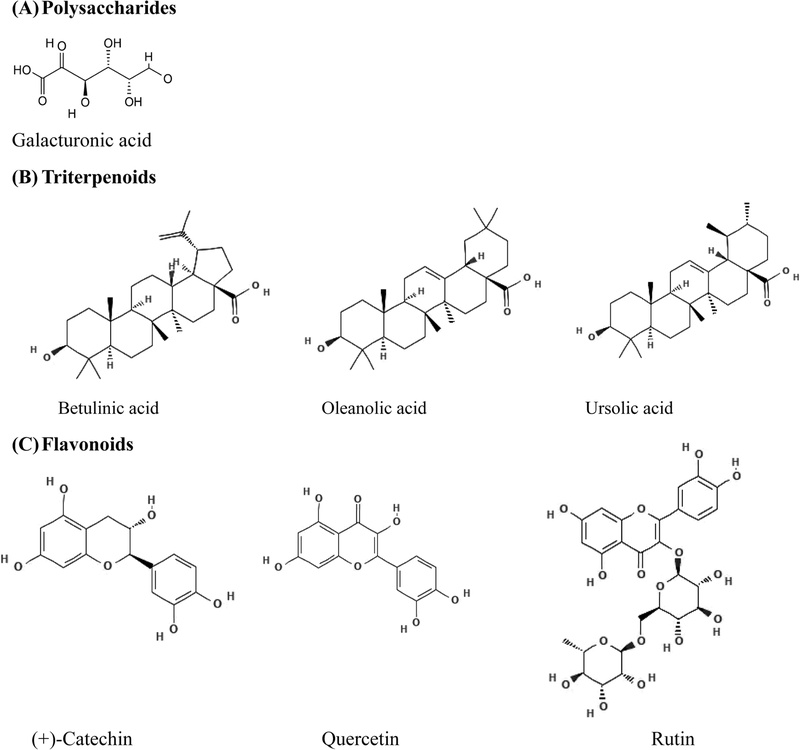
사포닌 – 사포닌은 트리테르펜 또는 스테로이드 비당체에 당 사슬이 결합한 배당체 화합물이다. Z. jujuba에서 트리테르펜산은 유리 산 형태 또는 트리테르펜 사포닌의 배당체 형태로 존재하며, Z. jujuba 식물의 가장 특징적인 활성 성분 중 하나로 알려져 있다.25) Z. jujuba 과실의 메탄올 추출물에서 사포닌을 분리하여 구조를 분석한 결과, jujubogenin을 비당체로 하고 람노스 및 글루코스가 글리코시드 결합된 배당체 구조가 확인되었다.31) Z. jujuba 과실로부터 트리테르펜 사포닌을 추출하기 위해서는 40% 에탄올이 적합한 용매로 보고되었다.32) 분리된 사포닌은 in vivo 실험에서 카라기난(carrageenan) 유도 족부종 모델에서 유의한 항염증 활성을 나타내었으며, 위궤양 모델에서 항궤양 효과와 함께 암세포주에 대한 중등도의 세포독성도 관찰되었다.31) 대추의 면역 활성 성분들의 화학적 특성을 Table II에 정리하였고, 주요 화학 구조를 Fig. 1에 나타내었다.
면역세포 활성화 효과
대식세포(macrophage) 활성화 – 앞서 기술한 다당류, 트리테르페노이드, 플라보노이드 등의 면역활성 성분들은 다양한 면역세포에 작용하여 그 기능을 조절한다. 대식세포는 선천면역계의 핵심 세포로서 병원체 인식, 식균작용, 사이토카인 분비를 통해 면역반응을 개시하고 조절한다. Z. jujuba 추출물은 대식세포에서 면역자극 및 항염증 효과를 동시에 나타내는 양방향 면역조절(bidirectional immunomodulatory) 활성이 보고되었다.33)
정상 상태의 RAW 264.7 세포에 Z. jujuba 물 추출물을 0-3 mg/ml 농도로 24시간 처리한 결과, 염증성 사이토카인인 인터루킨(interleukin; IL)-1β, IL-6, 종양괴사인자-알파(tumor necrosis factor-alpha; TNF-α)의 전사 발현이 농도 의존적으로 증가하였으며, 최대 효과는 각각 약 7배, 9배, 4배에 달하였다.34) 이러한 사이토카인 발현 증가는 대식세포의 면역감시 기능 강화를 시사한다. 아울러, Z. jujuba 추출물은 항산화 반응 요소(antioxidant response element; ARE) 매개 전사활성을 약 2배 상승시켜 대식세포의 항산화 방어 기전을 강화하는 것으로 확인되었다.35)
한편, 지질다당류(lipopolysaccharide; LPS)로 활성화된 염증 상태의 대식세포에서는 Z. jujuba 추출물이 상반된 효과를 나타내었다. Z. jujuba 물 추출물 전처리는 LPS 유도 IL-1β 및 IL-6의 mRNA와 단백질 발현을 유의하게 억제하였으나, TNF-α에 대해서는 억제 효과가 관찰되지 않았다.34) 이러한 항염증 효과는 핵인자-카파B (nuclear factor-kappa B; NF-κB) 전사활성의 억제와 병행하여 나타났다. 생체 내 연구에서도 Z. jujuba의 항염증 효과가 확인되었는데, 랫트(rat)에서 Z. jujuba 함수 알코올 추출물은 카라기난 유도 급성 족부종과 면봉 펠렛(pellet) 유도 만성 육아종을 용량 의존적으로 감소시켰으며, 혈청 아질산염(nitrite)/질산염(nitrate) 수준의 저하를 통해 일산화질소(nitric oxide; NO) 발현 억제가 기전으로 제시되었다.36) 유사하게, Z. jujuba 에탄올 추출물은 카라기난 유도 족부종을 유의하게 억제하고 혈청 C-반응단백질(C-reactive protein; CRP) 수준을 감소시켰다.16)
효소 처리를 통해 생리활성이 강화된 Z. jujuba 추출물에서도 항염증 효과가 보고되었다. 비스코자임(viscozyme) 처리 Z. jujuba 추출물은 RAW 264.7 세포에서 NO 및 염증성 사이토카인 생성을 감소시켰으며, 벤조(a)피렌(benzo(a)pyrene) 유도 마우스 폐 염증 모델에서 NF-κB, 유도성 산화질소 합성효소(inducible nitric oxide synthase; iNOS), 사이클로옥시제네이스(cyclooxygenase; COX)-2 단백질 발현을 억제하였다.37) 이상의 결과들은 Z. jujuba가 정상 상태에서는 대식세포를 활성화하여 면역기능을 강화하고, 염증 상태에서는 과도한 염증반응을 억제하는 양방향 면역조절 특성을 가짐을 입증한다.
비장세포(splenocytes) 및 림프구(lymphocytes) 증식 – 앞서 기술한 대식세포의 활성화는 선천면역반응의 핵심 요소로서, 이들 세포는 항원을 처리하고 T 림프구에 제시함으로써 적응면역반응을 개시하는 중요한 역할을 수행한다. 비장(spleen)은 이러한 면역반응이 조직적으로 이루어지는 이차 림프기관으로서, 림프구의 성숙, 분화 및 활성화가 진행되는 핵심 장소이다. 따라서 비장세포 및 림프구의 증식 능력은 면역기능 평가의 주요 지표로 활용된다.38,39)
Z. jujuba 다당류의 림프구 증식 촉진 효과는 다양한 in vitro 연구를 통해 확인되었다. Z. jujuba cv. Jinsixiaozao 품종의 과실에서 분리된 펙틴성 다당류 Ju-B-7은 분자량 2,000 kDa 이상의 고분자로서, 갈락투론산과 람노스가 8.1:1의 몰비로 구성된 폴리갈락투로난(polygalacturonic acid) 유형이다.40) 이 다당류를 랫트 비장세포에 10 μg/mL 농도로 처리한 결과 비장세포 증식이 유의하게 촉진되었다(P<0.01).40) 유사하게, Z. jujuba 다당류(10-100 μg/mL)를 림프구에 3일간 처리한 연구에서도 세포 부피 확대 및 세포 수 증가가 관찰되어 림프구 증식에 대한 직접적 효과가 확인되었다.33)
In vivo 연구에서는 Z. jujuba 다당류가 면역장기 발달을 촉진함이 보고되었다. 회조(Z. jujuba cv. Huizao) 품종에서 추출한 두 종의 산성 다당류 HP1 및 HP2를 마우스에 50, 100, 200 mg/kg 용량으로 7일간 경구 투여한 결과, 비장 지수 및 흉선 지수가 대조군 대비 유의하게 증가하였다(P<0.05).41) 흥미롭게도 HP2는 HP1에 비해 더 일관되고 강력한 면역조절 효과를 나타내었으며, 이러한 차이는 HP2의 높은 우론산(uronic acid) 함량(35.9% vs. 7.32%)과 분자량(111 kDa vs. 68.7 kDa)에 기인하는 것으로 제시되었다.41) 이는 Z. jujuba 다당류의 면역활성이 화학적 특성, 특히 산성 단당류 함량 및 분자량과 밀접하게 연관됨을 시사한다.
종합하면, Z. jujuba 유래 다당류는 in vitro에서 비장세포 및 림프구의 증식을 직접 촉진하고, in vivo에서 비장 및 흉선의 발달을 증진함으로써 적응면역반응의 세포적 기반을 강화하는 것으로 평가된다. 대추 및 유래 성분의 면역조절 효과에 관한 주요 연구들을 Table III에 요약하였다.
사이토카인 조절 효과
사이토카인은 면역세포 간 신호전달을 매개하는 저분자량 단백질로서, 염증 반응의 개시, 진행 및 해소 과정에서 중추적 역할을 수행한다. 사이토카인은 기능에 따라 염증성 매개체와 항염증성 매개체로 분류되며,42) 염증성 사이토카인으로는 TNF-α, IL-1β, IL-6 등이, 항염증성 사이토카인으로는 IL-10, IL-4 등이 대표적이다.43) 이들 사이토카인 간의 균형은 면역항상성 유지에 필수적이며, 불균형 시 만성 염증성 질환, 자가면역 질환 등 다양한 병리적 상태가 초래될 수 있다.44) Z. jujuba 및 그 유래 성분은 면역 상태에 따라 사이토카인 발현을 상반되게 조절하는 양방향 면역조절 특성을 나타낸다.
In vitro 연구에서 Z. jujuba 물 추출물은 RAW 264.7 대식세포의 활성화 상태에 따라 상이한 사이토카인 조절 효과를 나타내었다. 정상 상태의 대식세포에 화학적으로 표준화된 Z. jujuba 물 추출물(0-3 mg/mL)을 24시간 처리하였을 때, IL-1β, IL-6 및 TNF-α의 전사 발현이 농도의존적으로 증가하여 최대 약 7배, 9배 및 4배에 달하였다.34) 반면, LPS로 자극된 염증 상태의 대식세포에서는 Z. jujuba 추출물 전처리가 IL-1β 및 IL-6의 mRNA 및 단백질 발현을 억제하였다.34) 흑화처리된 Z. jujuba (blackened jujube) 유래 산성 다당류 BJP-4 역시 LPS 자극 RAW 264.7 세포에서 NO, IL-6, IL-1β 및 TNF-α의 과분비를 하향 조절하였다.45) 이러한 결과는 Z. jujuba가 정상 면역 상태에서는 면역세포를 활성화하여 병원체 방어 능력을 강화하고, 과도한 염증 상태에서는 염증 반응을 억제하여 조직 손상을 방지하는 양방향 조절 기능을 가짐을 시사한다.
이러한 in vitro 결과는 다양한 동물 모델에서도 확인되었다. 먼저, 면역억제 상태에서 Z. jujuba는 저하된 사이토카인 생성을 회복시켰다. 사이클로포스파마이드(cyclophosphamide) 처리로 면역이 억제된 ICR 마우스(Institute of Cancer Research mouse)에 Z. jujuba cv. Pozao 유래 다당류(JP)를 28일간 경구투여하였을 때, 혈청 IL-2, IL-4, IL-10, 인터페론-감마(interferon-gamma; IFN-γ) 및 TNF-α 수준이 유의하게 증가하였다.46) 이는 Z. jujuba 다당류가 면역억제 상태에서 도움 T세포(T helper cell; Th) 1 및 Th2 관련 사이토카인 생성을 모두 촉진하여 면역 기능을 회복시킴을 시사한다.
반면, 염증 유발 모델에서는 Z. jujuba가 과도하게 상승된 염증성 사이토카인을 억제하였으며, 이러한 효과는 다양한 조직 및 장기에서 관찰되었다. 소화기계에서, dextran sulfate sodium (DSS) 유도 대장염 마우스에 Z. jujuba 70% 에탄올 추출물을 투여하였을 때 혈청 TNF-α 및 IL-6가 하향 조절되었다.43) 아세트산(acetic acid) 유도 궤양성 대장염 마우스 모델에서도 Z. jujuba 함수 알코올 추출물은 myeloperoxidase (MPO), NO, IL-1β, IL-6 및 TNF-α 생성을 유의하게 감소시키고 iNOS 및 COX-2 유전자 발현을 하향 조절하였다.47) 간 조직에서, carbon tetrachloride (CCl4) 유도 급성 간손상 랫트에 Z. jujuba 근피 추출물을 투여한 결과, 상승된 TNF-α 및 IL-1β 수준이 억제되고 감소된 항염증성 사이토카인 IL-10 수준이 회복되었다.48)
신경계에서도 Z. jujuba의 사이토카인 조절 효과가 확인되었다. D-갈락토스 유도 기억손상 랫트 모델에서 Z. jujuba 물 추출물(41.5, 83, 166 mg/kg)을 14일간 경구투여한 결과, 전전두엽피질에서 TNF-α, IL-1β, IL-6 및 IFN-γ의 과발현이 유의하게 감소하였으며, 이는 신경세포 손실 감소와 연관되었다.49) Streptozotocin (STZ) 유도 당뇨병성 신경병증 랫트에서 Z. jujuba 근피 추출물의 메탄올 분획(ZJME) 및 물 분획(ZJWF)은 좌골신경의 산화 스트레스 및 염증성 사이토카인 분비를 정상화시켰다.50) 근골격계에서, monosodium iodoacetate (MIA) 유도 골관절염 마우스에 Z. jujuba 함수 알코올 추출물(250, 500 mg/kg)을 21일간 경구투여한 결과, 상승된 혈장 IL-1β, IL-6 및 TNF-α 수준이 유의하게 감소하였다.51) 호흡기계에서, LPS 유도 급성 폐손상 마우스 모델에서 Z. jujuba 추출물(100, 200 mg/kg) 투여는 폐 조직으로의 호중구 침윤을 감소시키고 TNF-α 수준을 유의하게 억제하였다.52) 또한, 카라기난 유도 급성 염증 랫트 모델에서 Z. jujuba 과실 추출물은 혈청 아질산염/질산염 수준을 감소시켜 NO 매개 염증 반응 억제 효과를 나타내었다.36)
종합하면, Z. jujuba는 면역억제 상태에서는 Th1/Th2 관련 사이토카인 생성을 촉진하여 면역 기능을 회복시키고, 염증 상태에서는 소화기계, 간, 신경계, 근골격계, 호흡기계 등 다양한 조직에서 과도한 염증성 사이토카인(TNF-α, IL-1β, IL-6)을 억제하며 항염증성 사이토카인(IL-10)을 회복시키는 양방향 면역조절 특성을 나타낸다. 이러한 사이토카인 수준의 조절은 특정 세포 내 신호전달 경로의 활성화 또는 억제를 통해 매개되며, 관련 분자적 기전은 다음 장에서 상세히 논의한다.
분자적 기전 및 신호전달 경로
NF-κB 경로 – NF-κB는 면역반응 및 염증조절에 핵심적인 역할을 수행하는 전사인자이다. 휴지 상태의 세포에서 NF-κB는 세포질 내 inhibitor kappa B alpha (IκBα)와 결합하여 비활성 상태로 존재한다. 톨 유사 수용체(Toll-like receptor; TLR)-4가 LPS와 같은 외인성 자극을 인식하면 IκBα가 인산화 및 분해되어 NF-κB로부터 해리되고, 활성화된 NF-κB p65 아단위는 핵 내로 전위하여 COX-2 및 iNOS를 포함한 염증 관련 효소의 발현을 유도한다.45) 앞서 기술한 바와 같이 Z. jujuba는 염증 환경에서 TNF-α, IL-1β, IL-6 등 염증성 사이토카인의 생성을 억제하는데, 이러한 효과의 분자적 기전으로 NF-κB 신호전달 경로 억제가 주목받고 있다.
In vitro 연구에서 Z. jujuba 추출물 및 유래 성분의 NF-κB 경로 억제 효과가 보고되었다. Z. jujuba 잎 에탄올 추출물은 LPS로 자극된 RAW264.7 대식세포에서 NF-κB 및 유사분열 자극 단백질 키나아제(mitogen-activated protein kinase; MAPK) 신호전달 경로 활성을 억제하여 NO, iNOS, COX-2 및 TNF-α의 발현을 감소시켰다.53) Z. jujuba뿌리에서 분리된 ceanothane형 트리테르페노이드인 3-dehydroxyceanothetric acid 2-methyl ester는 시스플라틴(cisplatin)으로 유도된 LLC-PK1 신장 상피세포 손상 모델에서 IκB kinase α/β (IKKα/β) 및 IκBα의 발현 증가를 억제하고 NF-κB p65 단백질 수준을 감소시켰으며, 하위 염증 매개 효소인 iNOS 및 COX-2의 발현도 억제하였다.54) 흑화처리된 Z. jujuba에서분리된산성다당류역시 LPS 자극 RAW264.7 세포에서 TLR-4 발현 조절, IκBα 인산화 수준 감소 및 NF-κB p65 핵 내 전위 억제를 통해 항염증 효과를 나타내었다.45)
이러한 NF-κB 경로 억제 효과는 다양한 in vivo 동물 모델에서도 확인되었다. 알코올 유발 간손상 마우스 모델에서 Z. jujuba cv. Jinsixiaozao 열수 추출물 투여는 간 조직 내 NF-κB p65, iNOS 및 COX-2 단백질 발현을 유의하게 하향 조절하였다.55) Z. jujuba cv. Muzao의 다당류는 cecal ligation and puncture로 유도된 패혈증 마우스에서 TLR-4/NF-κB 신호전달 경로를 억제하여 염증성 사이토카인 분비를 감소시키고 장벽 기능을 보호하였다.56) 효소 처리 Z. jujuba 추출물은 벤조(a) 피렌으로 유도된 폐손상 마우스에서 NF-κB 단백질 발현을 억제하고, 하위타겟인 iNOS 및 COX-2의 발현을 감소시켰다.37) Z. jujuba 플라보노이드는 아세트아미노펜(acetaminophen) 유발 간손상 마우스에서 NF-κB p65 활성화를 억제하여 염증매개체인 NO, TNF-α, IL-6, IL-1β의생성을 감소시켰다.57)
한편, NF-κB 경로와 nuclear factor erythroid 2-related factor 2 (Nrf2)/heme oxygenase-1 (HO-1) 경로는 상호 길항적 관계에 있는 것으로 알려져 있다. Z. jujuba 유래 3-dehydroxyceanothetric acid 2-methyl ester는 시스플라틴(cisplatin) 유발 세포 손상에서 NF-κB 경로를 억제하는 동시에 Nrf2 핵 내 전위를 촉진하고 HO-1 발현을 상향 조절하였다.54) Z. jujuba 플라보노이드 역시 아세트아미노펜 유발 간손상 모델에서 Nrf2 핵 내 전위 촉진 및 NAD(P)H:quinone oxidoreductase 1 (NQO1) 발현 상향 조절과 함께 NF-κB 활성 억제를 나타내어, 항산화 방어 기전 활성화와 염증 억제가 동시에 작용함을 시사하였다.57) 이러한 결과들은 Z. jujuba가 TLR-4/IκBα/NF-κB 경로의 다단계 억제와 Nrf2/HO-1 경로 활성화라는 이중기전을 통해 항염증 효과를 발휘함을 제시한다.
MAPK 경로 – MAPK 신호전달경로는 extracellular signal-regulated kinase (ERK), c-Jun N-terminal kinase (JNK) 및 p38 MAPK의 세 가지 주요 아군으로 구성되며, 세포의 증식, 분화, 스트레스 반응 및 세포사멸 조절에 관여한다. 일반적으로 ERK는 세포 생존에 중요한 역할을 수행하는 반면, p38 및 JNK는 스트레스 반응과 관련된 기능을 담당한다.58) 염증 반응에서 MAPK 경로는 NF-κB 경로와 상호작용하여 염증 관련 효소 및 염증성 사이토카인의 발현을 조절하는 것으로 알려져 있다.
In vitro 연구에서 Z. jujuba 추출물 및 유래 성분의 MAPK 경로 억제 효과가 확인되었다. Z. jujuba 잎 에탄올 추출물은 LPS로자극된 RAW264.7 대식세포에서 MAPK 신호전달경로 활성을 억제하였다.53) Z. jujuba뿌리에서 분리된 ceanothane형 트리테르페노이드인 3-dehydroxyceanothetric acid 2-methyl ester (3DC2ME)는 시스플라틴으로 유도된 LLC-PK1 신장 상피세포 손상 모델에서 JNK, ERK 및 p38의 발현을 현저히 억제하여 MAPK 경로 억제 효과를 나타내었다.58) 동일 성분에 대한 네트워크 약리학 분석(network pharmacological analysis)에서 274개의 잠재적 표적이 MAPK 및 세포사멸 경로와 유의하게 연관됨이 확인되어(adjusted P-value = 1.78 × 10–16), 다중 표적을 통한 시스템 수준의 작용 기전이 제시되었다.58)
이러한 MAPK 경로 억제 효과는 in vivo 동물 모델에서도 확인되었다. Z. jujuba cv. Junzao 폴리페놀 추출물은 DSS로 유도된 궤양성 대장염 마우스에서 MAPK 신호전달 경로 관련 단백질의 발현을 억제하였으며, 이는 nucleotide-binding oligomerization domain-like receptor family pyrin domain-containing 3 (NLRP3) 인플라마좀(inflammasome) 억제와 함께 나타나 항염증 효과에 기여하였다.59) 이 연구에서 MAPK 경로 억제는 염증성 사이토카인 발현 감소 및 장 장벽 기능 보호와 동반되어, Z. jujuba 폴리페놀이 다중 신호전달 경로를 통해 염증 반응을 조절함을 시사하였다.59)
MAPK 경로와 NF-κB 경로는 염증 반응에서 상호 연결되어 있으며, Z. jujuba는 이 두 경로를 동시에 조절하는 것으로 보인다. Z. jujuba 잎 추출물은 RAW264.7 세포에서 NF-κB 및 MAPK 신호전달 경로 활성을 모두 억제하였으며,53) Z. jujuba 뿌리 유래 3DC2ME 역시 동일 세포 모델에서 양 경로를 동시에 표적으로 하는 것으로 확인되었다.58) 이러한 결과들은 Z. jujuba가 MAPK 경로의 다중 아군(ERK, JNK, p38)을 표적으로 하여 NF-κB 경로와의 상호작용을 통해 항염증 효과를 발휘함을 제시한다. Z. jujuba의 면역조절 효과에 관여하는 주요 신호전달 경로를 Fig. 2에 나타내었다.
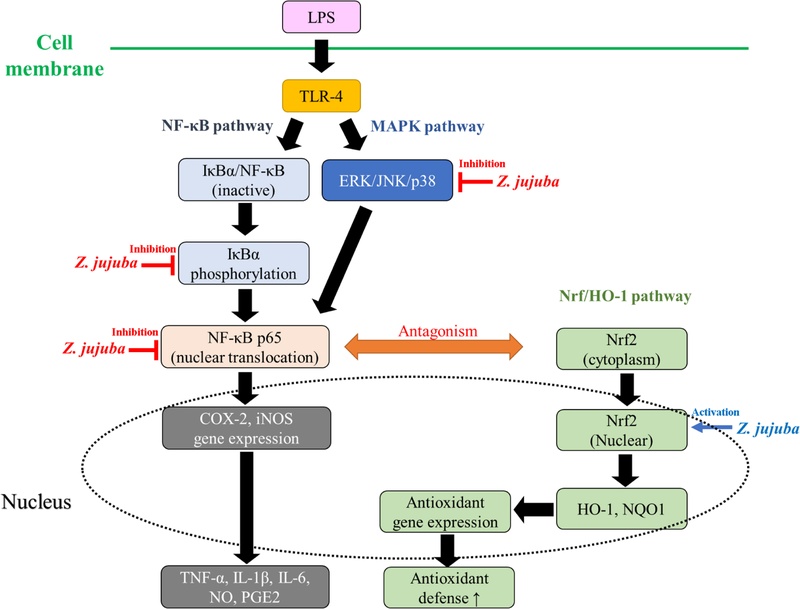
Proposed mechanisms of immunomodulatory effects of Zizipus jujuba. Lipopolysaccharide (LPS) activates Toll-like receptor 4 (TLR-4), which triggers the nuclear factor-kappa B (NF-κB) and mitogen-activated protein kinase (MAPK) signaling pathways, leading to the expression of pro-inflammatory mediators. Z. jujuba inhibits these inflammatory pathways by suppressing lκBα phosphorylation, NF-κB p65 nuclear translocation, and ERK/JNK/p38 MAPK activation. Simultaneously, Z. jujuba activates the nuclear factor erythroid 2-related factor 2 (Nrf2)/heme oxygenase-1 (HO-1) antioxidant pathway, which antagonizes the NF-κB pathway. COX-2, cyclooxygenase-2; iNOS, inducible nitric oxide synthase; NQO1, NAD(P)H:quinone oxidoreductase 1; PGE2, prostaglandin E2.
장내 미생물-면역 축 – Z. jujuba 다당류는 소화효소에 의해 분해되지 않고 대장에 도달하여 장내 미생물의 발효 기질로 작용한다. In vitro 소화 및 분변 발효 실험에서 Z. jujuba cv. Pozao 다당류는 인체 장내 미생물에 의해 발효되며, 이 과정에서 장내 미생물 구성에 영향을 미쳤다.60) Z. jujuba 과실 다당류는 8개 산지에서 수집한 시료를 분석한 결과, 총 함량이 1.31-2.22% 범위이고 분자량 분포가 1.14 × 105 에서 1.73 × 106 Da로 나타났으며, 장내 미생물 구성을 조절하고 이질(dysentery) 및 신경계 질환에 대한 잠재적 치료 효과가 보고되었다.18)
In vivo 연구에서 Z. jujuba 다당류의 프리바이오틱스(prebiotics) 효과가 확인되었다. Azoxymethane(AOM)/DSS 유도 대장암 마우스 모델에서 Z. jujuba 다당류는 장내 미생물 프로파일을 회복시켰으며, 프로피온산염(propionate) 및 낙산염(butyrate) 생성을 증가시켜 대장 종양의 성장을 억제하였다.61) DSS 유도 대장염 마우스 모델에서 분자량 2.01 × 104 Da의 Z. jujuba 다당류(ZJP-I)는 염증성 사이토카인 항상성 조절, 산화 스트레스 완화 및 단쇄지방산(short-chain fatty acids; SCFAs) 분비 회복을 통해 장염증을 억제하고 장 장벽 기능을 보호하였다.62) Z. jujuba 과실에서 추출한 펙틴은 케피어(kefir) 균에 첨가하였을 때 효모 성장을 자극하였으며, 특히 첫 번째 숙성 단계의 저메톡실화 펙틴(low-methoxyl pectin; PJ1K)이 비타민 C 생성을 0.83 µg/mL까지 증가시켰다.63) 이러한 연구들을 종합하면, Z. jujuba 다당류는 항염증, 면역조절, 항산화, 항암, 항바이러스, 장내 미생물 조절, 간보호 효과 및 프리바이오틱스 활성을 포함한 다양한 생리활성을 나타낸다.64)
다당류 외에 폴리페놀 성분도 장내 미생물 조절에 관여한다. Z. jujuba cv. Junzao 폴리페놀 추출물은 DSS 유도 궤양성 대장염 마우스에서 NLRP3 및 MAPK 신호전달 경로를 억제하고, Firmicutes의 상대적 풍부도를 증가시키며 Proteobacteria 및 Bacteroidetes를 감소시킴으로써 장내 미생물 항상성을 회복시켰다.59) 이러한 장내 미생물 조절 효과는 장-면역 축(gut-immune axis)을 통해 전신 면역반응에 영향을 미칠 수 있으며, Z. jujuba의 면역조절 기전에 있어 중요한 경로로 제시된다.
결 론
대추는 갈매나무과에 속하는 식물로서, 중의학, 아유르베다, 유나니 의학 등 다양한 전통의학 체계에서 수천 년간 활용되어 왔다. 대추 과실에는 다당류, 트리테르페노이드, 플라보노이드, 사포닌 등 다양한 생리활성 성분이 함유되어 있으며, 이들 성분은 면역조절을 포함한 다양한 약리활성에 기여한다. 본 종설에서는 대추 및 그 유래 성분의 면역조절 효과를 분자적 기전 및 사이토카인 조절을 중심으로 종합적으로 고찰하였다. 대추는 정상 또는 면역억제 상태에서는 면역기능을 강화하고, 염증 상태에서는 과도한 염증 반응을 억제하는 양방향 면역조절 특성을 나타낸다. 대식세포에서 대추 추출물은 정상 상태에서 염증성 사이토카인 발현을 증가시키는 반면, 지질다당류로 자극된 염증 상태에서는 염증 매개체를 억제한다. 대추 다당류는 in vitro에서 비장세포 및 림프구 증식을 촉진하고, in vivo에서 비장 및 흉선 지수를 증가시킨다. 항염증 효과는 NF-κB 및 MAPK 신호전달 경로의 억제와 함께 Nrf2/HO-1 항산화 경로의 활성화를 통해 매개된다. 또한, 대추 다당류는 장내 미생물의 발효 기질로 작용하여 유익균의 증식과 단쇄지방산 생성을 촉진하며, 장-면역 축을 통해 전신 면역반응에 영향을 미친다. 대추는 소화기계, 간, 신경계, 근골격계, 호흡기계 등 다양한 질환 모델에서 TNF-α, IL-1β, IL-6 등 염증성 사이토카인의 발현을 조절한다. 이러한 연구 결과들은 대추 및 그 유래 성분이 염증성 및 면역 관련 질환의 치료를 위한 면역조절제 개발의 유망한 후보물질임을 시사한다.
References
-
Nabavi, T. S., Farahani, F., Masoud, S., Katayoun, P. and Reza, N. M. (2020) Genetic and morphological variability in Ziziphus jujuba Mill. Genetika 52: 495-511.
[https://doi.org/10.2298/GENSR2002495N]

-
Rekha, U. V. B., S. and Shankar, P. R. (2021) Anticancer activity of “Ziziphus jujuba” - A Review. J. Pharm. Res. Int. 33: 261-269.
[https://doi.org/10.9734/jpri/2021/v33i59B34377]

-
Chen, J., Li, Z., Maiwulanjiang, M., Zhang, W. L., Zhan, J. Y., Lam, C. T., Zhu, K. Y., Yao, P., Choi, R. C., Lau, D. T., Dong, T. T. and Tsim, K. W. (2013) Chemical and biological assessment of Ziziphus jujuba fruits from China: different geographical sources and developmental stages. J. Agric. Food. Chem. 61: 7315-7324.
[https://doi.org/10.1021/jf402379u]

-
Gochade, M. N., Chandekar, A. and Tripathi, A. (2025) Ziziphus jujuba Mill.: A comprehensive review of its phytochemistry and pharmacological potential. Int. J. Multidiscip. Res. 7.
[https://doi.org/10.36948/ijfmr.2025.v07i03.49221]

-
Iqbal, K., Dar, E., Shaikh, A. R., Akhtar, S. and Marvi (2021) Antileishmanial activity of Cassia fistula L., Morus nigra L. and Ziziphus jujuba Mill., plant extracts. J. Pharm. Res. Int. 33: 466-471.
[https://doi.org/10.9734/jpri/2021/v33i46B32962]

-
Feng, J.-C., Yu, X. M., Shang, X. L., Li, J. D. and Wu, Y. X. (2010) Factors influencing efficiency of shoot regeneration in Ziziphus jujuba Mill. ‘Huizao’. Plant Cell Tiss. Organ Cult. 101: 111-117.
[https://doi.org/10.1007/s11240-009-9663-2]

-
Chen, K., Fan, D., Fu, B., Zhou, J. and Li, H. (2019) Comparison of physical and chemical composition of three chinese jujube (Ziziphus jujuba Mill.) cultivars cultivated in four districts of Xinjiang region in China. Food Sci. Technol. 39: 912-921.
[https://doi.org/10.1590/fst.11118]

-
Ji, X., Cheng, Y., Tian, J., Zhang, S., Jing, Y. and Shi, M. (2021) Structural characterization of polysaccharide from jujube (Ziziphus jujuba Mill.) fruit. Chem. Biol. Technol. Agric. 8: 54.
[https://doi.org/10.1186/s40538-021-00255-2]

-
Feng, R.-F., Wang, N., Kou, J.-J., An, X.-W., Meng, F.-H., Zheng, X.-J., Wang, W.-W., Wang, L.-L., Wang, Z.-H., Liu, M.-J., Ao, C.-W. and Zhao, Z.-H. (2021) Sulfated modification, characterization and potential bioactivities of polysaccharide from Ziziphus jujuba cv. Jinsixiaozao. Nat. Prod. Commun. 16: 1934578X211033673.
[https://doi.org/10.1177/1934578X211033673]

-
Xu, C., Gao, J., Du, Z., Li, D., Wang, Z., Li, Y. and Pang, X. (2016) Identifying the genetic diversity, genetic structure and a core collection of Ziziphus jujuba Mill. var. jujuba accessions using microsatellite markers. Sci. Rep. 6: 31503.
[https://doi.org/10.1038/srep31503]

-
Hua, Y., Xu, X.-x., Guo, S., Xie, H., Yan, H., Ma, X.-f., Niu, Y. and Duan, J.-A. (2022) Wild Jujube (Ziziphus jujuba var. spinosa): A review of Its phytonutrients, health benefits, metabolism, and applications. J. Agric. Food Chem. 70: 7871-7886.
[https://doi.org/10.1021/acs.jafc.2c01905]

-
Song, P., Zhang, Y., Ma, G., Zhang, Y., Zhou, A. and Xie, J. (2017) Gastrointestinal absorption and metabolic dynamics of jujuboside A, a saponin derived from the seed of Ziziphus jujuba. J. Agric. Food Chem. 65: 8331-8339.
[https://doi.org/10.1021/acs.jafc.7b02748]

-
Korkut, S. (2022) Biological activity and chemical composition of jujuba (Ziziphus jujuba) Fruit. BAUN Health Sci. J. 11(Supplement 1): 44-50.
[https://doi.org/10.53424/balikesirsbd.1159940]

-
Gao, Q. H., Wu, C. S. and Wang, M. (2013) The jujube (Ziziphus jujuba Mill.) fruit: a review of current knowledge of fruit composition and health benefits. J. Agric. Food Chem. 61: 3351-3363.
[https://doi.org/10.1021/jf4007032]

-
Cosmulescu, S., Trandafir, I., Nourv, V., Achim, G., Botu, M. and Iordanescu, O. (2018) Variation of bioactive compounds and antioxidant activity of jujube (Ziziphus jujuba) fruits at different stages of ripening. Not. Bot. Horti. Agrobo. 46: 134-137.
[https://doi.org/10.15835/nbha46110752]

-
Mansour, I., Ozay, C., Kose, F., Rahmanı, S. and Kharoubı, O. (2024) In vitro wound-healing activity of Ziziphus jujuba and its anti-inflammatory effects in rats. C. R. Acad. Bulg. Sci. 77: 118-126.
[https://doi.org/10.7546/CRABS.2024.01.14]

-
Popstoyanova, D., Gerasimova, A., Gentscheva, G., Nikolova, S., Gavrilova, A. and Nikolova, K. (2024) Ziziphus jujuba: Applications in the pharmacy and food industry. Plants 13: 2724.
[https://doi.org/10.3390/plants13192724]

-
Li, Z., Wu, M., Wei, W., An, Y., Li, Y., Wen, Q., Zhang, D., Zhang, J., Yao, C., Bi, Q. and Guo, D. (2023) Fingerprinting evaluation and gut microbiota regulation of polysaccharides from jujube (Ziziphus jujuba Mill.) fruit. Int. J. Mol. Sci. 24.
[https://doi.org/10.3390/ijms24087239]

-
Zhao, Z., Dai, H., Wu, X., Chang, H., Gao, X., Liu, M. and Tu, P. (2007) Characterization of a pectic polysaccharide from the fruit of Ziziphus jujuba. Chem. Nat. Compd. 43: 374-376.
[https://doi.org/10.1007/s10600-007-0141-y]

-
Ji, X., Zhang, S., Jin, X., Yin, C., Zhang, Y., Guo, X. and Lin, X. (2023) Systematic comparison of structural characterization of polysaccharides from Ziziphus jujuba cv. Muzao. Molecules 28: 562.
[https://doi.org/10.3390/molecules28020562]

-
Song, Q., You, X. and Liu, X. (2025) Structural characteristics of Ziziphus jujuba dates polysaccharide and its protective effect against colitis. Chem. Biodivers. 22: e202402568.
[https://doi.org/10.1002/cbdv.202402568]

-
Song, L., Zhang, L., Xu, L., Ma, Y., Lian, W., Liu, Y. and Wang, Y. (2020) Optimized extraction of total triterpenoids from jujube (Ziziphus jujuba Mill.) and comprehensive analysis of triterpenic acids in different cultivars. Plants 9: 412.
[https://doi.org/10.3390/plants9040412]

-
Chianese, A., Mushtaq, H., Nastri, B. M., Morone, M. V., Giugliano, R., Khan, H., Piccolella, S., Zannella, C., Pacifico, S., Galdiero, M. and De Filippis, A. (2024) Getting insights into chemical composition and antiherpetic capability of jujube (Ziziphus jujuba Mill.) drupes. Heliyon 10: e37037.
[https://doi.org/10.1016/j.heliyon.2024.e37037]

-
Bai, L., Zhang, H., Liu, Q., Zhao, Y., Cui, X., Guo, S., Zhang, L., Ho, C.-T. and Bai, N. (2016) Chemical characterization of the main bioactive constituents from fruits of Ziziphus jujuba. Food Funct. 7: 2870-2877.
[https://doi.org/10.1039/C6FO00613B]

-
Cai, W., Zhuang, H., Wang, X., Fu, X., Chen, S., Yao, L., Sun, M., Wang, H., Yu, C. and Feng, T. (2024) Functional nutrients and jujube-based processed products in Ziziphus jujuba. Molecules 29: 3437.
[https://doi.org/10.3390/molecules29143437]

-
Pan, F., Zhao, X., Liu, F., Luo, Z., Chen, S., Liu, Z., Zhao, Z., Liu, M. and Wang, L. (2023) Triterpenoids in jujube: A review of composition, content diversity, pharmacological effects, synthetic pathway, and variation during domestication. Plants 12: 1501.
[https://doi.org/10.3390/plants12071501]

-
Kang, K. B., Kim, J. W., Oh, W. K., Kim, J. and Sung, S. H. (2016) Cytotoxic ceanothane- and lupane-type triterpenoids from the roots of Ziziphus jujuba. J. Nat. Prod. 79: 2364-2375.
[https://doi.org/10.1021/acs.jnatprod.6b00525]

-
Xue, X., Zhao, A., Wang, Y., Ren, H., Du, J., Li, D. and Li, Y. (2021) Composition and content of phenolic acids and flavonoids among the different varieties, development stages, and tissues of Chinese jujube (Ziziphus jujuba Mill.). PLoS One 16: e0254058.
[https://doi.org/10.1371/journal.pone.0254058]

-
Shi, Q., Zhang, Z., Su, J., Zhou, J. and Li, X. (2018) Comparative analysis of pigments, phenolics, and antioxidant activity of Chinese jujube (Ziziphus jujuba Mill.) during fruit development. Molecules 23: 1917.
[https://doi.org/10.3390/molecules23081917]

-
Yan, M., Wang, Y., Watharkar, R. B., Pu, Y., Wu, C., Lin, M., Lu, D., Liu, M., Bao, J. and Xia, Y. (2022) Physicochemical and antioxidant activity of fruit harvested from eight jujube (Ziziphus jujuba Mill.) cultivars at different development stages. Sci. Rep. 12: 2272.
[https://doi.org/10.1038/s41598-022-06313-5]

-
Chowdari, A. M. and Giles, D. (2020) Anti-inflammatory, antiulcer and anticancer activities of saponin isolated from the fruits of Ziziphus jujuba. Nat. Prod. J. 10: 395-399.
[https://doi.org/10.2174/2210315509666190429145610]

-
Asaturov, Y. V., Semkina, O. A. and Dul, V. N. (2024) evelopment of technology for obtaining an extract of Ziziphus jujuba Mill. fruits. Farmaciya 73: 11-21.
[https://doi.org/10.29296/25419218-2024-08-02]

-
Chen, J. and Tsim, K. W. K. (2020) A review of edible jujube, the Ziziphus jujuba fruit: A heath food supplement for anemia prevalence. Front. Pharmacol. 11: 593655.
[https://doi.org/10.3389/fphar.2020.593655]

-
Chen, J., Du, C. Y., Lam, K. Y., Zhang, W. L., Lam, C. T., Yan, A. L., Yao, P., Lau, D. T., Dong, T. T. and Tsim, K. W. (2014) The standardized extract of Ziziphus jujuba fruit (jujube) regulates pro-inflammatory cytokine expression in cultured murine macrophages: Suppression of lipopolysaccharide-stimulated NF-κB activity. Phytother. Res. 28: 1527-1532.
[https://doi.org/10.1002/ptr.5160]

-
Chen, J., Lam, C. T., Li, Z., Yao, P., Lin, H., Dong, T. T. and Tsim, K. W. (2016) Extract of Ziziphus jujuba fruit (jujube) stimulates expression of enzymes responsible for heme recycle via antioxidant response element in cultured murine macrophages. Phytother. Res. 30: 267-271.
[https://doi.org/10.1002/ptr.5526]

-
Goyal, R., Sharma, P. L. and Singh, M. (2011) Possible attenuation of nitric oxide expression in anti-inflammatory effect of Ziziphus jujuba in rat. J. Nat. Med. 65: 514-518.
[https://doi.org/10.1007/s11418-011-0531-0]

-
Kim, Y., Oh, J., Jang, C. H., Lim, J. S., Lee, J. S. and Kim, J. S. (2020) In vivo anti-inflammatory potential of viscozyme (®)-treated jujube fruit. Foods 9: 1033.
[https://doi.org/10.3390/foods9081033]

-
Weih, F. and Caamaño, J. (2003) Regulation of secondary lymphoid organ development by the nuclear factor-kappaB signal transduction pathway. Immunol. Rev. 195: 91-105.
[https://doi.org/10.1034/j.1600-065X.2003.00064.x]

-
Cheminay, C., Möhlenbrink, A. and Hensel, M. (2005) Intracellular salmonella inhibit antigen presentation by dendritic cells. J. Immunol. 174: 2892-2899.
[https://doi.org/10.4049/jimmunol.174.5.2892]

-
Zhao, Z., Li, J., Wu, X., Dai, H., Gao, X., Liu, M. and Tu, P. (2006) Structures and immunological activities of two pectic polysaccharides from the fruits of Ziziphus jujuba Mill. cv. jinsixiaozao Hort. Food Res. Int. 39: 917-923.
[https://doi.org/10.1016/j.foodres.2006.05.006]

-
Zou, M., Chen, Y., Sun-Waterhouse, D., Zhang, Y. and Li, F. (2018) Immunomodulatory acidic polysaccharides from Zizyphus jujuba cv. Huizao: Insights into their chemical characteristics and modes of action. Food Chem. 258: 35-42.
[https://doi.org/10.1016/j.foodchem.2018.03.052]

-
Singh, B., Gautam, S., Dubey, B. K. and Basedia, D. K. (2022) Anti inflammatory and antioxidant activity of Ziziphus jujuba extract. Asian J. Pharm. Res. Dev. 10: 115-121.
[https://doi.org/10.22270/ajprd.v10i4.1164]

-
Yang, Y. J., Kim, M. J., Lee, H. J., Lee, W.-Y., Yang, J.-H., Kim, H. H., Shim, M. S., Heo, J. W., Son, J. D., Kim, W. H., Kim, G. S., Lee, H.-J., Kim, Y.-W., Kim, K. Y. and Park, K. I. (2024) Ziziphus jujuba Miller ethanol extract restores disrupted intestinal barrier function via tight junction recovery and reduces inflammation. Antioxidants 13: 575.
[https://doi.org/10.3390/antiox13050575]

-
Alsayari, A. and Wahab, S. (2021) Genus Ziziphus for the treatment of chronic inflammatory diseases. Saudi J. Biol. Sci. 28: 6897-6914.
[https://doi.org/10.1016/j.sjbs.2021.07.076]

-
Liu, C., Wang, F. and Zhang, R. (2022) An acidic polysaccharide with anti-Inflammatory effects from blackened jujube: Conformation and rheological properties. Foods 11: 2488.
[https://doi.org/10.3390/foods11162488]

-
Han, X., Bai, B., Zhou, Q., Niu, J., Yuan, J., Zhang, H., Jia, J., Zhao, W. and Chen, H. (2020) Dietary supplementation with polysaccharides from Ziziphus jujuba cv. Pozao intervenes in immune response via regulating peripheral immunity and intestinal barrier function in cyclophosphamide-induced mice. Food Funct. 11: 5992-6006.
[https://doi.org/10.1039/D0FO00008F]

-
Bahrami, S., Babaei, N., Esmaeili Gouvarchin Ghaleh, H., Mohajeri Borazjani, J. and Farzanehpour, M. (2024) Anti-inflammatory activity of Ziziphus jujuba hydroalcoholic extract in acetic acid-induced ulcerative colitis model. J. Complement. Integr. Med. 21: 481-489.
[https://doi.org/10.1515/jcim-2024-0178]

-
Kandimalla, R., Dash, S., Kalita, S., Choudhury, B., Malampati, S., Kalita, K., Kalita, B., Devi, R. and Kotoky, J. (2016) Protective effect of bioactivity guided fractions of Ziziphus jujuba Mill. root bark against hepatic injury and chronic inflammation via inhibiting inflammatory markers and oxidative stress. Front. Pharmacol. 7: 298.
[https://doi.org/10.3389/fphar.2016.00298]

-
Kandeda, A. K., Nguedia, D., Ayissi, E. R., Kouamouo, J. and Dimo, T. (2021) Ziziphus jujuba (Rhamnaceae) alleviates working memory impairment and restores neurochemical alterations in the prefrontal cortex of D-galactose-treated rats. Evid. Based Complement. Alternat. Med. 2021: 6610864.
[https://doi.org/10.1155/2021/6610864]

-
Kandimalla, R., Dash, S., Kalita, S., Choudhury, B., Malampati, S., Devi, R., Ramanathan, M., Talukdar, N. C. and Kotoky, J. (2017) Bioactivefraction of Annona reticulata bark (or) Ziziphus jujuba root bark along with insulin attenuates painful diabetic neuropathy through inhibiting NF-κB inflammatory cascade. Front. Cell Neurosci. 11: 73.
[https://doi.org/10.3389/fncel.2017.00073]

-
Khoramjouy, M., Bayanati, M., Noori, S., Faizi, M. and Zarghi, A. (2022) Effects of Ziziphus jujuba extract alone and combined with Boswellia serrata extract on monosodium iodoacetate model of osteoarthritis in mice. Iran. J. Pharm. Res. 21: e134338.
[https://doi.org/10.5812/ijpr-134338]

-
Shaban, P., Honari, N., Erfanian, N., Hosseini, M., Safarpour, H. and Nasseri, S. (2023) Anti-inflammatory effects of Ziziphus jujube Mill. on LPS-induced acute lung injury in mice. Iran. J. Allergy Asthma Immunol. 22: 281-289.
[https://doi.org/10.18502/ijaai.v22i3.13056]

-
Eo, H. J., Lee, S.-Y. and Park, G. H. (2023) UHPLC/TOFHRMS analysis and anti-inflammatory effect of leaf extracts from Zizyphus jujuba in LPS-stimulated RAW264.7 cells. J. Plant Biotechnol. 50: 27-33.
[https://doi.org/10.5010/JPB.2023.50.004.027]

-
Lee, D., Kang, K. B., Hwang, G. S., Choi, Y.-K., Kim, T. K. and Kang, K. S. (2021) Antioxidant and anti-inflammatory effects of 3-dehydroxyceanothetric acid 2-methyl ester isolated from Ziziphus jujuba Mill. against cisplatin-induced kidney epithelial cell death. Biomolecules 11: 1614.
[https://doi.org/10.3390/biom11111614]

-
Liu, N., Yang, M., Huang, W., Wang, Y., Yang, M., Wang, Y. and Zhao, Z. (2017) Composition, antioxidant activities and hepatoprotective effects of the water extract of Ziziphus jujuba cv. Jinsixiaozao. RSC Adv. 7: 6511-6522.
[https://doi.org/10.1039/C6RA27516H]

-
Zhou, H. C., Guo, C. A., Yu, W. W., Yan, X. Y., Long, J. P., Liu, Z. C., Liang, X. Q. and Liu, H. B. (2021) Zizyphus jujuba cv. Muzao polysaccharides enhance intestinal barrier function and improve the survival of septic mice. J. Food Biochem. 45: e13722.
[https://doi.org/10.1111/jfbc.13722]

-
Huang, W., Wang, Y., Jiang, X., Sun, Y., Zhao, Z. and Li, S. (2017) Protective effect of flavonoids from Ziziphus jujuba cv. Jinsixiaozao against acetaminophen-induced liver injury by inhibiting oxidative stress and inflammation in mice. Molecules 22: 1781.
[https://doi.org/10.3390/molecules22101781]

-
Lee, D., Kim, K. H., Lee, W. Y., Kim, C.-E., Sung, S. H., Kang, K. B. and Kang, K. S. (2019) Multiple targets of 3-dehydroxyceanothetric acid 2-methyl ester to protect against cisplatin-induced cytotoxicity in kidney epithelial LLC-PK1 cells. Molecules 24: 878.
[https://doi.org/10.3390/molecules24050878]

-
Wei, X., Ma, N., Yang, W., Tian, J., Liu, H. and Fang, H. (2024) Polyphenol extracts from Ziziphus jujuba Mill. “Junzao” attenuates ulcerative colitis by inhibiting the NLRP3 and MAPKs signaling pathways and regulating gut microbiota homeostasis in mice. Mol. Nutr. Food Res. 68: e2300643.
[https://doi.org/10.1002/mnfr.202300643]

-
Han, X., Zhou, Q., Gao, Z., Lin, X., Zhou, K., Cheng, X., Chitrakar, B., Chen, H. and Zhao, W. (2022) In vitro digestion and fecal fermentation behaviors of polysaccharides from Ziziphus jujuba cv. Pozao and its interaction with human gut microbiota. Food Res. Int. 162: 112022.
[https://doi.org/10.1016/j.foodres.2022.112022]

-
Ji, X., Hou, C., Gao, Y., Xue, Y., Yan, Y. and Guo, X. (2020) Metagenomic analysis of gut microbiota modulatory effects of jujube (Ziziphus jujuba Mill.) polysaccharides in a colorectal cancer mouse model. Food Funct. 11: 163-173.
[https://doi.org/10.1039/C9FO02171J]

-
Song, Q. and You, X. (2025) Protective bioactivity of Ziziphus jujuba dates polysaccharide on colitis via improving the intestinal barrier and modifying the gut microbiota. Carbohydr. Polym. Technol. Appl. 11: 100931.
[https://doi.org/10.1016/j.carpta.2025.100931]

-
Fazio, A., La Torre, C., Caroleo, M. C., Caputo, P., Cannataro, R., Plastina, P. and Cione, E. (2020) Effect of addition of pectins from jujubes (Ziziphus jujuba Mill.) on vitamin C production during heterolactic fermentation. Molecules 25: 2706.
[https://doi.org/10.3390/molecules25112706]

-
Jia, F., Wang, B., Ma, H., Bai, C. and Zhang, Y. (2025) Research progress on extraction, separation, structure, and biological activities of polysaccharides from jujube fruit (Ziziphus jujuba Mill.): a review. Front. Chem. 13: 1581947.
[https://doi.org/10.3389/fchem.2025.1581947]

-
Liu, X., Wang, Q., Wang, J., Guo, L., Chu, Y., Ma, C. and Kang, W. (2024) Structural characterization, chain conformation and immunomodulatory activity of a heteropolysaccharide from Inonotus hispidus. Int. J. Biol. Macromol. 260: 129187.
[https://doi.org/10.1016/j.ijbiomac.2023.129187]

-
Choi, S. H., Ahn, J. B., Kim, H. J., Im, N. K., Kozukue, N., Levin, C. E. and Friedman, M. (2012) Changes in free amino acid, protein, and flavonoid content in jujube (Ziziphus jujuba) fruit during eight stages of growth and antioxidative and cancer cell inhibitory effects by extracts. J. Agric. Food Chem. 60: 10245-10255.
[https://doi.org/10.1021/jf302848u]