
감(Diospyros kaki)의 면역조절에 관한 고찰
Abstract
Persimmon (Diospyros kaki) has been traditionally used in East Asian medicine and contains various bioactive compounds including condensed tannins, flavonoids, and polysaccharides. This review aims to comprehensively examine the dual immunomodulatory mechanisms of D. kaki-derived components. Flavonoids and triterpenoids exert anti-inflammatory effects through NF-κB and MAPK pathway inhibition, reducing pro-inflammatory cytokines and mediators. In contrast, polysaccharides exhibit immunostimulatory effects by activating macrophages through MAPK signaling. In disease models, persimmon extracts demonstrated therapeutic effects in atopic dermatitis, ulcerative colitis, and immediate-type hypersensitivity, while enhancing host defense in tumor and infection models. These findings indicate that persimmon possesses bidirectional immune regulatory properties depending on pathophysiological context, suggesting its potential as a functional material for immune balance modulation.
Keywords:
Diospyros kaki, Innate immunity, Anti-inflammatory, Immunomodulation, Immunostimulation, Polysaccharide감(persimmon)은 감나무과(Ebenaceae) Diospyros속에 속하는 과수이다.1) Diospyros속에는 전 세계적으로 400종 이상이 분포하고 있으며, 이 중 D. kaki, D. virginiana, D. oleifera, D. lotus 등이 주요 종으로 알려져 있다. 이들 중 D. kaki가 가장 널리 재배되고 있다.2) 감은 중국을 원산지로 하며, 수세기에 걸쳐 중국, 한국, 일본에서 중요한 과수로 재배되어 왔다.3) 감은 다양한 기후 조건에 적응할 수 있어 재배 지역이 점차 확대되고 있다.4) 세계 감 생산량은 약 250만 톤에 달하며, 중국이 약 74%, 한국이 10%, 일본이 9%를 차지하고 있다.1) 감 품종은 성숙 시 떫은맛의 유무에 따라 떫은감(astringent type)과 단감(non-astringent type)으로 분류되며, 수분 여부에 따른 과육 변화 양상에 따라 수분항상형(pollination constant; PC)과 수분변이형(pollination variant; PV)으로 구분된다. 이를 조합하면 수분항상성 단감형(pollination constant non-astringent; PCNA), 수분변이성 단감형(pollination variant non-astringent; PVNA), 수분변이성 떫은감형(pollination variant astringent; PVA), 수분항상성 떫은감형(pollination constant astringent; PCA)의 4가지 유형으로 분류된다.2) 대표적인 PCNA 품종으로는 '부유(D. kaki Thunb. ‘Fuyu’)'가 있으며,1) 한국에서는 '둥시', '둥출', '대봉' 등의 품종이 재배되고 있다.5)
감은 과육뿐만 아니라 잎, 껍질, 감 꼭지(D. kaki calyx) 등 다양한 부위가 활용되고 있다. 감 껍질에는 카로티노이드(carotenoids), 폴리페놀(polyphenols), 아스코르브산(ascorbic acid), 식이섬유(fibers) 등이 과육보다 풍부하게 함유되어 있어 기능성 소재로서의 활용 가치가 높다.6) 동아시아에서 감은 오랜 기간 전통 의약으로 활용되어 왔으며, 특히 감 꼭지(시체, 柿蒂)는 한방에서 중요한 약재로 사용된다. 시체를 생강, 정향과 배합한 시체탕(柿蒂湯)은 항암제 치료 후 발생하는 만성 딸꾹질 치료에 임상적으로 사용되고 있다.7) 한국에서 감 꼭지는 약용식물로 인정되어 연구되고 있으며,8) 감 잎에서 분리된 플라보노이드(flavonoids) 추출물은 신경보호 효과가 보고되어 있다.9)
감은 폴리페놀, 카로티노이드, 식이섬유, 무기질 등 다양한 생리활성 물질을 함유하고 있어 항산화, 항암, 항당뇨, 항비만, 항노화 등의 효능이 보고되어 있다.1,2) 최근 연구에서는 감 잎 유래 다당류가 톨-유사 수용체(Toll-like receptor; TLR)-2를 통해 대식세포를 활성화시키는 면역자극 효과가 확인되었으며,10) 감 꼭지 추출물은 비만세포 활성화를 억제하여 즉시형 과민반응을 완화시키는 것으로 보고되었다.11) 이처럼 감의 다양한 부위에서 면역조절 및 항염증 활성이 밝혀지고 있으나, 그 기전에 대한 종합적인 고찰은 부족한 실정이다. 특히 감 유래 성분은 염증 조건에서 NF-κB 및 MAPK 경로를 억제하여 항염증 효과를 나타내는 반면, 면역자극 조건에서는 대식세포 활성화 및 사이토카인 분비를 촉진하여 숙주 방어 기능을 강화하는 면역조절의 이중성을 나타낸다. 본 종설에서 '감'은 Diospyros 속 중 D. kaki 단일 종을 지칭하며, 해당 종의 항염증 및 면역증강 기전의 이중 조절 효과에 초점을 맞추어 최신 연구 동향을 고찰하고자 한다.
주요 생리활성 성분
감에는폴리페놀, 카로티노이드, 다당류등다양한생리활성 물질이 함유되어 있으며, 이들은 선천면역활성화 및 항염증 반응의 주요 활성 성분으로 작용한다. 본 장에서는 이러한 기전의 물질적 기반이 되는 주요 성분군의 화학적 특성과 함량 변이를 고찰한다.
축합형탄닌(condensed tannin; CT)–감의 떫은맛은 과육에 축적되는 수용성 CT, 즉 프로안토시아니딘(proanthocyanidin) 에기인한다. 감 CT의구조는플라반-3-올(flavan-3-ol) 단위체가 중합된 형태로, 주요 구성 단위로는 에피카테킨(epicatechin; EC), 에피갈로카테킨(epigallocatechin; EGC), 에피카테킨-3-O-갈레이트(epicatechin-3-O-gallate; ECG), 에피갈로카테킨-3-O-갈레이트(epigallocatechin-3-O-gallate; EGCG)가 보고되었다.12) 이들 구성 단위는 모두 2,3-cis 배열을 가지며, 2,3-trans 형태인카테킨(catechin) 및갈로카테킨(gallocatechin)은 감 과육에서 검출되지 않았다.13) 감 CT는 A형 결합(A-linked) 으로 연결된 고도 갈로일화(highly galloylated) 구조를 가지며, 말단 단위로 미리세틴(myricetin)이 결합된 독특한 구조적 특성을 보인다.14)
이러한 CT의 함량은 품종에 따라 상이하다. 품종 간 CT 함량을 비교한 결과, PCNA 품종인 '차랑(D. kaki Thunb. ‘Jiro’)' 과 '미카도(D. kaki Thunb. ‘Mikado’)'의 총 CT 함량은 각각 1,982.9 및 2,272.3 μg/10 mg 건조중량으로, PCA 품종인 '요코노(D. kaki Thunb. ‘Yokono’)'(3,114.3 μg/10 mg)와 '미야자키타네나시(D. kaki Thunb. ‘Miyazakitanenashi’)'(3,322.4 μg/10 mg)에 비해 현저히 낮았다. 특히 EGCG 함량은 PCNA 품종에서 645.8–902.7 μg/10 mg으로, PCA 품종의 1,754.5–1,864.1 μg/10 mg에 비해 약 50% 수준에 불과하였다. 또한 A형 결합으로 연결된 고도 갈로일화(highly galloylated), 즉 갈레이트형(gallate-type) CT의 비율은 PCNA 품종(43.7–54.7%)에서 PCA 품종(61.7–62.7%)보다 낮게 나타났다.12)
감 과육의 페놀성 화합물(phenolic compounds) 함량은 과실 성숙 과정에서 유의적으로 감소한다. 성숙 및 수상 연화 기간(120일) 동안 카테킨과 프로안토시아니딘 함량은 지속적으로 감소하였으며, 폴리페놀 손실과 성숙 기간 사이에는 높은 음의 상관관계(r = −0.811 ~ −0.916, P < 0.05)가 밝혀졌다.15) 수확 후 탈삽처리(deastringency treatment) 시에는 처리 방법에 따라 탄닌의 변화 양상이 상이하다. 에틸렌(ethylene) 처리 시 세포벽 및 세포막의 부분적 파괴로 인해 방출된 펙틴(pectin), 셀룰로오스(cellulose), 단백질이 프로안토시아니딘과 결합하여 불용성화되며, 이 과정에서 총 페놀 함량(total phenolic content; TPC)이 감소한다.16) 반면 이산화탄소(CO2) 처리 시에는 CT가 아세트알데히드(acetaldehyde) 매개 중합을 통해 고분자량의 불용성 중합체를 형성하며, 세포 구조가 유지되어 과실의 경도가 보존된다.16)
감 CT는 여러 생리활성을 나타낸다. 고분자량 CT는 생체 내외(in vitro 및 in vivo) 실험에서 강력한 항산화 활성이 확인되었으며,17) 담즙산 결합능을 통해 지질 대사 개선에 기여하는 것으로 보고되었다.18)
플라보놀(flavonol) 및 기타 페놀성 화합물 – 플라보놀을 포함한 페놀성 화합물은 감의 주요 생리활성 성분으로, 특히 잎에 풍부하게 함유되어 있다. 감 잎의 주요 성분으로는 퀘르세틴(quercetin) 및 캠페롤(kaempferol) 배당체가 확인되었으며, 구체적으로 하이페로사이드(hyperoside; quercetin-3-O-β-D-galactopyranoside), 이소퀘르시트린(isoquercitrin; quercetin-3-O-β-D-glucopyranoside), 트리폴린(trifolin; kaempferol-3-O-β-D-galactopyranoside), 아스트라갈린(astragalin; kaempferol-3-O-β-D-glucopyranoside), 퀘르세틴-3-O-(2″-O-galloyl-β-D-glucopyranoside) (QOG), 캠페롤-3-O-(2″-O-galloyl-β-D-glucopyranoside) (KOG) 및 크리손테민(chrysontemin; cyanidin3-O-β-D-glucopyranoside)이 동정되었다.19) 이 중 크리손테민은 감 잎에서 처음으로 확인된 안토시아닌(anthocyanin)으로, 가을철 단풍의 적색 발현에 기여하는 주요 색소 성분이다.19)
감잎의 총 페놀함량은 품종 및 수확시기에 따라 상이하다. 한국 주요 품종을 대상으로 한 연구에서, '갑주백목(Gabjubaekmok)' 품종의 총 페놀 함량이 112.09 ± 0.3 mg gallic acid equivalent (GAE)/g 건조중량으로 가장 높았으며, 총 플라보노이드 함량 역시 37.83 ± 0 mg catechin equivalent (CE)/g으로 다른 품종에 비해 유의적으로 높게 나타났다.20) 수확 시기별로는 개화기(5월 하순)에 채취한 잎이 결실기(6월 하순)에 비해 페놀 및 플라보노이드 함량이 높았으며, 이는 결실 과정에서 항산화 성분이 과실로 이동하기 때문인 것으로 제안되었다.20) 또한 한 잎의 단풍 진행에 따라 총 페놀 함량이 1.2–1.7배 증가하는 것으로 보고되었다.19)
이들 페놀성 화합물은 다양한 생리활성을 나타낸다. 감 잎 에탄올(ethanol) 추출물의 에틸아세테이트(ethyl acetate) 분획에서 분리된 (+)-카테킨, 하이페로사이드, 이소퀘르시트린 및 갈로일화 퀘르세틴/캠페롤 배당체는 온라인 high-performance liquid chromatography-2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid) (HPLC-ABTS) 분석에서 항산화 활성이 규명되었다.21) 특히 갈로일기(galloyl group)가 결합된 플라보놀 배당체가 쿠마로일(coumaroyl) 또는 페룰로일(feruloyl) 유도체에 비해 높은 항산화 활성을 나타냈다.21)
카로티노이드 – 카로티노이드는 감의 황색 내지 적색을 나타내는 주요 색소 성분으로, 프로비타민 A (provitamin A) 활성 및 항산화 기능을 가진다. 감 과실에서는 최소 11종의 카로티노이드가 검출되었으며, 이 중 올-트랜스-바이올락산틴(all-trans-violaxanthin), 올-트랜스-루테인(all-trans-lutein), 올-트랜스-제아잔틴(all-trans-zeaxanthin), 올-트랜스-β-크립토잔틴(all-trans-β-cryptoxanthin) 및 올-트랜스-β-카로틴(all-trans-β-carotene)이 규명되었다.22) 비검화 추출물(unsaponifiable extract) 분석 결과 β-크립토잔틴(cryptoxanthin), β-카로틴(carotene), 제아잔틴(zeaxanthin)이 주요 성분으로 확인되었으며, 라이코펜(lycopene) 함량은 품종에 따라 현저한 차이를 보여 'Rojo Brillante' 품종(D. kaki Thunb. ‘Rojo Brillante’)에서는 5.34 µg/g으로 높게 검출된 반면 'Sharon' 품종(D. kaki Thunb. ‘Sharon’)에서는 미량만 검출되었다.23)
감 과육의 총 카로티노이드 함량은 품종 및 성숙 단계에 따라 상이하다. 46개 품종을 대상으로 한 연구에서 총 카로티노이드 함량은 194.61–1,566.30 µg/100g 생중량 범위였으며, β-크립토잔틴과 제아잔틴이 총 카로티노이드의 37.84–85.11%를 차지하였다.24) 성숙 단계별로는 녹숙기(early green mature stage)에서 연숙기(soft mature stage)로 진행됨에 따라 총 카로티노이드 함량이 약 5.92배 증가하는 것으로 보고되었다.24) 또한 'Rojo Brillante'와 'Sharon' 품종의 총 카로티노이드 함량은 각각 22.11 µg/g 및 15.22 µg/g으로 품종 간 유의적 차이가 관찰되었다.23)
감 카로티노이드는 활성산소종(reactive oxygen species; ROS) 소거를 통한 항산화 활성을 나타낸다. β-크립토잔틴, β-카로틴, 라이코펜의 일중항산소(singlet oxygen; 1O2) 소거 속도상수(quenching rate constant, Kq)는 각각 1.6 × 109, 1.3 × 109, 1.1 × 109 M-1·s-1로, β-크립토잔틴이 가장 높은 소거 효율을 나타냈다.22) 한편, 이러한 카로티노이드가 체내에서 기능을 발휘하기 위해서는 생체접근성(bioaccessibility)이 중요한데, 감을 유제품에 첨가한 연구에서 전지유 사용 시 28.9%, 탈지유 사용 시 7.7%의 생체접근성을 보여 지방 함량이 높을수록 카로티노이드 흡수에 유리한 것으로 나타났다.25) β-카로틴과 β-크립토잔틴은 프로비타민 A로서 비타민 A 가치에 기여하며, 감 기반 유제품 200g 섭취 시 권장섭취량의 9–53%를 제공하는 것으로 보고되었다.25)
다당류 – 감의 잎과 과실에서는 다양한 수용성 다당류가 분리되며, 이들은 주로 펙틴 계열의 산성 헤테로다당류(heteropolysaccharide)에 해당한다. 감 잎에서 분리된 다당류 DL-2A는 람노스(rhamnose), 아라비노스(arabinose), 갈락토스(galactose), 자일로스(xylose), 갈락투론산(galacturonic acid)을 몰비 0.4:3.4:2.4:1.0:0.8로 함유하며, 갈락투론산의 약 16.7%가 메틸에테르(methyl ester) 형태로 존재한다.26) 감 과실 유래 다당류는 아라비노스, 만노스(mannose), 람노스, 갈락토스, 글루코스(glucose)로 구성된 헤테로다당류로 보고되었으며, 평균 분자량은 1.3×105 Da로 입증되었다.27) 한국산 감 과실에서 에탄올 분획을 통해 분리한 고분자 분획은 갈락투론산이 73.2 mol%로 가장 풍부하고, 아라비노스 7.4%, 갈락토스 7.1%, 글루코스 5.0%, 자일로스 2.9%, 람노스 2.3%, 만노스 2.2%를 함유하여 전형적인 갈락투론산 풍부 펙틴 다당류(galacturonic acid-rich pectic polysaccharide)의 특성을 나타낸다.28)
감 다당류의 분자량은 부위와 추출 조건에 따라 넓은 범위를 보인다. 잎 유래 펙틴 다당류 DL-2A는 8.5×105 Da의 고분자량을 가지며, α-(1→4)-갈락투로난(galacturonan)을 주쇄로 하고 일부 α-1,2- 람노피라노실(rhamnopyranosyl) 잔기가 삽입된 구조이다.26) 이 주쇄에는 아라비노-3,6-갈락탄(arabino-3,6-galactan) 측쇄가 람노스 잔기의 O-4 위치와 갈락투론산 잔기의 O-3 위치에 동시에 부착되어 있으며, 4-연결 자일로스 잔기가 짧은 선형 사슬을 형성하여 람노스의 O-4 위치에 직접 연결된다.26) 한국산 감 과실의 고분자 분획은 345 kDa 이상의 분자량을 가지며, 높은 갈락투론산 함량으로 인해 펙틴성 다당류로 추정된다.28)
감 잎 다당류의 특성은 수확 시기에 따라 현저하게 변화한다. 어린 단계(6월), 초기 녹숙기(8월), 완숙기(10월)에 수확한 잎에서 분리한 다당류의 수율은 각각 1.80%, 1.44%, 1.20%로 성숙이 진행됨에 따라 감소하였으나, 주요 분획의 평균 분자량은 7.3 kDa에서 21.6 kDa, 86.6 kDa로 증가하였다.29) 초기 녹숙기 다당류는 갈락토스, 아라비노스, 람노스, 자일로스, 갈락투론산 함량이 가장 높았으며, Fourier-transform infrared spectroscopy (FT-IR) 분석에서 890 cm-1의 β-피라노사이드(pyranoside) 결합 흡수가 관찰되어 람노갈락투로난-I (rhamnogalacturonan-I; RG-I) 측쇄 구조가 더 풍부할 가능성이 제시되었다.29)
이상에서 살펴본 축합형 탄닌, 플라보놀, 카로티노이드, 다당류의 주요 특성은 Table I에 요약하였으며, 대표적인 화학구조는 Fig. 1에 나타내었다. Table I에서 보는 바와 같이, 축합형 탄닌은 과실에, 플라보놀은 잎에 주로 분포하여 부위별 성분 조성이 상이하며, 다당류는 성숙 단계에 따라 분자량이 증가하는 특성을 나타낸다. 이러한 부위별·성숙 단계별 성분 차이는 면역조절 활성의 차별적 발현과 연관될 수 있다. 이들 성분군은 감의 면역조절 및 항염증 활성에 기여하는 주요 물질로, 다음 장에서는 이들이 선천면역계에 작용하는 분자적 기전을 고찰한다.

Major bioactive compounds in persimmon (Diospyros kaki) and their distribution by plant part. Condensed tannins are predominantly found in fruit, while flavonols are enriched in leaves. Polysaccharide molecular weight increases with leaf maturity
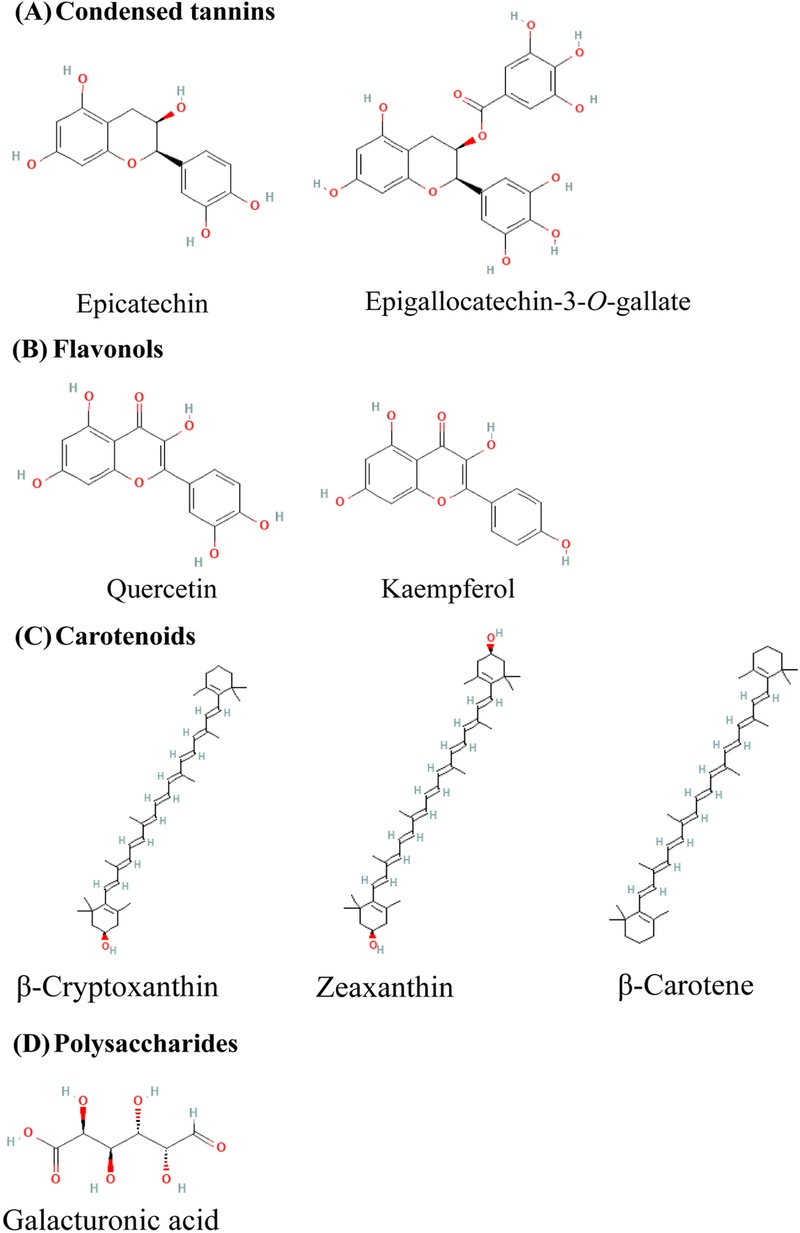
Chemical structures of major bioactive compounds from Diospyros kaki. (A) Condensed tannins: epicatechin, epigallocatechin-3-O-gallate. These flavan-3-ol polymers contribute to astringency and exhibit anti-inflammatory activity. (B) Flavonols: quercetin, kaempferol. These O-glycosides are enriched in leaves and inhibit MAPK phosphorylation. (C) Carotenoids: β-cryptoxanthin, zeaxanthin, β-carotene. All-trans forms predominant in fruit. (D) Polysaccharides: galacturonic acid, the major monosaccharide unit of pectic polysaccharides responsible for immunostimulatory effects. Structures were obtained from PubChem.
면역조절 및 항염증의 분자적 기전
핵 인자-카파 B (nuclear factor-kappa B; NF-κB) 신호 전달 억제 – NF-κB는 면역 및 염증 반응의 핵심 전사인자로, 포유류에서 p65 (RelA), c-Rel, RelB, p50/p105 (NF-κB1), p52/p100 (NF-κB2)의 다섯 가지 구성원으로 이루어진다. 비활성 상태에서 NF-κB 이합체는 세포질 내 inhibitor of NF-κB (IκB) 단백질과 결합하여 존재하며, IκB 키나아제(IκB kinase; IKK)에 의해 IκB가 인산화되면 유비퀴틴화(ubiquitination) 및 프로테아좀(proteosome) 분해가 유도되고, 유리된 NF-κB 이합체가 핵 내로 이동하여 표적 유전자의 전사를 촉진한다.30) 감 추출물 및 분리 성분의 NF-κB 신호전달 억제 효과는 다양한 세포 모델에서 보고되었다.
감 물추출물(aqueous extract of D. kaki, AEDK)은 phorbol 12-myristate 13-acetate (PMA)/칼슘이오노포어(calcium ionophore) A23187 (PMACI)로 자극한 human mast cell line-1 (HMC-1) 비만세포에서 p65의 핵 이동을 억제하고 IκBα 분해를 차단하는 것으로 확인되었으며, NF-κB-luciferase reporter 분석에서도 AEDK 100 μg/mL 처리 시 PMACI에 의해 증가한 luciferase 활성이 유의하게 감소하였다.31) 감 잎 에탄올 추출물은 PMACI로 자극된 사람 T 림프구 유래 Jurkat 세포에서 p65의 핵 이동을 억제하고 세포질 내 p65 수준을 유지하였으며, 동시에 IκBα 분해를 저해하는 효과를 나타냈다.32)
감 잎 유래 플라보노이드(flavonoids from persimmon leaves, FPL)는 H2O2 (250 μM)로 산화적 스트레스 조건의 마우스 골아세포주 MC3T3-E1에서 NF-κB/p65 발현을 농도 의존적으로 억제하였다.33) 감 잎의 트리테르펜(triterpene) 성분인 쿠사르산(coussaric acid)과 베툴리닉산(betulinic acid)은 지질다당류(lipopolysaccharide; LPS)로 자극된 마우스 대식세포 RAW 264.7에서 IκBα 분해를 억제하고 p65의 핵 이동을 차단하여 NF-κB 신호 전달을 저해하였다. 특히 베툴리닉산은 nuclear factor erythroid 2-related factor 2 (Nrf2) 경로를 활성화해 헤모옥시게나아제-1 (heme oxygenase-1; HO-1) 발현을 유도하였고, HO-1 억제제인 tin protoporphyrin IX (SnPP) 처리 시 항염증 효과가 부분적으로 감소함에 따라 HO-1 유도가 NF-κB 억제에 중요한 역할을 하는 것으로 밝혀졌다.34)
종합하면, 감의 플라보노이드 및 트리테르펜 계열 화합물은 IκBα-p65 축을 핵심 표적으로 하여 NF-κB 신호전달을 효과적으로 억제하는 항염증 기전을 갖는 것으로 판단된다.
유사분열 활성화 단백질 키나아제(mitogen-activated protein kinase; MAPK) 신호전달 조절 – MAPK 신호전달 경로는 세포외신호 조절 키나아제(extracellular signal-regulated kinase; ERK), c-Jun N말단 키나아제(c-Jun N-terminal kinase; JNK), p38 MAPK의 세 가지 주요 키나아제(kinase)로 구성되며, 외부 자극에 의해 활성화되어 염증 반응 및 면역 조절에 핵심적인 역할을 수행한다. 염증 조건에서 MAPK의 과활성화는 염증성 매개체의 과잉 생성을 유도하여 조직 손상을 초래하는 반면, 면역자극 조건에서 MAPK 활성화는 대식세포 활성화 및 사이토카인 분비를 촉진하여 숙주 방어 기능을 강화한다.35-37)
대식세포에서 감 유래 플라보노이드는 LPS 유도 MAPK 인산화를 효과적으로 억제한다. 감꽃받침에서 분리한 quercetin-3-O-β-D-(2″-galloyl)-glucopyranoside (Q32G)는 RAW 264.7 세포에서 50 μM 농도로 처리 시 p-ERK를 78%, p-JNK를 90%, p-p38을 80% 억제하였다. 동일 연구에서 퀘르세틴 역시 p-ERK 60%, p-JNK 35%, p-p38 62%의 억제 효과를 나타내었으며, 당화 유도체(glycosylated derivative)인 Q32G가 모화합물(parent compound)보다 우수한 MAPK 억제 활성을 보유함이 입증되었다.38)
T 림프구에서도 감 추출물의 MAPK 조절 효과가 확인되었다. PMACI로 자극된 사람 Jurkat T 림프구에서 감 잎 추출물(50 μg/mL)은 JNK 인산화를 감소시키고 하위 기질인 c-Jun의 인산화를 억제하였다. 동일 조건에서 ERK 및 p38 인산화는 영향을 받지 않아, 감 잎 추출물이 JNK 경로에 대한 선택성을 나타냄이 규명되었다. 이러한 JNK 억제는 T 림프구 활성화 억제 및 아토피 피부염 완화와 연관되었다.32)
한편, 감 다당류는 MAPK 경로를 활성화하여 면역자극 효과를 나타낸다. 발효 감에서 분리한 람노갈락투로난 I (rhamnogalacturonan I; RG-I) 풍부 다당류(FDK-H, 분자량 304 kDa)는 마우스 RAW 264.7 대식세포에서 p-ERK, p-JNK, p-p38의 인산화를 농도 의존적으로 증가시켰다. 이러한 MAPK 활성화는 종양괴사인자(tumor necrosis factor; TNF)-α (7.4배), 인터루킨(interleukin; IL)-6 (9.6배), IL-12 (33.2배)의 생성 증가와 연관되었다.39) 이상의 결과는 감의 저분자 플라보노이드 성분이 MAPK 억제를 통한 항염증 작용을, 고분자 다당류 성분이 MAPK 활성화를 통한 면역자극 작용을 각각 담당함을 시사한다.
사이토카인(cytokine) 조절 – 사이토카인은 면역세포 간 신호전달을 매개하는 단백질로서, 염증 반응의 개시, 유지, 종결에 핵심적인 역할을 수행한다. TNF-α, IL-1β, IL-6 등의 전염증성 사이토카인은 염증 조건에서 과잉 생성 시 만성 염증 및 조직 손상을 초래하므로 억제가 필요한 반면, 감염이 나 종양 등의 면역자극 조건에서는 이들 사이토카인의 적절한 분비가 숙주 방어에 필수적이다. 감 유래 성분들은 이러한 병태생리학적 조건에 따라 사이토카인 생성을 억제하거나 증가시키는 이중 조절 효과를 나타낸다.40)
대식세포에서 감 유래 성분들은 전염증성 사이토카인 분비를 효과적으로 억제한다. 감 잎에서 분리한 트리테르페노이드인 쿠사르산과 베툴리닉산은 LPS로 자극된 RAW 264.7 대식세포에서 TNF-α, IL-6, IL-1β의 분비를 농도 의존적으로 억제하였으며, 이러한 효과는 NF-κB 경로 억제를 통해 매개되었다. 특히 베툴리닉산은 HO-1 유도를 통한 추가적인 항염증 기전을 나타내었다.34) 감 유래 축합형 탄닌의 가수분해물 역시 대식세포에서 염증 유전자의 발현을 직접적으로 억제하는 것으로 확인되었다.41) 감 잎 추출물은 LPS로 자극된 RAW264.7 대식세포에서 IL-6 생성을 억제하였으며, PMACI로 자극된 HMC-1 인간 비만세포에서도 TNF-α 및 IL-6 분비를 유의하게 감소시켰다.42) T 림프구에서도 감 잎 추출물은 PMACI로 자극된 Jurkat 세포에서 IL-2 mRNA 발현을 효과적으로 억제하였으며, 이는 NF-κB 핵 전위 차단 및 JNK 신호전달 억제와 연관되었다.32)
한편, 감 유래 성분들은 면역자극 조건에서 사이토카인 생성을 증가시켜 숙주 면역 기능을 강화한다. 감 잎 유래 다당류는 대식세포에서 사이토카인 분비를 촉진한다. RAW264.7 세포에서 감 잎 다당류(PLE0) 처리는 TNF-α, IL-1β, IL-6의 분비를 농도 의존적으로 증가시켰으며, 100 µg/mL 농도에서 이들 사이토카인 수준은 LPS 처리군과 유사한 수준에 도달하였다. 이러한 사이토카인 분비 증가는 해당 유전자의 mRNA 발현 상향 조절과 연관되어, 다당류가 전사 수준에서 대식세포 활성화를 유도함이 입증되었다.29)
이상의 결과는 감 유래 성분들이 실험 조건 및 면역학적 맥락에 따라 사이토카인 생성을 억제하거나 증가시키는 이중 조절 효과를 나타냄을 보여준다. 트리테르페노이드와 탄닌은 염증 조건에서 전염증성 사이토카인을 억제하는 반면, 다당류와 플라보노이드는 면역자극 조건에서 사이토카인 분비를 촉진하여 숙주 방어에 기여한다.
염증 매개체 억제 – 산화질소(nitric oxide; NO)는 면역 반응 과정에서 생성되어 감염에 대한 방어 기전에 영향을 미치며, 대식세포에서 유도형 산화질소 합성효소(inducible nitric oxide synthase; iNOS)에 의해 합성된다. 프로스타글란딘(prostaglandin) E2 (PGE2)는 아라키돈산(arachidonic acid) 대사 경로를 통해 생성되는 지질 매개체로서 염증 반응을 매개한다. NO 및 PGE2의 과잉 생성은 염증성 질환의 발생과 연관되며, 이들의 생성 억제는 염증 반응 예방에 효과적인 전략이 될 수 있다.42)
감 유래 추출물 및 화합물들은 대식세포에서 NO 생성을 억제하는 것으로 보고되었다. 감 꼭지 추출물은 LPS로 자극된 RAW 264.7 세포에서 NO 생성을 억제하였으며, 미성숙 감 꼭지 추출물이 성숙 단계의 추출물에 비해 더 높은 억제 효과를 나타내었다. 이러한 NO 억제 효과는 iNOS의 mRNA 및 단백질 발현 감소를 동반하였으며, 100 μg/mL 농도에서 iNOS 발현이 현저히 억제되었다.43) 감으로부터 분리된 쿠사릭산 및 베툴리닉산 역시 동일 세포 모델에서 NO 생성을 억제하였으며, iNOS 발현을 mRNA 및 단백질 수준 모두에서 감소시켰다.34)
감 잎 추출물의 항염증 활성도 확인되었다. 감마선 조사 감 잎 추출물은 LPS로 자극된 RAW 264.7 세포에서 NO 및 PGE2 생성을 비조사 추출물에 비해 유의하게 억제하였다. 이러한 결과들은 감 유래 성분들이 NO 및 PGE2를 포함한 염증 매개체 생성을 조절함으로써 항염증 효과를 나타냄을 뒷받침한다.42)
비만세포 활성 억제 – 비만세포(mast cell)는 즉시형 과민 반응(immediate-type hypersensitivity)의 핵심 세포로서, 면역글로불린(immunoglobulin; Ig) E가 고친화성 수용체인 FcεRI에 결합한 후 항원에 의해 교차결합되면 활성화되어 탈과립(degranulation)이 유발된다. 탈과립 과정에서 히스타민(histamine), β-hexosaminidase, 사이토카인 등의 매개체가 방출되며, 이 중 히스타민은 즉시형 과민반응의 가장 중요한 매개체로 알려져 있다.11)
감 유래 추출물은 비만세포의 탈과립을 억제하는 것으로 보고되었다. 감 꼭지 물추출물은 IgE로 감작된 렛트(rat) RBL-2H3 비만세포주 및 일차 배양 복강 비만세포에서 dinitrophenyl-human serum albumin (DNP-HSA) 자극에 의한 히스타민 및 β-hexosaminidase 방출을 농도 의존적으로 억제하였으며, 세포내 칼슘 농도 감소 및 NF-κB 핵 이동 억제가 그 기전으로 확인되었다.11) 감 물추출물 역시 PMACI로 자극된 HMC-1 세포에서 히스타민 방출을 억제하였으며, 이는 cyclic adenosine monophosphate (cAMP) 증가 및 세포내 칼슘 감소와 연관되었다. Activity-guided fractionation을 통해 카테킨이 주요 활성 성분으로 동정되었다.31)
감에서 분리된 개별 화합물의 항알레르기 활성도 보고되었는데, 감 물추출물로부터 활성 유도 분획을 통해 카테킨이 항알레르기 활성 성분으로 동정되었으며, 감 껍질에서 분리된 플라보노이드 배당체인 이소퀘르시트린 및 하이페린(hyperin)은 RBL-2H3 세포에서 항원 자극에 의한 β-hexosaminidase 방출을 용량 의존적으로 억제하고, 세포내 칼슘 상승 및 ROS 생성을 억제하는 것으로 나타났다.44) 이상에서 고찰한 감 유래성분의 주요 면역조절 및 항염증 기전은 Table II에 요약하였다. Table II에 제시된 바와 같이, 저분자 화합물인 플라보노이드와 트리테르페노이드는 주로 NF-κB 및 MAPK 경로 억제를 통해 항염증 효과를 나타내는 반면, 고분자 다당류(FDK-H)는 동일한 MAPK 경로를 활성화하여 면역자극 효과를 유도한다. 이는 성분의 분자량 및 화학적 특성에 따라 면역조절 방향이 결정됨을 의미한다.

Molecular mechanisms of anti-inflammatory and immunomodulatory effects of persimmon (Diospyros kaki)-derived compounds. Low-molecular-weight compounds (flavonoids, triterpenoids) primarily inhibit NF-κB and MAPK pathways, whereas high-molecular-weight polysaccharides activate MAPK signaling for immunostimulation
염증성 질환모델에서의 효과
앞서 고찰한 분자적 기전을 바탕으로, 본 장에서는 감 유래 성분의 효과가 검증된 주요 염증성 질환 모델에서의 연구 결과를 고찰한다.
아토피 피부염(atopic dermatitis, AD) – AD는 심한 소양감, 피부 비후, 홍반 및 습진성 병변을 특징으로 하는 만성 알레르기성 피부 질환이다.45) AD의 병태생리에는 환경 요인, 피부 장벽 기능 이상 및 Th1/Th2 면역반응의 불균형이 복합적으로 관여한다.32) 급성기에는 Th2 반응 우세로 IgE 생성이 증가하고, 만성기에는 Th1 반응이 관여하는 것으로 알려져 있다.45) 현재 치료에 사용되는 국소 스테로이드제는 장기 사용 시 피부 위축 등의 부작용을 유발할 수 있어, 부작용이 적은 천연물 유래 치료제 개발이 요구된다.
NC/Nga 마우스는 일반 사육 환경에서 자연적으로 AD 유사 피부 병변을 발현하는 모델로, 인간 AD와 임상적·조직학적으로 유사한 특성을 나타낸다.46) 이 모델에서 감 잎 추출물 250 mg/kg을 경구 투여한 결과, 피부염 발생과 혈청 IgE 상승이 억제되었으며, 피부 장벽 기능의 지표인 경피수분손실(transepidermal water loss; TEWL)이 용량 의존적으로 감소하였다.47) 활성 성분으로는 플라보노이드인 아스트라갈린이 동정되어, AD 관리를 위한 대체 물질로서의 가능성이 제시되었다.
집 먼지 진드기 추출물(Dermatophagoides farinae extract, DFE)과 2,4-dinitrochlorobenzene (DNCB)으로 유도된 AD 마우스 모델에서 감 꼭지 물추출물의 효과가 평가되었다. 감 꼭지물추출물을 1, 10, 100 mg/kg 용량으로 3주간 경구 투여한 결과, 귀두께, 혈청총 IgE, DFE 특이 IgE 및 히스타민 수준이 감소하였으며, 표피와 진피 두께 및 호산구와 비만세포 침윤이 억제되었다. 기전 연구에서 TNF-α/IFN-γ로 자극된 사람 HaCaT 각질형성세포에서 염증성 사이토카인과 CCL17 발현이 NF-κB 및 signal transducer and activator of transcription (STAT) 1 억제를 통해 감소하였다.45)
감 잎 에탄올 추출물 역시 DNCB와 DFE로 유도된 AD 마우스 모델에서 치료 효과를 나타내었다. 감 잎 추출물 250 mg/kg을 4주간 경구 투여 시, 귀 두께와 혈청 IgE 수준이 현저히 감소하였으며, 비만세포 침윤 억제와 함께 배수 림프절의 크기와 무게가 감소하였다. 귀 조직에서 IL-4, IL-6, IL-13, IL-31 및 thymic stromal lymphopoietin (TSLP)의 mRNA 발현이 감소하였다. 기전적으로 감 잎 추출물은 앞서 기술한 바와 같이 NF-κB 및 JNK 경로를 억제하였다.32)
알레르기성 접촉 피부염 모델에서도 감 잎 추출물의 효과가 확인되었다. 프탈산 무수물(phthalic anhydride; PA)로 유도된 알레르기 마우스 모델에 감 잎 추출물 250 mg/kg을 31일간 경구 투여한 결과, 수동 피부 아나필락시스 반응이 억제되었으며, 귀 부종과 림프절 무게가 감소하였다. 배수 림프절 세포에서 PA 특이 IL-4 생성은 현저히 감소하였으나 IFN-γ에는 영향이 없어 Th2 선택적 억제가 확인되었다.47) 또한 귀 조직에서 thymus and activation-regulated chemokine (CCL17)과 cutaneous T cell-attracting chemokine (CCL27)의 발현이 억제되었다.47)
이상의 연구들을 종합하면, 감의 감 꼭지와 감 잎 추출물은 자연발생 및 유도성 AD 모델 모두에서 피부 병변, 면역글로불린 생성, TEWL, 염증세포 침윤 및 Th2 사이토카인 발현을 효과적으로 억제하였다. 이러한 효과는 NF-κB, STAT1, JNK 신호전달 경로 조절과 Th2 케모카인 억제를 통해 매개되며, 아스트라갈린을 포함한 플라보노이드가 주요 활성 성분으로 작용할 가능성이 제시되었다. 이 결과는 감 추출물이 국소 스테로이드제의 장기 사용에 따른 부작용을 회피할 수 있는 천연물 기반 AD 보조요법제로서 개발 가능성을 지님을 나타내며, 향후 유효 용량 및 투여 기간 최적화를 위한 임상 연구가 필요하다.
궤양성 대장염(ulcerative colitis, UC) – UC는 대장 점막의 만성 염증을 특징으로 하는 염증성 장질환(inflammatory bowel disease; IBD)의 주요 아형으로, 복통, 혈변, 설사 및 체중 감소 등의 임상 증상을 나타낸다.48) UC의 정확한 병인은 완전히 규명되지 않았으나, 유전적 소인, 환경 요인 및 면역학적 요인의 복합적 상호작용이 관여한다.49) 특히 장내미생물 불균형(gut microbiota dysbiosis)은 UC 발병의 핵심적 역할을 담당한다는 증거가 축적되고 있다.50) 건강한 개인과 비교하여 UC 환자에서는 장내미생물의 다양성이 감소하고, Bacteroides 및 Clostridium sub-cluster XIVab의 감소와 함께 유기산 농도의 저하가 관찰된다.48) 장내미생물은 식이섬유를 발효하여 단쇄지방산(short-chain fatty acids; SCFAs)을 생성하며, 부티레이트(butyrate)는 대장 상피세포의 주요 에너지원으로 작용하고 항염증 활성을 나타낸다.49) IBD 환자에서는 부티레이트 생성균인 Faecalibacterium prausnitzii의 감소가 보고되어 있으며, 이러한 SCFA 생성 감소가 점막 염증 반응에 기여하는 것으로 제시된다.49,50)
감 유래 성분의 UC 개선 효과에 관하여, DSS 유도 마우스 대장염 모델에서 감 유래 축합형 타닌의 효과가 평가되었다. 4주간의 타닌 보충 식이 후 DSS를 투여한 결과, 타닌 섭취군에서 질병활성지수(disease activity index; DAI)가 유의하게 감소하고 대장 염증이 완화되었다. 대장 조직 내 IL-1β 및 CXCL1 mRNA 발현이 유의하게 감소하였으며, IL-6 발현은 감소 경향을 보였으나 통계적 유의성에는 도달하지 않았다. 분변 미생물총 분석에서 타닌 보충군은 Bacteroides의 상대적 풍부도가 유의하게 증가하였으며, 대장염 유도 마우스에서 α-다양성(alpha-diversity) 지수가 대조군 대비 높게 나타났다. 또한 IBD 진행과 연관된 Enterobacteriaceae 및 Enterococcus의 확장이 타닌 식이군에서 현저히 억제되었다. 동일 연구의 in vitro 실험에서 타닌 가수분해물은 대식세포의 염증 유전자 발현을 직접적으로 억제하였으며, 이러한 결과는 감 유래 타닌이 장내미생물 조성 변화와 면역 반응 조절을 통해 UC를 개선함을 시사한다.41)
감 잎 유래 플라보노이드인 아스트라갈린의 항염증 효과도 UC 모델에서 확인되었다. DSS 유도 급성 마우스 대장염 모델에서 아스트라갈린은 대장 단축을 완화하고 병리학적 점수를 개선하였다. 기전 연구에서 아스트라갈린은 TNF-α 자극을 받은 인간 대장 상피세포(HCT-116, HT-29)에서 NF-κB 경로를 억제하였으며, 구체적으로 IκBα의 인산화 및 분해를 저해하고 NF-κB의 DNA 결합 활성을 감소시켰다. DSS 처리 대장 점막에서도 인산화 IκBα 수준이 감소하고 IL-6, IL-8 및 TNF-α 생성이 억제되었다.51)
종합하면, 감의 다양한 부위 및 성분은 UC 동물 모델에서 장내미생물 조성의 정상화, SCFA 생성 촉진, 염증성 사이토카인 억제 및 NF-κB 신호전달 경로 조절을 통해 대장 염증을 완화하는 것으로 나타났다. 이러한 연구 결과들은 감 유래 성분이 IBD 치료를 위한 기능성 식품 소재로서 가능성을 지님을 지지한다. 특히 장내미생물 조절과 NF-κB 억제라는 이중 기전은 기존 IBD 치료제와의 병용 또는 유지요법 소재로서의 적용 가능성을 제시하며, UC 환자를 대상으로 한 예비 임상시험이 요구된다.
즉시형 과민반응 – 즉시형(제1형) 과민반응은 감작된 비만세포가 항원에 의해 활성화되어 다양한 염증 매개체를 분비함으로써 유발되는 면역반응이다. 비만세포 표면의 고친화성 IgE 수용체인 FcεRI에 결합된 IgE가 항원에 의해 교차결합되면, 과립 내 저장된 히스타민 및 β-hexosaminidase와 같은 생체활성 아민, leukotriene C4 (LTC4) 및 prostaglandin D2 (PGD2) 등의 아라키돈산 대사산물, 그리고 TNF-α 및 IL-6 등의 염증성 사이토카인이 분비된다.52) 비만세포의 탈과립 과정에서 세포내 cAMP 농도 증가는 매개체 분비를 억제하며, 반대로 세포 외 칼슘의 세포막 통과 유입은 분비 개시에 필수적인 것으로 알려져 있다.53)
감의 즉시형 과민반응 억제 효과는 in vivo 아나필락시스 모델에서 규명되었다. AEDK는 마우스에서 수동 피부 및 전신 아나필락시스 반응을 유의하게 억제하였으며, 그 효과는 임상에서 사용되는 항알레르기 약물인 disodium cromoglycate와 유사한 수준이었다.31) 감 꼭지 추출물의 경구 투여(1-100 mg/kg)는 난알부민 유도 전신 아나필락시스 모델에서 직장 온도 저하를 억제하고 혈청 히스타민, 총 IgE, 난알부민 특이 IgE 및 IL-4 농도를 감소시켰으며, IgE 매개 수동 피부 아나필락시스 모델에서 Evans blue 색소 삼출이 용량 의존적으로 감소하였다.11) 이러한 in vivo 효과의 기전은 앞서 절에서 고찰한 바와 같이 비만세포 내 cAMP 증가, 세포내 칼슘 농도 감소 및 NF-κB 활성 억제와 연관된다.
감 꼭지 추출물 역시 마우스 수동 피부 아나필락시스 모델에서 피부 알레르기 반응을 유의하게 억제하였다. 이 효과는 비만세포 활성화 감소에 기인하며, 히스타민, 염증성 사이토카인 및 프로테아제(protease)의 분비 억제가 관여하는 것으로 확인되었다.11) 이러한 결과들은 감의 과육 및 꼭지 부위 모두 비만세포 매개 즉시형 과민반응에 대한 억제 활성을 가지며, cAMP/칼슘 신호전달 조절 및 NF-κB 억제가 공통적인 작용기전임을 뒷받침한다. 감 추출물이 기존 항알레르기 약물인 disodium cromoglycate와 유사한 효능을 나타낸 점은 식품 알레르기 및 아나필락시스 예방을 위한 기능성 식품 소재로서의 활용 가능성을 뒷받침하며, 알레르기 질환자를 대상으로 한 안전성 및 유효성 평가가 필요하다.
기타 염증 관련 효과 – 급성 염증 반응은 이상성(biphasic) 특성을 나타내며, 초기 단계(0-1시간)에서는 히스타민과 세로토닌(serotonin)이 주요 매개체로 작용하고, 후기 단계(1-4시간)에서는 TNF-α, PGE2, cyclooxygenase (COX)-2가 염증 반응을 지속시킨다.54) 염증 부위에서 iNOS에 의해 생성되는 NO는 혈관 확장과 혈관 투과성 증가를 유발하여 부종 형성에 기여한다.55) 혈관 내피세포의 COX-2에서 합성되는 PGE2는 발열 반응의 필수 매개체로 작용한다.56) 한편, TNF-α, IL-1β, PGE2, 브라디키닌(bradykinin), 신경성장인자(nerve growth factor; NGF) 등의 염증 매개체는 통각수용기(nociceptor)의 민감도와 흥분성을 증가시켜 말초 감작(peripheral sensitization)을 유발하며, 이는 염증성 통증과 통각과민의 주요 기전이 된다.57) 또한 TNF-α는 위점막에서 케모카인(chemokine) 발현을 유도하고 백혈구 침윤을 촉진하여 점막 손상과 궤양 형성에 관여한다.58) Nrf2에 의해 조절되는 HO-1은 헴(heme)을 빌리버딘(biliverdin), 일산화탄소(carbon monoxide; CO), 유리 철로 분해하는 효소로서, 강력한 항산화 및 항염증 작용을 나타내며 대식세포의 M2 표현형 전환을 촉진한다.59)
감의 다양한 부위 추출물은 이러한 염증 경로를 조절하는 것으로 보고되었다. 감 과육 클로로포름 추출물에서 분리된 나프토퀴논(naphthoquinone) 화합물은 카라기난 유발 족부 부종 모델에서 93.98% 및 89.54%의 억제율을 나타내었으며, 히스타민 유발 부종에서도 89.54%의 억제 효과를 보여 염증의 초기 및 후기 단계 모두에서 활성을 나타내었다.60) 감 잎 메탄올 추출물의 수성 분획(200 mg/kg)은 카라기난 유발 족부 부종에서 59.28%의 억제율을 보였다.61)
진통 효과에 있어서 감 잎 물 분획은 tail flick 모델에서 67.74%의 통각 억제율을 나타내었으며, 아세트산(acetic acid) 유발 경련(writhing) 및 핫플레이트(hot plate) 시험에서도 유의한 진통 활성을 보였다.61) 이러한 진통 효과는 COX 억제에 의한 PGE 합성 억제와 관련된 것으로 추정된다. 한편, 감 과육에서 분리된 나프토퀴논은 열 자극 유발 통각 모델에서 용량 의존적으로 잠복 시간을 증가시켜 중추성 진통 효과를 나타내었다.60)
해열 효과와 관련하여, 효모 유발 고열 마우스 모델에서 감 잎 물 분획(200 mg/kg) 투여 시 체온이 38°C에서 120분 후 36.65±0.12°C로 감소하여 정상 체온(35.21±0.29°C)에 근접하였다.61) 위장관 보호 효과도 보고되었는데, 에탄올 유발 위궤양 모델에서 감 과육 추출물은 IL-6, IL-1β, TNF-α 수준을 유의하게 감소시켰으며, caspase-3 및 NF-κB 발현을 억제하여 위점막 보호 효과를 나타내었다.62) 이러한 항염증, 진통, 해열 및 위장관 보호 효과는 앞선 장에서 고찰한 NF-κB 억제, 염증성 사이토카인 및 NO/PGE2 생성 억제 기전과 연관되는 것으로 추정된다.34) 이러한 다양한 항염증 효과는 감 추출물이 비스테로이드성 소염진통제(NSAIDs)의 위장관 부작용을 회피할 수 있는 천연 소염제 후보물질로서 가치를 지님을 나타내며, 특히 만성 통증 및 염증성 질환 관리를 위한 장기 복용 소재로서의 안전성 검증이 요구된다. 이상에서 고찰한 염증성 질환 모델에서의 감 추출물 효과는 Table III에 요약하였다. Table III에서 확인되는 바와 같이, 감잎 및 꼭지 추출물은 알레르기성 질환(AD, 즉시형 과민반응), 위장관 염증(UC, 위궤양), 급성 염증 모델에서 공통적으로 NF-κB 억제 및 염증성 사이토카인 감소를 통해 치료 효과를 나타내었다. 특히 250 mg/kg 용량의 경구 투여가 다수 연구에서 유효 용량으로 확인되어, 향후 용량-반응 관계 연구의 기준점을 제시한다.
면역증강 동물모델에서의 효과
앞서 고찰한 염증성 질환 모델에서의 항염증 효과와 더불어, 감 유래 성은 종양 동물 모델에서 면역계 활성화를 통한 효과를 나타내는 것으로 보고되고 있다. 본 장에서는 감 유래 성분의 면역활성화 기전에 대해 고찰한다.
종양모델에서의 면역증강 효과 – 천연물은 종양 면역요법에서 새로운 치료 전략으로 주목받고 있으며, 다양한 천연물이 면역조절과 항종양 활성을 동시에 나타내는 것으로 알려져 있다.63) 특히 식물 유래 다당류 및 플라보노이드는 상대적으로 낮은 독성과 부작용으로 인해 항암 보조요법제로서의 잠재력이 높이 평가되고 있다.63) 이들 천연물은 대식세포, 자연살해(natural killer; NK) 세포, 수지상세포, T 림프구 및 B 림프구의 활성을 촉진하고, 다양한 사이토카인과 케모카인의 분비를 유도하여 항종양 면역반응을 강화할 수 있다.64) 실제로 영지버섯(Ganoderma lucidum), 구기자(Lycium barbarum), 표고버섯(Lentinus edodes), 용안육(Dimocarpus longan) 등 에서 분리된 다당류-단백질 복합체가 비장세포 증식, 대식세포 식균작용, NK 세포의 종양세포 살해 활성을 촉진하는 것으로 보고되었다.65,66) 이들 다당류는 TNF-α, IL-1β, IFN-γ, IL-2, IL-6 등의 분비를 유도하여 간접적인 항종양 반응을 나타낸다.65)
감 잎에서 분리한 총 플라보노이드(total flavonoids extract from persimmon leaves; PLF)의 항종양 및 면역조절 효과가 H22 간암세포를 이식한 마우스 모델에서 검증되었다. PLF 투여군은 49.35%의 종양 억제율을 나타내었으며, 양성대조군인 사이클로포스파마이드(cyclophosphamide; CTX)와 비교하여 체중 감소나 섭식량 저하 없이 항악액질(anti-cachexia) 효과를 보였다. 면역학적 지표 분석에서 PLF는 흉선 및 비장 지수를 유의하게 증가시켰고, 단핵구/대식세포의 식균작용을 촉진하였으며, 혈청 용혈소(hemolysin) 수준과 NK 세포 활성을 향상시켰다. 또한 혈청 IL-18 농도가 증가하여 세포매개 면역반응의 활성화가 확인되었다.67) 이러한 결과는 PLF가 면역기능 강화를 통해 간암 성장을 억제하는 것으로 해석된다.
감염 모델에서의 면역강화 – 감염성 질환에서 숙주 면역계의 적절한 활성화는 병원체 제거와 질병 회복에 필수적이다. 플라보노이드를 포함한 식물 유래 폴리페놀은 NK 세포와 대식세포 등 선천면역세포의 기능을 조절하여 감염에 대한 방어능을 강화하는 것으로 알려져 있다.68) 특히 프로안토시아니딘은 장내 미생물총 조절을 통해 점막 면역을 강화하고, type-1 IFN 반응 증강을 통해 바이러스 감염에 대한 저항성을 높이는 효과가 보고되었다.69)
감 유래 탄닌의 항감염 면역 효과는 비결핵 항산균 감염 마우스 모델에서 입증되었다. Mycobacterium avium complex (MAC) 감염 BALB/c 마우스에 수용성 감 탄닌을 9주간 식이로 공급한 결과, 폐 내 MAC 균 수가 유의하게 감소하고 폐 육아종 형성이 억제되었다.70) 폐 조직에서 TNF-α와 iNOS 발현이 대조군 대비 유의하게 감소하였으며, 수용성 탄닌 가수분해물의 대조군 대비 산소 라디칼 흡수능(oxygen radical absorbance capacity; ORAC) 값은 비가수분해 탄닌 분말 대비 약 5배 높았다.70) In vitro에서 MAC에 대한 정균 활성은 가수분해물에서만 관찰되어, 탄닌이 장내 미생물에 의해 저분자로 분해된 후 흡수되어 전신적 항균 효과를 나타낼 수 있는 것으로 해석된다.
세포 수준에서 감 유래 성분의 항감염 기전도 보고되었다. 아스트라갈린은 감잎에서 분리되는 플라보노이드 배당체로, Escherichia coli 감염으로 유도된 양 자궁내막 상피세포에서 염증 반응 완화 효과가 확인되었다. 이러한 효과는 그람음성균의 주요 병원성 인자인 LPS에 의한 TLR4/NF-κB 신호경로 활성화 억제를 통해 나타났으며, 염증성 사이토카인 분비가 유의하게 감소하였다.71)
LPS 유발 급성 면역 반응 모델에서 탄닌의 면역글로린 생성 촉진 효과도 밝혀졌다. 성장기 돼지에 탄닌을 포함한 과일 부산물 추출물을 6주간 식이 공급한 후 E. coli LPS (100 µg/kg 체중)를 투여하여 급성 면역 반응을 유도한 결과, 탄닌 투여군에서 혈중 IgM, IgG, IgA 농도가 대조군 대비 유의하게 증가하였다. 이는 탄닌이 체액성 면역 반응을 강화함을 의미한다. 점막 면역 측면에서, 한국산 감식초 다당류를 경구 투여한 마우스에서 소장액 내 IgA 농도가 유의하게 증가하였으며, in vitro에서 소장 Peyer's patch 세포에 동일 다당류를 처리한 경우에도 IgA 분비가 용량 의존적으로 증가하였다.72) IgA는 점막 표면에서 병원체의 부착과 침입을 방어하는 핵심 면역글로불린으로, 감 유래 다당류가 장점막 면역 강화에 기여할 수 있음을 말한다. 이상에서 고찰한 감 유래 성분의 항염증 경로와 면역활성화 경로의 이중 조절 기전은 Fig. 2에 도식화하였다. Fig. 2의 좌측 패널에서 보는 바와 같이 플라보노이드와 트리테르페노이드는 NF-κB 신호전달 억제를 통해 염증 매개체 생성을 감소시키며, 우측 패널에서는 다당류와 탄닌이 TLR2-MAPK 경로 활성화를 통해 대식세포 기능과 면역글로불린 생성을 증강시킨다. 이러한 이중 기전은 감이 염증성 질환과 면역저하 상태 모두에 적용 가능한 양방향 면역조절 소재임을 나타낸다.
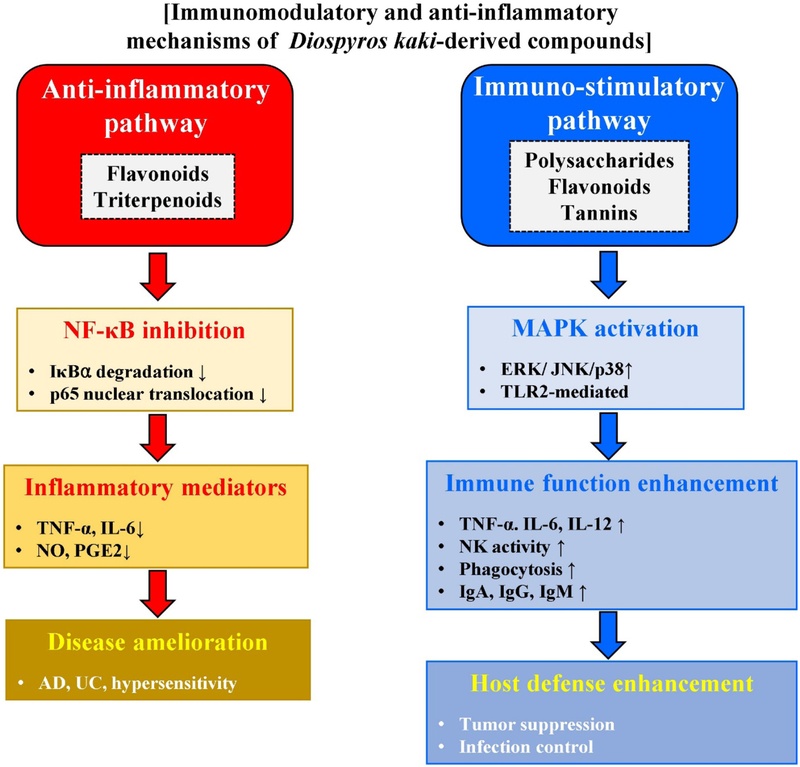
Schematic diagram of dual immunomodulatory mechanisms of Diospyros kaki-derived components illustrating the bidirectional regulation of immune responses. Left panel (red): Anti-inflammatory pathway—flavonoids and triterpenoids suppress IκBα degradation and p65 nuclear translocation, thereby inhibiting NF-κB signaling and reducing pro-inflammatory cytokines (TNF-α, IL-6) and mediators (NO, PGE2). This pathway is relevant to AD, UC, and hypersensitivity. Right panel (blue): Immunostimulatory pathway—polysaccharides and tannins activate TLR2-mediated MAPK (ERK/JNK/p38) signaling, enhancing macrophage phagocytosis, NK cell activity, and immunoglobulin production for host defense against tumors and infections. NF-κB, nuclear factor-kappa B; IκBα, inhibitor of NF-κB alpha; MAPK, mitogen-activated protein kinase; ERK, extracellular signal-regulated kinase; JNK, c-Jun N-terminal kinase; TLR2, Toll-like receptor 2; TNF-α, tumor necrosis factor-alpha; IL, interleukin; NO, nitric oxide; PGE2, prostaglandin E2; AD, atopic dermatitis; UC, ulcerative colitis; NK, natural killer; Ig, immunoglobulin.
결 론
본 종설에서는 감의 선천면역활성화 및 항염증 기전에 관한 최신 연구 동향을 고찰하였다. 감의 다양한 부위에는 축합형 탄닌, 플라보놀, 카로티노이드, 다당류 등의 생리활성 성분이 함유되어 있으며, 이들은 품종, 부위, 성숙 단계에 따라 함량 및 조성이 상이하다. 분자적 기전 측면에서, 감 유래 플라보노이드 및 트리테르페노이드는 IκBα 분해 억제 및 NF-κB p65 핵 이동 차단을 통해 NF-κB 신호전달을 억제하고, MAPK 경로의 인산화를 조절하며, TNF-α, IL-6, IL-1β 등 전염증성 사이토카인과 NO, PGE2 등 염증 매개체의 생성을 감소시킨다. 반면, 감 유래 다당류는 MAPK 활성화 및 사이토카인 분비 촉진을 통해 대식세포를 활성화시키는 면역자극 효과를 나타낸다. 이러한 이중 조절 효과는 감이 병태생리학적 상황에 따라 면역 균형 유지에 기여할 수 있음을 의미한다. 질환 모델에서 감 추출물은 아토피 피부염, 궤양성 대장염, 즉시형 과민반응 등 다양한 염증성 질환에서 치료 효과를 나타내었다. 또한 종양 및 감염 동물모델에서 감 유래 플라보노이드와 탄닌은 흉선 및 비장 지수 증가, NK 세포 활성 및 대식세포 식균작용 촉진, 혈청 면역글로불린 농도 상승을 통해 숙주 면역 기능을 강화하는 것으로 구명되었다. 그러나 현재까지의 연구는 대부분 세포 및 동물 모델에 국한되어 있어, 향후 임상적 유효성 및 안전성 검증을 위한 인체 적용 연구가 필요하다. 또한 감 품종 및 부위에 따른 활성 성분의 차이가 약리 효과에 미치는 영향에 대한 체계적인 비교 연구가 요구된다. 결론적으로, 감은 플라보노이드 및 트리테르페노이드에 의한 항염증 효과와 다당류에 의한 면역증강 효과를 동시에 나타내는 면역조절의 이중성을 보유하며, 이러한 특성은 병태생리학적 상황에 따른 맞춤형 면역조절 소재로서의 가능성을 제시한다. 본 종설이 향후 관련 연구의 기초 자료로 활용되기를 기대한다.
References
-
Choudhary, R., Singh, A., Upadhyay, A., Singh, R., Thangalakshmi, S., Dar, A. H., Bajpai, V. K. and Shukla, S. (2022) Exotic god fruit, persimmon (Diospyros kaki): Pharmacological importance and human health aspects. eFood 4: e52.
[https://doi.org/10.1002/efd2.52]

- Butt, M. S., Sultan, M. T., Aziz, M., Naz, A., Ahmed, W., Kumar, N. and Imran, M. (2015) Persimmon (Diospyros kaki) fruit: hidden phytochemicals and health claims. EXCLI J. 14: 542-561.
-
El-Baz, E. and Lo'ay, A. A. (2011) Vitamins application and persimmon (Diospyros kaki L. cv ’Costata’), fruit quality. J. Plant Prod. 2: 367-375.
[https://doi.org/10.21608/jpp.2011.85570]

-
Devashish, T., Mukesh, K. M. and Madhusudan, T. (2023) Marketing cost, producer's share, and marketing efficiency in different marketing channels of persimmon crop in Kullu district of Himachal Pradesh. Asian J. Agric. Ext. Econ. Sociol. 41: 209 216.
[https://doi.org/10.9734/ajaees/2023/v41i81998]

-
Kim, I.-D., Dhungana, S. K., Chae, Y.-G., Son, N.-K. and Shin, D.-H. (2016) Quality characteristics of ‘Dongchul’ persimmon (Diospyros kaki Thunb.) fruit grown in Gangwondo, Korea. Korean J. Plant Res. 29: 313-321.
[https://doi.org/10.7732/kjpr.2016.29.3.313]

-
Fukai, S., Tanimoto, S., Maeda, A., Fukuda, H., Okada, Y. and Nomura, M. (2009) Pharmacological activity of compounds extracted from persimmon peel (Diospyros kaki THUNB.). J. Oleo. Sci. 58: 213-219.
[https://doi.org/10.5650/jos.58.213]

-
Yoshimura, M., Mochizuki, A. and Amakura, Y. (2021) Identification of phenolic constituents and inhibitory activity of persimmon Calyx and Shiteito against tumor cell proliferation. Chem. Pharm. Bull. 69: 32-39.
[https://doi.org/10.1248/cpb.c20-00259]

-
Kang, Y. M., Choi, J. E., Komakech, R., Park, J. H., Kim, D. W., Cho, K. M., Kang, S. M., Choi, S. H., Song, K. C., Ryu, C. M., Lee, K. C. and Lee, J. S. (2017) Characterization of a novel yeast species Metschnikowia persimmonesis KCTC 12991BP (KIOM G15050 type strain) isolated from a medicinal plant, Korean persimmon calyx (Diospyros kaki Thumb). AMB Express 7: 199.
[https://doi.org/10.1186/s13568-017-0503-1]

-
Bei, W., Zang, L., Guo, J., Peng, W., Xu, A., Good, D. A., Hu, Y., Wu, W., Hu, D., Zhu, X., Wei, M. and Li, C. (2009) Neuroprotective effects of a standardized flavonoid extract from Diospyros kaki leaves. J. Ethnopharmacol. 126: 134-142.
[https://doi.org/10.1016/j.jep.2009.07.034]

-
Lee, S. G., Jung, J. Y., Shin, J. S., Shin, K. S., Cho, C. W., Rhee, Y. K., Hong, H. D. and Lee, K. T. (2015) Immunostimulatory polysaccharide isolated from the leaves of Diospyros kaki Thumb modulate macrophage via TLR2. Int. J. Biol. Macromol. 79: 971-982.
[https://doi.org/10.1016/j.ijbiomac.2015.06.023]

-
Kim, M. J., Park, H. R., Shin, T. Y. and Kim, S. H. (2017) Diospyros kaki calyx inhibits immediate-type hypersensitivity via the reduction of mast cell activation. Pharm. Biol. 55: 1946-1953.
[https://doi.org/10.1080/13880209.2017.1354386]

-
Amorim, C., Antoniolli, L. R., Orsi, B. and Kluge, R. A. (2023) Advances in metabolism and genetic control of astringency in persimmon (Diospyros kaki Thunb.) fruit: A review. Sci. Hortic. 308: 111561.
[https://doi.org/10.1016/j.scienta.2022.111561]

-
Akagi, T., Suzuki, Y., Ikegami, A., Kamitakahara, H., Takano, T., Nakatsubo, F. and Yonemori, K. (2010) Condensed tannin composition analysis in persimmon (Diospyros kaki Thunb.) fruit by acid catalysis in the presence of excess phloroglucinol. J. Japan Soc. Hort. Sci. 79: 275-281.
[https://doi.org/10.2503/jjshs1.79.275]

-
Li, C., Leverence, R., Trombley, J. D., Xu, S., Yang, J., Tian, Y., Reed, J. D. and Hagerman, A. E. (2010) High molecular weight persimmon (Diospyros kaki L.) proanthocyanidin: a highly galloylated, A-linked tannin with an unusual flavonol terminal unit, myricetin. J. Agric. Food Chem. 58: 9033-9042.
[https://doi.org/10.1021/jf102552b]

-
Sattar, A., Bibi, N. and Chaudry, M. A. (1992) Phenolic compounds in persimmon during maturation and on-tree ripening. Nahrung 36: 466-472.
[https://doi.org/10.1002/food.19920360507]

-
Persic, M., Jakopic, J. and Hudina, M. (2019) The effect of post-harvest technologies on selected metabolites in persimmon (Diospyros kaki Thunb.) fruit. J. Sci. Food Agric. 99: 854-860.
[https://doi.org/10.1002/jsfa.9255]

-
Tian, Y., Zou, B., Li, C.-m., Yang, J., Xu, S.-f. and Hagerman, A. E. (2012) High molecular weight persimmon tannin is a potent antioxidant both ex vivo and in vivo. Food Res. Int. 45: 26-30.
[https://doi.org/10.1016/j.foodres.2011.10.005]

-
Matsumoto, K., Kadowaki, A., Ozaki, N., Takenaka, M., Ono, H., Yokoyama, S. and Gato, N. (2011) Bile acid-binding ability of kaki-tannin from young fruits of persimmon (Diospyros kaki) in vitro and in vivo. Phytother. Res. 25: 624-628.
[https://doi.org/10.1002/ptr.3306]

-
Xue, Y.-L., Miyakawa, T., Hayashi, Y., Okamoto, K., Hu, F., Mitani, N., Furihata, K., Sawano, Y. and Tanokura, M. (2011) Isolation and tyrosinase inhibitory effects of polyphenols from the leaves of persimmon, Diospyros kaki. J. Agric. Food Chem. 59: 6011-6017.
[https://doi.org/10.1021/jf200940h]

-
Hossain, A., Moon, H. K. and Kim, J. K. (2018) Antioxidant properties of Korean major persimmon (Diospyros kaki) leaves. Food Sci. Biotechnol. 27: 177-184.
[https://doi.org/10.1007/s10068-017-0195-y]

-
Kwon, J., Park, J.-E., Lee, J.-S., Lee, J.-H., Hwang, H., Jung, S.-H., Kwon, H.-C. and Jang, D.-S. (2021) Chemical constituents of the leaves of Diospyros kaki (persimmon). Plants 10: 2032.
[https://doi.org/10.3390/plants10102032]

-
Zaghdoudi, K., Ngomo, O., Vanderesse, R., Arnoux, P., Myrzakhmetov, B., Frochot, C. and Guiavarc’h, Y. (2017) Extraction, identification and photo-physical characterization of persimmon (Diospyros kaki L.) carotenoids. Foods 6: 4.
[https://doi.org/10.3390/foods6010004]

-
de Ancos, B., Gonzalez, E. and Cano, M. P. (2000) Effect of high-pressure treatment on the carotenoid composition and the radical scavenging activity of persimmon fruit purees. J. Agric. Food Chem. 48: 3542-3548.
[https://doi.org/10.1021/jf990911w]

-
Zhou, C., Zhao, D., Sheng, Y., Tao, J. and Yang, Y. (2011) Carotenoids in fruits of different persimmon cultivars. Molecules 16: 624-636.
[https://doi.org/10.3390/molecules16010624]

-
García-Cayuela, T., Nuño-Escobar, B., Welti-Chanes, J. and Cano, M. P. (2018) In vitro bioaccessibility of individual carotenoids from persimmon (Diospyros kaki, cv. Rojo Brillante) used as an ingredient in a model dairy food. J. Sci. Food Agric. 98: 3246-3254.
[https://doi.org/10.1002/jsfa.8827]

-
Duan, J., Zheng, Y., Dong, Q. and Fang, J. (2004) Structural analysis of a pectic polysaccharide from the leaves of Diospyros kaki. Phytochemistry 65: 609-615.
[https://doi.org/10.1016/j.phytochem.2003.12.002]

-
Lu, X., Mo, X., Guo, H. and Zhang, Y. (2012) Sulfation modification and anticoagulant activity of the polysaccharides obtained from persimmon (Diospyros kaki L.) fruits. Int. J. Biol. Macromol. 51: 1189-1195.
[https://doi.org/10.1016/j.ijbiomac.2012.08.028]

-
Hwang, K. C., Shin, H. Y., Kim, W. J., Seo, M. S. and Kim, H. (2021) Effects of a high-molecular-weight polysaccharides isolated from Korean persimmon on the antioxidant, anti-inflammatory, and antiwrinkle activity. Molecules 26: 1600.
[https://doi.org/10.3390/molecules26061600]

-
Song, Y.-R., Han, A.-R., Lim, T.-G., Kang, J.-H. and Hong, H.-D. (2019) Discrimination of structural and immunological features of polysaccharides from persimmon leaves at different maturity stages. Molecules 24: 356.
[https://doi.org/10.3390/molecules24020356]

-
Ghosh, S. and Hayden, M. S. (2012) Celebrating 25 years of NF-κB research. Immunol. Rev. 246: 5-13.
[https://doi.org/10.1111/j.1600-065X.2012.01111.x]

-
Kim, H. H., Kim, D. S., Kim, S. W., Lim, S. H., Kim, D. K., Shin, T. Y. and Kim, S. H. (2013) Inhibitory effects of Diospyros kaki in a model of allergic inflammation: role of cAMP, calcium and nuclear factor-κB. Int. J. Mol. Med. 32: 945-951.
[https://doi.org/10.3892/ijmm.2013.1465]

-
Lee, H. S., Kim, E. N., Kim, G. R. and Jeong, G. S. (2021) Persimmon leaf extract protects mice from atopic dermatitis by inhibiting T cell activation via regulation of the JNK pathway. Phytother. Res. 35: 2545-2556.
[https://doi.org/10.1002/ptr.6985]

-
Sun, L., Zhang, J., Fang, K., Ding, Y., Zhang, L. and Zhang, Y. (2014) Flavonoids from persimmon (Diospyros kaki) leaves (FPL) attenuate H2O2-induced apoptosis in MC3T3-E1 cells via the NF-κB pathway. Food Funct. 5: 471-479.
[https://doi.org/10.1039/c3fo60522a]

-
Kim, K. S., Lee, D. S., Kim, D. C., Yoon, C. S., Ko, W., Oh, H. and Kim, Y. C. (2016) Anti-inflammatory effects and mechanisms of action of coussaric and betulinic acids isolated from Diospyros kaki in lipopolysaccharide-stimulated RAW 264.7 macrophages. Molecules 21: 1206.
[https://doi.org/10.3390/molecules21091206]

-
Jiang, A., Craxton, A., Kurosaki, T. and Clark, E. A. (1998) Different protein tyrosine kinases are required for B cell antigen receptor-mediated activation of extracellular signal-regulated kinase, c-Jun NH2-terminal kinase 1, and p38 mitogen-activated protein kinase. J. Exp. Med. 188: 1297-1306.
[https://doi.org/10.1084/jem.188.7.1297]

-
Lanna, A., Gomes, D. C., Muller-Durovic, B., McDonnell, T., Escors, D., Gilroy, D. W., Lee, J. H., Karin, M. and Akbar, A. N. (2017) A sestrin-dependent Erk-Jnk-p38 MAPK activation complex inhibits immunity during aging. Nat. Immunol. 18: 354-363.
[https://doi.org/10.1038/ni.3665]

-
Zhou, Y., Takano, T., Li, X., Wang, Y., Wang, R., Zhu, Z., Tanokura, M., Miyakawa, T. and Hachimura, S. (2022) β-elemene regulates M1-M2 macrophage balance through the ERK/JNK/P38 MAPK signaling pathway. Commun. Biol. 5: 519.
[https://doi.org/10.1038/s42003-022-03369-x]

-
Cho, Y.-H., Kim, N.-H., Khan, I., Yu, J. M., Jung, H. G., Kim, H. H., Jang, J. Y., Kim, H. J., Kim, D.-i., Kwak, J.-H., Kang, S. C. and An, B. J. (2016) Anti-inflammatory potential of quercetin-3-O-β-D-(“2”-galloyl)-glucopyranoside and quercetin isolated from Diospyros kaki calyx via suppression of MAP signaling molecules in LPS-induced RAW 264.7 macrophages. J. Food Sci. 81: C2447-C2456.
[https://doi.org/10.1111/1750-3841.13497]

-
Shin, H. Y., Hwang, K. C., Mi, X.-J., Moon, S.-K., Kim, Y.-J. and Kim, H. (2022) Rhamnogalacturonan I-rich polysaccharide isolated from fermented persimmon fruit increases macrophage-stimulatory activity by activating MAPK and NF-κB signaling. J. Sci. Food Agric. 102: 2846-2854.
[https://doi.org/10.1002/jsfa.11625]

-
Chen, S., Saeed, A., Liu, Q., Jiang, Q., Xu, H., Xiao, G. G., Rao, L. and Duo, Y. (2023) Macrophages in immunoregulation and therapeutics. Signal Transduct. Target Ther. 8: 207.
[https://doi.org/10.1038/s41392-023-01452-1]

-
Kitabatake, M., Matsumura, Y., Ouji-Sageshima, N., Nishioka, T., Hara, A., Kayano, S. I. and Ito, T. (2021) Persimmon-derived tannin ameliorates the pathogenesis of ulcerative colitis in a murine model through inhibition of the inflammatory response and alteration of microbiota. Sci. Rep. 11: 7286.
[https://doi.org/10.1038/s41598-021-86608-1]

-
Cho, B. O., Nchang Che, D., Yin, H. H. and Jang, S. I. (2017) Enhanced biological activities of gamma-irradiated persimmon leaf extract. J. Radiat. Res. 58: 647-653.
[https://doi.org/10.1093/jrr/rrx013]

-
Choi, J., Kim, M. J., Komakech, R., Jung, H. and Kang, Y. (2019) Anti-inflammatory activities of astringent persimmons (Diospyros kaki Thunb.) stalks of various cultivar types based on the stages of maturity in the Gyeongnam province. BMC Complement. Altern. Med. 19: 262.
[https://doi.org/10.1186/s12906-019-2659-5]

-
Itoh, T., Ohguchi, K., Nakajima, C., Oyama, M., Iinuma, M., Nozawa, Y., Akao, Y. and Ito, M. (2011) Inhibitory effects of flavonoid glycosides isolated from the peel of Japanese persimmon (Diospyros kaki Fuyu) on antigen-stimulated degranulation in rat basophilic leukaemia RBL-2H3 cells. Food Chem. 126: 289-294.
[https://doi.org/10.1016/j.foodchem.2010.10.058]

-
Yu, J. H., Jin, M., Choi, Y. A., Jeong, N. H., Park, J. S., Shin, T. Y. and Kim, S. H. (2017) Suppressive effect of an aqueous extract of Diospyros kaki calyx on dust mite extract/2,4-dinitrochlorobenzene-induced atopic dermatitis-like skin lesions. Int. J. Mol. Med. 40: 505-511.
[https://doi.org/10.3892/ijmm.2017.3017]

-
Sumiyoshi, K., Nakao, A., Ushio, H., Mitsuishi, K., Okumura, K., Tsuboi, R., Ra, C. and Ogawa, H. (2002) Transforming growth factor-beta1 suppresses atopic dermatitis-like skin lesions in NC/Nga mice. Clin. Exp. Allergy 32: 309-314.
[https://doi.org/10.1046/j.1365-2222.2002.01221.x]

-
Mok, J. Y., Jeon, I. H., Cho, J. K., Park, J. M., Kim, H. S., Kang, H. J., Kim, H. S. and Jang, S. I. (2012) Effect of persimmon leaf extract on phthalic anhydride-induced allergic response in mice. Prev. Nutr. Food Sci. 17: 14-21.
[https://doi.org/10.3746/pnf.2012.17.1.014]

-
Guo, X. Y., Liu, X. J. and Hao, J. Y. (2020) Gut microbiota in ulcerative colitis: insights on pathogenesis and treatment. J. Dig. Dis. 21: 147-159.
[https://doi.org/10.1111/1751-2980.12849]

-
Zhang, M., Sun, K., Wu, Y., Yang, Y., Tso, P. and Wu, Z. (2017) Interactions between intestinal microbiota and host immune Response in inflammatory bowel disease. Front. Immunol. 8: 942.
[https://doi.org/10.3389/fimmu.2017.00942]

-
Zakerska-Banaszak, O., Tomczak, H., Gabryel, M., Baturo, A., Wolko, L., Michalak, M., Malinska, N., Mankowska-Wierzbicka, D., Eder, P., Dobrowolska, A., Slomski, R. and Skrzypczak-Zielinska, M. (2021) Dysbiosis of gut microbiota in Polish patients with ulcerative colitis: a pilot study. Sci. Rep. 11: 2166.
[https://doi.org/10.1038/s41598-021-81628-3]

-
Han, Y. M., Koh, J., Kim, J. H., Lee, J., Im, J. P. and Kim, J. S. (2021) Astragalin inhibits nuclear factor-κB signaling in human colonic epithelial cells and attenuates experimental colitis in mice. Gut Liver 15: 100-108.
[https://doi.org/10.5009/gnl19268]

-
Malaviya, R., Zhu, D., Dibirdik, I. and Uckun, F. M. (1999) Targeting Janus kinase 3 in mast cells prevents immediate hypersensitivity reactions and anaphylaxis. J. Biol. Chem. 274: 27028-27038.
[https://doi.org/10.1074/jbc.274.38.27028]

-
Elieh Ali Komi, D., Wöhrl, S. and Bielory, L. (2020) Mast cell biology at molecular level: a comprehensive review. Clin. Rev. Allergy Immunol. 58: 342-365.
[https://doi.org/10.1007/s12016-019-08769-2]

-
Nathulal, D. A., Acharya, R. and Nariya, M. B. (2022) Anti-inflammatory activity of Atavijambira (Atalantia monophylla DC.) root and stem. Ayu. 43: 105-108.
[https://doi.org/10.4103/ayu.ayu_118_21]

-
Zhang, Z., Chen, X., Chen, H., Wang, L., Liang, J., Luo, D., Liu, Y., Yang, H., Li, Y., Xie, J. and Su, Z. (2016) Anti-inflammatory activity of β-patchoulene isolated from patchouli oil in mice. Eur. J. Pharmacol. 781: 229-238.
[https://doi.org/10.1016/j.ejphar.2016.04.028]

-
Simmons, D. L., Wagner, D. and Westover, K. (2000) Non-steroidal anti-inflammatory drugs, acetaminophen, cyclooxygenase 2, and fever. Clin. Infect. Dis. 31 Suppl 5: S211-218.
[https://doi.org/10.1086/317517]

-
Gold, M. S. and Gebhart, G. F. (2010) Nociceptor sensitization in pain pathogenesis. Nat. Med. 16: 1248-1257.
[https://doi.org/10.1038/nm.2235]

-
Watanabe, T., Higuchi, K., Hamaguchi, M., Shiba, M., Tominaga, K., Fujiwara, Y., Matsumoto, T. and Arakawa, T. (2004) Monocyte chemotactic protein-1 regulates leukocyte recruitment during gastric ulcer recurrence induced by tumor necrosis factor-alpha. Am. J. Physiol. Gastrointest. Liver Physiol. 287: G919-928.
[https://doi.org/10.1152/ajpgi.00372.2003]

-
Saha, S., Buttari, B., Panieri, E., Profumo, E. and Saso, L. (2020) An overview of Nrf2 signaling pathway and its role in inflammation. Molecules 25: 5474.
[https://doi.org/10.3390/molecules25225474]

-
Bawazeer, S. and Rauf, A. (2021) In vivo anti-inflammatory, analgesic, and sedative studies of the extract and naphthoquinone isolated from Diospyros kaki (persimmon). ACS Omega 6: 9852-9856.
[https://doi.org/10.1021/acsomega.1c00537]

-
Shahat, A. A., Alqahtani, A. S., Ullah, R., Al-Mishari, A. and Ahmed, W. S. (2020) Anti-inflammatory, antipyretic and analgesic activities of persimmon (Diospyros kaki) leaves in animal model. Int. J. Agric. Res. 54: 1000-1005.
[https://doi.org/10.18805/ijar.B-1170]

-
Güler, M. C., Tanyeli, A., Eraslan, E., Bozhüyük, M. R., Ekinci Akdemir, F. N., Toktay, E., Kurt, N., Çapanoğlu Güven, E. and Özkan, G. (2021) Persimmon (Diospyros Kaki L.) alleviates ethanol-induced gastric ulcer in rats. South Clin. Ist. Euras. 32: 1-7.
[https://doi.org/10.14744/scie.2020.94546]

-
Nuzzo, G., Senese, G., Gallo, C., Albiani, F., Romano, L., d'Ippolito, G., Manzo, E. and Fontana, A. (2022) Antitumor potential of immunomodulatory natural products. Mar. Drugs 20: 386.
[https://doi.org/10.3390/md20060386]

-
Xu, Q., Cheng, W., Wei, J., Ou, Y., Xiao, X. and Jia, Y. (2023) Synergist for antitumor therapy: Astragalus polysaccharides acting on immune microenvironment. Discov. Oncol. 14: 179.
[https://doi.org/10.1007/s12672-023-00798-w]

-
Leung, M. Y., Liu, C., Zhu, L. F., Hui, Y. Z., Yu, B. and Fung, K. P. (2004) Chemical and biological characterization of a polysaccharide biological response modifier from Aloe vera L. var. chinensis (Haw.) Berg. Glycobiology 14: 501-510.
[https://doi.org/10.1093/glycob/cwh050]

-
Yi, Y., Liao, S.-T., Zhang, M.-W., Zhang, R.-F., Deng, Y.-Y., Yang, B. and Wei, Z.-C. (2011) Immunomodulatory activity of polysaccharide-protein complex of longan (Dimocarpus longan Lour.) pulp. Molecules 16: 10324-10336.
[https://doi.org/10.3390/molecules161210324]

-
Chen, L., Wei, Y., Zhao, S., Zhang, M., Yan, X., Gao, X., Li, J., Gao, Y., Zhang, A. and Gao, Y. (2018) Antitumor and immunomodulatory activities of total flavonoids extract from persimmon leaves in H(22) liver tumor-bearing mice. Sci. Rep. 8: 10523.
[https://doi.org/10.1038/s41598-018-28440-8]

-
Han, L., Fu, Q., Deng, C., Luo, L., Xiang, T. and Zhao, H. (2022) Immunomodulatory potential of flavonoids for the treatment of autoimmune diseases and tumour. Scand. J. Immunol. 95: e13106.
[https://doi.org/10.1111/sji.13106]

-
Andersen-Civil, A. I. S., Arora, P. and Williams, A. R. (2021) Regulation of enteric infection and immunity by dietary proanthocyanidins. Front. Immunol. 12: 637603.
[https://doi.org/10.3389/fimmu.2021.637603]

-
Matsumura, Y., Kitabatake, M., Ouji-Sageshima, N., Yasui, S., Mochida, N., Nakano, R., Kasahara, K., Tomoda, K., Yano, H., Kayano, S. I. and Ito, T. (2017) Persimmon-derived tannin has bacteriostatic and anti-inflammatory activity in a murine model of Mycobacterium avium complex (MAC) disease. PLoS One 12: e0183489.
[https://doi.org/10.1371/journal.pone.0183489]

-
Hu, X., Wang, M., Pan, Y., Xie, Y., Han, J., Zhang, X., Niayale, R., He, H., Li, Q., Zhao, T., Cui, Y. and Yu, S. (2020) Anti-inflammatory effect of astragalin and chlorogenic acid on Escherichia coli-Induced inflammation of sheep endometrial epithelium cells. Front. Vet. Sci. 7: 201.
[https://doi.org/10.3389/fvets.2020.00201]

-
Du, H., Xing, Y., Xu, Y., Jin, X., Yan, S. and Shi, B. (2023) Dietary Artemisia ordosica polysaccharide enhances spleen and intestinal immune response of broiler chickens. Biology 12: 1390.
[https://doi.org/10.3390/biology12111390]
