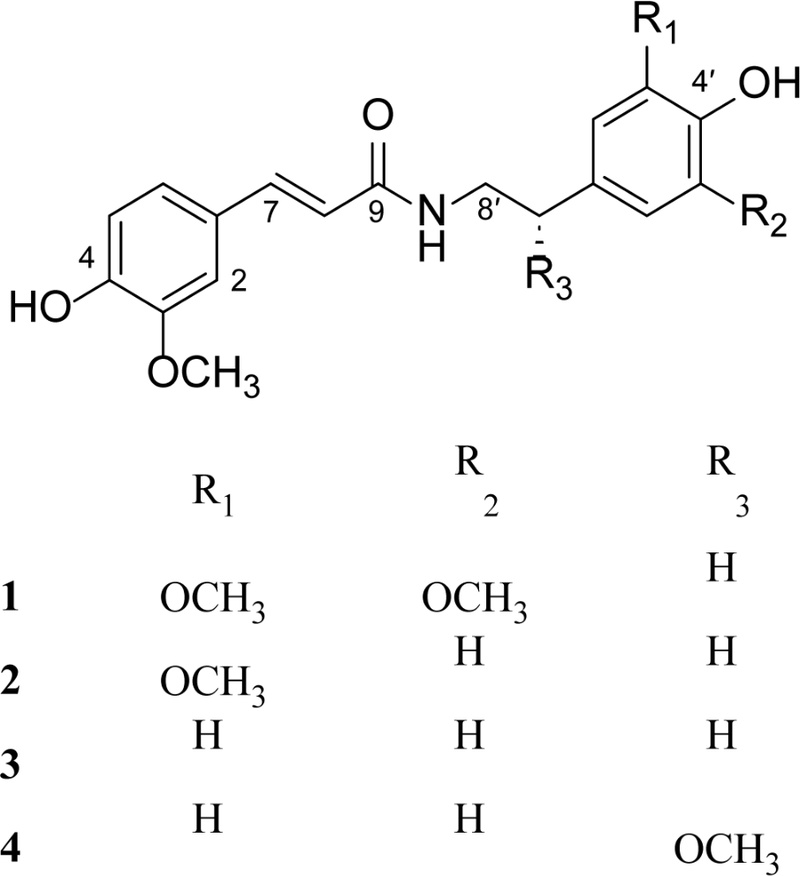
비트(Beta vulgaris)로부터 acid amide 성분의 분리 및 in silico 분석
Abstract
Beta vulgaris L. (Amaranthaceae), commonly known as beetroot, is distributed across regions of the Americas, Europe, and Asia and is rich in diverse phytochemicals such as betalains, flavonoids, polyphenols, and saponins. These metabolites have been associated with a broad spectrum of biological effects, including regulation of lipid metabolism, anti-inflammatory effects, prevention of cardiovascular diseases and diabetes. As part of our ongoing efforts to discover compounds with novel pharmacological potential, the roots of B. vulgaris were investigated. This study led to the isolation of four feruloyl amide derivatives from the EtOAc fraction: N-trans-hibiscusamide (1), N-trans-feruloylhomovanillylamine (2), N-trans-feruloyltyramine (3), and S-(−)-3-(4-hydroxy-3-methoxyphenyl)-N-[2-(4-hydroxy-phenyl)-methoxyethyl]acrylamide (4). Their chemical structures were identified through comprehensive spectroscopic analyses, such as 1D/2D NMR and LC-MS analyses. Among the isolates, compounds 1 and 4 were isolated from B. vulgaris for the first time. Moreover, in silico molecular docking simulation revealed that all of the compounds exhibited stronger binding affinities toward PPAR-α than the control ligand, highlighting their potential as promising PPAR-α agonists.
Keywords:
Beta vulgaris, Feruloyl amide, Molecular docking simulation, PPAR-αBeta 속은 분류학적으로 비름과(Amaranthaceae)에 속하는 식물군으로, 과거 분류체계에서는 명아주아과(Chenopodiaceae)에 포함되기도 하였다. 비름과는 약 165개 속과 2,050종 이상의 식물을 포함하는 비교적 큰 과이며, 그 가운데 Beta 속은 재배종과 야생종을 모두 갖는 중요한 분류군으로 알려져 있다.1-3) Beta 속은 크게 B. vulgaris, B. maritima, B. adanensis의 세 아군으로 구분되며, 이 중 B. maritima (sea beet)는 재배용 beet류의 조상종으로 인정된다.4) 재배 형태의 Beta는 주요 용도와 형태적 특성에 따라 sugar beet (B. vulgaris ssp. saccharifera), leaf beet (B. vulgaris ssp. cicla), forage beet (B. vulgaris ssp. crassa), garden beet (B. vulgaris ssp. rubra) 등으로 나뉜다.1) 이러한 그룹들은 뿌리 형태, 잎 구조, 색소 조성, 함유된 phytochemical 구성 등에서 폭넓은 변이를 보이며, 식량·사료·기능성 원료로서 높은 농업적 및 영양학적 가치를 지닌다.
비트(Beta vulgaris L.)는 일반적으로 1–2년생 작물로 재배되며 그 기원은 중동 지역으로 추정된다. 이후 아시아, 유럽, 아메리카 등 다양한 지역으로 확산되어 전 세계적으로 널리 재배되고 있다.5) 국내에서는 제주, 강원 지역 등을 중심으로 비트를 활발히 재배하고 있다.6) 비트 뿌리는 betalains, flavonoids, polyphenols, saponins 등 다양한 계열의 성분을 함유하고 있는 것으로 보고되었으며,7) 최근 연구에서는 비트 뿌리가 지질 대사 조절,8) 항염 활성9) 등 다양한 생리적 효능이 있는 것으로 보고되었다. 특히 심혈관계 질환,10) 당뇨병,11) 간 지방축적 개선12) 등에 기여할 수 있다는 결과들이 제시되면서 대사 질환 관련 기능성 소재로서의 잠재성이 주목받고 있다. 또한 비트 유래 성분 중 feruloyl amide 계열 화합물들은 항산화 및 항염 활성이 있는 것으로 잘 알려져 있다.13-16)
본 연구에서는 비트 뿌리에서 분리한 feruloyl amide 계열 화합물에 대해 정밀한 분광학적 분석을 통해 화학 구조를 규명하고 실험실에서 지속적으로 활용해 온 분자도킹시뮬레이션을 수행하여17,18) AMPK, CTSS, PPAR-α/δ/γ 등 여러 핵 수용체와의 결합 잠재능력을 평가하였다. 분자도킹 결과는 사용된 알고리즘과 스코어링 함수에 따라 변동될 수 있기 때문에, 결과의 신뢰성과 재현성을 확보하기 위해 네 가지 도킹 소프트웨어를 병행하여 활용하였다. 그 결과, 분리한 화합물들이 대상 수용체들 중 PPAR-α에 대해 가장 우수한 결합 에너지를 보이는 것으로 나타났다. 따라서 본 연구에서는 PPAR-α를 중심으로 분리된 화합물들의 결합 특성과 상호작용 양상을 세부적으로 분석함으로써, 비트 유래 feruloyl amide 계열 화합물들이 지질대사 및 항염 기전에 기여할 가능성을 확인하고자 하였다.
이러한 연구 접근은 비트 유래 feruloyl amide 계열 화합물의 생리활성 탐색 범위를 확장하고, 향후 기능성 소재로서의 응용 가능성을 탐색하는 데 중요한 기초 자료를 제공한다는 점에서 학술적 의미를 갖는다.
재료 및 방법
실험재료 – 비트(B. vulgaris) 뿌리(건조중량 11.3 kg)를 제주도 서귀포시 소재의 한국약용식물원 영농조합법인에서 2021년 12월에 구매하였으며 한국약용식물원 박대양 원장이 동정하였다. 확증표본(EA393)은 이화여자대학교 약학대학 천연물화학연구실에 보관하였다.
기기 및 시약 – 비선광도는 JASCO사의 polarimeter P-2000를 이용하여 측정하였다. CD spectra는 JASCO사의 J-1500 CD spectrophotometer를 이용하여 측정하였다. NMR spectra는 Agilent사의 400-MR DD2를 이용하여 측정하였다. Mass spectra는 Agilent사의 6230 TOF LC/MS를 이용하여 측정하였다. 화합물의 분리는 Merck사의 silica gel (63-200 µm), YMC사의 RP-18 (150 µm), GE Healthcare사의 Sephadex LH-20을 이용한 open column chromatography와 Teledyne Isco사의 CombiFlash® Rf MPLC를 이용하여 RediSep® C18 컬럼으로 수행하였다. TLC 분석은 Merck사의 Silica gel 60 F254와 RP-18 F254s를 사용하였다. HPLC는 YL사의 quaternary pump (YL9110 Plus), UV/Vis detector (YL9120) 장비와 Waters사의 controller (600), PDA detector (996) 장비로 총 2가지 시스템을 사용하였고, 컬럼은 YMC사의 Actus Triart C18 (250 × 20 mm I.D., 5 μm, 12 nm)와 Actus Triart C18 ExRS (250 × 20 mm I.D., 5 μm, 8 nm)를 사용하였다. 사용한 유기 용매는 모두 대정화금에서 구입하였으며, NMR 용 용매로 사용된 메탄올은 Cambridge Isotope Laboratories사에서 구입하여 사용하였다.
추출 및 분리 – 건조한 비트 뿌리 11.3 kg에 메탄올 36 L를 가하여 실온에서 4회 추출하였으며, 이를 감압 농축하여 2.6 kg의 메탄올 추출물을 얻었다. 이를 증류수에 현탁하여 n-hexane, EtOAc, n-BuOH의 순으로 분획하고 감압 농축하여 n-hexane 분획 37 g, EtOAc 분획 6 g 및 n-BuOH 분획 171 g을 얻었다. 이중 EtOAc 분획 6 g을 silica gel column (Ø 4×40 cm)에 걸고 CH2Cl2:MeOH (19:1)와 EtOAc:MeOH (7:3) 용매로 용출시킨 후 메탄올 100%로 세척하였으며, 이를 TLC 분석을 통하여 일곱 개의 분획(F-1~F-7)으로 나누었다. 분획 F-2 (2.8 g)에 대하여 Sephadex LH-20 column (Ø 3×80 cm)을 사용하여 CH2Cl2:MeOH (1:4)을 용매로 용출시켜 여섯 개의 분획(F-2-1~F-2-6)으로 나누었다. 이중 분획 F-2-3 (2.4 g)을 RP-18 column을 이용하여 MeOH:H2O (1:4)를 용매로 용출시켜 다섯 개의 분획(F-2-3-1~F-2-3-5)으로 나누었다. 이중 분획 F-2-3-1 (1.9 g)에 대하여 RP-MPLC를 실시하여 MeOH:H2O (1:4)를 용매로 용출시켜 여섯 개의 분획(F-2-3-1-1~F-2-3-1-6)으로 나누었다. 이중 분획 F-2-3-1-4와 F-2-3-1-5 (282 mg)를 합하여 silica gel column (Ø 2×30 cm)에 걸고 CH2Cl2:MeOH (49:1)을 용매로 용출시켜 스무 개의 분획(F-2-3-1-4+5-1~F-2-3-1-4+5-20)으로 나누었다. 이중 분획 F-2-3-1-4+5-4 (47 mg)에 대하여 RP-HPLC (ACN:H2O=1:4, 0.05% TFA in H2O)를 수행하여 화합물 1 (28 mg)과 화합물 2 (16 mg)를 분리하였다. 분획 F-2-3-1-4+5-5 (10 mg)에 대하여 RP-HPLC (MeOH:H2O=7:3, 0.05% TFA in H2O)를 수행하여 화합물 1 (5 mg)을 추가로 분리하였다. 분획 F-2-3-1-4+5-6 (34 mg)에 대하여 RP-HPLC (ACN:H2O=1:4)를 수행하여 화합물 3 (17 mg)과 화합물 4 (2 mg)를 분리하였다.
N-trans-hibiscusamide (1) – dark brown oil; HRESIMS m/z 374.1597 [M + H]+ (calcd for C20H24NO6, 374.1598); 1H NMR (CD3OD, 400MHz) δ 7.44 (1H, d, J=15.6 Hz, H-7), 7.11 (1H, d, J=2 Hz, H-2), 7.02 (1H, dd, J=2, 8.4 Hz, H-6), 6.79 (1H, d, J=8.4 Hz, H-5), 6.52 (2H, s, H-2′ and H-6′), 6.41 (1H, d, J=15.6 Hz, H-8), 3.88 (3H, s, OCH3-3), 3.82 (6H, s, OCH3-3′ and OCH3-5′), 3.50 (2H, t, J=6.8 Hz, H2-8′), 2.77 (2H, t, J=7.2 Hz, H2-7′); 13C NMR (CD3OD, 100MHz) δ 169.3 (C=O, C-9), 149.9 (C-4), 149.34 (C-3), 149.29 (C-3′ and C-5′), 142.1 (CH, C-7), 135.1 (C-4′), 131.3 (C-1′), 128.3 (C-1), 123.2 (CH, C-6), 118.8 (CH, C-8), 116.5 (CH, C-5), 111.6 (CH, C-2), 107.1 (CH, C-2′ and C-6′), 56.8 (CH3, OCH3-3′ and OCH3-5′), 56.4 (CH3, OCH3-3), 42.4 (CH2, C-8′), 36.7 (CH2, C-7′).
N-trans-feruloylhomovanillylamine (2) – dark brown oil; HRESIMS m/z 344.1493 [M + H]+ (calcd for C19H22NO5, 344.1492); 1H NMR (CD3OD, 400MHz) δ 7.43 (1H, d, J=15.6 Hz, H-7), 7.11 (1H, d, J=1.6 Hz, H-2), 7.02 (1H, dd, J=2, 8.4 Hz, H-6), 6.82 (1H, d, J=1.6 Hz, H-2′), 6.79 (1H, d, J=8 Hz, H-5), 6.72 (1H, d, J=8 Hz, H-5′), 6.67 (1H, dd, J=2, 8 Hz, H-6′), 6.41 (1H, d, J=15.6 Hz, H-8), 3.88 (3H, s, OCH3-3), 3.83 (3H, s, OCH3-3′), 3.49 (2H, t, J=7.2 Hz, H2-8′), 2.77 (2H, t, J=7.2 Hz, H2-7′); 13C NMR (CD3OD, 100MHz) δ 169.3 (C=O, C-9), 149.9 (C-4), 149.4 (C-3), 149.0 (C-3′), 146.1 (C-4′), 142.1 (CH, C-7), 132.1 (C-1′), 128.3 (C-1), 123.3 (CH, C-6), 122.3 (CH, C-6′), 118.8 (CH, C-8), 116.5 (CH, C-5), 116.3 (CH, C-5′), 113.5 (CH, C-2′), 111.6 (CH, C-2), 56.45 (CH3, OCH3-3), 56.4 (CH3, OCH3-3′), 42.5 (CH2, C-8′), 36.3 (CH2, C-7′).
N-trans-feruloyltyramine (3) – yellow oil; HRESIMS m/z 314.1383 [M + H]+ (calcd for C18H20NO4, 314.1387); 1H NMR (CD3OD, 400MHz) δ 7.43 (1H, d, J=15.6 Hz, H-7), 7.10 (1H, d, J=1.6 Hz, H-2), 7.05 (2H, d, J=8.4 Hz, H-2′ and H-6′), 7.01 (1H, dd, J=2, 8 Hz, H-6), 6.78 (1H, d, J=8.4 Hz, H-5), 6.72 (2H, d, J=8.4 Hz, H-3′ and H-5′), 6.39 (1H, d, J=15.6 Hz, H-8), 3.87 (3H, s, OCH3-3), 3.46 (2H, t, J=7.2 Hz, H2-8′), 2.75 (2H, t, J=7.2 Hz, H2-7′); 13C NMR (CD3OD, 100MHz) δ 168.3 (C=O, C-9), 156.0 (C-4′), 149.5 (C-4), 148.5 (C-3), 141.2 (CH, C-7), 130.3 (C-1′), 129.8 (CH, C-2′ and C-6′), 127.0 (C-1), 122.4 (CH, C-6), 117.5 (CH, C-8), 115.6 (CH, C-5), 115.3 (CH, C-3′ and C-5′), 110.5 (CH, C-2), 55.4 (CH3, OCH3-3), 41.6 (CH2, C-8′), 34.9 (CH2, C-7′).
S-(−)-3-(4-hydroxy-3-methoxyphenyl)-N-[2-(4-hydroxyphenyl)-methoxyethyl]acrylamide (4) – yellow oil; = -22.5o (c 0.04, MeOH); CD (MeOH) λ (Δε) 198 (-7.92), 208 (-2.71), 223 (-5.48), 289 (-1.84), 319 (-2.36) nm; HRESIMS m/z 344.1494 [M + H]+ (calcd for C19H22NO5, 344.1492); 1H NMR (CD3OD, 400MHz) δ 7.43 (1H, d, J=15.6 Hz, H-7), 7.16 (2H, d, J=8.4 Hz, H-2′ and H-6′), 7.09 (1H, d, J=2 Hz, H-2), 7.00 (1H, dd, J=2, 8.4 Hz, H-6), 6.78 (2H, d, J=8.4 Hz, H-3′ and H-5′), 6.75 (1H, d, J=8 Hz, H-5), 6.43 (1H, d, J=15.6 Hz, H-8), 4.24 (1H, dd, J=4.8, 8.2 Hz, H-7′), 3.87 (3H, s, OCH3-3), 3.50 (1H, dd, J=4.8, 13.8 Hz, H-8′b), 3.40 (1H, dd, J=8.4, 14 Hz, H-8′a), 3.21 (3H, s, OCH3-7′); 13C NMR (CD3OD, 100MHz) δ 168.5 (C=O, C-9), 157.9 (C-4′), 151.3 (C-4), 149.0 (C-3), 141.6 (CH, C-7), 130.3 (C-1′), 128.3 (CH, C-2′ and C-6′), 126.0 (C-1), 122.7 (CH, C-6), 116.7 (CH, C-8), 116.1 (CH, C-5), 115.5 (CH, C-3′ and C-5′), 110.4 (CH, C-2), 82.4 (CH, C-7′), 55.8 (CH3, OCH3-7′), 55.3 (CH3, OCH3-3), 46.1 (CH2, C-8′).
분자도킹시뮬레이션(Molecular docking simulation) – 본 연구에서는 비트 뿌리에서 분리한 네 가지 화합물에 대해 PPAR-α와 결합하는 능력을 평가하기 위해 분자도킹시뮬레이션을 수행하였다. 이를 위해 PPAR-α의 3차원 결정 구조는 RCSB Protein Data Bank로부터 확보하였으며, 사용된 단백질 구조는 PDB ID: 1K7L이다. 네 가지 후보 화합물 및 양성대조군으로 사용된 fenofibric acid의 구조정보는 PubChem 데이터베이스에서 다운로드하였다. 도킹 작업은 Autodock Vina 1.1.2, Autodock 4.2.6, LeDock 1.0, Dock 6 네 가지 소프트웨어를 이용하여 독립적으로 진행하였다. 각 프로그램의 기본 알고리즘 및 스코어링 함수에 따라 리간드를 PPAR-α의 결합 부위에 도킹하였으며, 생성된 여러 포즈 중 최소결합 에너지 상태를 최종 분석대상으로 선정하였다. 리간드–수용체 간 상호작용 분석은 LIGPLOT 소프트웨어를 활용해 평가하였으며, 이는 수소결합 및 소수성 상호작용을 2차원 도식화 형태로 제공함으로써 결합 양상을 시각적으로 파악하는 데 사용되었다.
결과 및 고찰
비트(B. vulgaris) 뿌리의 메탄올 추출물로부터 유기용매 분획, 각종 컬럼 크로마토그래피 및 HPLC 정제 방법을 이용하여 총 4종의 feruloyl amide 화합물을 분리하였다(Fig. 1). 이 중 화합물 1 및 4는 비트에서 처음 분리 보고되었다. 화합물 2 및 3은 비트의 성분으로 기존 문헌에 보고된 물질이어서 화합물 1 및 4의 구조 동정에 대하여 기재하기로 한다.19,20)
화합물 1은 짙은 갈색의 오일상 화합물로, HRESIMS에서 m/z 374.1597 [M + H]+ 피크를 나타내어 분자식이 C20H23NO6 임을 확인하였다. 분자식 내 질소원자의 존재가 예상되었고, Dragendorff 시약반응에서 양성을 보임에 따라 염기성 질소를 함유한 amide 계열 화합물임을 확인하였다. 1H NMR spectrum 에서 δ 7.11 (1H, d, J=2 Hz), 6.79 (1H, d, J=8.4 Hz), 7.02 (1H, dd, J=2, 8.4 Hz)로 구성된 1,2,4-trisubstituted benzene ring 패턴의 피크를 확인하였고, δ 3.88 (3H, s), 3.82 (6H, s)의 피크를 통해 세 개의 methoxy기가 있음을 확인하였다. 또한 δ 7.44 (1H, d, J=15.6 Hz), δ 6.41 (1H, d, J=15.6 Hz)의 피크를 통해 trans-형 이중결합 구조가 있음을 예상하였다. 13C NMR spectrum에서는 carbonyl기 탄소(δ 169.3) 1개를 포함한 총 20개의 탄소 신호가 검출되어 phenolic amide 구조임을 뒷받침하였다. HMBC spectrum에서 δ 2.77 (H2-7′) 피크는 δ 169.3 (C-9), 42.4 (C-8′), 131.3 (C-1′)와의 correlation을 나타냈고, δ 3.50 (H2-8′) 피크는 δ 36.7 (C-7′) 및 δ 107.1 (C-2′, C-6′)과의 correlation을 보였다. 또한 δ 6.41 (H-8) 피크는 δ 169.3 (C-9) 및 δ 128.3 (C-1)과 correlation을 나타내어 amide 결합 및 이중결합의 위치를 명확히 확인하였다. NOESY spectrum에서도 δ 3.82 (6H, s)의 두 methoxy기 피크가 δ 6.52 (H-2′, H-6′) 피크와 상호작용을 나타냈으며, δ 3.88 (3H, s)의 methoxy기 피크는 δ 7.11 (H-2) 피크와의 correlation을 보였다. 이러한 모든 스펙트럼 정보와 기존의 문헌 자료를 비교한 결과, 화합물 1은 이미 보고된 N-trans-hibiscusamide와 일치하여 본 연구에서 해당 구조로 최종 동정하였다.
화합물 4는 황색의 오일상 물질로, HRESIMS에서 m/z 344.1494 [M + H]+ 피크를 나타내어 분자식이 C19H21NO5 임을 확인하였다. 화합물 1과 같이 분자식 구성으로부터 질소 원자의 존재가 예상되어, Dragendorff 시약 양성 반응을 통해 확인하였다. ¹H 및 ¹³C NMR spectrum 분석 결과, 화합물 4의 스펙트럼 패턴은 화합물 1과 매우 유사한 것을 알 수 있었다. 하지만, 1,2,4-trisubstituted aromatic ring에 존재하던 두 개의 methoxy기 피크 대신 aliphatic chain (C-7′)에 새로운 methoxy기 피크가 결합된 것이 차이점으로 확인되었다. 2003년 Xing, X. 등은 C-7′ 위치의 입체이성질체(S형 및 R형)를 합성하여 비선광도를 측정하였으며, S형과 R형 화합물에 대해 각각 = -5.6o (c 1.0, MeOH)과 = +6.1o (c 1.0, MeOH)의 값을 나타냈다.21) 앞서 보고된 선행 연구 결과를 바탕으로 화합물 4의 절대입체구조를 S형으로 확정하였다( = -22.5o (c 0.04, MeOH)). CD spectrum에서도 208 nm (–2.71), 223 nm (–5.48), 289 nm (–1.84)의 결과를 통해 음의 Cotton effect가 관찰되었으며(Fig. 2), 이는 문헌상 화합물 4와 유사한 키랄성 구조를 가진 phenylethylamine A에서 보고된 CD spectrum 패턴과 매우 유사하였다.22) 이러한 결과는 화합물 4의 C-7′ 위치에서 S-형의 절대구조를 갖는 것에 대한 타당성을 뒷받침하면서, 화합물 4의 CD spectrum을 처음으로 보고하는 의의를 가진다. 이상의 모든 스펙트럼 데이터를 종합하여 문헌 보고치와 비교한 결과, 화합물 4는 S-(−)-3-(4-hydroxy-3-methoxyphenyl)-N-[2-(4-hydroxyphenyl)-methoxyethyl]acrylamide로 최종 동정하였다. 그 외 2종의 화합물들은 MS, 1H NMR, 13C NMR 등의 분광분석 자료와 문헌을 참고하여 그 구조를 각각 N-trans-feruloylhomovanillylamine (2), N-trans-feruloyltyramine (3)으로 동정하였다.
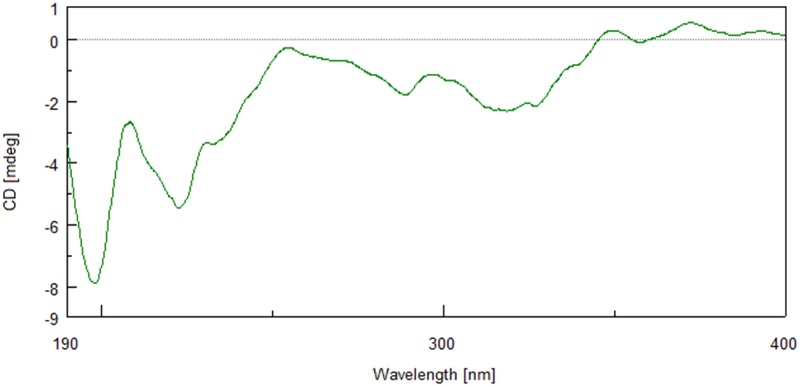
CD spectrum of 4 in MeOH: λ (Δε) 198 (-7.92), 208 (-2.71), 223 (-5.48), 289 (-1.84), 319 (-2.36) nm.
분리한 4종의 화합물에 대해 PPAR-α 수용체에 대한 결합 친화력을 평가하고자 Autodock Vina, Autodock 4, LeDock, Dock 6 네 가지 분자 도킹 프로그램을 이용하여 분석을 수행하였다(Table I). 모든 도킹 시스템에서 네 가지 화합물은 양성 대조군(fenofibric acid)보다 일관되게 낮은 결합 에너지 값을 나타내어, PPAR-α 수용체와 더 강하고 안정적인 상호 작용을 형성함을 확인하였다. 이러한 결과는 향후 실제 in vitro 실험을 통해 PPAR-α 작용제(agonist)로서의 가능성을 연구할 가치가 있음을 제시한다. 또한, 결합 양상을 보다 구체적으로 파악하기 위해, 주요 비공유결합 상호작용을 분석하는 약리 단의 특징에 대한 고찰(pharmacophoric insights)을 하였다 (Fig. 3). 그 결과, 화합물 2은 Tyr334 잔기와 2.83 Å 거리에서 수소결합을 형성하였으며, 화합물 3는 Ala333과 2.95 Å 거리에서 수소결합을 형성하였다. 화합물 4는 Ala333 및 Ser280과 각각 2.94 Å, 3.23 Å 거리에서 두 개의 수소결합을 형성하여 보다 안정적인 결합 양상을 나타냈다. 중요한 활성 부위 잔기들과의 안정적인 수소결합은 대조 리간드 대비 높은 결합 친화도의 주요 요인으로 작용한 것으로 판단된다. 소수성 상호작용 측면에서는, 네 가지 화합물과 대조군 모두가 Val332, Cys276, Met355, Leu321, Thr279 잔기들과 공통적인 소수성 접촉을 보였다. 이는 PPAR-α 결합 부위 내에서 보존된 소수성 상호작용 패턴을 공유하고 있음을 의미한다. 또한 네 가지 화합물은 대조 리간드에서는 관찰되지 않았던 His440, Phe273, Ile354 등 잔기와의 소수성 접촉을 추가적으로 형성하였다. 이러한 독특한 상호작용은 결합 안정성을 향상시키고, 향후 구조 최적화를 통해 결합 친화력 및 선택성을 개선할 수 있는 잠재적 결합 부위를 제공한다. 한편, 도킹 소프트웨어에 따른 결과의 차이가 일부 관찰되었다. 예를 들어 Autodock 4에서는 화합물 2 (–9.6 kcal/mol)와 3 (–9.5 kcal/mol)이 가장 높은 결합 친화력을 나타낸 반면, Dock 6에서는 화합물 4 (–45.6 kcal/mol)와 1 (–44.5 kcal/mol)이 가장 강한 결합을 형성하는 것으로 예측되었다(Table I). 이러한 차이는 소프트웨어별 스코어링 함수, 결합 포즈 예측 알고리즘, 기능기 민감도 차이 등에 기인한 것으로 판단된다. 이러한 경향성을 보완하고 도킹 결과의 신뢰성을 높이기 위해서는 추후 다단계 검증이 요구된다.
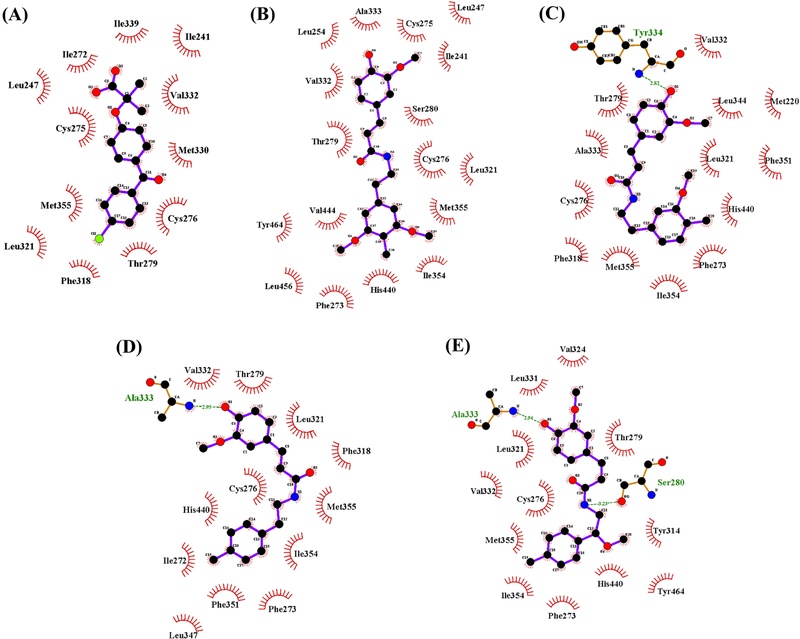
In silico docking simulations of the compounds 1-4 against PPAR-α in Autodock Vina. (A) Pharmacophore analysis of PPAR-α with the control, fenofibric acid. (B) Pharmacophore analysis of PPAR-α with compound 1. (C) Pharmacophore analysis of PPAR-α with compound 2. (D) Pharmacophore analysis of PPAR-α with compound 3. (E) Pharmacophore analysis of PPAR-α with compound 4.
종합적으로, 본 도킹 연구는 화합물 1–4가 PPAR-α 수용체에 대해 대조 리간드보다 더 우수한 결합 친화도와 구조적 적합성을 지님을 보여주어, 새로운 PPAR-α 작용제 후보 물질로서의 가능성을 뒷받침한다. 특히 PPAR-α가 지질 대사 및 세포 보호와 연관된 생리적 경로에 관여한다는 점을 고려할 때, 이러한 후보 물질들은 향후 피부 장벽 강화와 같은 관련 생리활성으로의 응용 가능성도 간접적으로 시사한다.23) 이들의 약리학적 효능 및 치료적 가치를 확립하기 위해 molecular dynamics (MD) 시뮬레이션 및 후속 in vitro 실험을 진행하고자 한다.
결 론
본 연구에서는 비트(B. vulgaris) 뿌리 추출물로부터 얻은 EtOAc 분획에 대해 일련의 분리 및 정제 과정을 수행하여 4종의 feruloyl amide 화합물 N-trans-hibiscusamide (1), N-trans-feruloylhomovanillylamine (2), N-trans-feruloyltyramine (3), S-(−)-3-(4-hydroxy-3-methoxyphenyl)-N-[2-(4-hydroxyphenyl)-methoxyethyl]acrylamide (4)를 분리하였다. 이 중 화합물 1과 4는 B. vulgaris에서 처음으로 분리 보고되었다. 분리된 화합물들의 구조는 기존 문헌에 보고된 MS, 1H NMR, 13C NMR, DEPT-135, COSY, NOESY, HSQC, HMBC 등의 스펙트럼 자료와 비선광도, CD spectra 분석을 바탕으로 동정하였다. 또한, 분리된 네 가지 화합물의 PPAR-α에 대한 결합 능력 평가를 위해 네 종류의 소프트웨어 프로그램을 활용한 분자 도킹 시뮬레이션을 수행하였다. 그 결과 모든 화합물은 양성 대조군보다 더 강하고 안정적인 결합 에너지를 보였다. Pharmacophore 분석에서도 활성부위 내 주요 아미노산 잔기와의 수소결합 및 소수성 상호작용이 관찰되어 결합양상을 분자 수준에서 뒷받침하였다. 이상의 결과는 비트 유래 feruloyl amide 계열 화합물이 신규 PPAR-α 표적 후보물질로 활용될 가능성을 제시하며, 향후 MD 시뮬레이션 및 in vitro 실험을 통해 그 효능을 보다 명확히 규명할 필요가 있다. 본 연구는 비트 뿌리 추출물의 약리학적 가치를 확장하는 기초 자료로서 의미를 가지며, 향후 PPAR-α 관련 대사질환 치료제 개발의 기반을 마련할 것으로 기대된다.
Acknowledgments
이 연구는 한국연구재단(NRF)의 지원을 받아 수행되었으며, 과학기술정보통신부(MSIT)의 중견연구자지원사업(과제번호: 2021R1A2C1003350)과 창의도전연구기반지원사업(과제번호: RS-2023-00243759)의 지원을 받았습니다. 또한 본 연구는 서울여자대학교 교내연구과제(과제번호: 2025-0190)의 지원을 받았습니다.
References
-
Thiruvengadam, M., Chung, I. M., Samynathan, R., Chandar, S. R. H., Venkidasamy, B., Sarkar, T., Rebezov, M., Gorelik, O., Shariati, M. A. and Simal-Gandara, J. (2024) A comprehensive review of beetroot (Beta vulgaris L.) bioactive components in the food and pharmaceutical industries. Critical Reviews in Food Science and Nutrition 64: 708-739.
[https://doi.org/10.1080/10408398.2022.2108367]

-
Stadnicka-Futoma, A. and Nobis, M. (2024) Geographical–historical analysis of the herbarium specimens representing the economically important family Amaranthaceae (Chenopodiaceae-Amaranthaceae clade) collected in 1821–2022 and preserved in the herbarium of the Jagiellonian University in Krakow. Biology 13: 435.
[https://doi.org/10.3390/biology13060435]

-
Christenhusz, M. J. and Byng, J. (2016) The number of known plants species in the world and its annual increase. Phytotaxa 261: 201-217.
[https://doi.org/10.11646/phytotaxa.261.3.1]

-
Punia Bangar, S., Singh, A., Chaudhary, V., Sharma, N. and Lorenzo, J. M. (2023) Beetroot as a novel ingredient for its versatile food applications. Critical Reviews in Food Science and Nutrition 63: 8403-8427.
[https://doi.org/10.1080/10408398.2022.2055529]

-
Punia Bangar, S., Sharma, N., Sanwal, N., Lorenzo, J. M. and Sahu, J. K. (2022) Bioactive potential of beetroot (Beta vulgaris). Food Research International 158: 111556.
[https://doi.org/10.1016/j.foodres.2022.111556]

- 김석철(2021) 비트의 수익성과 경영시사점, p 9. 진영인쇄, 서울.
-
Baião, D. d. S., da Silva, D., Del Aguila, E. M. and Paschoalin, V. M. F. (2017) Nutritional, bioactive and physicochemical characteristics of different beetroot formulations. Food Additives 6: 21-43.
[https://doi.org/10.5772/intechopen.69301]

-
Markou, M., Katsouda, A., Papaioannou, V., Argyropoulou, A., Vanioti, M., Tamvakopoulos, C., Skaltsounis, L. A., Halabalaki, M., Mitakou, S. and Papapetropoulos, A. (2024) Anti‐obesity effects of Beta vulgaris and Eruca sativa‐based extracts. Phytotherapy Research 38: 4757-4773.
[https://doi.org/10.1002/ptr.8291]

-
Thiruvengadam, M., Chung, I. M., Samynathan, R., Chandar, S. R. H., Venkidasamy, B., Sarkar, T., Rebezov, M., Gorelik, O., Shariati, M. A. and Simal-Gandara, J. (2024) A comprehensive review of beetroot (Beta vulgaris L.) bioactive components in the food and pharmaceutical industries. Critical Reviews in Food Science and Nutrition 64: 708-739.
[https://doi.org/10.1080/10408398.2022.2108367]

-
Mirmiran, P., Houshialsadat, Z., Gaeini, Z., Bahadoran, Z. and Azizi, F. (2020) Functional properties of beetroot (Beta vulgaris) in management of cardio-metabolic diseases. Nutrition & Metabolism 17: 1-15.
[https://doi.org/10.1186/s12986-019-0421-0]

-
Aliahmadi, M., Amiri, F., Bahrami, L. S., Hosseini, A. F., Abiri, B. and Vafa, M. (2021) Effects of raw red beetroot consumption on metabolic markers and cognitive function in type 2 diabetes patients. Journal of Diabetes & Metabolic Disorders 20: 673-682.
[https://doi.org/10.1007/s40200-021-00798-z]

-
Al-Harbi, L. N., Alshammari, G. M., Al-Dossari, A. M., Subash-Babu, P., Binobead, M. A., Alhussain, M. H., AlSedairy, S. A., Al-Nouri, D. M. and Shamlan, G. (2021) Beta vulgaris L.(Beetroot) methanolic extract prevents hepatic steatosis and liver damage in T2DM rats by hypoglycemic, insulin-sensitizing, antioxidant effects, and upregulation of PPARα. Biology 10: 1306.
[https://doi.org/10.3390/biology10121306]

-
Cho, J.-Y., Yang, X., Park, K.-H., Park, H. J., Park, S.-Y., Moon, J.-H. and Ham, K.-S. (2013) Isolation and identification of antioxidative compounds and their activities from Suaeda japonica. Food Science and Biotechnology 22: 1547-1557.
[https://doi.org/10.1007/s10068-013-0250-2]

-
Lai, Y., Wang, S., Hu, Y., Hwang, T., Cheng, M., Chen, I., Sung, P. and Chen, J. (2020) Anti-inflammatory alkaloids from the root bark of Hernandia nymphaeifolia. Phytochemistry 173: 7.
[https://doi.org/10.1016/j.phytochem.2020.112326]

-
Li, W., Cheng, X., Liu, J., Lin, R., Wang, G., Du, S. and Liu, Z. (2012) Phenolic compounds and antioxidant activities of Liriope muscari. Molecules 17: 1797-1808.
[https://doi.org/10.3390/molecules17021797]

-
Jiang, Y., Yu, L. and Wang, M. (2015) N-trans-feruloyltyramine inhibits LPS-induced NO and PGE2 production in RAW 264.7 macrophages: Involvement of AP-1 and MAP kinase signalling pathways. Chemico-Biological Interactions 235: 56-62.
[https://doi.org/10.1016/j.cbi.2015.03.029]

-
Piao, D., Youn, I., Huynh, T.-H., Kim, H. W., Noh, S. G., Chung, H. Y., Oh, D.-C. and Seo, E. K. (2024) Identification of new polyacetylenes from Dendropanax morbifera with PPAR-α activity study. Molecules 29: 5942.
[https://doi.org/10.3390/molecules29245942]

-
Youn, I., Han, S., Jung, H. J., Noh, S. G., Chung, H. Y., Koo, Y. K., Shin, S. and Seo, E. K. (2023) Anti-inflammatory activity of the constituents from the leaves of Perilla frutescens var. acuta. Pharmaceuticals 16: 1655.
[https://doi.org/10.3390/ph16121655]

-
Seo, G., Cho, J., Moon, J. and Park, K. (2011) Isolation and identification of cinnamic acid amides as antioxidants from Allium fistulosum L. and their free radical scavenging activity. Food Science and Biotechnology 20: 555-560.
[https://doi.org/10.1007/s10068-011-0078-6]

-
Li, W., Cheng, X., Liu, J., Lin, R., Wang, G., Du, S. and Liu, Z. (2012) Phenolic compounds and antioxidant activities of Liriope muscari. Molecules 17: 1797-1808.
[https://doi.org/10.3390/molecules17021797]

-
Xing, X., Ho, P., Bourquin, G., Yeh, L.-A. and Cuny, G. D. (2003) Synthesis, stereochemistry confirmation and biological activity evaluation of a constituent from Isodon excisus. Tetrahedron 59: 9961-9969.
[https://doi.org/10.1016/j.tet.2003.10.025]

-
Liu, C., Tian, J., An, T., Lyu, F., Jia, P., Zhou, M., Liu, Z. and Feng, Y. (2019) Secondary metabolites from Solanum rostratum and their antifeedant defense mechanisms against Helicoverpa armigera. Journal of Agricultural and Food Chemistry 68: 88-96.
[https://doi.org/10.1021/acs.jafc.9b06768]

-
Kim, B. (2024) Citronellic acid improves skin barrier function by activation of PPAR-α. Natural Product Sciences 30: 268-274.
[https://doi.org/10.20307/nps.2024.30.4.268]