
Ginsenoside Rg1에 의한 NLRP3 발현 조절 및 IL-1β 생성 억제 효과
Abstract
Neuroinflammation is a major contributor to the pathogenesis of neurodegenerative diseases such as Alzheimer’s and Parkinson’s disease. A key mediator of this process is the NLRP3 inflammasome in microglia, which activates caspase-1 and drives the maturation and release of pro-inflammatory cytokines including IL-1β. Excessive or sustained activation of the NLRP3 inflammasome promotes neuronal dysfunction, highlighting it as a potential therapeutic target. Ginsenoside Rg1, a predominant bioactive compound of Panax ginseng C. A. Meyer, is known for its antioxidant and anti-inflammatory properties; however, its direct role in regulating NLRP3 remains poorly understood. In this study, we examined the effects of Rg1 on NLRP3 expression and IL-1β production in BV2 microglial cells. MTT assay confirmed that Rg1 up to 300 μg/mL had no cytotoxic effect. Western blot analysis demonstrated that Rg1 pretreatment significantly suppressed LPS-induced NLRP3 protein expression and reduced IL-1β levels, whereas qPCR analysis revealed no change in NLRP3 mRNA expression. These findings suggest that Rg1 regulates NLRP3 at the post-transcriptional level. Consistent with this, the DARTS assay indicated a direct binding interaction between Rg1 and NLRP3. Taken together, these results identify ginsenoside Rg1 as a promising candidate for the prevention or treatment of neuroinflammatory diseases.
Keywords:
Ginsenoside Rg1, NLRP3, Inflammasome, Neuroinflammation신경염증(neuroinflammation)은 중추 및 말초신경계에서 나타나는 면역 반응으로, 외부 감염이나 손상에 대한 방어기전일 뿐 아니라 다양한 신경 퇴행성 질환(neurodegenerative disorders)의 병태생리학적 핵심 기전으로 알려져 있다.1,2) 단기적이고 적절한 염증 반응은 조직 회복과 방어에 기여하지만, 만성적이고 과도한 염증 반응은 신경세포 손상, 시냅스 가소성 저해, 인지기능 저하로 이어질 수 있다.3-5) 실제로 알츠하이머병, 파킨슨병, 다발성 경화증, 주요 우울장애 등에서 과도한 신경염증이 공통적으로 보고되었으며, 이는 치료 표적으로서 염증 경로의 조절이 주목받는 이유이다.6,7)
이 과정에서 미세아교세포(microglia)는 중추신경계 면역 반응의 중심적인 역할을 담당한다. 미세아교세포는 병원체 인식 수용체(pattern recognition receptors, PRRs)를 통해 병원체 연관분자(pathogen-associated molecular patterns, PAMPs) 나 손상 연관분자(damage-associated molecular patterns, DAMPs)를 인식하고, 염증성 사이토카인을 분비한다.6) 이러한 반응은 초기 방어에는 유리하나, 장기간 지속되면 신경세포 사멸과 신경회로 붕괴를 유발한다.8,9) 특히, 미세아교세포 내에서 활성화되는 NLRP3 (NOD-like receptor family pyrin domain-containing 3) inflammasome은 interleukin-1 beta (IL-1β) 및 IL-18의 성숙과 분비를 매개하는 대표적인 분자 복합체로, 신경염증 반응의 중심 역할을 한다.10)
NLRP3 inflammasome은 다양한 자극에 의해 활성화되며, 이는 ATP, ROS (reactive oxygen species), 요산 결정, 아밀로이드 베타(amyloid-β) 등 광범위한 자극원에 의해 나타날 수 있다.11) 활성화 과정에서 NLRP3 단백질은 ASC (apoptosis-associated speck-like protein containing a CARD) 및 procaspase-1과 결합하여 복합체를 형성하고, 이어서 caspase-1이 활성화되어 proIL-1β와 proIL-18을 성숙한 형태로 절단한다.12) 이와 같은 염증성 사이토카인의 분비는 신경계 전반의 면역 반응을 증폭시키고, 장기적으로는 신경세포 손상을 가속화한다.11) 실제로 알츠하이머병 환자에서 아밀로이드 베타가 NLRP3 inflammasome을 활성화하여 질환 진행을 촉진한다는 보고가 있으며,13) 파킨슨병 모델에서도 α-synuclein이 NLRP3 활성화를 유도하여 도파민 신경세포 손실을 심화시키는 것으로 알려져 있다.14) 따라서 NLRP3 inflammasome은 신경 퇴행성 질환뿐만 아니라 다양한 만성 염증성 질환의 유망한 치료 표적으로 간주된다.
한편, 동양 전통 약용자원인 인삼(Panax ginseng)은 수 세기 동안 피로 회복, 면역 증진, 노화 억제 및 다양한 질환의 치료에 활용되어 왔다.15) 인삼에 함유된 활성 성분 중 대표적인 것이 바로 ginsenoside이며, 그 중 ginsenoside Rg1은 가장 연구가 활발히 이루어진 사포닌(saponin) 성분으로 다수의 약리학적 작용을 지니는 것으로 알려져 있다.16) Rg1은 항산화 및 항노화 효과를 통해 산화 스트레스에 의한 세포 손상을 완화하고, 항우울작용과 인지기능 개선 효과를 통해 신경 정신 질환 연구의 잠재적 후보물질로도 주목받고 있다.15,17) 더 나아가 최근의 분자·세포 수준 연구에서는 Rg1이 면역 균형(immune homeostasis)을 조절하는 중요한 기전으로 염증 매개 신호 경로의 억제에 관여한다는 결과들이 제시되고 있다.18) 예를 들어, Rg1은 NF-κB 및 MAPK 신호전달을 억제하여 염증성 사이토카인의 발현을 감소시키고, microglia 활성화를 억제하여 신경세포 보호 효과를 나타낸 바 있다.17,19)
그럼에도 불구하고, Rg1이 NLRP3 inflammasome 활성에 직접적으로 미치는 기전적 영향에 대해서는 아직 연구가 부족하다. 일부 연구에서는 인삼 추출물이 전신 염증 반응을 조절할 수 있음을 보여 주었지만, NLRP3 inflammasome을 표적으로 하는 연구는 제한적이다. 따라서, Rg1이 미세아교세포 수준에서 NLRP3 발현을 조절하고, 이어 NLRP3 inflammasome의 활성을 제어할 수 있는지 세부 기전을 규명하는 것은 학문적·치료적 의의가 크다.
이에 본 연구에서는 BV2 미세아교세포를 대상으로 Rg1의 세포 독성 여부를 평가하고, qPCR과 Western blot을 통해 NLRP3 및 inflammasome 활성화와 결과적인 염증성 사이토카인의 생성에 미치는 영향을 규명하고자 하였다. 이를 통해 Rg1이 신경염증 억제에 기여할 수 있는 가능성을 제시하고, 향후 신경염증 관련 질환 치료제 개발의 기초 자료를 제공하고자 한다.
재료 및 방법
실험 재료 및 세포 배양 – BV2 세포는 ATCC (Manassas, VA, USA)에서 구입하였으며, 1% penicillin/streptomycin (Corning, NY, USA)와 10% fetal bovine serum (Corning)이 포함된 DMEM (Corning) 배지를 이용하여 37℃, 5% CO2 조건의 인큐베이터에서 배양하였다. 실험에 사용한 모든 시약은 Sigma-Aldrich (St. Louis, MO, USA)에서 구입하였다.
세포생존률 평가 – Ginsenoside Rg1에 대한 세포 생존률은 3-(4,5-Dimethylthiazol-2-yl)-2,5-Diphenyltetrazolium Bromide (MTT)를 사용하여 분석하였다. BV2 세포를 48 well plate에 1.7×105 cells/plate의 밀도로 분주하여 37℃, 5% CO2 조건에서 배양하였다. 24시간 배양 후 새로운 배지로 바꾸고 Rg1을 100-300 μM 농도로 처리하였다. 48시간 이후, 배지를 제거하고 0.2 mg/mL 농도의 MTT 용액을 넣고 37℃에서 차광 조건에서 추가로 1시간 배양하였다. 이후 생성된 formazan crystals을 DMSO에 녹이고 Microplate reader (490 nm; Versamax, USA)로 흡광도를 측정하였다. 실험은 동일한 조건에서 3회 반복되었으며, 얻어진 결과값은 통계적으로 분석하였다.
정량적 중합효소 연쇄 반응(Quantitative polymerase chain reaction, qPCR) – INFUSION TECH 사의 PureTM Cell & Tissue RNA extraction kit (Anyang, Korea)를 사용하여 BV2 세포의 total RNA를 추출하였다. 추출한 mRNA는 ReverTraAce® qPCR RT Master Mix (Toyobo, Osaka, Japan)를 사용하여 cDNA로 역전사하고, 유전자의 상대적 발현양을 분석하기 위해 CFX96 Real-Time PCR System (Bio-Rad, Hercules, CA, USA)으로 qPCR을 수행하였다. Table I에 사용된 primer sequence를 제시하였다. PCR 반응 조건은 95℃에서 10초, 60℃에서 15초, 60℃에서 30초씩 45회 반복하였다. 상대적 mRNA 발현량은 2^–ΔΔCt 방법을 이용하여 계산하였으며, 18S rRNA를 발현량 보정을 위한 기준 유전자(reference gene)로 사용하였다.
Western Blotting – BV2 세포를 60 mm culture dish에 1.0×105 cells/dish로 분주하여 24시간 배양하였다. 이후 신선한 배지로 교체한 뒤, Rg1을 1시간 동안 전처리하고, LPS (0.2 μg/mL)를 처리하였다. LPS 처리 후 48시간을 기준으로 세포 수확 30분 전에 ATP (1 mM)를 추가하였다. 세포를 PBS로 세척한 후, protease/phosphatase inhibitor가 포함된 RIPA buffer로 용해하였다. 이후 15,000×g, 30분, 4℃에서 원심분리 후 상층액을 회수하였으며, 단백질 농도는 Bradford 방법 (Bio-Rad, Hercules, CA, USA)으로 단백질을 정량하였다. 각 시료(10–20 μg 단백질)에 5×loading dye를 섞고, 100℃, 5분 변성 후 8–12% SDS-PAGE로 분리하고 PVDF membrane (Millipore, Burlington, MA, USA)으로 transfer하였다. Membrane은 5% 탈지분유를 포함한 1×Tris-buffered saline with 0.05% Tween-20 (TBS-T) 용액에서 실온 1시간 동안 blocking한 후, 1차 항체(NLRP3, ASC, caspase-1, IL-1β, NF-κB p65, Vinculin, α-actin, α-tubulin)로 4℃에서 overnight 반응시켰다. TBS-T로 세척(10분×2회) 후 HRP-conjugated 2차 항체를 실온 1시간 반응시키고 다시 세척한 뒤 ECL 기질로 신호를 검출하였으며(ImageQuant LAS-4000; Fujifilm, Tokyo, Japan), 밴드 강도는 ImageJ로 정량하였다. 각 표적 단백질은 Vinculin이나 α-tubulin 같은 loading control 대비로 정규화하였다. 모든 실험은 최소 3회 독립 반복으로 수행하였고, 통계는 one-way ANOVA (사후검정 Tukey)를 사용하여 p < 0.05를 유의 수준으로 판단하였다.
Drug Affinity Responsive Target Stability (DARTS) assay – DARTS assay는 Rg1과 NLRP3 단백질 간의 직접 결합 여부를 확인하기 위해 수행하였다.20) BV2 세포에 protease inhibitor와 phosphatase inhibitor가 포함된 M-PER buffer를 넣고 4℃, 10분 incubation 후 4℃, 18000×g, 10분 동안 원심분리하였다. 상층액을 옮겨 10×TNC buffer와 섞어준 후 vehicle군과 Rg1 처리군(300 μM)으로 나누어 상온에서 1시간 동안 반응시켰다. 이후 pronase를 여러 농도로 첨가하여 30분간 제한적 단백질 분해를 유도하였다. 해당 반응은 protease inhibitor를 사용하여 중단시키고 Western blot으로 분석하여 NLRP3 단백질 수준을 비교하였다.
통계분석 – 통계자료의 값은 평균±표준오차(S.E.M) 값으로 나타내었으며, 그룹간의 통계적 유의성은 ANOVA 분석을 수행하였다(GraphPad Software, San Diego, CA, USA). *P < 0.05, **P < 0.01, ***P < 0.001일 때 유의성이 있는 것으로 간주하였다.
결과 및 고찰
Rg1에 의한 미세아교세포 BV2의 세포생존률 측정 – 본 연구에서는 마우스 미세아교세포 BV2를 사용하여, ginsenoside Rg1 (Fig. 1A)의 NLRP3 inflammasome 활성 조절에 대한 평가를 진행하기에 앞서, Rg1의 독성 여부를 확인하기 위해 MTT assay를 사용하여 세포생존률을 평가하였다(Fig. 1B). 먼저 BV2 세포에 Rg1을 100-300 μM의 농도로 48시간 처리한 후 세포 생존률을 분석한 결과 모든 농도에서 BV2 세포의 생존률이 대조군과 유사하여 이후 실험에서는 모두 최고 300 μM의 농도 조건으로 실험을 수행하였다. 이는 이후의 분석에서 관찰된 NLRP3 발현 억제가 비특이적 세포 사멸에 기인하지 않음을 뒷받침한다.
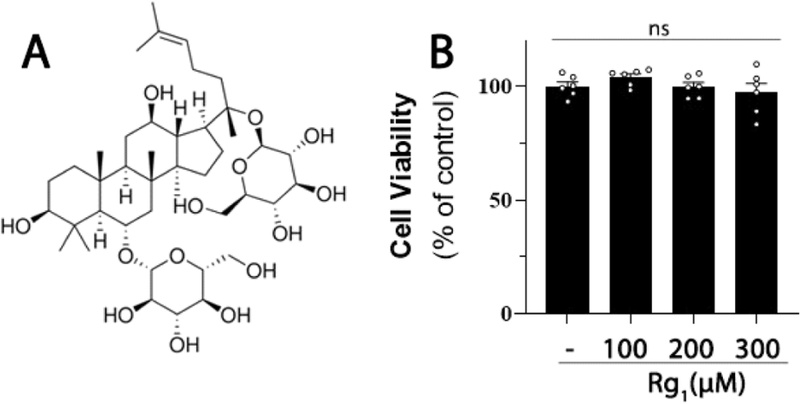
Cytotoxicity of Rg1 on mouse microglial BV2 cell. BV2 microglial cells were treated with increasing concentrations of Rg1 (up to 300 μM) for 24 h, and cell viability was measured by MTT assay. Data represent mean ± S.E.M of at least three independent experiments. Statistical analysis was performed using one-way ANOVA followed by Tukey’s post hoc test (ns=not significant).
Ginsenoside Rg1에 의한 NLRP3 발현 변화 – Ginsenoside Rg1은 인삼의 주요 활성 성분 중 하나로 항산화, 항노화, 항우울, 인지기능 개선 등 다수의 약리작용이 보고되었다. 이 연구에서는 Rg1에 의한 신경염증의 제어 가능성을 알아보고자 미세아교세포 BV2에 LPS 및 ATP를 처리하여 신경염증 유발 in vitro 모델을 구축하였다. Western blot 분석을 통해 Rg1 전처리군에서 NLRP3 발현이 유의하게 감소함을 확인하였으나(Fig. 2A), NLRP3의 mRNA 발현수준에는 유의미한 차이가 관찰되지 않았다(Fig. 2B). 이는 Rg1에 의한 NLRP3의 발현 조절은 전사 단계가 아닌 단백 생성 이후의 조절임을 의미하며, NLRP3의 상위 단계 전사인자인 NF-κB p65의 발현에도 큰 변화가 없는 것이 이 결과를 뒷받침한다(Fig. 2C). 따라서 단백 발현 단계에서의 Rg1에 의한 NLRP3의 감소와 관련된 세부 기전에 대한 연구가 필요하다. 추가로 NLRP3와 함께 inflammasome을 구성한다고 알려진 ASC와 caspase-1 등의 mRNA 및 단백질의 변화도 함께 평가하였으나 유의미한 변화는 관찰되지 않았다(Fig. 2D-E).
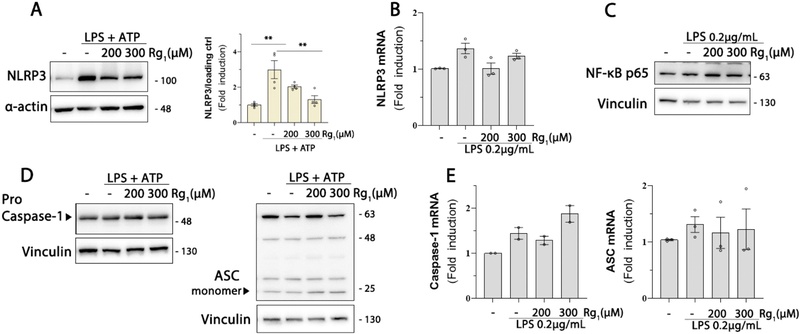
Selective down-regulation of NLRP3 protein by Rg1. (A) Western blot analysis demonstrating that Rg1 pretreatment markedly reduced LPS-induced NLRP3 protein expression. Densitometric quantification of NLRP3, normalized to loading control. (B) qPCR analysis showing no significant changes in NLRP3 mRNA levels following Rg1 pretreatment in LPS-stimulated BV2 microglial cells. (C-D) Western blot for NF-κB p65, procaspase-1 and ASC indicating no significant difference in protein expression with Rg1 treatment. (E) qPCR analysis showing no significant changes in caspase-1 and ASC mRNA levels following Rg1 pretreatment in LPS-stimulated BV2 microglial cells. Data are expressed as mean ± S.E.M of at least three independent experiments. Statistical significance was determined by one-way ANOVA followed by Tukey’s post hoc test (**p < 0.01 and *p < 0.05).
Rg1과 NLRP3의 결합 가능성 평가 – Fig. 2에서 제시된 바와 같이, Rg1은 전사 단계에서 NLRP3의 발현을 조절하지는 않는 것으로 보인다. MCC950은 NLRP3에 직접적으로 결합함으로써 NLRP3의 억제 활성을 보인다고 알려진 물질로, NLRP3와의 직접적인 결합으로 항염 활성을 나타낸다.21) 본 연구에서는 DARTS assay를 통해 Rg1과 NLRP3 단백질의 결합 가능성을 확인하였다(Fig. 3A). Vehicle 처리군에서는 pronase 처리 후 NLRP3 단백질이 현저히 분해되어 band intensity가 감소한 반면, Rg1 처리군에서는 NLRP3 단백질이 상대적으로 안정하게 유지되는 것을 확인하였다(Fig. 3B). 이는 Rg1이 NLRP3 단백질에 직접 결합하여 구조적 안정성을 부여함으로써 pronase에 대한 저항성을 증가시킨 결과로 해석된다.
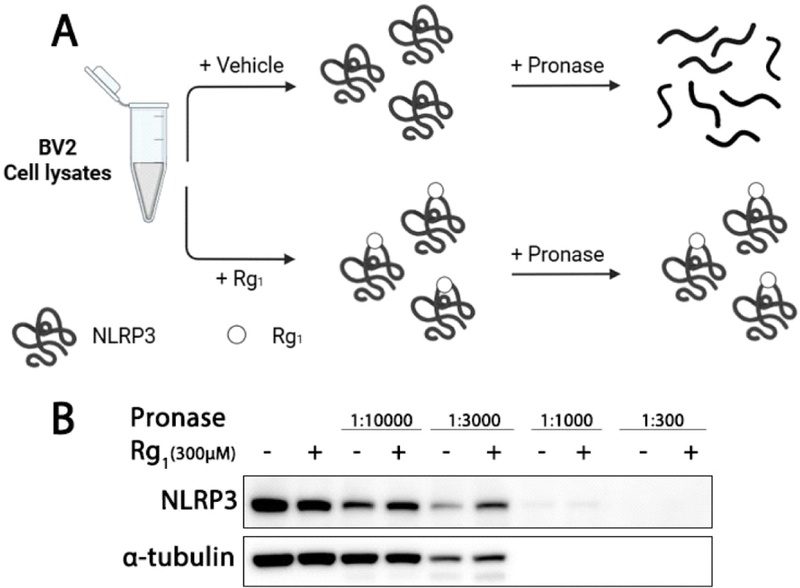
Stabilization of NLRP3 protein by Rg1. (A) BV2 cell lysates were incubated with vehicle or Rg1, followed by limited proteolysis with pronase. (B) Western blot analysis of NLRP3 revealed that Rg1 treatment preserved protein levels compared with vehicle control.
본 연구에서 수행한 DARTS assay 결과는 Rg1이 NLRP3 단백질에 직접적으로 결합할 가능성을 보여주었다. 일반적으로 소분자와 단백질의 결합은 구조적 안정화를 유도하여 protease 분해에 대한 저항성을 증가시키는 것으로 해석되지만, 반대로 특정 결합은 단백질의 구조를 변화시켜 ubiquitin–proteasome system이나 autophagy 경로를 통한 분해를 촉진할 수도 있다.22,23) NLRP3는 ubiquitination 및 선택적 autophagy에 의해 발현 수준이 조절되는 것으로 보고되어 있으며,24,25) Rg1이 이러한 단백질 품질 관리 경로에 영향을 주었을 가능성도 배제할 수 없다. 따라서 본 연구에서 관찰된 Rg1의 효과가 단순히 단백질 안정화에 의한 것인지, 혹은 UPS/autophagy 매개 분해 촉진에 의한 것인지를 명확히 하기 위해서는 proteasome inhibitor (MG132)나 autophagy inhibitor (3-MA, Bafilomycin A1 등)를 활용한 보완 실험이 필요하다. Autophagy 매개 가능성을 알아보기 위해 LC3B의 변화도 확인하였으나 큰 변화는 관찰되지 않았다(data not shown). 또한 cycloheximide chase assay를 통해 NLRP3 단백질의 half-life 변화를 직접 측정한다면 Rg1의 작용 기전을 보다 정밀하게 규명할 수 있을 것이다.
Ginsenoside Rg1에 의한 IL-1β 생성 감소 – NLRP3 inflammasome의 활성화는 caspase-1 절단을 유도하여, 염증성 사이토카인 IL-1β의 성숙과 분비를 촉진한다. LPS/ATP 자극에 의해 유의하게 증가한 IL-1β 단백질 발현이 Rg1 전처리에 따라 감소하는 경향을 보였으며(Fig. 4), 이는 Fig. 2A에서 보여준 NLRP3 발현 억제와도 유사한 양상이다. 이러한 결과는 Rg1이 inflammasome 활성화의 하위 산물인 IL-1β 단백질 생성 또한 효과적으로 억제함을 보여준다. 추가로 NLRP3 inflammasome에 의해 활성화되어 실제 세포 밖으로 유리된 성숙한 IL-1β를 측정하는 실험을 진행 중이다.
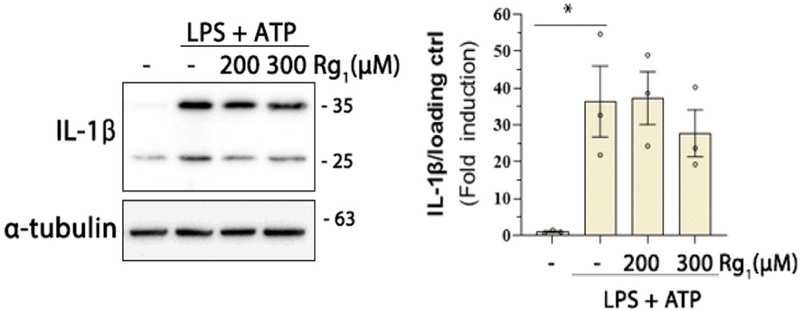
Suppression of IL-1β production by Rg1. Western blot analysis showing that LPS stimulation increased IL-1β protein levels, which were significantly reduced by Rg1 pretreatment. Quantitative analysis of IL-1β protein expression normalized to loading control. Results are expressed as mean ± S.E.M of at least three independent experiments. Statistical analysis was conducted by one-way ANOVA with Tukey’s post hoc test (*p < 0.05).
본 연구에서 확인된 Rg1의 IL-1β 생성 억제 효과는 NLRP3 발현 조절이 실제로 기능적 결과로 이어진다는 점에서 중요한 의미를 갖는다. NLRP3 발현이 줄어들더라도 IL-1β 단백질 수준이 변하지 않는다면 Rg1이 갖는 생리적 의의가 제한될 수 있으나, IL-1β 생성 역시 감소하여 Rg1의 항염증 효과가 분자적 차원을 넘어 염증 매개 사이토카인 생성 억제까지 연결됨을 보여주었다. 이는 기존 연구에서 보고된 Rg1의 항염증 및 신경 보호 효과26,27)를 확장하는 결과로, 특히 NLRP3 inflammasome–IL-1β 축을 직접 조절할 수 있음을 제시한다. 이러한 기전은 알츠하이머병이나 파킨슨병과 같이 IL-1β 과발현이 병리 진행에 중요한 역할을 하는 신경염증성 질환에서 Rg1이 치료적 잠재력을 가질 수 있음을 시사한다.
결 론
본 연구는 ginsenoside Rg1이 BV2 미세아교세포에서 NLRP3 inflammasome 활성을 억제하여 염증성 사이토카인 IL-1β의 생성을 줄일 수 있다는 사실을 보고하였다. 이는 Rg1에 의한 신경염증 반응 완화의 새로운 기전을 제시하며, 알츠하이머병, 파킨슨병 등 inflammasome 매개 질환에서 잠재적 치료 후보물질이 될 수 있음을 시사한다. 향후 연구에서는 동물 모델을 활용해 통해 Rg1의 NLRP3 inflammasome 활성 억제 효과를 검증하고, inflammasome 억제와 연관된 세부 신호전달 경로를 규명할 필요가 있다.
Acknowledgments
이 논문은 2025년도 교육부 및 전북특별자치도의 재원으로 전북RISE센터의 지원을 받아 수행된 지역혁신중심 대학지원체계(RISE)의 결과입니다(2025-RISE-13-WSU).
이해 상충
모든 저자는 이해 상충을 가지고 있지 않음을 선언한다.
References
-
Heneka, M. T., Carson, M. J., El Khoury, J., Landreth, G. E., Brosseron, F., Feinstein, D. L., Jacobs, A. H., Wyss-Coray, T., Vitorica, J., Ransohoff, R. M., Herrup, K., Frautschy, S. A., Finsen, B., Brown, G. C., Verkhratsky, A., Yamanaka, K., Koistinaho, J., Latz, E., Halle, A., Petzold, G. C., Town, T., Morgan, D., Shinohara, M. L., Perry, V. H., Holmes, C., Bazan, N. G., Brooks, D. J, Hunot, S., Joseph, B., Deigendesch, N., Garaschuk, O., Boddeke, E., Dinarello, C. A., Breitner, J. C., Cole, G. M., Golenbock, D. T. and Kummer, M. P. (2015) Neuroinflammation in Alzheimer's disease. Lancet Neurol. 14: 388-405.
[https://doi.org/10.1016/S1474-4422(15)70016-5]

-
DiSabato, D. J., Quan, N. and Godbout, J. P. (2016) Neuroinflammation: the devil is in the details. J. Neurochem. 139 Suppl 2: 136-153.
[https://doi.org/10.1111/jnc.13607]

-
Lecca, D., Jung, Y. J., Scerba, M. T., Hwang, I., Kim, Y. K., Kim, S., Modrow, S., Tweedie, D., Hsueh, S. C., Liu, D., Luo, W., Glotfelty, E., Li, Y., Wang, J. Y., Luo, Y., Hoffer, B. J., Kim, D. S., McDevitt, R. A. and Greig, N. H. (2022) Role of chronic neuroinflammation in neuroplasticity and cognitive function: A hypothesis. Alzheimers Dement. 18: 2327-2340.
[https://doi.org/10.1002/alz.12610]

-
Zhang, W., Xiao, D., Mao, Q. and Xia, H. (2023) Role of neuroinflammation in neurodegeneration development. Signal Transduct. Target. Ther. 8: 267.
[https://doi.org/10.1038/s41392-023-01486-5]

-
Tastan, B. and Heneka, M. T. (2024) The impact of neuroinflammation on neuronal integrity. Immunol. Rev. 327: 8-32.
[https://doi.org/10.1111/imr.13419]

-
Salter, M. W. and Stevens, B. (2017) Microglia emerge as central players in brain disease. Nat. Med. 23: 1018-1027.
[https://doi.org/10.1038/nm.4397]

-
Wilson, D. M., 3rd, Cookson, M. R., Van Den Bosch, L., Zetterberg, H., Holtzman, D. M. and Dewachter, I. (2023) Hallmarks of neurodegenerative diseases. Cell 186: 693-714.
[https://doi.org/10.1016/j.cell.2022.12.032]

-
Colonna, M. and Butovsky, O. (2017) Microglia function in the central nervous system during health and neurodegeneration. Annu. Rev. Immunol. 35: 441-468.
[https://doi.org/10.1146/annurev-immunol-051116-052358]

-
Gao, C., Jiang, J., Tan, Y. and Chen, S. (2023) Microglia in neurodegenerative diseases: mechanism and potential therapeutic targets. Signal Transduct. Target. Ther. 8: 359.
[https://doi.org/10.1038/s41392-023-01588-0]

-
Swanson, K. V., Deng, M. and Ting, J. P. (2019) The NLRP3 inflammasome: molecular activation and regulation to therapeutics. Nat. Rev. Immunol. 19: 477-489.
[https://doi.org/10.1038/s41577-019-0165-0]

-
Xu, W., Huang, Y. and Zhou, R. (2025) NLRP3 inflammasome in neuroinflammation and central nervous system diseases. Cell. Mol. Immunol. 22: 341-355.
[https://doi.org/10.1038/s41423-025-01275-w]

-
Blevins, H. M., Xu, Y., Biby, S. and Zhang, S. (2022) The NLRP3 inflammasome pathway: a review of mechanisms and inhibitors for the treatment of inflammatory diseases. Front. Aging Neurosci. 14: 879021.
[https://doi.org/10.3389/fnagi.2022.879021]

-
Heneka, M. T., Kummer, M. P., Stutz, A., Delekate, A., Schwartz, S., Vieira-Saecker, A., Griep, A., Axt, D., Remus, A., Tzeng, T. C., Gelpi, E., Halle, A., Korte, M., Latz, E. and Golenbock, D. T. (2013) NLRP3 is activated in Alzheimer’s disease and contributes to pathology in APP/PS1 mice. Nature 493: 674-678.
[https://doi.org/10.1038/nature11729]

-
Gordon, R., Albornoz, E. A., Christie, D. C., Langley, M. R., Kumar, V., Mantovani, S., Robertson, A. AB., Butler, M. S., Rowe, D. B., O'Neill, L. A., Kanthasamy, A. G., Schroder, K., Cooper, M. A. and Woodruff, T. M. (2018) Inflammasome inhibition prevents alpha-synuclein pathology and dopaminergic neurodegeneration in mice. Sci. Transl. Med. 10: 465.
[https://doi.org/10.1126/scitranslmed.aah4066]

-
Yang, Y., Ren, C., Zhang, Y. and Wu, X. (2017) Ginseng: an nonnegligible natural remedy for healthy aging. Aging Dis. 8: 708-720.
[https://doi.org/10.14336/AD.2017.0707]

-
Shin, S. W. and Cho, I. H. (2023) Panax ginseng as a potential therapeutic for neurological disorders associated with COVID-19; Toward targeting inflammasome. J. Ginseng Res. 47: 23-32.
[https://doi.org/10.1016/j.jgr.2022.09.004]

-
Yang, X., Chu, S. F., Wang, Z. Z., Li, F. F., Yuan, Y. H. and Chen, N. H. (2021) Ginsenoside Rg1 exerts neuroprotective effects in 3-nitropronpionic acid-induced mouse model of Huntington’s disease via suppressing MAPKs and NF-kappaB pathways in the striatum. Acta Pharmacol. Sin. 42: 1409-1421.
[https://doi.org/10.1038/s41401-020-00558-4]

-
Im, D. S. (2020) Pro-resolving effect of ginsenosides as an anti-inflammatory mechanism of Panax ginseng. Biomolecules 10: 444.
[https://doi.org/10.3390/biom10030444]

-
Sun, Y., Yang, Y., Liu, S., Yang, S., Chen, C., Lin, M., Zeng, Q., Long, J., Yao, J., Yi, F., Meng, L., Ai, Q. and Chen, N. (2022) New therapeutic approaches to and mechanisms of ginsenoside Rg1 against neurological diseases. Cells 11: 2529.
[https://doi.org/10.3390/cells11162529]

-
Pai, M. Y., Lomenick, B., Hwang, H., Schiestl, R., McBride, W., Loo, J. A. and Huang, J. (2015) Drug affinity responsive target stability (DARTS) for small-molecule target identification. Methods Mol. Biol. 1263: 287-298.
[https://doi.org/10.1007/978-1-4939-2269-7_22]

-
Coll, R. C., Hill, J. R., Day, C. J., Zamoshnikova, A., Boucher, D., Massey, N. L., Chitty, J. L., Fraser, J. A., Jennings, M. P., Robertson, A. A. B. and Schroder, K. (2019) MCC950 directly targets the NLRP3 ATP-hydrolysis motif for inflammasome inhibition. Nat. Chem. Biol. 15: 556-559.
[https://doi.org/10.1038/s41589-019-0277-7]

-
Lai, A. C. and Crews, C. M. (2017) Induced protein degradation: an emerging drug discovery paradigm. Nat. Rev. Drug Discov. 16: 101-114.
[https://doi.org/10.1038/nrd.2016.211]

-
He, M., Lv, W. and Rao, Y. (2021) Opportunities and challenges of small molecule induced targeted protein degradation. Front. Cell Dev. Biol. 9: 685106.
[https://doi.org/10.3389/fcell.2021.685106]

-
Zhao, J., He, B., Zhang, S., Huang, W. and Li, X. (2021) Ginsenoside Rg1 alleviates acute liver injury through the induction of autophagy and suppressing NF-kappaB/NLRP3 inflammasome signaling pathway. Int. J. Med. Sci. 18: 1382-1389.
[https://doi.org/10.7150/ijms.50919]

-
O'Keefe, M. E., Dubyak, G. R. and Abbott, D. W. (2024) Post-translational control of NLRP3 inflammasome signaling. J. Biol. Chem. 300: 107386.
[https://doi.org/10.1016/j.jbc.2024.107386]

-
Gao, X. Q., Du, Z. R., Yuan, L. J., Zhang, W. D., Chen, L., Teng, J. J., Wong, M. S., Xie, J. X. and Chen, W. F. (2019) Ginsenoside Rg1 exerts anti-inflammatory effects via G protein-coupled estrogen receptor in lipopolysaccharide-induced microglia activation. Front. Neurosci. 13: 1168.
[https://doi.org/10.3389/fnins.2019.01168]

-
Yang, S. J., Wang, J. J., Cheng, P., Chen, L. X., Hu, J. M. and Zhu, G. Q. (2023) Ginsenoside Rg1 in neurological diseases: from bench to bedside. Acta Pharmacol. Sin. 44: 913-930.
[https://doi.org/10.1038/s41401-022-01022-1]

