식용곤충 배지에서 배양한 동충하초의 성분 및 효능 연구
Abstract
Although edible insects are recognized as excellent protein sources enriched with diverse nutrients, their consumption and utilization remain limited. Cordyceps militaris is a representative entomopathogenic fungus with notable pharmacological activities. Although it is commercially cultivated on rice substrates, insect-based cultivation has been reported to yield higher levels of valuable metabolites such as cordycepin. In this study, the metabolites and the bioactivities of C. militaris were compared by the cultivation on conventional grains and edible insects. Cordyceps was cultivated on rice, barley, and three edible insects such as Protaetia brevitarsis (white-spotted flower chafer), Tenebrio molitor (mealworm), and Gryllus bimaculatus (two-spotted cricket) and both mycelia and fruiting bodies were subjected to metabolite profiling and bioactivity evaluation. The cordycepin content was moderately increased on barley compared to rice but was markedly elevated by approximately 10- to 20-fold when cultivated on insect substrates. Both mycelia and fruiting bodies produced cordycepin, with C. militaris grown on cricket showing 9.2-fold and 22.4-fold higher levels in fruiting bodies and mycelia, respectively, compared to those cultivated on rice. Metabolite profiles also differed significantly between grain and insect substrates, as well as between mycelia and fruiting bodies. Furthermore, anti-inflammatory activity assays revealed that fruiting bodies cultivated on P. brevitarsis exhibited strong efficacy, although variations were observed depending on substrate and tissue types. Therefore, cultivation of C. militaris using edible insects enables the production of high-quality sources enriched with bioactive compounds and represents an important strategy for the utilization of edible insects.
Keywords:
Cordyceps militaris, Edible insects, Cordycepin, Metabolites, Anti-inflammatory activity식용 곤충은 인류가 오랫동안 식량 자원으로 이용해 온 전통적 식품으로, 필수 아미노산을 포함하는 양질의 단백질 공급원이다. 또한 불포화지방산, 철·아연·칼슘 등의 미네랄, 비타민 B군 등 다양한 영양소를 함유하고 있어 영양학적 가치가 높다.1-3) 최근 기후 위기와 전 세계 인구 증가로 인해 지속 가능한 식량자원 확보가 중요한 과제로 대두되면서, 곤충은 가축에 비해 온실가스 배출량이 낮고 사료 및 물 소비량이 적으며, 사육 공간 효율성이 높다는 점에서 환경적으로 우수한 대체 식품 자원으로 평가받고 있다.4,5) 나아가 곤충 유래 성분은 면역조절, 항산화, 항염증, 항균 등 다양한 생리활성을 보이며, 건강기능식품, 의약품, 화장품 소재로의 활용 가능성이 활발히 시도되고 있다. 그러나 식용 곤충의 영양적·환경적 장점에도 불구하고 심리적 거부감과 특유의 향미는 소비 확산의 주요 장애 요인으로 작용한다. 이러한 한계를 극복하기 위해 곤충을 분말, 단백질 분리물, 추출물 등 다양한 가공 형태로 개발하려는 노력이 이어지고 있다.6-8)
버섯은 인류의 주요 식량자원으로 오랜 세월 소비되어 왔으며, 최근에는 건강식품으로서의 가치가 부각되며 소비가 증가하고 있다. 또한 다양한 생리활성 물질이 보고됨에 따라 약용 자원으로서도 중요한 위치를 차지한다. 버섯은 품종에 따라 다양한 대사산물을 생성하며 면역조절, 항산화, 항염, 항종양 등의 활성을 보유하고 있어 식의약 및 천연 기능성 소재로서 활용 가치가 높다.9,10) 동충하초(Cordyceps militaris)는 곤충을 기주로 자라는 특이한 생태적 특성을 지닌 약용버섯으로, 건강식품 소재로 이용되어 왔다.11,12) 뛰어난 약리 활성으로 인해 동충하초의 수요와 산업적 응용 연구는 활발히 진행되고 있으나, 자연 상태에서의 희소성과 까다로운 생육 조건으로 인해 자원 확보에 어려움이 따른다. 이에 따라 인공 배양을 통한 동충하초 자원 확보 연구가 활발히 수행되고 있다.13-15)
현재 동충하초는 경제성과 편의성으로 인해 주로 현미 배지에서 배양·공급되고 있다. 보다 우수한 품질의 동충하초를 확보하기 위한 연구가 진행되고 있으며, 배지 조성 등 배양 조건이 생산성 및 성분 함량에 중요한 영향을 미치는 것으로 보고되고 있다. 특히 곤충을 기주로 자라는 특성을 고려할 때, 식용 곤충을 활용한 배양은 동충하초 생산의 중요한 연구 방향으로 주목받고 있다.16,17)
동충하초의 다양한 생리활성 중 대표적인 성분인 코디세핀은 항암, 항균, 항염 등의 활성이 보고된 바 있으며, 배양 조건에 따른 함량 변화가 연구되어 왔다.18-20) 최근 연구에서 식용곤충 배지를 이용할 경우 코디세핀 함량이 현저히 증가하며, 이는 곤충 내 특정 지질 성분인 올레인산과 관련성이 있는 것으로 제시되었다.21) 또한 곤충의 종류 및 처리 방식에 따라 동충하초의 생장 속도와 대사산물 조성이 달라지며,16) 곤충 부산물을 활용한 배양은 효소 활성과 기능성 대사산물 생산에 긍정적인 영향을 주는 것으로 보고되었다.23) 따라서 곤충은 동충하초 생육 및 대사산물 생합성에 영향을 줄 수 있는 중요한 소재로 제기되고 있으나 다양한 곤충 배지가 미치는 영향에 대한 연구는 아직 미비한 실정이다.
이에 본 연구는 산업곤충을 활용한 동충하초 배양을 통해 새로운 자원을 발굴하고, 기능성 물질의 개발 가능성을 탐색하고자 하였다. 다양한 곤충 배지를 활용하여 동충하초를 배양하고 코디세핀의 함량과 대사체를 분석하였으며 항염 효능을 분석하여 곤충산업과 천연물 기반 기능성 산업의 융합을 통해 고부가가치 곤충 유래 제품 개발의 기반을 마련하는 것을 목적으로 하였다.
재료 및 방법
동충하초의 확보 – 본 연구에 사용된 동충하초(C. militaris)는 2021년 7월 충남 서산에서 채집하였으며, 표본(표본번호 YD2021V01)은 국립농업과학원에 보관되어 있다.
WA (Water agar)와 PDA (Potato dextrose agar) 배지에 채집한 동충하초의 자실체를 부착하여 배지 표면에 낙하한 자낭포자를 수집하고 자낭포자가 수집된 페트리디시를 24℃에서 2일간 배양한 후 백금구 등을 이용하여 단포자를 분리한 후 SDA (Sabouraud dextrose agar) 배지에 접종 후 24℃에서 36-48시간 배양하였다. 교잡하고자 하는 두 개의 단포자를 분리하여 SDB (Sabouraud dextrose broth) 배지에 넣고 24℃에서 60시간 배양 후, 121℃ 25분 동안 멸균한 곡물 배지에 액체배지에서 배양한 배양액을 접종하였으며 자실체에서 발아가 된 것을 확인하고 추후 배양에 활용하였다.
동충하초의 배양 – 갈색거저리(Tenebrio molitor) 및 흰점박이꽃무지(Protaetia brevitarsis)는 살아있는 유충을 세척한 후 사용하였으며 쌍별귀뚜라미(Gryllus bimaculatus)는 건조된 성충을 101℃에서 30분 동안 삶은 후 사용하였다. 이렇게 준비한 곤충을 배양병에 넣고 121℃에서 40분간 살균한 후 24℃로 냉각 후 동충하초를 접종하였다.21) 배양 온도 24℃, 상대습도 30%, 조도 500 lx 배양조건에서 10일간 배양하여 균사체를 생성하였으며, 이후 배양 온도 50°C, 상대습도 70-80%, 조도 500 lx 배양조건에서 50일간 자실체를 배양하였다.
코디세핀 정량 – 동충하초 자실체와 균사체를 분리하여 50℃에서 열풍 건조한 뒤 분말화하고, 시료 약 100 mg에 70% 메탄올 10 mL를 가해 40℃ 초음파 수조에서 60분간 추출하였다. 추출액을 12,000 rpm에서 10분간 원심 분리한 후 상등액을 0.22 μm PTFE 실린지 필터로 여과하여 HPLC (Agilent 1200 series) 분석에 사용하였으며, C18 컬럼(4.6 × 250 mm, 5 μm)과 0.1% TFA 함유 증류수/아세토니트릴(95:5, v/v) 이동상, 유속 1.0 mL/min, 검출 파장 260 nm, 주입량 10 μL의 등용리 조건에서 코디세핀을 분리·측정하였다. Cordycepin 표준용액을 여러 농도로 조제하여 외부 표준 검량 곡선을 작성하고, 시료 피크 면적을 이용해 건조 중량(g)당 코디세핀 함량(μg/g)으로 환산하였다.21)
대사체 분석 – 동충하초 자실체 및 균사체의 건조 분말로부터 메탄올 추출물을 제조하여 대사체 분석을 수행하였다. UPLC 분석은 Column: ACQUITY UPLC HSS T3 (100Å, 1.8μm 2.1 mm × 100 mm), Flow rate: 0.35 mL/min, Injection vol: 1 μL, Column Temp.: 40℃, Mobile phase: H2O containing 0.1% formic acid (A), Acetonitrile containing 0.1% formic acid (B) 조건에서, QTOF/MS은 Capillary voltage: 2.5 Kv, Scan range: m/z 50·600, Cone voltage: 40 V, Desolvation temp.: 150℃, Ion source temp.: 100℃, Calibrator: 0.5 mM sodium formate, Lock mass: leucine-enkephalin 조건에서 수행하였다.
항염 효능 측정 – 마우스의 대식세포인 RAW 264.7 세포에 10% FBS DMEM 배지를 넣고 37℃, 5% CO2의 조건 하에서 배양하였으며, 96 well plate에 5 × 104 cells/well의 세포수로 분주하고 24시간 후 동충하초 시료를 25, 50, 100 μg/mL 농도로 처리하였다. 1시간 후 1 μg/mL lipopolysaccharide를 처리한 후 24시간 동안 배양하여 NO의 생성을 유도하였다. 세포의 생존율은 5 mg/mL MTT solution이 10% 포함된 serum-free 배지를 넣고 2시간 동안 배양한 후 배지를 제거하고 DMSO를 넣은 후 ELISA reader를 이용해 540 nm에서 흡광도를 측정하여 평가하였으며 생성된 NO의 양은 배지 상등액을 NO 측정 시약(1% sulfanilamide와 0.1% N-(1-naphthyl) ethylenediamine dihydrochloride reagent를 1:1로 섞은 용액)과 1:1로 섞어주고 10분간 상온에 보관한 후 540 nm에서 ELISA 측정하여 NO 생성 억제능을 측정하였다.
통계처리 – 모든 실험은 3회 반복으로 실시하였고, 그 결과를 평균 ± 표준편차(mean ± SD)로 표시하였다. 통계학적 비교 분석은 one-way analysis of variance (ANOVA)로 처리하였으며, p값이 0.05 미만인 경우에 통계적으로 유의성이 있는 것으로 판정하였다.
결과 및 고찰
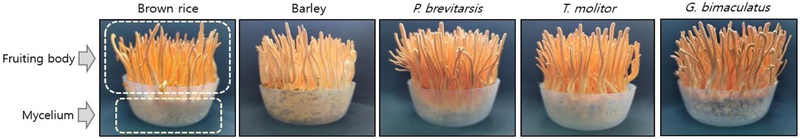
현미, 보리, 쌍별귀뚜라미, 갈색거저리, 흰점박이꽃무지 배지에서 동충하초의 자실체가 모두 형성되었다(Fig. 1). 코디세핀은 동충하초의 대표적인 생리활성 성분으로, 자실체(fruiting body) 뿐만 아니라 균사체(mycelium)에도 존재하며 배양 조건에 따라 함량 차이가 크게 나타난다. 본 연구에서는 현미, 보리, 그리고 세 가지 식용곤충(흰점박이꽃무지, 갈색거저리, 쌍별귀뚜라미)을 배지로 사용하여 동충하초를 배양한 후 자실체 및 균사체의 코디세핀 함량을 측정하였다(Table I).
곡물 배지 중에서는 보리가 현미보다 더 높은 코디세핀 함량을 나타내어, 자실체에서는 2.2배, 균사체에서는 5.2배 증가하였다. 식용곤충을 활용한 경우에는 세 종류 모두 현미보다 유의적으로 높은 함량을 보였다. 자실체 중 코디세핀의 함량은 쌍별귀뚜라미, 갈색거저리, 흰점박이꽃무지에서 배양한 동충하초 순으로 높은 함량을 나타내어 현미 배지에서 배양한 동충하초 대비 각각 9.1배, 5.3배, 3.2배 증가하였다. 균사체에서도 동일한 경향을 보여 각각 22배, 16.1배, 5.6배의 증가가 관찰되었다. 쌍별귀뚜라미 배지에서 배양한 동충하초는 자실체와 균사체 모두에서 가장 높은 수준을 보여, 건조 중량 대비 각각 0.92%와 0.91%의 코디세핀을 함유하였으며 이는 흰점박이꽃무지 배지에서 배양한 것과 비교했을 때 자실체에서 약 2.9배, 균사체에서 약 4.0배 더 높은 수치였다.
이러한 결과는 동충하초 배양에 있어 기존에 널리 사용되는 현미 배지보다 보리와 같은 대체 곡물이 코디세핀 생산성을 높일 수 있으며 곤충을 배지로 활용할 경우 곡물에 비해 현저히 높은 코디세핀 함량을 확보할 수 있음을 시사한다. 또한 곤충의 종류에 따라서도 큰 차이가 나타나 곤충의 종류 및 성장 단계 등 여러 조건의 최적화 연구를 통해 더욱 우수한 동충하초 소재를 개발할 수 있음을 보여준다. 쌍별귀뚜라미(Gryllus bimaculatus)를 배지로 활용한 경우 자실체 및 균사체 모두에서 가장 높은 함량을 나타내었으며, 이는 현미 배지 대비 각각 약 9.2배 및 22.4배 증가한 수치로, 곤충 배지가 동충하초의 생리적 특성과 높은 적합성을 지님을 시사한다. 선행연구에서 곤충 내 지질 성분, 특히 올레산과 같은 생합성 유도물질 함량은 곤충별로 차이가 있으며 이러한 인자들이 코디세핀 생산에 영향을 주는 것으로 보고하였다.21,22,23) 본 연구에서 수행한 곤충 종류에 따른 코디세핀의 함량은 기존의 연구21)와 다소 차이를 보이며 이는 곤충하초의 균주, 배양 조건 및 곤충의 생육에 따른 조성 등이 영향을 주는 것으로 보이며 추후 이러한 영향 인자의 분석 및 배양조건의 최적화 연구를 통하여 우수한 동충하초의 개발이 가능할 것으로 사료된다.
동충하초에는 코디세핀 외에도 다양한 대사산물을 함유하고 있으며, 이들이 복합적으로 효능에 기여할 것으로 예상되나 그 성분에 대한 연구는 아직 미비하였다. 이에 현미, 보리, 갈색거저리, 흰점박이꽃무지, 쌍별귀뚜라미 배지에서 배양한 자실체 및 균사체를 대상으로 대사체를 분석하고, 배지 및 부위별 대사체 분포를 비교하였다.
LC-MS 분석 결과 총 42개의 피크가 확인되었으며, 데이터베이스를 활용한 성분 유추 과정에서 코디세핀과 같은 주요 성분 외에도 다수의 성분을 확인하였다. 그러나 많은 성분이 기존 데이터베이스와 일치하지 않았다(Table II). 이는 곤충 기반 배지에서 배양한 동충하초에 대한 연구가 아직 제한적이며, 관련 대사체 데이터베이스가 충분히 축적되지 않았기 때문으로 판단된다. 따라서 이러한 미확인 성분에 대한 구조 규명 및 생리활성 연구가 필요하다.
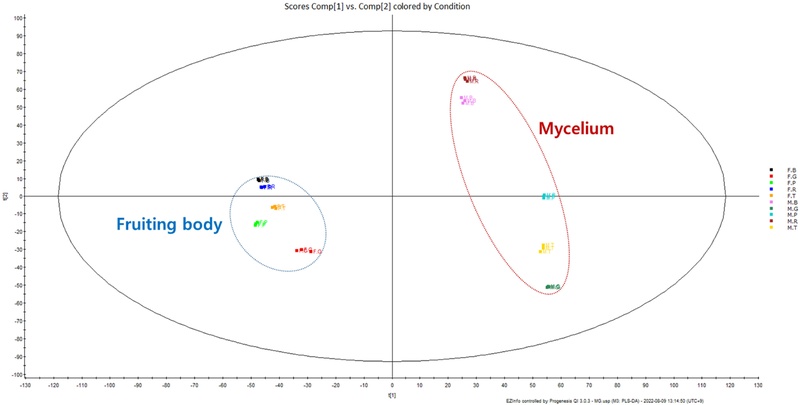
동충하초의 대사체를 부위별 비교 분석한 결과, 자실체와 균사체는 서로 다른 대사체 조성을 가지며 뚜렷하게 구분되는 그룹을 형성하였다(Fig. 2). 특징적인 성분을 살펴보면, 자실체에서는 beauveriolides 계열 화합물이 관찰되었으며, 균사체에서는 ustiloxins 계열 물질 및 다양한 새로운 성분이 확인되었다(Fig. 3). 이는 자실체와 균사체가 공통적으로 코디세핀을 함유하고 있으면서도, 추가적인 대사산물의 구성에서 뚜렷한 차이를 나타냄을 시사한다. 이러한 차별적 대사산물은 새로운 기능성 소재로서 발굴될 가능성이 있으며, 향후 연구를 통해 그 구조와 효능을 규명할 필요가 있다.
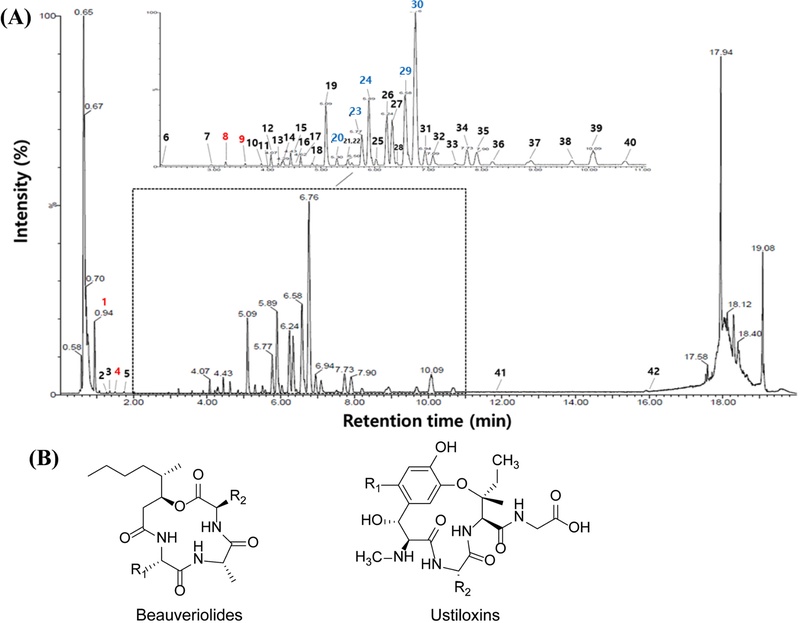
LC-MS Chromatograms of C. militaris extract (A) and characteristic compounds in fruiting body and mycelium (B).
자실체와 균사체를 곡식과 식용곤충별로 비교 분석한 결과에서도 곤충에서 배양한 성분은 곡물에서 배양한 동충하초와 차이를 보였으며 식용곤충별로도 대사체의 조성에 차이를 보였다(Fig. 4). 따라서 동충하초의 성분은 배지 및 부위에 따라 다르며,24) 이러한 조건의 최적화를 통하여 우수한 소재의 발굴이 가능하다고 사료된다.
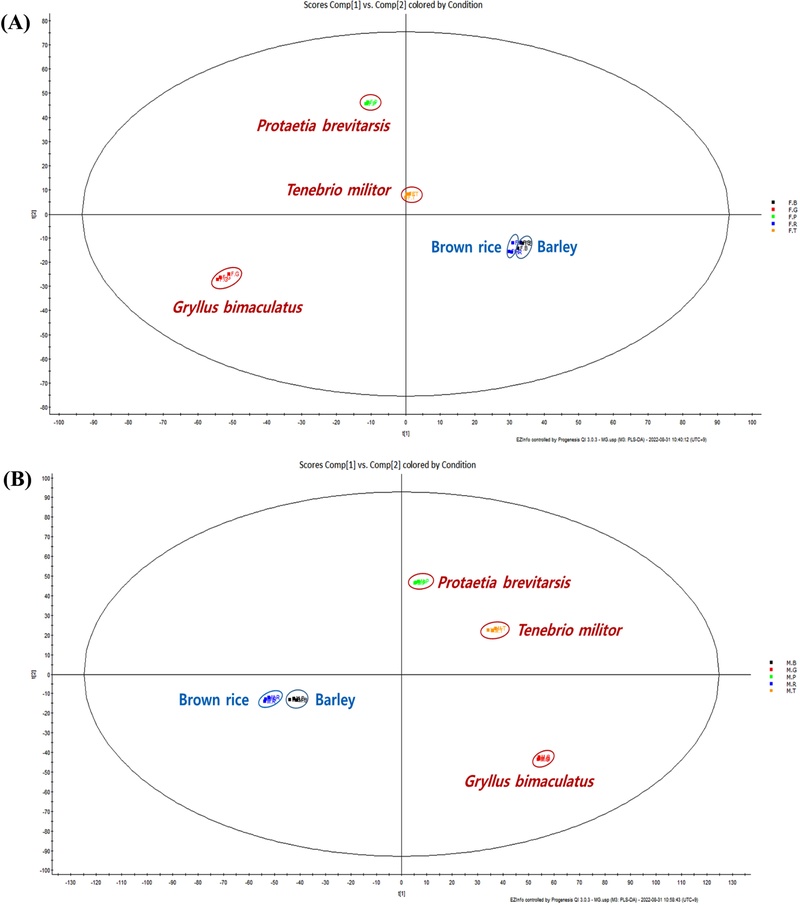
PLS-DA score plot of fruiting body (A) and mycelium (B) of C. militaris cultivated on different substrates.
동충하초는 항염을 포함한 다양한 효능이 보고되어 있으며 이에 다양한 배지에서 배양한 동충하초의 자실체 및 균사체의 항염 효능을 분석하였다. 보리에 배양한 동충하초의 자실체의 경우 현미에서 배양한 자실체보다 우수한 항염효능을 나타내어 곡물배지에 따른 효능의 차이를 보였다(Table III). 또한 곤충을 배지로 활용한 경우 전체적으로 우수한 항염 효능을 나타내었으며 흰점박이꽃무지에서 배양한 동충하초 자실체가 가장 뛰어난 효능을 나타내었다. 이러한 항염 효능은 코디세핀의 함량과는 일치하지 않았다. 대사체 분석 결과에서 곤충에서 배양한 동충하초는 코디세핀 뿐만 아니라 다양한 대사체를 함유하고 있으며 따라서 이러한 효능은 동충하초에 함유된 다양한 대사체가 함께 관여하는 것으로 생각된다.18)
결 론
본 연구에서는 동충하초를 기존에 널리 사용되는 현미 배지 이외에도 보리 및 세 종의 식용곤충(갈색거저리, 흰점박이꽃무지, 쌍별귀뚜라미)을 이용하여 배양하였다. 코디세핀 함량 분석 결과, 식용곤충 배지에서 배양한 경우 곡물 배지보다 현저히 높은 수치를 보였으며, 곤충의 종류에 따라 차이가 존재하였다. 또한 LC-MS/MS 기반의 대사체 분석에서는 자실체와 균사체가 뚜렷하게 구분되는 조성을 보였으며, 곤충별로도 대사체 차이가 나타났다. 항염 효능 평가에서는 흰점박이꽃무지 배지에서 배양한 자실체가 가장 높은 활성을 보였으며, 배지의 종류와 부위에 따라 효능이 달라지는 양상을 확인하였다.
현재 식용곤충은 지속가능한 식량자원으로서 환경적 장점과 영양학적 우수성을 지니고 있으나, 소비 확산에는 심리적·기호적 장벽이 존재한다. 본 연구는 식용곤충을 동충하초 배양의 기주로 활용함으로써 기능성 성분의 함량 증진과 생리활성 강화라는 두 가지 측면에서 곤충자원의 새로운 활용 가능성을 제시하였다. 특히 곤충의 종류에 따라 성분 및 효능이 달라지는 점은 향후 배양 조건의 정밀한 최적화를 통해 고부가가치 기능성 소재 개발이 가능함을 보여준다. 이러한 결과는 식용곤충 기반 동충하초 배양이 산업적·학술적 측면의 중요한 가치를 뒷받침하며 곤충산업과 천연물 기반 기능성 산업의 융합을 통한 전략적 연구 방향으로 제시될 수 있다.
Acknowledgments
이 논문은 농촌진흥청 박민지 전문연구원의 농업과학기술 개발 공동연구사업(과제번호 RS-2021-RD010149) 및 2025 농촌진흥청 펠로우십 프로그램의 지원을 받아 수행되었으며 이에 감사드립니다.
References
-
Nowakowski, A. C., Miller, A. C., Miller, M. E., Xiao, H. and Wu, X. (2022) Potential health benefits of edible insects. Crit. Rev. Food Sci. Nutr. 62: 3499-3508.
[https://doi.org/10.1080/10408398.2020.1867053]

-
Rumpold, B. A. and Schlüter, O. K. (2013) Nutritional composition and safety aspects of edible insects. Mol. Nutr. Food Res. 57: 802-823.
[https://doi.org/10.1002/mnfr.201200735]

-
Alejandro, R. F. E., Ortega, J. F., Tejera, E. and Alvarez-Suarez, J. M. (2025) Edible insects as functional foods: bioactive compounds, health benefits, safety concerns, allergenicity, and regulatory considerations. Front. Nutr. 12: 1571084.
[https://doi.org/10.3389/fnut.2025.1571084]

-
Nachtigall, L., Grune, T. and Weber, D. (2025) Proteins and amino acids from edible insects for the human diet-A narrative review considering environmental sustainability and regulatory challenges. Nutrients 17: 1245.
[https://doi.org/10.3390/nu17071245]

-
Berggren, Å., Jensen, A. B., Copplestone, D., Guidetti, R., Heer, M. and Pittia, P. (2025) Insects in bioregenerative life support systems: unlocking their role in space sustainability. Front. Physiol. 16: 1621099.
[https://doi.org/10.3389/fphys.2025.1621099]

-
Ishara, J., Ekaette, I., Matendo, R., Vandenberg, G., Niassy, S., Katcho, K. and Kinyuru, J. (2025) Potential health benefits of insect bioactive metabolites and consumer attitudes towards edible insects. NPJ Sci. Food 9: 195.
[https://doi.org/10.1038/s41538-025-00549-x]

-
Zołnierczyk, A. K. and Szumny, A. (2021) Sensory and chemical characteristic of two insect species: Tenebrio molitor and Zophobas morio larvae affected by roasting processes. Molecules 26: 2697.
[https://doi.org/10.3390/molecules26092697]

-
Kim, B. S., Turk, A., Lee, S., Lee, H. H., Kim, M. H., Jeong, S. Y., Kwon, E. B., Hwang, B. Y. and Lee, M. K. (2025) Anti-diabetic activity of Cordyceps-fermented edible insects by the promotion of glucose absorption. J. Med. Food 28: 105-111.
[https://doi.org/10.1089/jmf.2024.k.0230]

-
Chang, S. T. and Wasser, S. P. (2018) Current and future research trends in agricultural and biomedical applications of medicinal mushrooms and mushroom products (Review). Int. J. Med. Mushrooms 20: 1121-1133.
[https://doi.org/10.1615/IntJMedMushrooms.2018029378]

-
Ishara, J., Buzera, A., Mushagalusa, G. N., Hammam, A. R. A., Munga, J., Karanja, P. and Kinyuru, J. (2022) Nutraceutical potential of mushroom bioactive metabolites and their food functionality. J. Food Biochem. 46: e14025.
[https://doi.org/10.1111/jfbc.14025]

-
Phull, A. R., Ahmed, M. and Park, H. J. (2022) Cordyceps militaris as a biofunctional food source: Pharmacological potential, anti-Inflammatory actions and related molecular mechanisms. Microorganisms 10: 405.
[https://doi.org/10.3390/microorganisms10020405]

-
Łysakowska, P., Sobota, A. and Wirkijowska, A. (2023) Medicinal mushrooms: Their bioactive components, nutritional value and application in functional food production-A Review. Molecules 28: 5393.
[https://doi.org/10.3390/molecules28145393]

-
Cui, J. D. (2015) Biotechnological production and applications of Cordyceps militaris, a valued traditional Chinese medicine. Crit. Rev. Biotechnol. 35: 475-484.
[https://doi.org/10.3109/07388551.2014.900604]

-
Krishna, K. V., Balasubramanian, B., Park, S., Bhattacharya, S., Kadanthottu, S. J., Liu, W. C., Pappuswamy, M., Meyyazhagan, A., Kamyab, H., Chelliapan, S. and Malaviya, A. (2025) Conservation of endangered Cordyceps sinensis through artificial cultivation strategies of C. militaris, an alternate. Mol. Biotechnol. 67: 1382-1397.
[https://doi.org/10.1007/s12033-024-01154-1]

-
Raethong, N., Wang, H., Nielsen, J. and Vongsangnak, W. (2019) Optimizing cultivation of Cordyceps militaris for fast growth and cordycepin overproduction using rational design of synthetic media. Comput. Struct. Biotechnol. J. 18: 1-8.
[https://doi.org/10.1016/j.csbj.2019.11.003]

-
Wongsorn, D., Surasilp, T. and Rattanasuk, S. (2021) Effects of edible insects on the mycelium formation of Cordyceps militaris. Pak. J. Biol. Sci. 24: 881-887.
[https://doi.org/10.3923/pjbs.2021.881.887]

-
Turk, A., Kim, B. S., Ko, S. M., Yeon, S. W., Ryu, S. H., Kim, Y. G., Hwang, B. Y. and Lee, M. K. (2021) Optimization of cultivation and extraction conditions of pupae-Cordyceps for cordycepin production. Nat. Prod. Sci. 27: 187-192.
[https://doi.org/10.20307/nps.2021.27.3.187]

-
Yu, J., Sun, M., Wang, X., Qi, D. and Han, C. (2023) Poly-pathways metabolomics for high-yielding cordycepin of Cordyceps militaris. Biomed. Chromatogr. 37: e5551.
[https://doi.org/10.1002/bmc.5551]

-
Wang, L., Yan, H., Zeng, B. and Hu, Z. (2022) Research progress on cordycepin synthesis and methods for enhancement of cordycepin production in Cordyceps militaris. Bioengineering 9: 69.
[https://doi.org/10.3390/bioengineering9020069]

-
Kontogiannatos, D., Koutrotsios, G., Xekalaki, S. and Zervakis, G. I. (2021) Biomass and cordycepin production by the medicinal mushroom Cordyceps militaris-A Review of various aspects and recent trends towards the exploitation of a valuable fungus. J. Fungi. 7: 986.
[https://doi.org/10.3390/jof7110986]

-
Turk, A., Abdelhamid, M. A. A., Yeon, S. W., Ryu, S. H., Lee, S., Ko, S. M., Kim, B. S., Pack, S. P., Hwang, B. Y. and Lee, M. K. (2022) Cordyceps mushroom with increased cordycepin content by the cultivation on edible insects. Front. Microbiol. 13: 1017576.
[https://doi.org/10.3389/fmicb.2022.1017576]

-
Trung, N. Q., Dat, N. T., Anh, H. N., Tung, Q. N., Nguyen, V. T. H., Van, H. N. B., Van, N. M. N. and Minh, T. N. (2024). Substrate influence on enzymatic activity in Cordyceps militaris for health applications. Chemistry 6: 517-530.
[https://doi.org/10.3390/chemistry6040030]

-
Krishna, K. V., Ulhas, R. S. and Malaviya, A. (2023) Bioactive compounds from Cordyceps and their therapeutic potential. Crit. Rev. Biotechnol. 44: 753-773.
[https://doi.org/10.1080/07388551.2023.2231139]

- Park, M. J., Kim, E., Park, K., Song, J. -H., Ji, S., Koo, B. and Kim, S. Y. (2025) Nutritional enhancement of Cordyceps militaris cultivated on insect-based substrates using Tenebrio molitor larvae. Int. J. Indust. Entomol. Biomater. 49: 180-190.