도라지 뿌리의 부위별 사포닌 함량 및 항산화활성
Abstract
Platycodon grandiflorus, a member of the Campanulaceae family, is found throughout East Asia, including Korea, China, and Japan. This plant is abundant in antioxidant compounds, including triterpenoid saponins, flavonoids, phenolics, and polysaccharides. In this study, we evaluated the antioxidant activity of 70% methanol extracts from various parts of the P. grandiflorus root, specifically the head root, taproot, rootlet, and fine root. We measured the DPPH and ABTS radical scavenging activities, conducted the FRAP assay, and determined the total saponin, total phenolic, and total flavonoid contents. Additionally, we used Pearson’s correlation coefficients to explore the relationships between the antioxidant constituents and their activities. Our results suggest that each part of the P. grandiflorus root has potential as a valuable antioxidant treatment and provide a foundation for the standardization of its root.
Keywords:
Platycodon grandiflorus, Antioxidant activity, Antioxidant constituents, Correlation analysis산화적 손상은 체내에서 과도하게 생성된 활성산소종에 의하여 발생하며, 일정 수준에서는 세포 신호전달과 면역 반응 등에 관여하지만, 과도하게 생성될 경우에는 세포막과 단백질, DNA 등을 손상시킴으로써 생리적 기능을 떨어뜨린다. 또한, 산화적 스트레스에 대한 노출은 노화나 암, 당뇨병, 심혈관질환 등의 다양한 만성질환의 발생과 밀접한 관련이 있는 것으로 알려져 있다.1)
인체는 이와 같은 산화적 손상을 억제하기 위하여 항산화효소를 만들어 방어하고 있으며,1) 외부로부터 항산화 활성을 가진 성분을 섭취함으로써 이를 보완한다. 최근에는 천연 항산화 소재에 대한 관심이 높아지고 있고, 특히 식물 유래 항산화 물질은 부작용이 적고 생리활성이 우수한 것으로 밝혀지면서, 기능성 식품, 의약품, 화장품 등 다양한 산업 분야에서 활발히 활용되고 있다.2-4)
항산화작용은 일반적으로 자유라디칼을 직접 소거시키거나 금속 이온과 결합하거나 불활성시키고, 항산화 효소의 활성을 조절하여 활성산소종의 생성을 억제하거나 제거하는 방식으로 이루어진다.5) 이러한 작용을 나타내는 대표적인 천연 성분으로는 플라보노이드, 페놀화합물, 사포닌 등이 있으며, 이 중 사포닌은 항산화작용 뿐만 아니라 항염증, 항암 활성 또한 지니는 것으로 알려져 있다.6,7)
따라서 이러한 사포닌이 다량 함유되어 있는 도라지는 천연 항산화 물질로서의 가치를 가지고 있다. 도라지 Platycodon grandiflorus (Jacq.) A.DC.는 초롱꽃과(Campanulaceae)에 속하는 다년생 초본식물로, 한국, 중국, 일본 등의 지역에서 자생하며, 전통적으로 기침, 가래, 인후통 등의 호흡기 질환의 치료에 사용되어 왔다.8) 한의학에서는 도라지의 뿌리를 길경(桔梗)이라 하며, 고(苦), 신(辛)한 약미(藥味)에 평(平)한 약성(藥性)을 가지고 있고, 선폐이인(宣肺利咽), 거담지해(祛痰止咳), 배농소종(排膿消腫)의 효능을 가지고 있다고 알려져 있다.9)
도라지 뿌리의 주요 활성성분으로는 platycodin A, C, D, D2, D3, deapioplatycodin D, 16-oxo-platycodin D, polygalacin D 등과 같은 triterpenoid saponin 계열의 성분들이 분리보고되었고, luteolin-7-O-glucoside, apigenin-7-O-glucoside, platyconin, platycoside 등의 flavonoid 계열의 성분들과 그 외 lobetyol, palmitic acid, oleic acid, γ-aminobutyric acid, caffeic acid, ferulic acid, chlorogenic acid, lobetyolinin, α-spinasteryl-3-O-β-D-glucoside, inulin 등이 분리보고되었다.10)
이러한 활성성분을 기반으로 도라지 뿌리는 항산화활성을 비롯하여 항염증, 항균 및 항종양활성 등 다양한 생리활성을 나타내는 것으로 알려져 있다.11,12) 즉, 도라지 뿌리의 추출물은 활성산소종을 소거하여 세포손상을 억제할 뿐만 아니라 체내 면역시스템을 활성화하고, 염증매개인자의 발현을 조절하는 등의 중요한 역할을 하는 것으로 보고되었다.13) 이에 더하여 최근에는 항산화활성에 기반한 항비만작용 및 간보호작용와 같은 대사성 질환의 개선효과까지 보고되면서 천연 항산화제로서의 가능성을 입증하였다.10)
한편, 그 동안 인삼이나 당귀, 홍삼, 백지와 같은 일부 근류 생약에 대하여 뿌리의 부위에 따른 성분 및 활성연구가 이루어져, 세근(細根)이나 지근(枝根) 부위가 주근(主根)에 비하여 사포닌 및 페놀성 화합물 등의 유효성분의 함량이 월등히 높거나 생리활성이 더 높다는 연구결과들이 보고되었다.14-17) 그러나 도라지의 경우에는 세척의 용이성이나 상품의 모양을 좋게 하기 위하여 세근 등의 부위는 깎여져 버려진 채로 주근 위주로 소비되고 있다. 또한, 도라지 뿌리는 가공 방법에 따른 차이나 지상부와 지하부의 차이에 대한 연구는 다수 진행되었으나,18-21) 뿌리의 각 부위에 따른 성분연구 및 생리활성 비교연구가 아직 미흡한 실정이다. 이에 본 연구에서는 우리나라 재래종에서 계통분리한 품종으로 흰꽃이 피며 뿌리가 길고 굵으며 수량성이 높다고 알려진 장백도라지 품종22)을 대상으로 도라지 뿌리의 각 부위별 사포닌성분 함량과 항산화능을 비교분석하고자 하였다.
재료 및 방법
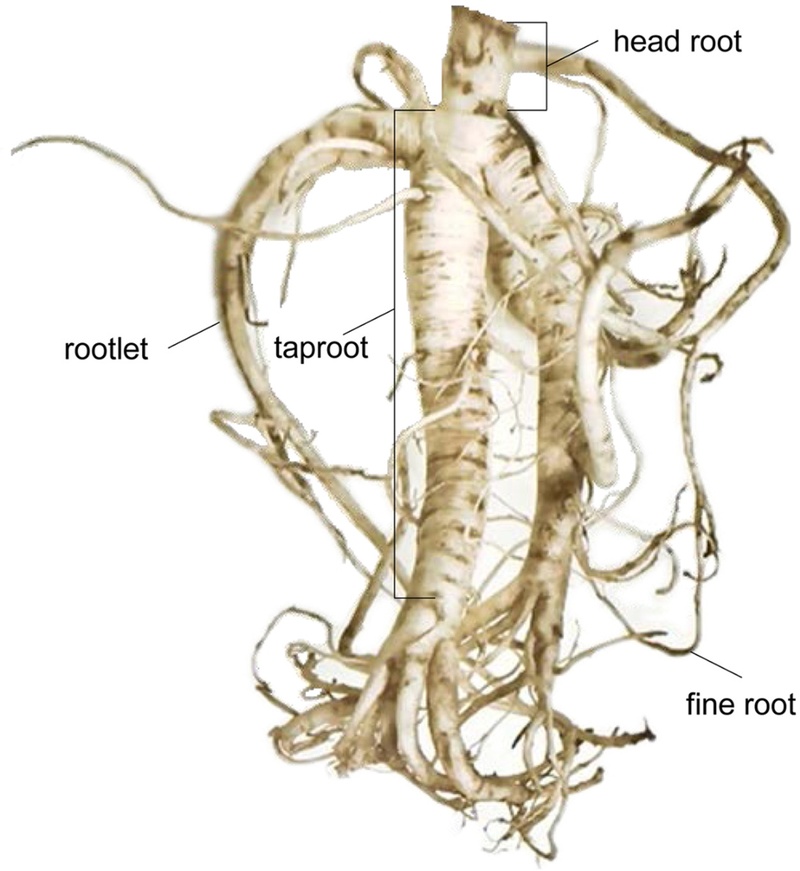
식물재료 – 경상남도 함양군 안의면 경상남도농업기술원 약용자원연구소 부속농장에서 2024년 4월에 파종한 재래종 백도라지(장백도라지)의 뿌리를 2024년 11월에 채취하여 수확한 당일 흐르는 수돗물로 세척하였다. 세척한 1년근 도라지 일곱 뿌리를 뿌리별로 뇌두와 주근, 지근, 세근으로 나누어 각각의 무게를 측정하였다(Fig. 1). 수확한 도라지는 경상국립대학교 안미정 교수의 감정을 받은 후 사용하였으며, 일부는 표본(PGSC-660)으로 제작하여 경상국립대학교 표본실(Herbarium of the College of Pharmacy, Gyeongsang National University)에 보관 중이다.
시약 – 추출에 사용된 메탄올과 물은 Daejung Chemicals & Metals (Siheung, South Korea)에서 구입하여 사용하였으며, 총사포닌 함량 측정에 사용한 vanillin은 Sigma-Aldrich Co. (ST. Louis, MO, USA)에서 구입하여 사용하였다. 대조물질로 사용한 Trolox, FeSO4·7H2O, gallic acid, quercetin은 Sigma-Aldrich Co. (ST. Louis, MO, USA)에서 구입하여 사용하였다. Platycodin D는 Ambo Institute (Daejeon, South Korea)에서 구입하여 사용하였다. 그 외 시약은 1급시약을 사용하였다.
추출 – 앞에서 나눈 뇌두, 주근, 지근, 세근 각 부위를 부위별로 합친 다음 분쇄기로 간 다음 분석시료로 사용하였다(Fig. 1). 각 시료들을 5 g씩 취하여 70% 메탄올 100 mL로 60분씩 3회 초음파 추출하여 얻은 추출물로 DPPH와 ABTS 라디칼 소거능 및 FRAP 환원능 실험과 총페놀과 총플라보노이드, 총사포닌 함량을 측정하였다.
총사포닌 함량 측정 – 총사포닌 함량은 vanillin-H2SO4 비색법을 사용하여 측정하였다.23) 즉, 도라지 뿌리 부위별 추출물 각각 100 µL에 8% vanillin-ethanol 용액 250 µL를 가한 후, 60% sulfuric acid 용액을 2.5 mL를 넣고 잘 섞어준 다음 70℃에서 10분간 가열하였다. 이후 ice bath에서 5분 동안 식혀준 다음 UV-Vis 측정기(Optical Spectrum Analyzer, Optizen, Daejeon, South Korea)를 이용하여 545 nm에서의 흡광도를 측정하였다. 총사포닌 함량은 platycodin D를 표준물질로 하여 µmol platycodin D equivalent (PDE)/g·FW 값으로 표시하였다.
총페놀 및 총플라보노이드 함량 측정 – 총페놀 및 총플라보노이드 함량은 이전에 보고된 방법을 이용하여 분석하였다.24,25) 즉, 도라지 뿌리추출물 100 µL에 10% Folin-Ciocaleu’s phenol reagent (FCPR; Sigma-Aldrich Co., ST. Louis, MO, USA) 500 µL를 가한 후, 200 mM의 Na2CO3 용액 400 µL를 넣고, 차광조건 하에서 5분 동안 실온에서 반응시켜 준 다음 60 × g에서 3분간 원심분리하였다. 상등액 200 µL를 취하여 96 well에 넣고 micro plate reader (PerkinElmer, Inc., Victor X5, Shelton, CT, USA)를 이용하여 765 nm에서 흡광도를 측정하였다. 총페놀 함량은 gallic acid를 표준물질로 하여 µmol gallic acid equivalent (GAE)/g·FW 값으로 표시하였다. 총플라보노이드 함량은 96 well에 각 시료용액 20 µL를 넣고 90% diethyl glycerol 160 µL를 가한 후, 2M의 NaOH 용액 20 µL를 넣고 차광조건 하에서 10분 동안 실온에서 교반하면서 반응시킨 다음 micro plate reader를 이용하여 420 nm에서의 흡광도를 측정하였다. 총플라보노이드 함량은 quercetin을 표준물질로 하여 µmol quercetin equivalent (QE)/g·FW 값으로 표시하였다.
DPPH 라디칼 소거활성 측정 – DPPH 라디칼 소거능은 이전에 보고된 방법을 이용하여 분석하였다.26) 즉, 2,2-diphenyl-1-picrylhydrazyl (DPPH; Sigma-Aldrich Co., ST. Louis, MO, USA)을 1 mM의 농도로 메탄올에 용해시킨 후 520 nm 파장에서의 흡광도 값이 0.7–1 사이의 값이 되도록 희석하여 사용하였다. 96 well plate에 시료를 20 μL씩 넣고 희석한 DPPH 용액 180 μL를 넣은 다음, 차광조건 하에서 10분 동안 실온에서 교반하면서 반응시킨 후 micro plate reader를 이용하여 520 nm에서의 흡광도를 측정하였다. 라디칼 소거활성 정도는 trolox를 표준물질로 하여 µmol trolox equivalent (TE)/g·FW 값으로 표시하였다.
ABTS 라디칼 소거활성 측정 – ABTS 라디칼 소거능은 이전에 보고된 방법을 이용하여 분석하였다.27) 즉, 2.45 mM 과황산칼륨(Sigma-Aldrich Co., ST. Louis, MO, USA) 수용액에 최종농도가 7 mM이 되도록 2,2'-Azino-bis(3-ethylbenzothiazoline-6-sulfonic acid) diammonium salt (ABTS; Thermo Fisher Scientific, Waltham, MA, USA)를 녹인 다음 차광조건 4℃에서 16시간 반응시켜 ABTS·+ 라디칼 용액을 만들었다. 이상으로 제조한 라디칼 용액을 405 nm에서의 흡광도 값이 약 0.7이 나오도록 물로 희석하였다. 20 μL의 시료액에 980 μL의 희석한 ABTS·+ 라디칼 용액을 가하고 차광조건 하에서 5분 동안 실온에서 교반하여 반응시킨 후 405 nm에서의 흡광도를 측정하였다. 라디칼 소거활성 정도는 trolox를 표준물질로 하여 µmol trolox equivalent(TE)/g·FW 값으로 표시하였다.
FRAP (ferric reducing antioxidant power)를 이용한 항산화능 측정 – Fe3+ 이온이 Fe2+ 이온으로 환원되어 짙은 푸른색의 ferrous-tripyridyltriazine 복합체를 형성하는 반응을 이용하여 도라지 추출물의 항산화능을 측정하였다.28) 즉, 300 mM sodium acetate buffer (pH 3.6) (A 용액)(Junsei, Seitama, Japan)와 40 mM HCl (Matsunoen Chem., Osaka, Japan) 5 mL에 10 mM의 TPTZ (2,4,6-tripyridyl-s-triazine, Fluka, Buchs, Switzerland) 5 mL를 혼합한 용액(B 용액), 그리고 20 mM FeCl3·6H2O 수용액(C 용액)(Sigma, Shanghai, China)을 10:1:1 (A:B:C, v/v/v)의 비율로 혼합하여 FRAP 시약을 만들었다. 96 well plate에 20 μL의 시료액을 넣고 FRAP 시약 180 μL를 넣은 다음 37℃에서 5분간 반응시킨 후 593 nm에서의 흡광도를 측정하였다. 시료의 항산화능은 FeSO4·7H2O (Junsei, Seitama, Japan)를 표준물질로 하여 µmol Fe/g·FW 값으로 표시하였다.
통계처리 – 모든 데이터는 3회 반복으로 시행하였으며, 평균값(mean) ± 표준편차(standard deviation, SD)로 그 결과값을 표현하였다. 일원배치 분산분석(One-way ANOVA)을 통한 통계학적 비교분석과 Pearson’s 상관관계 분석에는 IBM SPSS Statistics 24.0 (Armonk, NY, USA)를 이용하였으며, 신뢰구간 p < 0.05로 유의성을 검증하였다.
결과 및 고찰
본 연구에 사용한 장백도라지 1년근의 뿌리 하나당 중량의 평균값은 41.87 ± 27.66g으로 각 뿌리마다 중량에 있어서의 차이가 큰 편이었다. 주근(taproot)과 지근(rootlet)이 차지하는 비율이 각각 29.58 ± 21.04%와 64.93 ± 23.92%로 주근보다 지근이 차지하는 비율이 월등이 높았다(Table I). 이는 일반 재래종의 경우 1년근의 지근이 0~2개인데 비해 장백도라지의 경우 2~5개로 많은 것에 기인한다고 볼 수 있다.29) 뇌두(head root)가 차지하는 비율이 1.19 ± 1.72%로 가장 낮았으며, 그 다음으로 세근(fine root)이 4.30 ± 2.46%로 낮았다. 이상으로 도라지 뿌리를 각 부위별로 나누어 총사포닌 함량을 비롯한 항산화활성을 측정하여 다음과 같은 결과를 얻었다.

Weight and total saponin, total phenolic and flavonoid contents of different parts of P. grandiflorus root#
바닐린-황산법을 이용한 총사포닌 함량 비교 – 바닐린-황산 비색법을 통하여 도라지 뿌리의 각 부위에 따른 총사포닌 함량을 비교분석하였다(Table I). 그 결과, 세근의 총사포닌 함량이 372.91 ± 13.70 µmol PDE/g·FW로 가장 높았으며, 다음으로 지근(312.71 ± 15.92 µmol PDE/g·FW)과 뇌두(312.44 ± 14.52 µmol PDE/g·FW)가 높았다. 주근의 총사포닌 함량은 288.16 ± 8.65 µmol PDE/g·FW로 가장 낮았다(Table I). 이러한 결과는 같은 근류생약인 인삼에서의 총사포닌 함량이 미삼(세근), 뇌두, 동체(주근) 순으로 높았다는 기존의 연구결과와 일치한다.30)
도라지 뿌리의 부위별 총페놀 및 총플라보노이드 함량 비교 – 도라지 뿌리의 각 부위별 총페놀 함량을 측정한 결과, 세근의 총페놀 함량이 98.75 ± 5.22 µmol GAE/g·FW로 가장 높았으며, 그 다음으로 지근(42.30 ± 0.97 µmol GAE/g·FW)과 뇌두(42.01 ± 0.99 µmol GAE/g·FW)였으며, 주근의 총페놀 함량은 25.07 ± 1.08 µmol GAE/g·FW로 가장 낮았다(Table I). 총플라보노이드 함량에 있어서는 뇌두(59.92 ± 6.57 µmol QE/g·FW)와 세근(54.48 ± 4.08 µmol QE/g·FW)이 지근(24.98 ± 4.51 µmol QE/g·FW)과 주근(7.91 ± 1.51 µmol QE/g·FW)보다 높은 총플라보노이드 함량을 보였다. 주근의 총플라보노이드 함량이 가장 낮았다.
도라지 뿌리의 부위별 항산화활성 비교 – 도라지의 항산화능은 DPPH와 ABTS 라디칼 소거활성, FRAP 환원능을 이용하여 평가하였다. DPPH 라디칼 소거활성을 측정한 결과(Fig. 2A), 세근이 18.58 ± 2.00 µmol TE/g·FW로 가장 높은 DPPH 라디칼 소거활성을 보였으며, 그 다음으로 뇌두(10.10 ± 1.15 µmol TE/g·FW), 지근(7.39 ± 1.49 µmol TE/g·FW), 주근(4.17 ± 0.78 µmol TE/g·FW)의 순이었다. ABTS 라디칼 소거활성에 있어서도 세근이 117.12 ± 4.60 µmol TE/g·FW로 가장 높은 ABTS 라디칼 소거활성을 보였으며, 그 다음으로 뇌두(95.79 ± 2.90 µmol TE/g·FW)와 지근(61.20 ± 4.25 µmol TE/g·FW), 주근(36.63 ± 3.50 µmol TE/g·FW)의 순이었다(Fig. 2B). FRAP 환원능을 측정한 결과에서도 세근이 24.37 ± 0.44 µmol Fe/g·FW로 가장 높은 환원능을 보였으며, 그 다음으로뇌두(21.44±0.45 µmol Fe/g·FW)의 환원능이 높았으며, 지근(20.00 ± 0.41 µmol Fe/g·FW)과 주근(19.34 ± 0.26 µmol Fe/g·FW)의 환원능은 유사하였다(Fig. 2C). 이상으로 DPPH와 ABTS 라디칼을 이용한 항산화활성과 FRAP 환원능에서 모두세근, 뇌두, 지근, 주근순으로 항산화활성이 높게 나타나는 것을 확인할 수 있었다.
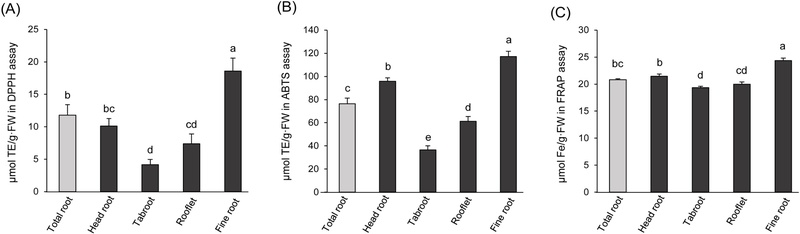
Antioxidant activity from different parts of P. grandiflorus root by DPPH radical (A), ABTS radical (B) scavenging, and FRAP assays (C), respectively. Different letters above the bars indicate statistically significant differences (p < 0.05).
다른 근류 생약인 인삼의 경우에도 세근이 주근이나 지근보다 높은 DPPH, ABTS 라디칼 소거활성능과 높은 FRAP 환원능을 보였다.31) 백지의 경우에서도 세근이 주근보다 높은 DPPH 라디칼 소거활성을 보였으며, 참당귀의 경우에서도 세근이 지근과 주근보다 높은 DPPH 라디칼 소거활성을 보였다.14,17,32) 이러한 기존의 연구결과들은 도라지 세근의 항산화활성이 주근을 비롯한 다른 부위보다 높게 나온 본 연구에서의 실험결과와 일치한다. 한편, 도라지 뿌리의 전체부위를 포함한 부위별 DPPH 라디칼 소거활성능 측정값(trolox equivalent)보다 ABTS 라디칼 소거활성능 측정값이 6배 이상 높게 나왔다. 이는 DPPH는 자유라디칼이고 ABTS는 양이온 라디칼이므로 항산화활성 측정에서 두 측정법이 차이를 보일 수 있으며, 이 두 가지 라디칼 기질과 반응물과의 결합정도에 따라서도 라디칼 제거능에서 차이를 보일 수 있다는 사실에 기인한다.33) 일반적으로 DPPH 라디칼보다 ABTS 라디칼을 사용하는 방법이 수용성 또는 지용성 항산화물질에 의한 항산화활성 측정에 모두 적용 가능하며, oxygen radical absorbance capacity (ORAC) assay와의 상관관계가 DPPH 라디칼을 사용하는 방법보다 높다.33,34)
Pearson 상관계수 분석 – 도라지 뿌리의 부위별 항산화 성분을 규명하기 위하여 총페놀 및 총플라보노이드 함량과 총사포닌 함량을 측정하였고, Pearson 상관관계 분석으로 이들 함량과 항산화활성 간의 상관관계를 확인하였다. 그 결과, 세 가지 항산화활성 측정법을 이용하는 각각의 측정법 간에는 상관계수가 모두 0.9 이상으로 높은 양의 상관관계를 보였다. 총페놀 함량은 ABTS 라디칼 소거활성(r = 0.844)보다는 DPPH 라디칼 소거활성(r = 0.942*)과 FRAP 환원능(r = 0.963**) 결과값과 매우 높은 양의 상관관계를 보인데 반하여, 총플라보노이드 함량은 DPPH 라디칼 활성과 FRAP 환원능 보다는 ABTS 라디칼 소거활성(r = 0.909*)과 뚜렷한 양의 상관관계를 보였다(Table II). 실제로 앞서 ABTS 라디칼 소거활성 측정법에서의 trolox equivalent (TE) 값이 DPPH 라디칼 소거활성 측정법에서의 TE값보다 높았는데 이는 도라지 뿌리 전체와 부위별 추출물의 항산화활성에 페놀성 화합물보다 플라보노이드 화합물의 기여도가 높을 수 있다는 점을 시사한다. 총사포닌 함량은 다섯 가지 인자 모두와 양의 상관관계를 보였고, 특히 FRAP 환원능 결과와는 상관계수가 0.882로 가장 높은 상관관계를 나타내었다. 이로써 도라지 뿌리의 항산화 활성에 사포닌 성분이 기여한다는 사실을 추정할 수 있었다.
결 론
도라지 뿌리를 뇌두, 주근, 지근, 세근으로 구분하여 부위별 총사포닌 함량과 항산화활성을 비교분석하기 위하여 본 실험을 수행하였다. 그 결과, DPPH와 ABTS 라디칼 소거능 및 FRAP 환원능을 이용하여 도라지 뿌리의 부위별 항산화 활성을 측정한 결과, 세근, 뇌두, 지근, 주근 순으로 높은 항산화활성을 보였다. 총페놀과 총플라보노이드, 총사포닌 함량도 이와 비슷한 경향을 보였는데, 이는 세근과 뇌두가 다른 부위보다 더 많은 항산화물질을 함유하고 있으며, 페놀성 화합물 및 플라보노이드 화합물, 사포닌 계열의 화합물들이 도라지 뿌리의 항산화활성과 관련이 높다는 것을 보여주었다. 이러한 결과는 향후 도라지 뿌리의 부위별 표준화 및 품질관리 기준 확립을 위한 기초자료로 사용될 수 있을 것이며, 상품성이 낮아 가공 과정에서 제거되거나 비품으로 여겨지던 도라지의 세근이 실제로는 고농도의 기능성 물질을 함유한 천연물 소재로서의 개발가능성을 시사한다.
Acknowledgments
본 연구는 농촌진흥청의 지역특화작목기술개발사업의 일환으로 수행되었으며, 경남지역 도라지 거점 생산단지 구축 및 고기능성 제품화 기술 개발(RS-2025-14383142) 과제의 지원에 의해 이루어진 결과로 이에 감사드립니다.
References
-
Lachance, P. A., Nakat, Z. and Jeong, W. S. (2001) Antioxidants: an integrative approach. Nutrition 17: 835-838.
[https://doi.org/10.1016/S0899-9007(01)00636-0]

- Lee, S.-E., Seong, N.-S., Bang, J.-K., Park, C.-G., Sung, J.-S. and Song, J. (2003) Antioxidative activities of Korean medicinal plants. Korean J. Medicinal Crop Sci. 11: 127-134.
- Son, J. W., Seung N. K. and Kwon H.-W. (2024) Antioxidation, antimicrobial and antithrombosis activities of natural products. IPR. 9: 143-151.
- Lee, J. H and Park, J.-S. (2020) Antioxidant effect of traditional food ingredient. J. Korea Converg. Soc. 11: 309-314.
-
Losada-Barreiro, S., Sezgin-Bayindir, Z., Paiva-Martins, F. and Bravo-Díaz, C. (2022) Biochemistry of antioxidants: mechanisms and pharmaceutical applications. Biomedicines 10: 3051.
[https://doi.org/10.3390/biomedicines10123051]

-
Park, H.-J., Kim, M.-M. and Lee. D.-H. (2011) Effect of saponin with antioxidant activity on matrix metalloproteinase in human dermal fibroblasts. J. Life Sci. 21: 1266-1273.
[https://doi.org/10.5352/JLS.2011.21.9.1266]

-
Hwang, E.-S. (2017) Antioxidant and quinone reductase activity of soyasaponins in hepa1c1c7 mouse hepatocarcinoma cells. J. Agric. Food Chem. 58: 1569-1576.
[https://doi.org/10.3746/pnf.2017.22.4.300]

-
Lee, B. J., Jeon, S. H., No, I. R., Kim, Y. G. and Cho, Y. S. (2015) Effect of saponin content and antioxidant activities of Platycodon gradiflorum radix by cutting length. Korean J. Medicinal Crop Sci. 23: 363-369.
[https://doi.org/10.7783/KJMCS.2015.23.5.363]

- 김길춘(2012) 쉽게 배우는 본초학 해설, pp 491-495. 신일북스, 서울.
-
Ji, M.-Y., Bo, A., Yang, M., Xu, J.-F., Jiang, L.-L., Zhou, B.-C. and Li, M.-H. (2020) The pharmacological effects and health benefits of Platycodon grandiflorus–A medicine food homology species. Foods 9: 142.
[https://doi.org/10.3390/foods9020142]

-
Kim, J. (2014) Antibacterial and anti-inflammatory effects of Platycodon grandiflorum extracts. J. Digit. Converg. 12: 359-366.
[https://doi.org/10.14400/JDC.2014.12.3.359]

-
Zhang, S., Chai, X., Hou, G., Zhao, F. and Meng, Q. (2022) Platycodon grandiflorum (Jacq.) A. DC.: A review of phytochemistry, pharmacology, toxicology and traditional use. Phytomedicine 106: 154422.
[https://doi.org/10.1016/j.phymed.2022.154422]

-
Nyakudya, E., Jeong, J. H., Lee, N. K. and Jeong, Y. S. (2014) Platycosides from the roots of Platycodon grandiflorum and their health benefits. Prev. Nutr. Food Sci. 19: 59-68.
[https://doi.org/10.3746/pnf.2014.19.2.059]

- Youn, U. J., Yoo, J. K., Chen, Q. C., Lee, I. S., Na, M. K., Min, B.-S., Jung, H.-J., Seo, E.-K. and Bae, K. H. (2010) The comparison of constituents distributed in the root of Angelica dahurica, Kor. J. Pharmacogn. 41: 186-189.
-
Shi, W., Wang, Y., Li, J., Zhang, H. and Ding, L. (2007) Investigation of ginsenosides in different parts and ages of Panax ginseng. Food Chem. 102: 664-668.
[https://doi.org/10.1016/j.foodchem.2006.05.053]

- Hwang, E.-Y. and Choi, S.-Y. (2006) Quantitative analysis of phenolic compounds in different parts of Panax ginseng C.A. Meyer and its inhibitory effect on melanin biosynthesis. Korean J. Medicinal Crop Sci. 12: 148-152.
- Lee, S. H., Lee, S.-H., Jin, M., Hong, C.-O., Hur, M., Han, J.-W., Lee, W.-M., Yun, H. M., Kim, Y. B., Lee, Y. and Koo, S. C. (2019) Analysis of index component content and antioxidant activity according to the root diameter of Angelica gigas Nakai. Korean J. Plant Res. 32: 116-123.
-
Hwang, C.-R., Oh, S.-H., Kim, H.-Y., Lee, S.-H., Hwang, I.-G., Shin, Y.-S., Lee, J.-S. and Jeong, H.-S. (2011) Chemical composition and antioxidant activity of Deoduk (Codonopsis lanceolata) and Doragi (Platycodon grandiflorum) according to temperature. J. Korean Soc. Food Sci. Nutr. 40: 798-803.
[https://doi.org/10.3746/jkfn.2011.40.6.798]

-
Choi, S. Y., Lee, S. Y., Munkhugs, D., Yoo, S. M., Choi, M.-J. and Han, H. M. (2014) Effect of blanching conditions and thawing methods on quality properties of Platycodon grandiflorum. Culi. Sci. Hos. Res. 20: 211-222.
[https://doi.org/10.20878/cshr.2014.20.6.018]

-
Lee, S.-J., Kim, H.-W., Lee, S. J., Kwon, R. H., Na, H. M., Kim, J. H., Wee, C.-D., Yoo, S. M. and Lee S. H. (2021) Characterization of saponins from various parts of Platycodon grandiflorum using UPLC-QToF/MS. Molecules 27: 107.
[https://doi.org/10.3390/molecules27010107]

-
Wang, C., Zhang, N., Wang, C., Zhang, N., Wang, Z., Qi, Z., Zhu, H., Zheng, B., Li, P. and Liu, J. (2017) Nontargeted metabolomic analysis of four different parts of Platycodon grandiflorum grown in Northeast China. Molecules 22: 1280.
[https://doi.org/10.3390/molecules22081280]

- 농촌진흥청(2009) 도라지를 이용한 텃밭 가꾸기, p.2, 농사로 농업기술포털.
-
Aguiar, N. S. D., Hansel, F. A., Reis, C. A. F., Lazzarotto, M. and Wendling, I. (2024) Optimizing the vanillin-acid sulfuric method to total saponin content in leaves of Yerba Mate clones. Chem. Biodivers. 21: e202301883.
[https://doi.org/10.1002/cbdv.202301883]

-
Abeysinghe, D. C., Li, X., Sun, C., Zhang, W., Zhou, C. and Chen, K. (2007) Bioactive compounds and antioxidant capacities in different edible tissues of citrus fruit of four species. Food Chem. 104: 1338-1344.
[https://doi.org/10.1016/j.foodchem.2007.01.047]

-
Kang, D.-M., Kwon, J.-M., Jeong, W.-J., Jung, Y. J., Kang, K. K. and Ahn, M.-J. (2022) Antioxidant constituents and activities of the pulp with skin of Korean tomato cultivars. Molecules 27: 8741.
[https://doi.org/10.3390/molecules27248741]

-
Yoon, K. F., Kang, S.-N., Bae, J.-Y., Lee, H.-S., Kwak, S.-S., Jang, I., Kim, I.-S., Lee, C. H., Bae, J. M., Lee, S. W. and Ahn, M.-J. (2013) Enhanced antioxidant and protective activities on retinal ganglion cells of carotenoids-overexpressing transgenic carrot. Curr. Drug Targets. 14: 999-1005.
[https://doi.org/10.2174/1389450111314090008]

-
Kang, D.-M., Kwon, J.-M., Jeong, W.-J., Neupane, B. D. and Ahn, M.-J. (2024) Antioxidant compounds of Sambucus pendula stem. Nat. Prod. Sci. 30: 275-281.
[https://doi.org/10.20307/nps.2024.30.4.275]

-
Benzie, F. F. and Strain, J. J. (1999) Ferric reducing/antioxidant power assay: direct measure of total antioxidant activity of biological fluids and modified version for simultaneous measurement of total antioxidant power and ascorbic acid concentration. Methods Enzymol. 299: 15-27.
[https://doi.org/10.1016/S0076-6879(99)99005-5]

- Ahn, M.-J., Bae, J. Y. and Park, J. H. (2011) Pharmacognostical studies of the ‘Gil Gyung’. Kor. J. Pharmacogn. 42: 213-217.
- Park, C.-K., Jeon, B.-S. and Yang, J.-W. (2003) The chemical components of Korean Ginseng. Prev. Nutr. Food Sci. 8: 10-23.
-
Jo, J.-E., Kim, K.-H., Kim, M.-S., Choi, J. E., Byun, M.-W. and Yook, H.-S. (2011) Antioxidant activity from different root parts of 6-year-old Panax ginseng C.A. Meyer (Yunpoong). J. Korean Soc. Food Sci. Nutr. 40: 493-499.
[https://doi.org/10.3746/jkfn.2011.40.4.493]

-
Piao, X. L., Park, I. H., Baek, S. H., Kim, H. Y., Park, M. K. and Park, J. H. (2004) Antioxidative activity of furanocoumarins isolated from Angelica dahurica J. Ethnopharmacol. 93: 243-246.
[https://doi.org/10.1016/j.jep.2004.03.054]

-
Floegel, A., Kim, D. O., Chung, S. J., Koo, S. I. and Chun, O.K. (2011) Comparison of ABTS/DPPH assays to measure antioxidant capacity in popular antioxidant-rich US foods. J. Food Compos. Anal. 24: 1043-1048.
[https://doi.org/10.1016/j.jfca.2011.01.008]

-
Re, R., Pellegrini, N., Proteggente, A., Pannala, A., Yang, M., Rice-Evans, C. (1999) Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Radic. Biol. Med. 26: 1231-1237.
[https://doi.org/10.1016/S0891-5849(98)00315-3]