
U46619로 유도된 사람 혈소판에서 순환 뉴클레오타이드 조절을 통한 고려홍삼 유래 saponin fraction의 항혈소판 효과
Abstract
Physiological platelet activation plays a crucial role in hemostasis; however, excessive or dysregulated activation contributes to the pathogenesis of cardiovascular disorders such as atherosclerosis, thrombosis, and stroke. Consequently, discovering novel bioactive compounds capable of modulating platelet function represents an important strategy for preventing and managing these diseases. Recent studies have indicated that the saponin fraction isolated from Korean red ginseng (Panax ginseng) exhibits anti-inflammatory, antioxidant, and immunoregulatory activities. Despite these findings, its specific influence on platelet activation and thrombus formation, and the signaling mechanisms involved, remain insufficiently characterized. The present study aimed to elucidate the effects of the ginseng-derived saponin fraction on platelet responses and thrombus development. Exposure of platelets to the saponin fraction resulted in a marked elevation of intracellular cyclic nucleotides (cAMP and cGMP) and promoted phosphorylation of vasodilator-stimulated phosphoprotein (VASP) and inositol 1,4,5-trisphosphate receptor (IP3R). These alterations in signaling cascades led to reduced cytosolic Ca2+ mobilization and impaired activation of integrin αIIb/β3, thereby diminishing fibrinogen binding affinity. Furthermore, the formation of thrombin-induced fibrin clots was significantly attenuated in a concentration-dependent manner. Chemical profiling by HPLC coupled with evaporative light scattering detection (HPLC–ELSD) revealed that the saponin fraction contained high levels of ginsenosides Rg1, Rg2, and Rg3—components previously associated with antiplatelet activity. Taken together, these findings demonstrate that the Korean red ginseng–derived saponin fraction, enriched in Rg1, Rg2, and Rg3, may exert protective cardiovascular effects by suppressing platelet activation and thrombus formation, highlighting its potential as a natural therapeutic candidate for cardiovascular health.
Keywords:
Korean red ginseng, Saponin, Intracellular Ca2+, Cyclic nucleotides, Fibrinogen binding심혈관 질환은 인류 건강을 위협하는 질환으로써 전 세계적인 문제로 대두되고 있다. 최근 워싱턴대학교 의과대학의 한 연구팀이 지난 20년동안의 자료를 분석한 결과, 1990년의 2억 7,100만 명이었던 심혈관 질환자가 20년 사이에 5억 2,300만 명으로 두 배 가까이 증가하였음을 보고하였다.1) 같은 기간 심혈관 질환에 의한 사망자도 1,210만 명에서 1,860만 명으로 급격히 증가하였으며, 심혈관 질환이 전 세계 사망 원인 1위일 뿐 아니라 전체 사망자의 3분의 1을 차지함을 보여주었다.1) 심혈관 질환을 일으키는 주요 원인 중 하나로써 혈관 내에서 혈액이 응고되어 형성되는 덩어리인 혈전이 지목되고 있는데, 이는 과도한 혈소판 활성화와 응고 반응에 기인된다.2) 혈소판이 혈관의 손상 부위에 달라붙어 응집을 일으키면서 1차 혈전을 생성하고, 이후 활성화된 응고 인자들이 섬유소를 만들어 혈전을 안정화시킨다.2) 이 과정을 통해 생성된 혈전은 심장이나 뇌로 가는 혈관을 막음으로써 심근경색 및 뇌졸증과 같이 심각한 심혈관 질환을 유발할 수 있다.3) 따라서, 혈소판 활성화를 조절 및 혈전 생성의 억제가 심혈관 질환 예방 및 치료에서 핵심 전략으로 주목받고 있다.
혈관의 손상이 일어나면 순환 중이던 혈소판들이 상처 부위로 모여들고 혈소판 활성유도물질(ADP, collagen 및 TXA2 등)들을 만나 활성화된다. 혈소판이 활성화될 때, 혈소판 막에 있는 phospholipase C를 작동하게 함으로써 phosphatidylinositol 4,5-bisphosphate를 분해하여 inositol 1,4,5-triphosphate (IP3) 과 diacylglycerol (DG)을 상승되게 한다.4) 그 결과 IP3의 수용체로 알려진 혈소판의 dense tubular system의 막에 있는 Ca2+ 채널을 통해 세포질 내 Ca2+ 농도가 급격하게 증가하게 된다.4) 이와 함께, 혈소판 막에서 분해된 인지질 중 arachidonic acid는 TXA synthase 및 cyclooxygenase-1와 반응하여 TXA2로 전환되어 혈소판외부로 방출되는데, 증가된 TXA2는 또 다른 혈소판들의 막에 결합되어 추가적인 혈소판 활성화와 응집을 촉진시킨다.5-7)
정상적인 경우, prostanglandin I2과 nitric oxide가 혈관 내 피세포에서 분비되며 혈소판 내 cAMP 또는 cGMP 생성을 유도하는데, 이는 protein kinase A (PKA) 및 protein kinase G (PKG)의 활성화로 이어져 vasodilator stimulated phosphoprotein (VASP)이나 IP3 receptor (IP3R)의 인산화를 일으킨다.8) IP3R가 인산화되어 세포질로의 Ca2+동원을 막고, VASP의 인산화되어 αIIb/β3의 친화도를 떨어뜨림으로써 actin filament의 신장을 통한 혈소판 활성화 및 응집을 저해한다.9-12) 따라서, cAMP 또는 cGMP 생성 및 IP3R 및 VASP의 인산화 조절은 항혈소판 물질을 평가하는데 중요하다.
고려홍삼(Korea red ginseng) 유래의 saponin fraction은 Rg1, Rb1, Rc 등을 포함한 다양한 진세노사이드 계열로 구성된 복합체로써, 이들에 의한 항염, 항산화, 면역조절 등 여러 생리활성 효과가 보고되었다.13,14) 최근에는 saponin fraction이 혈소판 활성화 및 응집을 억제할 수 있다는 항혈소판 효과도 주목받고 있으나, 세포 내 신호 전달에 있어서 기전이 명확하게 밝혀지지 않았다.15-18) 본 연구에서는 TXA2 유사체인 U46619의 자극에 의한 혈소판 활성화에서 saponin fraction이 혈소판 활성화 및 응집에 미치는 영향과 작용 기전을 체계적으로 확인함으로써 항혈전제로서의 응용 가능성 및 잠재적 가치를 제시하고자 한다. 이를 통해 고려홍삼을 유래로 한 안전하고 효과적인 항혈전 치료제 개발 가능성을 모색하고, 혈전성 질환의 예방 및 치료에 새로운 방향성을 제안하고자 한다.
재료 및 방법
고려홍삼 유래 saponin fraction의 준비 – 고려홍삼 유래 saponin fraction은 KGC 한국인삼공사(대전, 한국)에서 제공한 것을 그대로 실험에 사용하였다. 준비 과정은 다음과 같다. 건조 상태의 고려홍삼을 분쇄하여 40–60 mesh 크기의 분말로 제조한 후 지방성분 제거를 위해 분말을 헥산(또는 petroleum ether)에 1–2시간 동안 교반 혹은 환류시킨 후 감압여과하여 용매를 제거한다. 전처리된 홍삼 분말(100 g)에 70% 에탄올 (1~2 L)을 첨가한 뒤 60–70℃에서 2시간 환류 추출을 2회 반복한 다음, 여과하여 고형물을 제거한 후 합쳐서 로터리 증발기 하에서 감압 농축한다. 농축된 에탄올 추출물을 물 (200–500 mL)에 용해한 뒤 동일 부피의 n-butanol과 3회(각 200–300 mL) 분별추출한 후, 상부의 n-butanol층을 수거하여 합친 뒤 로터리 증발기로 용매를 제거하여 saponin fraction을 획득하였다.
혈소판 현탁액의 준비 – 대한적십자사 혈액원(수원, 대한민국)으로부터 제공받은 사람 전혈 유래 농축 혈소판 제제를 사용하였다. 제제를 1,650×g에서 8분간 원심분리하여 혈소판을 분리하고, pH 7.4로 조정된 현탁 완충액(138 mM NaCl, 12 mM NaHCO3, 5.5 mM glucose, 2.6 mM KCl, 0.48 mM MgCl2, 0.36 mM NaH2PO4)에 재부유시켜 세척하였다. 이후 혈소판을 1×108 cells/mL의 농도로 조정하여 현탁액을 제조하였다. 혈소판의 온도 민감성을 고려하여 모든 과정은 실온에서 수행하였다. 본 연구는 남서울대학교 기관생명윤리위원회의 승인을 받았다(승인번호: 1041479-BR-202410-001-01).
cAMP 및 cGMP 농도 측정 – 1×108 cells/mL의 혈소판 현탁액에서 서로 다른 농도의 saponin fraction을 처리한 뒤, 37℃에서 3분간 반응시켰다. 이후 2 mM CaCl2와 응집 유도제를 첨가하여 5분간 혈소판 응집을 유도하였다. 반응 종료를 위해 동일 부피의 에탄올을 첨가한 후, 상등액을 회수하여 cAMP 및 cGMP의 농도를 각각 측정하였다. 정량에는 cAMP 및 cGMP ELISA kit (Cayman Chemical, Ann Arbor, MI, USA)를 사용하였다.
세포 내 Ca2+ 농도 측정 – 농축 혈소판에 Fura 2-AM (5 µM)을 처리하여 37℃에서 1시간 동안 교반시킨 후, 앞선 방법으로 세척하여 최종 1×108 cells/mL의 혈소판 현탁액을 준비하였다. 준비된 시료에 2 mM CaCl2와 응집 유도제를 첨가하고 37℃에서 5분간 반응시키면서, 형광 분광광도계(F7000, Hitachi High-Tech, Seongnam, Korea)를 사용해 형광 강도를 측정하였다. 여기 파장은 340–380 nm 범위에서 0.5초 간격으로 변화시켰으며, 방출 파장은 510 nm로 설정하였다. 측정된 형광 비율은 Grynkiewicz의 계산식을 이용하여 세포 내 Ca2+ 농도로 환산하였다.19)
단백질 인산화 분석(Western blot) – 혈소판 반응은 1× lysis buffer로 종료하였으며, 단백질 농도는 BCA protein assay kit (Pierce Biotechnology, Rockford, IL, USA)를 이용해 정량하였다. 각 시료를 20 µg 단백질이 되도록 조정하여 8% SDS-PAGE로 전기영동한 뒤, PVDF membrane으로 전이하였다. Membrane은 1차 항체(1:1000)와 2차 항체(1:2000)에 각각 반응시켰으며, ECL 시약(Thermo Scientific, Seoul, Korea)을 사용하여 밴드를 검출하였다.
혈소판 표면 αIIb/β3에 대한 fibrinogen 결합 측정 – 혈소판 현탁액에 Alexa Fluor 488로 표지된 fibrinogen (20 µg/mL)을 첨가하고, 2 mM CaCl2와 응집 유도제를 넣어 5분간 반응시켰다. 이어서 0.5% paraformaldehyde가 포함된 phosphate buffer (pH 7.4)를 동량으로 추가하여 반응을 종료하였다. 모든 단계는 형광의 광퇴색을 방지하기 위해 암조건에서 수행되었다. 혈소판 표면에 결합된 fibrinogen의 형광 강도는 유세포분석기(FACS, BD Biosciences, San Jose, CA, USA)로 측정하였고, 데이터는 CellQuest 소프트웨어(BD Biosciences)를 이용해 정량하였다.
혈소판 매개 fibrin clot 형성 측정 – 혈소판이 시험관 벽에 부착되어 비의도적 활성화가 일어나는 것을 방지하기 위해 polyethylene 재질의 시험관을 사용하였다. 2 mM CaCl2 및 thrombin (0.05 U/mL)을 첨가하여 37℃에서 20분간 반응시켜 fibrin clot이 형성되도록 하였다. 형성된 혈전은 디지털 카메라로 촬영하고, ImageJ 소프트웨어(v1.46, NIH, Bethesda, MD, USA)를 이용해 응고 면적을 계산하여 혈전 생성 정도를 정량화하였다.
HPLC-ELSD를 이용한 고려홍삼의 saponin fraction 내 ginsenosides 분석 – Saponin fraction을 100% 메탄올에 용해한 후 HPLC로 분석하였다.20,21) 진공 탈기 장치, 4차 기울기 펌프, 자동 시료 주입기를 갖춘 Dionex-Ultimate 3000 시리즈 HPLC 장치(Dionex, Sunnyvale, CA, USA)를 사용하였고, Zorbax ODS C18 컬럼(250 mm×4.6 mm id, 5 μm)과 Zorbax ODS C18 가드 컬럼(12.5 mm×4.6 mm id, 5 μm)을 컬럼 온도 35℃에서 사용하였다. 이동상은 물(a)과 아세토니트릴(b)로 구성되었으며, 다음 기울기 프로그램을 사용하였다. 0~30분, 18%~19% b; 30~40분, 19%~31% b; 40~60분, 31%~56% b. 유속은 1.5 mL/분이었고 시료 주입량은 10 μL였다. 증발 광산란 검출(ELSD)은 probe 온도 70℃로 설정되었고 분무기 질소 가스 유속은 1.4 L/분이었다.22) 8가지 진세노사이드 용액을 세 가지 농도로 2회 주입한 후, 각 분석물질의 농도에 대한 피크 면적을 그래프로 표시하여 검량선을 작성하여 함유량을 분석하였다.
통계 분석 – 모든 실험 결과는 평균 ± 표준편차(Mean ± SD)로 표현하였다. 통계 분석은 Student’s t-test 또는 ANOVA를 통해 수행하였으며, 집단 간 유의성이 발견된 경우 Scheffé의 다중비교 검정을 추가로 적용하였다. p < 0.05 수준에서 통계적 유의성을 인정하였다.
결과 및 고찰
Saponin fraction이 cyclic nucleotides 생성에 미치는 영향 – 세포 내에서 생성되는 cAMP와 cGMP는 세포질 내 Ca2+ 농도를 조절함으로써 혈소판 활성화를 억제하는 것으로 알려져 있다. 이러한 효과에는 각각 cAMP 의존성 단백질 인산화효소(PKA)와 cGMP 의존성 단백질 인산화효소(PKG)의 활성화가 관여한다.23)
본 연구에서는 saponin fraction이 혈소판 내 cyclic nucleotide의 생성 수준에 어떤 영향을 미치는지를 확인하였다. Fig. 1A의 결과에서, 250 μg/mL의 saponin fraction 처리 시 cAMP 농도는 6.41±0.93 pmoL/108 cells에서 12.31±3.33 pmoL/108 cells로, cGMP 농도는 3.65±0.59 pmoL/108 cells에서 7.20±0.11 pmoL/108 cells로 유의하게 상승하였다. 이로써 saponin fraction은 cAMP 및 cGMP 생성을 증가시켜 혈소판 활성화 억제 경로를 자극함을 확인할 수 있었다.
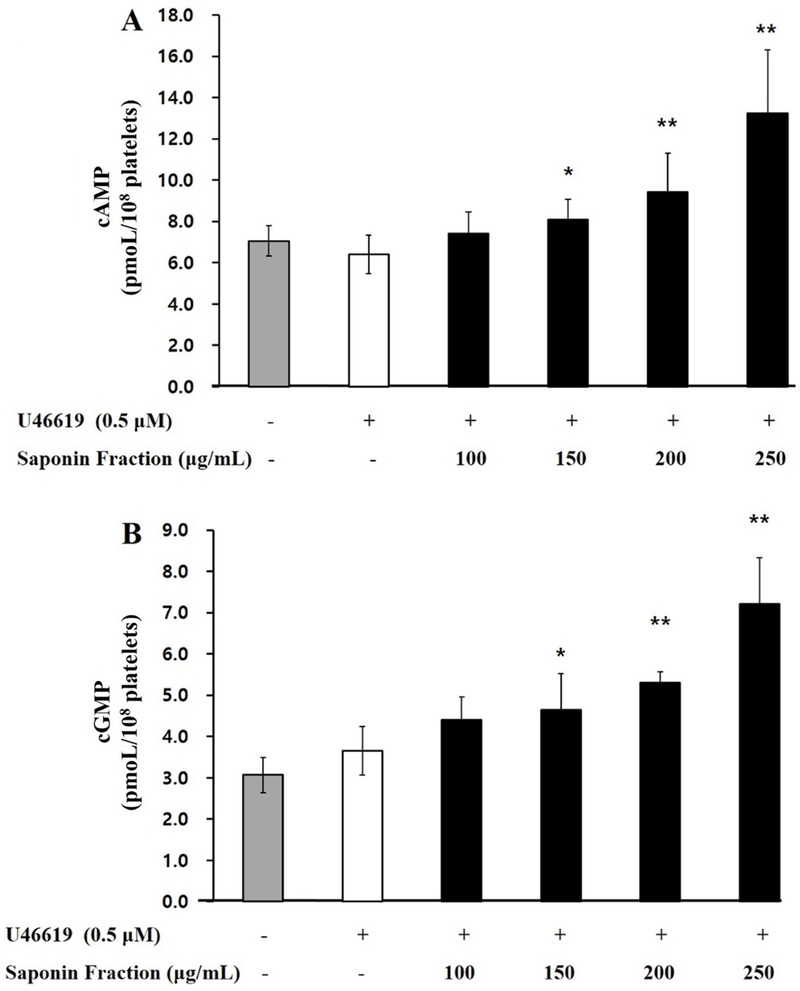
Effects of saponin fraction on cyclic nucleotides production. (A) Effects of saponin fraction on cAMP production. (B) Effects of saponin fraction on cGMP production. Results are presented as mean ± SD (n=4). Statistical significance was indicated as follows: ap < 0.05 compared to non-stimulated platelets, *p < 0.05, **p < 0.001 compared to U46619-induced platelets.
Saponin fraction이 세포 내 Ca2+ 동원 및 IP3R 인산화에 미치는 영향 – 혈소판막의 인지질인 phosphatidylinositol 4,5-bisphosphate (PIP2)는 phospholipase C-γ2 (PLC-γ2)에 의해 가수분해되어 diacylglycerol (DAG)과 inositol 1,4,5-triphosphate (IP3)를 생성한다.24) IP3는 dense tubular system의 IP3 수용체(IP3R)를 개방시켜 세포질 내 Ca2+ 농도를 상승시키며, 이 과정은 myosin light chain (MLC)과 pleckstrin의 인산화를 통해 혈소판 응집을 촉진한다.25)
U46619로 자극된 혈소판에서 Ca2+ 농도의 변화를 분석한 결과, [Ca2+]i가 50.77±11.37 nM에서 395.34±34.38 nM으로 급격히 증가하였다. 그러나, saponin fraction(100–250 μg/mL)을 처리한 경우 이 상승폭이 현저히 감소하였다(Fig. 2A). 또한 IP3R의 인산화 수준을 평가한 결과, saponin fraction이 농도 의존적으로 IP3R 인산화를 촉진하였으며(Fig. 2B), 이는 Ca2+ 유입을 제한함으로써 혈소판 활성화를 억제하는 기전을 시사한다.
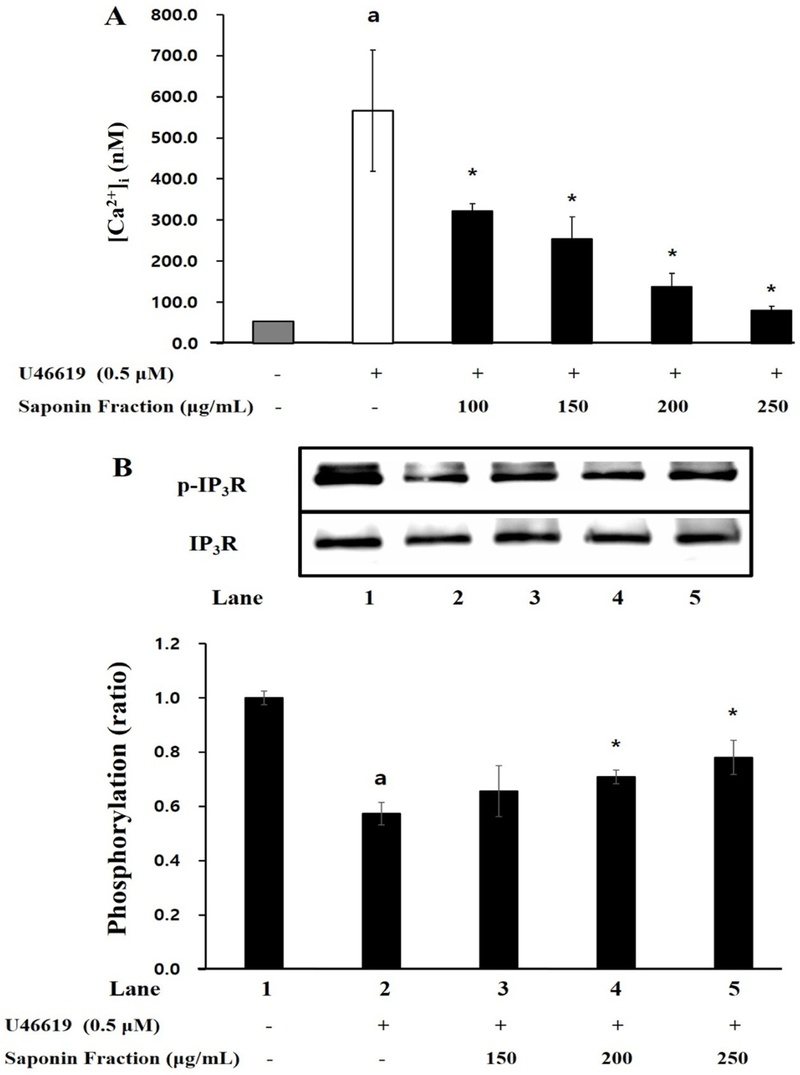
Effects of saponin fraction on intracellular Ca2+ mobilization and 1P3R phosphorylation. (A) Effects of saponin fraction on intracellular Ca2+ mobilization. (B) Effects of saponin fraction on 1P3R phosphorylation. Fura 2 fluorescence was measured using a fluorescence spectrophotometer. Results are presented as mean ± SD (n=4). Statistical significance was indicated as follows: ap < 0.05 compared to non-stimulated platelets, *p < 0.05 compared to U46619-induced platelets.
Saponin fraction이 VASP 인산화에 미치는 영향 – VASP (vasodilator-stimulated phosphoprotein)는 cAMP/PKA 및 cGMP/PKG 경로의 대표적 표적 단백질로, 인산화가 촉진되면 integrin αIIb/β3의 활성이 저해되어 혈소판 응집이 감소한다.26,27) 본 연구에서 saponin fraction은 U46619로 자극된 혈소판의 cAMP 및 cGMP 농도를 유의하게 증가시켰으며(Fig. 1), U46619로 유도한 혈소판에서 VASP의 Ser157과 Ser239 인산화를 농도 의존적으로 강화시켰다(Fig. 3). 특히 150 μg/mL 이상의 농도에서 유의한 변화가 관찰되었으며, 이는 saponin fraction이 상승된 cAMP 및 cGMP를 통해 VASP 인산화를 유도함을 의미한다.
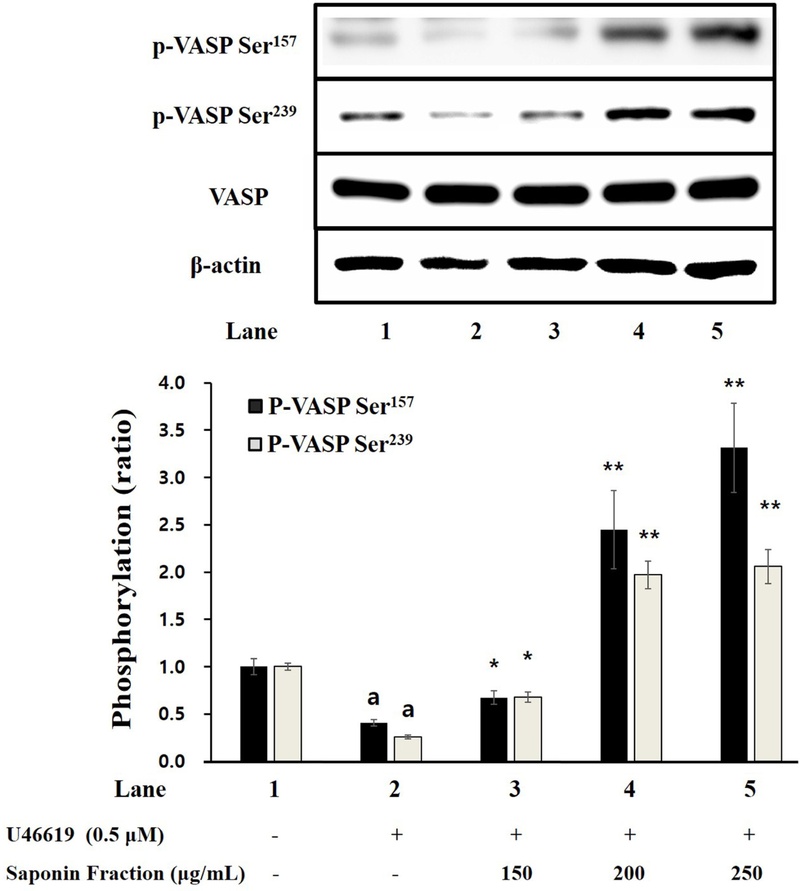
Effects of saponin fraction on VASP phosphorylation. Results are expressed as mean ± SD (n=4). Statistical significance was indicated as follows: ap< 0.05 compared to non-stimulated platelets, *p < 0.05, **p < 0.001 compared to U46619-induced platelets.
Saponin fraction이 fibrinogen–αIIb/β3 결합에 미치는 영향 – 혈소판의 αIIb/β3 수용체는 응집 과정에서 fibrinogen 과 결합하여 세포 간 연결을 매개하며, 그 활성은 VASP 인산화 수준과 밀접한 관련이 있다.24,25) 평상시 낮은 결합 친화도를 보이는 αIIb/β3 는 자극 시 구조적 변형을 통해 fibrinogen에 대한 친화도를 높이고, 이는 혈소판 응집과 혈전 형성으로 이어진다.28,29)
U46619 처리 시 fibrinogen의 결합률은 60.1±1.4%로 상승하였으나, saponin fraction 투여는 이 결합을 농도 의존적으로 억제하였다(Fig. 4A–f, 4B). 특히 250 μg/mL 농도에서 fibrinogen 결합이 약 21.1%까지 감소하였다. 이러한 결과는 saponin fraction이 αIIb/β3 의 활성화를 저해함으로써 혈소판 응집을 차단하는 효과를 갖는다는 것을 뒷받침한다.
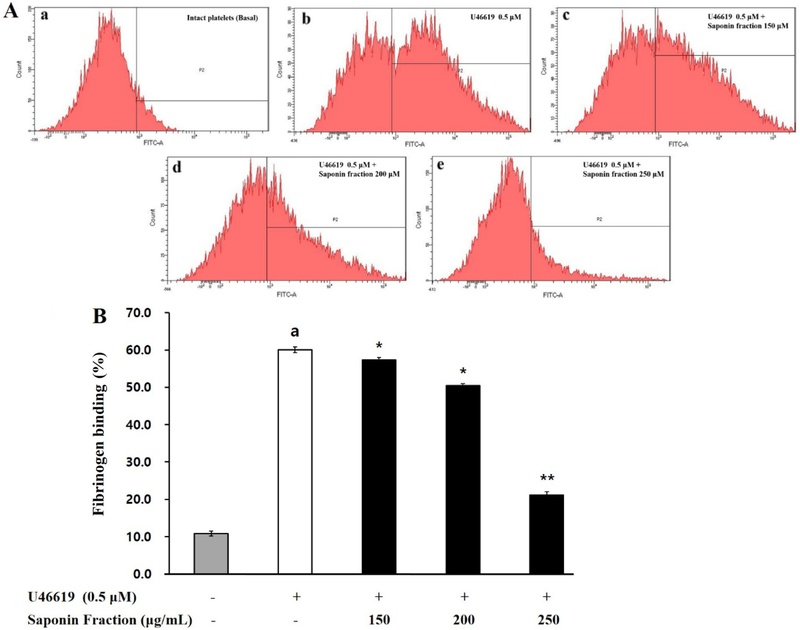
Effects saponin fraction on fibrinogen binding. (A) The flow cytometry histograms on fibrinogen binding. a, Intact platelets (base); b, U46619; c, U46619 + saponin fraction (150 μg/mL); d, U46619+ saponin fraction (200 μg/mL); e, U46619+ saponin fraction (250 μg/mL). (B) Effects of saponin fraction on U46619-induced fibrinogen binding (%). Results are expressed as mean ± SD (n=4). Statistical significance was indicated as follows: ap < 0.05 compared to non-stimulated platelets, *p < 0.05, **p < 0.001 compared to U46619-induced platelets.
Saponin fraction이 혈소판 매개 fibrin clot 형성에 미치는 영향 – 활성화된 혈소판은 αIIb/β3 를 매개로 세포 골격 재배열과 fibrin망 형성을 촉진하며, 이는 손상된 혈관의 지혈 과정에서 핵심적 역할을 한다.28) 반면, αIIb/β3 활성을 억제하는 물질은 혈전 형성을 차단하는 것으로 알려져 있다.
이에 따라 본 연구에서는 thrombin으로 유도된 fibrin 응고 형성에 saponin fraction이 미치는 영향을 평가하였다. Fig. 5A에서 thrombin 자극은 강한 fibrin 응고를 유발하였으나, saponin fraction (150, 200, 250 μg/mL) 처리 시 응고 형성이 각각 16.0%, 23.1%, 31.4% 감소하였다(Fig. 5B). 이는 saponin fraction이 혈전 형성을 유의하게 억제하는 잠재적 항혈전 후보물질임을 시사한다.
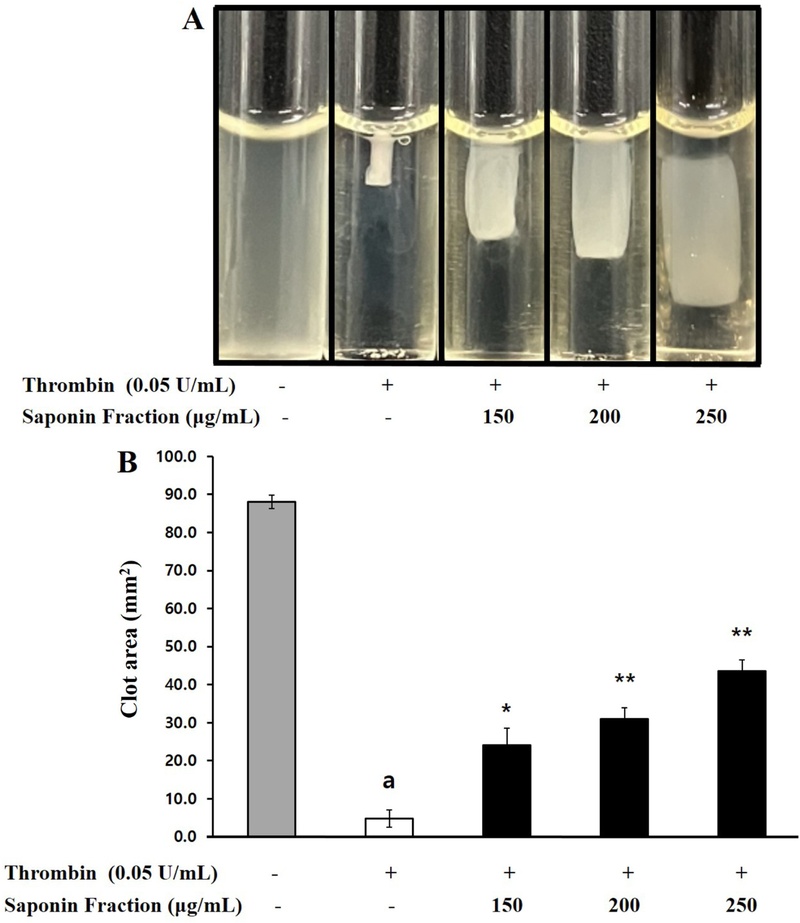
Effects of saponin fraction on platelet-mediated fibrin clot formation. (A) Effects of saponin fraction on thrombin-retracted fibrin clot photographs (B) Effects of saponin fraction on thrombin-retracted fibrin clot area. Results are expressed as mean ± SD (n=4). Statistical significance was indicated as follows: ap < 0.05 compared to non-stimulated platelets, *p < 0.05, **p < 0.001 compared to thrombin-induced platelets.
고려홍삼 유래 saponin fraction 내 함유된 ginsenosides 함유량 – Table I에 나타낸 바와 같이, HPLC-ELSD 분석결과로부터 계산된 진세노사이드 함량에서 Rb1, Rb2, Rc, Rd, Rg3의 총 함량은 186.80±4.65 mg/g이고, Re, Rg1, Rg2의 총 함량은 109.37±2.29 mg/g이었다(Fig. 6). 고려홍삼의 saponin fraction에는 혈소판 응집을 억제하는 것으로 알려진 Rg1, Rg2, Rg3를 다량 함유하고 있다.30-32) 항혈소판 효과 측면에서는 saponin fraction에 함유된 이들 ginsenoside가 작용하여 강한 항혈소판 효과를 보여주었다고 사료된다.
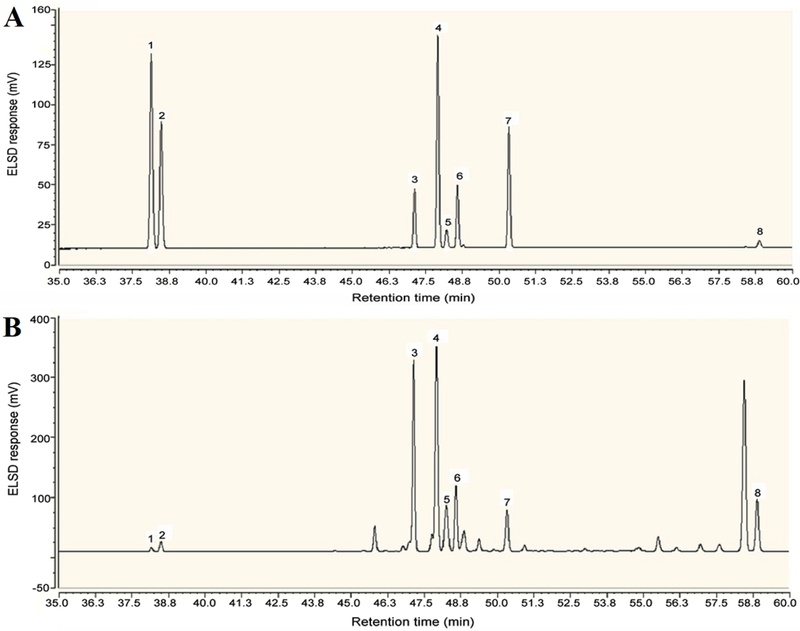
HPLC-evaporative light scattering detection (ELSD) chromatograms of standard ginsenosides and saponin fraction from Korean red ginseng. (A) The chromatograms of standard ginsenosides. (B) The chromatograms of ginsenosides in saponin fraction. HPLC was performed on a Zorbax ODS C18 column (250 mm×4.6 mm id, 5 µm) and a Zorbax ODS C18 guard column (12.5 mm×4.6 mm id, 5 µm) were used at a column of 35°C. The mobile phase consisted of water (a) and ACN (b) using the following gradient program: 0 to 30 min, 18% to 19% b; 30 to 40 min, 19% to 31% b; 40 to 60 min, 31% to 56% b. The flow rate was at 1.5 mL/min and sample injection volume was 10 µL. ELSD was set to a probe temperature of 70°C and nebulizer nitrogen gas flow rate was at 1.4 L/min. 1 to 8, ginsenoside Rg1, Re, Rb1, Rc, Rg2, Rb2, Rd, and Rg3 in order.
결 론
지혈 과정이 원활하게 이루어지기 위해서는 혈소판의 적절한 활성화가 필수적이다. 그러나 혈소판이 과도하게 혹은 비정상적으로 활성화될 경우, 이는 죽상동맥경화증, 혈전증, 뇌졸중 등과 같은 다양한 심혈관 질환의 주요한 병태생리적 원인이 된다. 따라서 혈소판의 활성화를 조절하거나 억제할 수 있는 새로운 생리활성 물질을 탐색하는 일은 심혈관계 질환의 예방 및 치료 전략 개발에 있어 매우 중요하다. 최근 고려홍삼에서 분리된 saponin fraction은 항염증, 항산화 및 면역조절 작용을 나타낸다는 여러 연구가 보고되고 있다. 그럼에도 불구하고, 이 saponin fraction이 혈소판의 활성화 및 혈전 형성 과정에 미치는 영향과 그 세포 내 신호전달 기전은 아직 충분히 규명되지 않았다. 이에 본 연구에서는 saponin fraction이 혈소판 활성화와 혈전 형성에 어떠한 생리적 변화를 유도하는지를 실험적으로 분석하였다. 그 결과, saponin fraction 처리 시 혈소판 내에서 cAMP 및 cGMP의 생성이 유의하게 증가하였으며, 이에 따라 VASP와 IP3R의 인산화 수준 또한 현저히 상승하였다. 이 신호 변화는 IP3R의 인산화를 매개로 세포질 내로의 Ca2+ 유입을 억제하였고, 동시에 VASP의 인산화 증가를 통해 혈소판막의 integrin αIIb/β3 활성화를 저해함으로써 fibrinogen 결합 능력을 감소시켰다. 또한, thrombin에 의해 유도되는 fibrin clot 형성이 saponin fraction 농도에 비례하여 억제되는 현상이 확인되었다. 추가적으로, HPLC-ELSD 분석을 통해 saponin fraction 내에 항혈소판 활성이 알려진 Rg1, Rg2, Rg3 등의 주요 ginsenosides 성분이 다량 포함되어 있음을 확인하였다. 이상의 결과를 종합하면, Rg1, Rg2, Rg3를 함유한 고려홍삼 유래의 saponin fraction은 혈소판의 과도한 활성화와 혈전 형성을 억제함으로써 심혈관 질환의 예방 및 개선에 유의미한 생리활성 물질로 활용될 가능성을 제시한다.
Conflict of interest
No conflict of interest.
References
-
Mozaffarian, D., Benjamin, E. J., Go, A. S., Arnett, D. K., Blaha, M. J., Cushman, M., Das, S. R., de Ferranti, S., Després, J. P., Fullerton, H. J., Howard, V. J., Huffman, M. D., Isasi, C. R., Jiménez, M. C., Judd, S. E., Kissela, B. M., Lichtman, J. H., Lisabeth, L. D., Liu, S., Mackey, R. H., Magid, D. J., McGuire, D. K., Mohler, E. R., Moy, C. S., Muntner, P., Mussolino, M. E., Nasir, K., Neumar, R. W., Nichol, G., Palaniappan, L., Pandey, D. K., Reeves, M. J., Rodriguez, C. J., Rosamond, W., Sorlie, P. D., Stein, J., Towfighi, A., Turan, T. N., Virani, S. S., Woo, D., Yeh, R. W. and Turner, M. B. (2016) Heart disease and stroke statistics–2016 update: a report from the American Heart Association. Circulation 133: e38-e48.
[https://doi.org/10.1161/CIR.0000000000000350]

-
Ji, X. and Hou, M. (2011) Novel agents for anti-platelet therapy. J. Hematol. Oncol. 4: 44.
[https://doi.org/10.1186/1756-8722-4-44]

-
Xu, X. R., Zhang, D., Oswald, B. E., Carrim, N., Wang, X., Hou, Y., Zhang, Q., Lavalle, C., McKeown, T., Marshall, A. H., Ni, H. and Weiss, H. J. (2016) Platelets are versatile cells: new discoveries in hemostasis, thrombosis, immune responses, tumor metastasis and beyond. Crit. Rev. Clin. Lab. Sci. 53: 409-430.
[https://doi.org/10.1080/10408363.2016.1200008]

-
Payrastre, B., Missy, K., Trumel, C., Bodin, S., Plantavid, M. and Chap, H. (2000) The integrin αIIbβ3 in human platelet signal transduction. Biochem. Pharmacol. 60: 1069-1074.
[https://doi.org/10.1016/S0006-2952(00)00417-2]

-
Jennings, L. K. (2009) Role of platelets in atherothrombosis. Am. J. Cardiol. 103: 4A-10A.
[https://doi.org/10.1016/j.amjcard.2008.11.017]

-
Morello, F., Perino, A. and Hirsch, E. (2009) Phosphoinositide 3-kinase signalling in the vascular system. Cardiovasc. Res. 82: 261-271.
[https://doi.org/10.1093/cvr/cvn325]

-
Sabatine, M. S. and Jang, I. K. (2000) The use of glycoprotein IIb/IIIa inhibitors in patients with coronary artery disease. Am. J. Med. 109: 224-237.
[https://doi.org/10.1016/S0002-9343(00)00474-5]

- Schwarz, U. R., Walter, U. and Eigenthaler, M. (2001) Taming platelets with cyclic nucleotides. Biochem. Pharmacol. 62: 1153-1161.
-
Quinton, T. M. and Dean, W. L. (1992) Cyclic AMP-dependent phosphorylation of the inositol-1,4,5-trisphosphate receptor inhibits Ca2+ release from platelet membranes. Biochem. Biophys. Res. Commun. 184: 893-899.
[https://doi.org/10.1016/0006-291X(92)90675-B]

-
Cavallini, L., Coassin, M., Borean, A. and Alexandre, A. (1996) Prostacyclin and sodium nitroprusside inhibit the activity of the platelet inositol 1,4,5-trisphosphate receptor and promote its phosphorylation. J. Biol. Chem. 271: 5545-5551.
[https://doi.org/10.1074/jbc.271.10.5545]

-
Laurent, V., Loisel, T. P., Harbeck, B., Wehman, A., Gröbe, L., Jockusch, B. M., Wehland, J., Gertler, F. B. and Carlier, M. F. (1999) Role of proteins of the Ena/VASP family in actin-based motility of Listeria monocytogenes. J. Cell Biol. 144: 1245-1258.
[https://doi.org/10.1083/jcb.144.6.1245]

-
Sudo, T., Ito, H. and Kimura, Y. (2003) Phosphorylation of the vasodilator-stimulated phosphoprotein (VASP) by the anti-platelet drug, cilostazol, in platelets. Platelets 14: 381-390.
[https://doi.org/10.1080/09537100310001598819]

-
Kim, K. A., Yoo, J. H., Hwang, I. H., Kim, J. H., Park, J. Y. and Jung, J. H. (2023) Antioxidant and anti-inflammatory effect of red ginseng by different extraction methods. Korean J. Hum. Ecol. 32: 457-465.
[https://doi.org/10.5934/kjhe.2023.32.4.457]

-
Attele, A. S., Wu, J. A. and Yuan, C. S. (1999) Ginseng pharmacology: multiple constituents and multiple actions. Biochem. Pharmacol. 58: 1685-1693.
[https://doi.org/10.1016/S0006-2952(99)00212-9]

-
Lee, D. H., Cho, H. J., Kim, H. H., Lee, M. H., Kim, E. K. and Park, J. H. (2013) Inhibitory effects of total saponin from Korean red ginseng via vasodilator-stimulated phosphoprotein-Ser157 phosphorylation on thrombin-induced platelet aggregation. J. Ginseng Res. 37: 176-186.
[https://doi.org/10.5142/jgr.2013.37.176]

-
Lee, D. H., Cho, H. J., Kim, H. H., Lee, M. H. and Park, J. H. (2012) Total saponin from Korean red ginseng inhibits thromboxane A₂ production associated microsomal enzyme activity in platelets. J. Ginseng Res. 36: 40-47.
[https://doi.org/10.5142/jgr.2012.36.1.40]

-
Kwon, H. W., Lee, D. H., Kim, H. H. and Park, J. H. (2016) Total saponin from Korean red ginseng inhibits binding of adhesive proteins to glycoprotein IIb/IIIa via phosphorylation of VASP (Ser157) and dephosphorylation of PI3K and Akt. J. Ginseng Res. 40: 76-85.
[https://doi.org/10.1016/j.jgr.2015.05.004]

-
Shin, J. H., Lee, D. H., Kim, H. H. and Park, J. H. (2015) Inhibitory effects of total saponin from Korean red ginseng on [Ca2+]i mobilization through phosphorylation of cyclic AMP-dependent protein kinase catalytic subunit and inositol 1,4,5-trisphosphate receptor type I in human platelets. J. Ginseng Res. 39: 354-364.
[https://doi.org/10.1016/j.jgr.2015.03.006]

-
Ko, S. N., Park, H. H., Kim, J. H., Kim, H. H. and Lee, D. H. (2023) The inhibitory effects of Glycyrrhiza uralensis on human platelet aggregation and thrombus formation. Biomed. Sci. Lett. 29: 242-248.
[https://doi.org/10.15616/BSL.2023.29.4.242]

-
Kim, S. N., Kang, S. J., Kim, H. H. and Lee, D. H. (2007) Simultaneous quantification of 14 ginsenosides in Panax ginseng C.A. Meyer (Korean red ginseng) by HPLC–ELSD and its application to quality control. J. Pharm. Biomed. Anal. 45: 164-170.
[https://doi.org/10.1016/j.jpba.2007.05.001]

-
Wan, J. B., Yang, F. Q., Li, S. P., Wang, Y. T. and Cui, X. M. (2006) Simultaneous determination of nine saponins from Panax notoginseng using HPLC and pressurized liquid extraction. J. Pharm. Biomed. Anal. 41: 274-279.
[https://doi.org/10.1016/j.jpba.2005.10.023]

-
Wan, J. B., Yang, F. Q., Li, S. P., Wang, Y. T. and Cui, X. M. (2006) Simultaneous determination of 11 saponins in Panax notoginseng using HPLC–ELSD and pressurized liquid extraction. J. Sep. Sci. 29: 2190-2196.
[https://doi.org/10.1002/jssc.200600103]

-
Kuo, J. F., Andersson, R. G. G., Wise, B. C. and Wrenn, R. W. (1980) Calcium-dependent protein kinase: widespread occurrence in various tissues and comparison of effects of phospholipid, calmodulin, and trifluoperazine. Proc. Natl. Acad. Sci. U.S.A. 77: 7039-7043.
[https://doi.org/10.1073/pnas.77.12.7039]

-
Berridge, M. J. and Irvine, R. F. (1989) Inositol phosphates and cell signalling. Nature 341: 197-205.
[https://doi.org/10.1038/341197a0]

-
Nishikawa, M., Tanaka T. and Hidaka, H. (1980) Ca2+-calmodulin-dependent phosphorylation and platelet secretion. Nature 287: 863-865.
[https://doi.org/10.1038/287863a0]

-
Wentworth, J. K., Pula, G. and Poole, A. W. (2006) Vasodilator-stimulated phosphoprotein (VASP) is phosphorylated on Ser157 by protein kinase C-dependent and -independent mechanisms in thrombin-stimulated human platelets. Biochem. J. 393: 555-564.
[https://doi.org/10.1042/BJ20050796]

-
Napeñas, J., Oost, F. C. and DeGroot, A. (2013) Review of postoperative bleeding risk in dental patients on antiplatelet therapy. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. 115: 491-499.
[https://doi.org/10.1016/j.oooo.2012.11.001]

-
Calderwood, D. A. (2004) Integrin activation. J. Cell Sci. 117: 657-666.
[https://doi.org/10.1242/jcs.01014]

-
Phillips, D. R., Nannizzi-Alaimo, L. and Prasad, K. S. (2001) β3 tyrosine phosphorylation in αIIbβ3 (platelet membrane GP IIb–IIIa) outside-in integrin signaling. Thromb. Haemost. 86: 246-258.
[https://doi.org/10.1055/s-0037-1616222]

-
Kimura, Y., Okuda, H. and Arichi, S. (1988) Effects of various ginseng saponins on 5-hydroxytryptamine release and aggregation in human platelets. J. Pharm. Pharmacol. 40: 838-843.
[https://doi.org/10.1111/j.2042-7158.1988.tb06285.x]

-
Kuo, S. C., Teng, C. M., Lee, J. C., Ko, F. N., Chen, S. C. and Wu, T. S. (1990) Antiplatelet components in Panax ginseng. Planta Med. 56: 164-167.
[https://doi.org/10.1055/s-2006-960916]

- Lee, S. R., Park, J. H., Choi, K. J. and Kim, N. D. (1997) Inhibitory effects of ginsenoside Rg3 on platelet aggregation and its mechanism of action. Korean J. Ginseng Sci. 21: 132-140.
