
산수유 ethyl acetate 분획의 예쁜꼬마선충에 대한 항산화 및 수명연장 효과
Abstract
Reactive oxygen species (ROS) induce cell death and are associated with the development of cancer, cardiovascular, and neurodegenerative diseases. Therefore, antioxidants that suppress ROS are considered essential. In this study, the polyphenol and flavonoid contents of the ethanol extract of Cornus officinalis and its solvent fractions were determined, and their radical scavenging activities were evaluated using DPPH, ABTS, and xanthine-derived superoxide assays. The ethyl acetate fraction exhibited the strongest scavenging activity. In Caenorhabditis elegans, this fraction dose-dependently enhanced the activities of antioxidant enzymes such as superoxide dismutase (SOD) increased resistance to oxidative stress, and prolonged lifespan. It also improved thermotolerance and significantly upregulated the expression of SOD-3::GFP in the transgenic strain CF1553. These findings suggest that the ethyl acetate fraction of C. officinalis exerts potent antioxidant effects and contributes to stress resistance and longevity in C. elegans.
Keywords:
Cornus officinalis, Caenorhabditis elegans, Antioxidant, SOD생명유지에 결정적인 역할을 하는 산소는 약 2-3%가 체내에서 활성산소종(ROS, Reactive Oxygen Species)의 형태로 축적되어 악영향을 미쳐 신경세포의 사멸을 유발시킨다.1) 대표적인 활성산소종으로는 superoxide anion radical, peroxide radical, hydroxyl radical 등이 있으며 암, 심장질환 및 신경퇴행성 질환을 초래하는 것으로 알려져 있다.2,3) 활성산소종으로부터 체내를 보호하는 항산화 효소로는 superoxide dismutase (SOD), catalase, glutathione 등이 존재하지만 나이가 들어감에 따라 이 효소들의 활성이 점차 줄어들게 되어 과도하게 생성되는 활성산소종을 억제하기에는 한계가 있다.4,5) 이에 따라 합성 항산화제가 대표적으로 사용되었지만 이들의 독성 문제가 알려져 사용에 제한이 따르기에, 천연물 유래 항산화제에 대한 필요성이 증가하고 있다.6)
층층나무과(Cornaceae)에 속하는 낙엽교목인 산수유(Cornus officinalis)는 흔히 중부이남에 자생하며, 약간 따뜻한 성질에 기운을 북돋아주고 이뇨작용과 혈압강하작용, 단백질의 소화를 돕는다고 알려져 있다.7) 산수유에 대한 생리활성으로는 항균 활성,8) 항히스타민 활성,9) 항산화 활성10) 등이 보고되어 있으며 황색포도상구균을 억제하는 것으로도 보고되어 있다.11) 산수유 추출물에서 항종양, 항염, 항균 및 항바이러스 효과가 뛰어난 ursolic acid를 분리한 흥미로운 연구 결과도 보고되어 있으며,12) 이 외에도 채취시기에 따른 특성,13) 항염증,14) 항비만15) 등 다양한 연구결과가 보고되어 있지만 아직까지 예쁜꼬마선충(Caenorhabditis elegans; C.elegans) 모델을 활용한 생리활성에 대한 연구가 이루어지지 않았다.
따라서 본 연구에서는 동물실험에 대한 윤리적인 문제를 해결할 수 있으며,16) 유전자의 구성이 인간의 유전자와 60% 이상 유사하여17) 수명연장, 에너지 대사 증후군 등 다방면에서 실험 모델로 이용되는 예쁜꼬마선충을 모델로 항산화 기전에 대한 연구를 진행하였다. 산수유 추출물 및 분획물의 radical 소거 활성을 측정하여 가장 우수한 소거 활성을 나타낸 ethyl acetate 분획물에 대하여 선충 체내 항산화 효소인 superoxide dismutase (SOD)의 활성증가 여부와 선충 세포 내 활성산소종의 축적 억제 능력, 산화적 스트레스 저항성 및 열 스트레스 저항성에 미치는 영향, 형질전환 선충(CF1553)내 SOD-3::GFP (Green fluorescent protein)의 발현 여부 확인, 선충에 수명에 미치는 영향에 대하여 확인하였다.
재료 및 방법
추출 및 분획 – 산수유 분말 600 g에 2 L의 ethanol을 가하여 50℃ 수욕상에서 6시간씩 3회 반복하여 추출 하였으며 추출액을 감압농축하여 339.51 g의 추출물을 얻었다. 추출물 339.51 g을 500 mL의 증류수로 현탁시킨 후 동량의 n-hexane (2.02 g), methylene chloride (1.38 g), ethyl acetate (4.37 g), n-butanol (17.88 g) 순서대로 분획하여 각각의 분획물을 확보하였으며, 추출물 및 분획물은 밀봉 후 차광하여 실험에 필요한 시료로 사용하였다.
Polyphenol, flavonoids 함량 분석 – 산수유 추출물 및 분획물의 polyphenol 함량을 분석하기 위해 시료 100 μL와 Folin & Ciocalteu’s phenol reagent 용액 100 μL를 혼합한 뒤 0.1 M의 Na2CO3 용액 800 μL를 가하여 40℃ 수욕상에서 20분간 반응시켰다. 이후 10분간 냉각시킨 뒤 700 nm에서 흡광도를 측정하였으며, 표준물질은 tannic acid를 사용하여 검량선을 작성하였다. 산수유 시료 내 polyphenol 함량은 시료 g 중 tannic acid equivalents (μg TAE/g)로 나타내었다.18) 산수유 추출물 및 분획물 시료 내 flavonoid 함량 분석은 시료 1 mL에 5% NaNO2 용액 30 μL를 혼합하여 5분간 반응시킨 후 10% AlCl3 30 μL와 1 M의 NaOH 200 μL를 가하여 510 nm에서 흡광도를 측정하였다. 표준물질은 quercetin을 사용하여 검량선을 작성하였으며, 산수유 시료 내 flavonoid 함량은 시료 g 중 quercetin equivalents (μg QE/g)로 나타내었다.19)
DPPH, ABTS radical 소거 활성 측정 – 산수유 추출물 및 분획물의 DPPH radical 소거 활성 측정을 위해 시료를 에탄올을 용매로 하여 농도별로 제조하였다. 농도별 시료 50 μL와 에탄올을 용매로 제조한 0.2 mM의 1,1-diphenyl-2-picrylhrazyl (DPPH)용액 200 μL를 혼합하여 실온의 암소에서 정확히 30분간 반응시킨 후 microplate reader를 이용하여 517 nm에서 흡광도를 측정하였다.20) ABTS radical 소거 활성 측정은 7.4 mM의 ABTS 용액과 2.6 mM의 potassium persulfate 용액을 동량 혼합하여 24시간 반응시켜 radical의 형성을 유도시킨 후 ABTS 용액의 흡광도 값이 0.7±0.03이 되도록 phosphate buffer saline (pH 7.4)으로 희석하여 사용하였다. 농도별 시료 10 μL와 ABTS용액 190 μL를 혼합하여 실온의 암소에서 10분간 반응시킨 후 732 nm에서 흡광도를 측정하였다. 실험은 3회 반복 측정하였으며, 대조약물로 L-ascorbic acid를 사용하였다.21)
Superoxide radical 소거 활성 – 산수유 추출물 및 분획물의 superoxide radical 소거 활성을 측정하기 위해 시료 농도별 시료 10 μL와 100 μM의 nitro blue tetrazolium (NBT), 250 μM의 xanthine을 포함한 20 mM의 phosphate buffer (pH 7.8)를 혼합하여 5분간 반응시켰다. 5분 후 xanthine oxidase (0.05 U/mL) 100 μL를 가하여 37℃에서 20분간 반응시킨 후 570 nm에서 흡광도를 측정하였으며, 시료에 대한 NBT의 환원 정도를 대조군과 비교하여 superoxide radical 소거 활성을 측정하였다.22)
예쁜꼬마선충의 배양 – 본 실험에 사용된 예쁜꼬마선충(Caenorhabditis elegans)은 Caenorhabditis Genetic Center (CGC; University of Minnesota, Minneapis, MN)로부터 제공받은 것을 사용하였으며, 야생형(wild type, N2) 선충과 형질전환 선충 CF1553 muls84[pAD76(SOD-3::GFP)]을 사용하였다. 예쁜꼬마선충은 Escherichia coli (E.coli) OP50이 도말된 nematode growth medium (NGM) agar plate 상에서 배양하였으며(20℃), 선충의 알을 회수하기 위해 bleaching solution (NaClO, 5 M KOH)용액 1 mL을 가하여 알을 회수하였다. 실험에 사용된 NGM plate를 제조하기 위해 시료는 stock solution 상태로 DMSO를 용매로 하여 NGM plate (50℃)에 첨가되었으며, 최종 DMSO 농도는 0.1% (v/v) 상태를 유지하였다.23)
항산화 효소(SOD) 활성 측정 – 산수유 ethyl acetate 분획이 선충 체내의 항산화 효소(SOD)의 활성에 미치는 영향을 확인하기 위해 농도별(250, 500 μg/mL)로 제조한 산수유 ethyl acetate 분획 시료를 첨가한 NGM plate에 성장 단계를 동일시한 선충을 배양하였다. 성체가 된지 2일째의 선충을 사용하였으며, M9 buffer를 가하여 표피를 세척한 선충을 분쇄하여 항산화 효소 활성 측정에 사용하였으며 homogenization buffer의 조성은 다음과 같다(10 mM Tris-HCl, 150 mM NaCl, 0.1 mM EDTA, pH 7.5). SOD의 활성을 확인하기 위해 10 mM의 phosphate buffer (pH 8.0)를 용매로 한 반응혼합물(1.6 mM xanthine, 0.48 mM NBT; nitro blue tetrazolium) 0.49 mL를 제조하여 농도별 시료 10 μL와 혼합하여 5분간 pre-incubation 시켰다. 정확히 5분 후 0.05 U/mL의 xanthine oxidase 100 μL를 가하고 37℃에서 20분간 incubation한 후 69 mM의 SDS (Sodium Dodecyl Sulfate)를 가하여 반응을 멈춘 뒤 570 nm에서 흡광도를 측정하였다.22)
산화적 스트레스 저항성 및 열 스트레스 저항성 측정 – 선충의 산화적 스트레스 저항성 미치는 영향을 확인하기 위해 산수유 ethyl acetate 분획을 농도별(250, 500 μg/mL)로 첨가한 plate에 성장단계를 동일시한 선충을 배양하여 성체가 된지 7일째의 선충을 사용하였다. 건강한 선충 25마리를 1 mM의 juglone이 함유된 M9 buffer가 담긴 96 well plate로 선충을 옮긴 뒤 20℃에서 배양하면서 매 시간마다 선충의 생존율을 확인하였다. 열 스트레스 저항성에 미치는 영향을 확인하기 위해 성체가 된지 4일째의 선충을 사용하였으며 25마리의 선충을 신선한 NGM plate로 옮긴 뒤 선충에게는 고온 조건인 36℃에서 배양하면서 매 시간마다 선충의 생존율을 확인하였다. 선충의 사망은 platinum wire의 끝으로 여러번 조심스럽게 자극하였을 때 반응이 없는 경우를 사망상태로 간주하였다.24,25)
SOD-3::GFP 발현량 측정 – 산수유 ethyl acetate 분획이 형질전환 된 SOD-3::GFP를 포함한 CF1553 선충 내 SOD-3::GFP의 발현율에 미치는 영향을 확인하기 위해 산수유 ethyl acetate 분획 시료를 농도별(250, 500 μg/mL)로 첨가한 plate에 선충을 배양하여 성체가 된지 3일째의 선충을 사용하였다. 실험에 사용된 선충의 표피를 사진 촬영을 용이하게 하기 위해 M9 buffer로 세척한 뒤 sodium azide (4%)로 마취시키고 발현 강도를 정량하고 분석하기 위해 형광 실체 현미경(Olympus, Japan)으로 사진을 촬영 및 관찰하였으며, Image J 소프트웨어를 사용하여 분석하였다.26)
수명연장 효능평가 – 선충의 수명연장 효능평가를 확인하기 위해 산수유 추출물과 분획물을 첨가(500 μg/mL)한 plate에 알만을 따로 분리하여 배양하였다. 성체가 된지 1일째의 선충 50마리를 각각의 plate로 옮겨준 뒤 20℃에서 배양하면서 24시간 간격으로 선충의 생존율을 확인하였다. 7일째 까지는 24시간 간격으로 선충은 신선한 plate로 옮겨주었으며, 7일 이후에는 48시간 간격으로 옮겨주면서 생존율을 측정하였다. 선충의 사망은 platinum wire의 끝으로 조심스럽게 자극하였을 때 반응이 없는 경우를 사망상태로 간주하였다.27)
통계분석 – 통계 자료의 값은 평균값 ± 표준오차(mean ± S.E.M.)로 표시하였으며, 그룹 간에 대한 통계적 유의성 검정은 ANOVA를 이용하여 분석하였다. 선충의 연속적인 생존도는 Log-rank test 분석 방법을 이용하였으며. P값은 *P<0.05, **P<0.01, ***P<0.001일 때 유의성이 있는 것으로 간주하였다.
결과 및 고찰
Polyphenol, flavonoids 함량 분석 – 항산화 활성에 크게 기여하는 polyphenol과 flavonoids는 항암,28) 항염증29) 등 다양한 생리활성이 보고되어 있으며, 산수유 추출물 및 분획물의 polyphenol 함량을 분석한 결과 ethyl acetate fraction (2,823 ± 0.01 μg TAE/g)이 가장 우수하게 측정되었으며, n-butanol fraction (767.25 ± 0.01 μg TAE/g), n-hexane fraction (575.08 ± 0.02 μg TAE/g), methylene chloride fraction (512.08 ± 0.02 μg TAE/g), ethanol extract (333.71 ± 0.01 μg TAE/g)순으로 높은 함량을 나타내었다. Flavonoids 함량은 ethyl acetate fraction (610.25 ± 0.04 μg QE/g)의 함량이 가장 우수하게 측정되었으며, n-butanol fraction (274.87 ± 0.08 μg QE/g), ethanol extract (287.34 ± 0.23 μg QE/g), n-hexane fraction (207.23 ± 0.24 μg QE/g), methylene chloride raction (188.15 ± 0.16 μg QE/g) 순서로 측정되었다(Table I). 이전에 보고된 결과를 살펴보면 산수유 에탄올 추출물의 폴리페놀 함량이 2.79 mg/100 g, 플라보노이드 함량이 1.81 mg/100 g으로 본 연구의 에탄올 추출물과 ethyl acetate 분획에서의 함량이 더 높은 것으로 측정되었으며,30) 이러한 이유는 페놀성 화합물이 ethyl acetate와 같은 유기 용매 또는 수용성 에탄올 등에 쉽게 용해되기 때문이라고 판단된다.
DPPH, ABTS radical 소거 활성 측정 – DPPH radical 소거 활성 측정법은 시료의 항산화능과 반응하면 DPPH radical이 탈색이 되는 원리를 이용한 방법으로 천연물 소재로부터 항산화제 개발에 대한 연구에 다양하게 이용되는 방법이다.31) 본 연구에서는 산수유 ethanol 추출물과 용매 분획물에 대한 DPPH radical 소거 활성을 측정하였으며, 50%의 소거 활성을 나타내는 시료의 농도(IC50 value, μg/mL)로 값을 나타내었다. 산수유 추출물 및 분획물의 DPPH radical 소거 활성 측정 결과 ethanol extract (IC50 value, 248.5 μg/mL), n-hexane fraction (IC50 value, 331.7 μg/mL), methylene chloride fraction (IC50 value, 377.6 μg/mL), ethyl acetate fraction (IC50 value, 21.6 μg/mL), n-butanol fraction (IC50 value, 84.4 μg/mL)으로 ethyl acetate 분획의 radical 소거 활성이 타 분획에 비해 가장 우수하게 측정되었다(Fig. 1A). 이전에 보고된 연구결과에 따르면 50% ethanol을 용매로 추출한 산수유 시료의 DPPH radical 소거 활성이 농도 의존적으로 증가하여 IC50값이 330.0 μg/mL으로 측정되었다고 보고한 바 있으며,32) 70% ethanol을 용매로 추출한 산수유의 radical 소거 활성이 농도 의존적으로 증가한다고 보고한 바 있다.33) ABTS radical 소거 활성은 ABTS와 postassium persulfate로 인해 생성된 radical 이 항산화능에 의해 제거되면서 탈색되는 원리를 이용한 방법으로 DPPH radical 소거 활성 측정법과 더불어 시료의 항산화 활성에 대한 연구에 널리 이용되어지고 있다.21) 산수유 추출물과 분획물의 ABTS radical 소거 활성 측정 결과 ethanol extract (IC50 value, 270.4 μg/mL), n-hexane fraction (IC50 value, 352.7 μg/mL), methylene chloride fraction (IC50 value, 128.1 μg/mL), ethyl acetate fraction (IC50 value, 22.1 μg/mL), n-butanol fraction (IC50 value, 80.7 μg/mL)으로 ethyl acetate 분획의 radical 소거 활성이 가장 우수하게 측정되었다(Fig. 1B). 이전에 보고된 연구결과를 살펴보면 80% methanol을 용매로 추출한 산수유 추출물과 분획물의 ABTS radical 소거 활성에 대하여 ethyl acetate 분획의 radical 소거 활성이 가장 우수하게 측정되었다고 보고한 바 있다.10) 또한, 70% ethanol을 용매로 추출한 산수유 추출물의 ABTS radical 소거 활성이 진달래 추출물, 박달나무 추출물, 비목나무 추출물 등 산림지역 자생식물의 추출물에 비해 매우 우수하게 측정되었다고 보고한 바,34) 이상의 결과를 토대로 산수유 추출물 및 ethyl acetate 분획은 매우 뛰어난 radical 소거 활성을 나타냄을 확인할 수 있다.
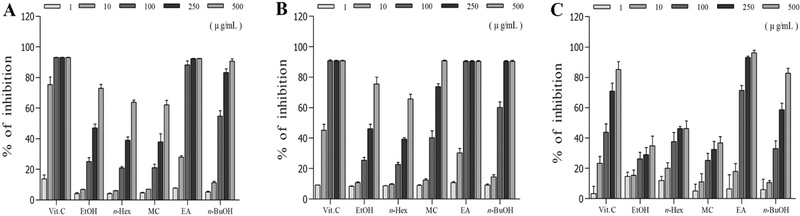
Radical scavenging effects of the ethanol extract, and its fractions from the Cornus officinalis. (A) DPPH free radical scavenging effects. (B) ABTS radical scavenging effects. (C) Superoxide radical scavenging effects. Vit.C, vitamin C; EtOH, ethyl alcohol; n-Hex, n-hexane; MC, methylene chloride; EA, ethyl acetate; n-BuOH, n-butanol.
Xanthine/xanthine 유래 superoxide radical 소거 활성 – Xanthine oxidase는 xanthine을 기질로 uric acid를 생성하는 과정에서 superoxide radical을 생성하는 효소로써 염증과 통증을 유발시킨다.35-36) 따라서, xanthine oxidase의 활성을 억제하면 항산화 및 항염증에 대한 효과를 기대할 수 있게 된다. Xanthine/xanthine oxidase에 의해 생성된 superoxide radical 소거 활성을 측정한 결과 ethanol extract (IC50 value, 5,619 μg/mL), n-hexane fraction (IC50 value, 477.5 μg/mL), methylene chloride fraction (IC50 value, 1,491 μg/mL), ethyl acetate fraction (IC50 value, 36.2 μg/mL), n-butanol fraction (IC50 value, 140.8 μg/mL)으로 산수유 ethyl acetate 분획의 소거 활성이 가장 우수하게 측정되었다(Fig. 1C). 이전에 보고된 결과에서는 70% ethanol을 용매로 추출한 산수유 추출물을 백혈병 바이러스로 유도된 수컷 쥐의 종양으로부터 생성된 대식세포주인 RAW 264.7 세포에 처리하였을 때 농도 의존적으로 xanthine oxidase의 활성을 저해시켰다고 보고한 바 있으며,37) reverse osmotic water(역삼투압 물)로 추출한 산수유 추출물의 xanthine oxidase 저해 활성이 증가하였다고 보고한 바 있다(IC50 value, 2,620 μg/mL).38) 이상의 결과를 토대로 산수유 추출물 및 산수유 ethyl acetate 분획은 우수한 xanthine oxidase 저해 활성으로 superoxide radical 소거 활성을 증가시켜 염증과 통증을 억제할 수 있을 것으로 생각된다.
항산화 효소(SOD) 활성 측정 – 본 연구에서는 산수유 ethyl acetate 분획의 뛰어난 radical 소거 활성을 확인하여 예쁜꼬마선충 모델을 활용하였을 때의 항산화 및 수명연장 활성에 대한 분석을 실시하였다. 산수유 ethyl acetate 분획의 처리에 따른 선충 체내의 SOD의 활성 증가 여부를 확인한 결과 산수유 ethyl acetate 분획 250 μg/mL 처리군은 SOD의 활성을 34.3%, 500 μg/mL 처리군은 SOD의 활성을 63.7% 증가시켰다(Fig. 2). 이전에 보고된 결과를 살펴보면 추출 온도에 따른 산수유 에탄올 추출물의 SOD 유사활성이 농도의존적으로 증가하여 최대 SC50 값이 125,1 μg/mL으로 우수한 SOD 유사활성을 나타내었다고 보고한 바 있다.39) SOD는 생체 내 존재하는 항산화 효소로써, 체내의 활성산소를 과산화수소로 전환하여 peroxidase에 의해 제거될 수 있도록 촉매하는 역할을 한다.40) 따라서, 산수유 ethyl acetate 분획은 선충 체내의 SOD의 활성에 관여하여 활성산소종으로 인한 세포의 손상으로부터 방어에 어느정도 도움을 줄 수 있을 것으로 사료된다.
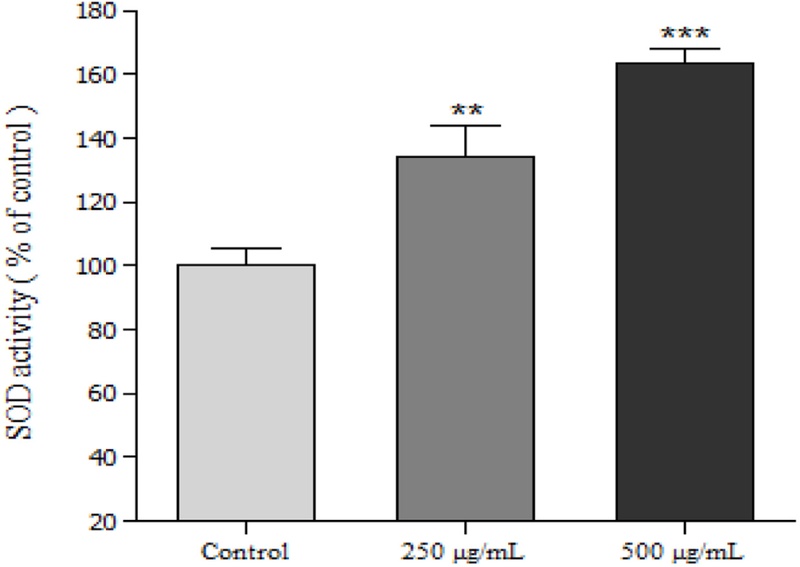
Effects of ethyl acetate fraction from Cornus officinalis on the antioxidant enzyme activity. SOD activity as a percentage of superoxide scavenged per control. Data are expressed as the mean±S.E.M. of three independent experiments. Differences compared to the control were considered significant at **P<0.01 and ***P<0.001.
산화적스트레스 저항성 및 열 스트레스 저항성 – 호두나무에 의해 생성되는 천연 독소로 알려진 juglone은 타감작용으로 주위의 식물들의 발육을 억제시키며 semiquinone radical을 형성하여 O2–와 과산화수소를 생성하고 산화적스트레스 유발, 세포막 손상 및 사멸 등을 일으킨다고 알려져 있다.41,42) 본 연구에서는 juglone으로 산화적스트레스를 유발시킨 선충의 생존율에 산수유 ethyl acetate 분획이 미치는 영향을 확인하였다. 산수유 ethyl acetate 분획을 처리하지 않은 대조군의 평균 생존시간은 15.4 ± 0.6시간, 최대 생존시간은 26시간으로 측정되었으며 산수유 ethyl acetate 250 μg/mL 처리군의 평균 생존시간은 19.9 ± 0.7시간, 최대 생존시간은 32시간으로 측정되었다. 산수유 ethyl acetate 분획 500 μg/mL 처리군의 평균 생존시간은 21.8 ± 0.7시간, 최대 생존시간은 34시간으로 각각 28.9%, 41.6% 증가된 생존율을 나타내었다 (Fig. 3A, B, Table II). 예쁜꼬마선충은 온도에 민감한 생물로써 최적의 성장 온도는 20℃이지만 고온에 노출되게 되면 섭취, 생식 등의 기능이 저하되고 장 기능이 손상되어 사망에 이르게 된다.43) 산수유 ethyl acetate 분획이 선충의 열 스트레스 저항성에 미치는 영향을 확인해본 결과 대조군 선충의 평균 생존시간은 14.7 ± 0.4시간, 최대 생존시간은 18시간으로 측정되었으며 산수유 ethyl acetate 분획 250 μg/mL 처리군의 평균 생존시간은 17.3 ± 0.4시간, 최대 생존시간은 23시간, 500 μg/mL 처리군의 평균 생존시간은 18.9 ± 0.5시간, 최대 생존시간은 24시간으로 측정되었다(Fig. 3C, D, Table II). 예쁜꼬마선충은 35℃ 이상의 고온에서는 약 24시간 정도의 생존시간을 가지며 열 충격으로부터 세포를 보호하는 Heat shock transcription factor-1 (HSF-1)유전자의 발현으로 자신의 몸을 보호한다.44) 산수유 ethyl acetate 분획은 고온의 조건에서 선충의 생존율을 유의성 있게 증가시켰으며, 이는 산수유 ethyl acetate 분획이 선충에게서 열 스트레스에 대항하는 단백질의 발현에 관여하였다고 판단된다.
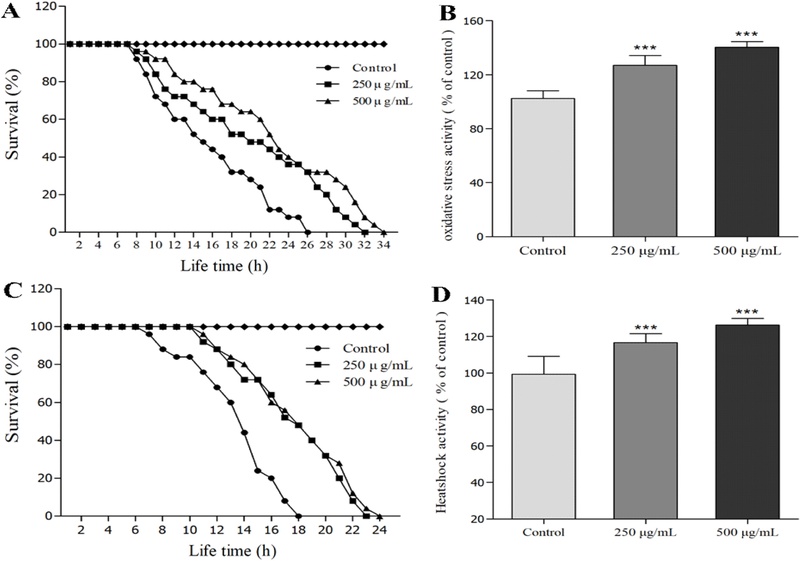
Effects of ethyl acetate fractions from Cornus officinalis on the stress tolerance and thermal stress tolerance of wild-type N2 nematodes. (A, B) For the oxidative stress assays, worms were transferred to 96 well plate containing 1 mM of juglone liquid culture, and then their viability was scored. (C, D) To assess thermal tolerance, worms were incubated at 36°C and then their viability was scored. Statistical difference between the curves was analyzed by log-rank test. All experiments were done in triplicates. Differences compared to the control were considered significant at ***P<0.001.
SOD-3::GFP 발현량 측정 – SOD-3::GFP의 활성화 및 과발현은 산화적 손상 이후 선충의 장수 반응을 유도하며, CF1553 모델은 SOD-3::GFP를 포함한 형질전환 선충으로써 GFP의 발현율에 따라 분석하고자 하는 시료 내 항산화 활성을 나타내는 물질이 함유되어 있는 모델로 이용되어지고 있다.45-47) 산수유 ethyl acetate 분획을 농도별로 처리하였을 때 CF1553 선충 내 GFP의 발현율을 관찰한 결과 250 μg/mL 처리군은 대조군 선충에 비해 15.9% 증가된 SOD-3::GFP 발현율을 나타내었으며, 500 μg/mL 처리군은 대조군 선충에 비해 25.5% 증가된 SOD-3::GFP 발현율을 나타내어 머리와 꼬리, 특히 배부분에서 강하게 발현된 GFP를 확인할 수 있다(Fig. 4A,B). SOD-3::GFP는 외부 환경으로 인해 과발현될 수 있으며, 이 GFP의 과발현은 산화적스트레스에 대한 저항성을 증가시키고 수명을 연장시킬 수 있어 선충의 수명연장에 지표로 사용되고 있다.50-52) 따라서, 산수유 ethyl acetate 분획은 형질전환 된 CF1553 선충 내 SOD-3::GFP의 발현 증가에 관여하여 산화적 손상으로부터 방어에 도움을 줄 것으로 판단된다.
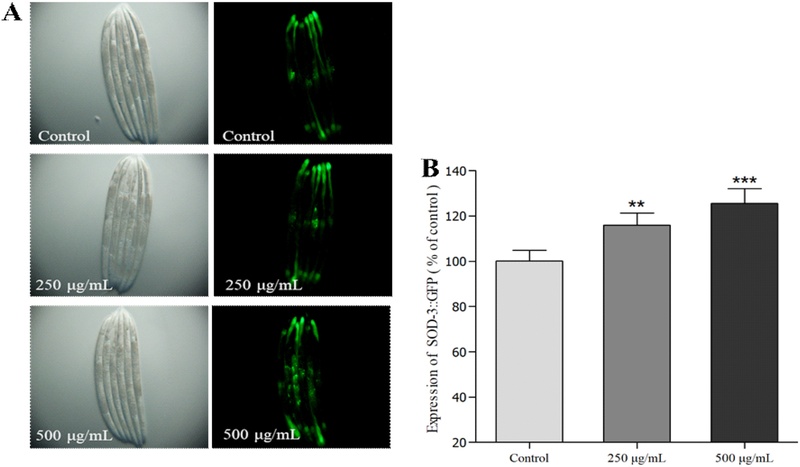
Effects of ethyl acetate fraction of the Cornus officinalis on the expression of SOD-3(CF1553) was determined using transgenic nematodes. (A) Images of SOD-3::GFP expressions of CF1553 nematodes in presence or absence of the ethyl acetate fraction of Cornus officinalis. The mean GFP-expressing intensity of CF1553 mutants was expressed as mean S.E.M. of values from 100 worms experiment (B). Data are expressed as the mean±standard deviation of three independent experiments (N=3). Differences compared with the control were considered significant at **P<0.01 and ***P<0.001.
수명연장 효능평가 – 예쁜꼬마선충의 수명은 약 3주로 매우 짧은 생명주기를 가지고 있지만, 최대 80%의 환경적인 요인으로 수명이 결정되며 NGM agar plate의 영양소를 섭취하여 수명을 연장 또는 단축시킬 수 있다.53-54) 본 연구에서는 산수유 추출물과 분획물이 선충의 수명연장에 미치는 영향을 확인하였으며, 대조군 선충의 평균 수명은 11.0 ± 0.2일, 최대 생존일은 20일이었으며, ethanol 추출물 처리군의 평균 수명은 12.5 ± 0.2일, 최대 생존일은 21일, n-hexane 분획물 처리군의 평균 수명은 12.2 ± 0.2일, 최대 생존일은 20일, methylene chloride 분획물 처리군의 평균 수명은 11.9 ± 0.2일, 최대 생존일은 21일, ethyl acetate 분획물 처리군의 평균 수명은 14.0 ± 0.3일, 최대 생존일은 22일, n-butanol 분획물 처리군의 평균 수명은 12.5 ± 0.2, 최대 생존일은 21일로 ethyl acetate 분획물 처리군에게서 26.4% 증가된 수명연장 활성을 나타내었다(Fig. 5, Table III). 이전에 보고된 결과에서는 산수유 에탄올 추출물(100, 300 mg/kg/day)을 투여한 복수암 유발 ICR mice의 수명이 산수유 추출물을 처리하지 않은 대조군에 비해 29.3%, 39.3% 증가하였다고 보고한 바 있다.55) 수명연장은 항스트레스와 크게 관련이 있다는 보고가 이루어져 있는데,56,57) 산수유 ethyl acetate 분획이 선충의 산화적스트레스 및 열 스트레스에 대한 저항성을 높여주어 수명연장에 일부 영향을 미쳤음을 추측할 수 있다.
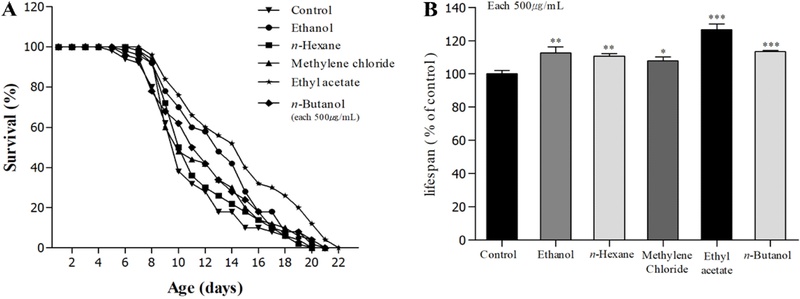
Effects of the fractions from Cornus officinalis on the lifespan of wild-type N2 nematodes. Worms were grown in the NGM agar plate at 20°C in the absence or presence of fractions. The number of worms used per each lifespan assay experiment was 47-48 and three independent experiments were repeated (N=3). (A) The mortality of each group was determined by daily counting of surviving and dead animals. (B) The mean lifespan of the N2 worms was calculated from the survival curves. Statistical difference between the curves was analyzed by log-rank test. Error bars represent the standard error of mean (S.E.M.). Differences compared to the control were considered significant *P<0.05 and **P<0.01 and ***P<0.001.
결 론
본 연구에서는 산수유 에탄올 추출물을 극성에 따라 n-hexnae, methylene chloride, ethyl acetate, n-butanol 순서로 분획하여 추출물과 분획물의 폴리페놀, 플라보노이드 함량을 측정하고 DPPH, ABTS, superoxide radical 소거 활성을 측정하여 가장 뛰어난 radical 소거활성을 나타낸 ethyl acetate 분획의 예쁜꼬마선충에 대한 항산화 및 수명연장 활성에 대하여 규명하였다. 산수유 ethyl acetate 분획을 농도별로 처리하였을 때 선충 체내의 SOD의 활성을 농도 의존적으로 증가시켰으며, juglone에 의해 유도된 산화적 스트레스와 고온에 의한 열 스트레스에 대한 저항성을 나타내어 생존율을 증가시켰다. 형질전환 된 SOD-3::GFP를 포함한 CF1553 선충 내 SOD-3::GFP의 발현율을 농도 의존적으로 증가시켰고 선충의 수명을 유의성 있게 증가시켰다. 이는 산수유에 존재하는 주요 성분이 항산화 및 수명연장 시스템의 활성을 통해 항산화 활성을 나타내고 수명을 연장 시키는 것으로 보인다. 따라서, 산수유 ethyl acetate 분획은 항산화제의 개발 및 수명연장 관련 질환의 치료와 예방에 도움을 줄 수 있을 것으로 사료되며 산수유 ethyl acetate 분획 내 성분과 항산화 활성과의 구체적인 상관관계에 대한 추가적인 연구가 이루어져야 할 것으로 판단된다.
References
-
Tai, A., Iomori, A. and Ito, H. (2017) Structural evidence for the DPPH radical-scavenging mechanism of 2-O-α-d-glucopyranosyl-l-ascorbic acid. Bioorganic & Medicinal Chemistry 25: 5303-5310.
[https://doi.org/10.1016/j.bmc.2017.07.044]

-
Saidi Merzouk, A., Hafida, M., Medjdoub, A., Loukidi, B., Cherrak, S., Merzouk, S. A. and Elhabiri, M. (2017) Alterations of hepatocyte function with free radical generators and reparation or prevention with coffee polyphenols. Free Radical Research 51: 294-305.
[https://doi.org/10.1080/10715762.2017.1307979]

-
Niki, E. (2016). Antioxidant capacity of foods for scavenging reactive oxidants and inhibition of plasma lipid oxidation induced by multiple oxidants. Food Funct. 7: 2156-2168.
[https://doi.org/10.1039/C6FO00275G]

-
Dröge, W. (2002) Free radicals in the physiological control of cell function. Physilo. Rev. 82: 47-95.
[https://doi.org/10.1152/physrev.00018.2001]

-
Willcox, J. K, Ash, S. L., and Catignani, G. L. (2004) Antioxidants and prevention of chronic disease. Crit. Rev. Food Sci. 44: 275-295.
[https://doi.org/10.1080/10408690490468489]

- Jun, B. S, Cha, J. Y. and Cho, Y. S. (2001) Antioxidative activities of fruit extracts of Paulownia tomentosa stuffed. Korean J. Postharvest Sci. Technol. 8: 231-238.
- Seo, K. I., Lee, S. W. and Yang, K. H. (1999) Antimicrobial and antioxidative activities of Corni fructus extracts. Korean J. Postharvest Sci. Technol. 6(1): 99-103.
-
Kim, Y. D., Kim, H. K. and Kim, K. J. (2003) Antimicrobial activity of solvent fraction from Cornus officianalis. J. Korean Soc. Food Sci. Nutr. 32: 829-832.
[https://doi.org/10.3746/jkfn.2003.32.6.829]

- Seo, Y. B., Choi, Y. B., Lee, Y. K. and Lee, Y. C. (2002) Study on the effects of Xanthii Fructus about the anti-allergic action on IC-2 Cell. Herbology 17: 39-54.
- Kim, O. K. (2005) Antidiabetic and antioxidative effects of Corni fructus in streptozotocin-induced diabetic rats. KSAST 22: 157-167.
-
Gaw, H. Z. and Wang, H. P. (1949) Survey of Chinese drugs for presence of antibacterial substances. Science 110: 11-12.
[https://doi.org/10.1126/science.110.2844.11.b]

- Kim, D. K., Kwak, J. H., Ryu, J. H., Kwon, H. C., Song, K. W., Kang, S. S. and Zee, O. P. (1996) A component from Cornus officinalis enhances hydrogen peroxide generation from macrophages. Kor. J. Pharmacogn. 27: 101-104.
-
Kim, S. H., Kang, C. J., Seong, G. U. and Chung, S. K. (2019) Physicochemical quality characteristics of Corni Fructus depending on the picking periods. Korean J. Food Preserv. 26: 740-744.
[https://doi.org/10.11002/kjfp.2019.26.7.740]

-
Kim, Y. J. and Son, D. Y. (2016) Antioxidant activity and suppression of pro-inflammatory mediator of Corni fructus extracts in activated RAW 264.7 macrophage. Korean J. Food Preserv. 23: 876-882.
[https://doi.org/10.11002/kjfp.2016.23.6.876]

-
Lim, J. M. Li, G. Z., Chai, O. H. and Song, C. H. (2004) Inhibitory effect of Corni Fructus on compound 48/80-induced mast cell activation and vascular permeability. Kor. J. Phys. Anthrop. 17: 19-30.
[https://doi.org/10.11637/kjpa.2004.17.1.19]

- Oh, S., Park, M. R. and Kim, Y. (2013) Development of dscovering method for functional probiotics using smart animal. Food Sci. Anim. Respor. 2: 36-42.
-
Bargmann, C. I. (1998) Neurobiology of the Caenorhabditis elegans genome. Science 282: 2028-2033.
[https://doi.org/10.1126/science.282.5396.2028]

-
Cicco, N., Lanorte, M. T., Paraggio, M., Viggiano, M. and Lattanzio, V. (2009) A reproducible, rapid and inexpensive Folin–Ciocalteu micro-method in determining phenolics of plant methanol extracts. Microchemical journal. 91: 107-110.
[https://doi.org/10.1016/j.microc.2008.08.011]

-
Lee, M. Y., Yoo, M. S., Whang, Y. J., Jin, Y. J., Hong, M. H., and Pyo, Y. H. (2012) Vitamin C, total polyphenol, flavonoid contents and antioxidant capacity of several fruit peels. Korean F. Food Sci. Technol. 44: 540-544.
[https://doi.org/10.9721/KJFST.2012.44.5.540]

-
Yoshida, T., Mori, K., Hatano, T., Okumura, T., Uehara, I., Komagoe, K., Fujita, Y. and Okuda, T. (1989) Studies on inhibition mechanism of autooxidation by tannins and flavonoids. V: Radical scavenging effects of tannins and related polyphenols on 1,1-diphenyl-2-picrylhydrazyl radical. Chem. Pharm. Bull. 37: 1919-1921.
[https://doi.org/10.1248/cpb.37.1919]

-
Re, R., Pellegrini, N., Proteggente, A., Pannala, A., Yang, M. and Rice-Evans, C. (1999) Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Radic. Biol. Med. 26: 1231-1237.
[https://doi.org/10.1016/S0891-5849(98)00315-3]

-
Thuong, P. T., Kang, H. J., Na, M., Jin, W., Youn, U. J., Seong, Y. H. and Bae, K. (2007) Anti-oxidant constituents from Sedum takesimense. Phytochemistry 68: 2432-2438.
[https://doi.org/10.1016/j.phytochem.2007.05.031]

-
Brenner, S. (1974) The genetics of Caenorhabditis elegans. Genetics 77: 71-94.
[https://doi.org/10.1093/genetics/77.1.71]

-
Chen, W., Rezaizadehnajafi, L. and Wink, M. (2013) Influence of resveratrol on oxidative stress resistance and life span in Caenorhabditis elegans. J. Pharm. Pharmacol. 65: 682-688.
[https://doi.org/10.1111/jphp.12023]

-
del Valle Carranza, A., Saragusti, A., Chiabrando, G. A., Carrari, F. and Asis, R. (2020) Effects of chlorogenic acid on thermal stress tolerance in C. elegans via HIF-1, HSF-1 and autophagy. Phytomedicine 66: 153132.
[https://doi.org/10.1016/j.phymed.2019.153132]

-
Qi, Z., Ji, H., Le, M., Li, H., Wieland, A., Bauer, S. and Herr, I. (2021) Sulforaphane promotes C. elegans longevity and healthspan via DAF-16/DAF-2 insulin/IGF-1 signaling. Aging (Albany NY). 13: 1649.
[https://doi.org/10.18632/aging.202512]

-
Lithgow, G. J., White, T. M., Melov, S. and Johnson, T. E. (1995) Thermotolerance and extended life-span conferred by single-gene mutations and induced by thermal stress. PNAS. 92: 7540-7544.
[https://doi.org/10.1073/pnas.92.16.7540]

-
Williams, R. J., Spencer, J. P. and Rice-Evans, C. (2004) Flavonoids: antioxidants or signalling molecules?. Free Radic. Biol. Med. 36: 838-849.
[https://doi.org/10.1016/j.freeradbiomed.2004.01.001]

-
Heim, K. E., Tagliaferro, A. R. and Bobilya, D. J. (2002) Flavonoid antioxidants: chemistry, metabolism and structure-activity relationships. J. Nutr. Biochem. 13: 572-584.
[https://doi.org/10.1016/S0955-2863(02)00208-5]

-
Ju, J. C., Shin, J. H., Lee, S. J., Cho, H. S. and Sung, N. J. (2006) Antioxidative activity of hot water extracts from medicinal plants. J. Korean Soc. Food Nutr. 35: 7-14.
[https://doi.org/10.3746/jkfn.2006.35.1.007]

-
Dudonne, S., Vitrac, X., Coutiere, P., Woillez, M. and Mérillon, J. M. (2009) Comparative study of antioxidant properties and total phenolic content of 30 plant extracts of industrial interest using DPPH, ABTS, FR Pharmacognosy AP, SOD, and ORAC assays. J. Agric. Food Chem. 57: 1768-1774.
[https://doi.org/10.1021/jf803011r]

- Kim, T., Jung, H., Jang, J., Sim, M., Lee, M., Cho, J. and Cho, H. (2016) Effect of Corni Fructus on testosterone deficiency syndrome in in vitro and in vivo. Kor. J. Pharmacogn. 47: 264-272.
- Lim, H. J., Lee, H. J. and Lim, M. H. (2015) Antioxidant activity of acaiberry, blueberry, corni, and mulberry. Kor. J. Aesthet. Cosmetol. 13: 445-452.
-
Cho, M., Lee, J. S., Lee, S., Son, Y. K., Bae, C. H., Yeo, J. and Kim, J. Y. (2015) Antioxidant activity of 11 species in Korean native forest plants. J. Korean Soc. Food Sci. Nutr. 28: 1098-1106.
[https://doi.org/10.9799/ksfan.2015.28.6.1098]

-
Duke, E. J., Joyce, P. and Ryan, J. P. (1973) Characterization of alternative molecular forms of xanthine oxidase in the mouse. Biochem. J. 131: 187-190.
[https://doi.org/10.1042/bj1310187]

-
Wyngaarden, J, B. and Holmes, E, W. (1977) Molecular nature of enzyme regulation in purine biosynthesis. Purine and Pyrimidine Metabolism 48: 43-64.
[https://doi.org/10.1002/9780470720301.ch4]

-
Hwang, K. A., Hwang, Y. J. and Song, J. (2016) Antioxidant activities and oxidative stress inhibitory effects of ethanol extracts from Cornus officinalis on raw 264.7 cells. BMC complement. Altern. Med. 16: 1-9.
[https://doi.org/10.1186/s12906-016-1172-3]

-
Chang, J. S., Chiang, L. C., Hsu, F. F. and Lin, C. C. (2004) Chemoprevention against hepatocellular carcinoma of Cornus officinalis in vitro. Am. J. Chin. Med. 32: 717-725.
[https://doi.org/10.1142/S0192415X04002296]

-
Lee, M. H., Kim, J. M. and Park, E. J. (2011) Antioxidant and antigenotoxic effects of sansuyu fruit (Corni Fructus) extracted with water at different temperatures. J. Korean Soc. Food Sic. Nutr. 40: 149-155.
[https://doi.org/10.3746/jkfn.2011.40.2.149]

-
Marklund, S. and Marklund, G. (1974) Involvement of the superoxide anion radical in the autoxidation of pyrogallol and a convenient assay for superoxide dismutase. Eur. J. Biochem. 47: 469-474.
[https://doi.org/10.1111/j.1432-1033.1974.tb03714.x]

-
Aithal, B. K., Kumar, M. S., Rao, B. N., Udupa, N. and Rao, B. S. (2009) Juglone, a naphthoquinone from walnut, exerts cytotoxic and genotoxic effects against cultured melanoma tumor cells. Cell Biol. Int. 33: 1039-1049.
[https://doi.org/10.1016/j.cellbi.2009.06.018]

-
Inbaraj, J. J. and Chignell, C. F. (2004) Cytotoxic action of juglone and plumbagin: a mechanistic study using HaCaT keratinocytes. Chem. Res. Toxicol. 17: 55-62.
[https://doi.org/10.1021/tx034132s]

-
Lara L. J. and Rostagno M. H. (2013) Impact of heat stress on poultry production. Animals 3: 356-369.
[https://doi.org/10.3390/ani3020356]

-
Labbadia, J. and Morimoto, R. I. (2015) The biology of proteostasis in aging and disease. Annu. Rev. Bioehcm. 84: 435-464.
[https://doi.org/10.1146/annurev-biochem-060614-033955]

-
Darr, D. and Fridovich, I. (1995) Adaptation to oxidative stress in young, but not in mature or old, Caenorhabditis elegans. Free Radic. Biol. Med. 18: 195-201.
[https://doi.org/10.1016/0891-5849(94)00118-4]

-
Seo, H. W., Cheon, S. M., Lee, M. H., Kim, H. J., Jeon, H. and Cha, D. S. (2015) Catalpol modulates lifespan via DAF-16/FOXO and SKN-1/Nrf2 activation in Caenorhabditis elegans. Evid. Based Complement Alternat. Med.
[https://doi.org/10.1155/2015/524878]

-
Salgueiro, W. G., Goldani, B. S., Peres, T. V., Miranda-Vizuete, A., Aschner, M., da Rocha, J. B. T. and Ávila, D. S. (2017) Insights into the differential toxicological and antioxidant effects of 4-phenylchalcogenil-7-chloroquinolines in Caenorhabditis elegans. Free Radic. Biol. Med. 110: 133-141.
[https://doi.org/10.1016/j.freeradbiomed.2017.05.020]

-
Wu, H., Zhao, Y., Guo, Y., Xu, L. and Zhao, B. (2012) Significant longevity-extending effects of a tetrapeptide from maize on Caenorhabditis elegans under stress. Food Chem. 130: 254-260.
[https://doi.org/10.1016/j.foodchem.2011.07.027]

-
Hsu, A. L., Murphy, C. T. and Kenyon, C. (2003) Regulation of aging and age-related disease by DAF-16 and heat-shock factor. Science 300: 1142-1145.
[https://doi.org/10.1126/science.1083701]

-
Rea, S. L., Wu, D., Cypser, J. R., Vaupel, J. W. and Johnson, T. E. (2005) A stress-sensitive reporter predicts longevity in isogenic populations of Caenorhabditis elegans. Nature Genetics 37: 894-898.
[https://doi.org/10.1038/ng1608]

-
Gill, M. S. (2006) Endocrine targets for pharmacological intervention in aging in Caenorhabditis elegans. Aging Cell 5: 23-30.
[https://doi.org/10.1111/j.1474-9726.2006.00186.x]

-
Johnson, T. E. and Wood, W. B. (1982) Genetic analysis of life-span in Caenorhabditis elegans. PNAS 79: 6603-6607.
[https://doi.org/10.1073/pnas.79.21.6603]

-
Kwon, S. H., Kwon, S. J., Kim, J. Y., Kang, K. S., Shim, K. H., Lee, M. K. and Seo, K. I. (2010) Antitumor activity of Corni Fructus ethanol extract in sarcoma-180 cancer cells. J. Korean Soc. Food Sci. Nutr. 39: 960-965.
[https://doi.org/10.3746/jkfn.2010.39.7.960]

-
Harman, D. (2002) Aging: a theory based on free radical and radiation chemistry. SAGE KE 2002: cp14-cp14.
[https://doi.org/10.1126/sageke.2002.37.cp14]

-
Bokov, A., Chaudhuri, A. and Richardson, A. (2004) The role of oxidative damage and stress in aging. Mech. Ageing Dev. 125: 811-826.
[https://doi.org/10.1016/j.mad.2004.07.009]

