
선복화 추출물의 스트레스 관련 인자 조절을 통한 코르티코스테론 유도 PC12세포 보호효과
Abstract
The flowers of Inula britannica var. japonica (Asteraceae) has been listed in the Korean Herbal Pharmacopoeia as a medicinal herb used to alleviate cough, phlegm, and gastrointestinal discomfort. Traditionally, it has been prescribed for inflammatory disorders such as bronchitis, as well as for metabolic diseases including diabetes and hypertension. Recent pharmacological studies have validated its traditional uses and revealed novel bioactivities such as anti-inflammatory, antioxidant, anti-obesity, and neuroprotective effects, largely attributed to its sesquiterpene lactones and flavonoid constituents. To investigate the neuroprotective and anti-stress potential of Inulae Flos, the present study employed a corticosterone-induced PC12 cell model, which mimics stress-induced neuronal dysfunction. In this study, hot-water and ethanolic extracts of Inulae Flos were evaluated for their protective effects on ROS generation, inflammatory cytokines, apoptosis and neurotrophic signaling including BDNF, NGF, and CREB activation in corticosterone-induced PC12 cells. The extracts significantly restored cell viability and reduced ROS production and apoptotic cell death. Western blot analysis revealed that Inulae Flos extracts upregulated the phosphorylation of CREB and enhanced the expression of BDNF and NGF, while suppressing the phosphorylation of ERK and p38 MAPK involved in inflammatory signaling. Markedly, Inulae Flos extract increased BDNF expression to the level comparable to the positive controls, L-theanine and fluoxetine. These findings demonstrate that Inulae Flos exerts a potent neuroprotective effect against glucocorticoid-induced neuronal stress by modulating oxidative, inflammatory, and neurotrophic pathways. The results suggest that Inulae Flos extract has promising potential as a functional ingredient for stress alleviation and brain health improvement.
Keywords:
Inula britannica, Stress, Corticosterone, PC12, BDNF, Neuroprotection선복화는 국화과(Asteraceae) 식물인 금불초(Inula britannica Linne. var. japonica Thunb)의 꽃을 이르는 생약명으로 대한민국약전외한약(생약) 규격(KHP)에 기재되어 있다.1) Inula 속 식물은 유럽과 아시아, 지중해, 아프리카 등의 온대 지역에 널리 분포하며 전세계적으로 약 100종 이상이 서식한다고 보고된다.2) 이 중 선복화는 우리나라를 비롯한 중국, 일본, 대만, 유럽, 지중해, 아프리카 등지에 분포하며 주로 습지나 물가를 중심으로 자란다.
선복화는 기침 및 가래 완화, 위장관 보호, 이뇨 등의 효능이 보고되었고, 전통적으로 기관지염을 포함한 각종 염증성 질환의 치료, 당뇨병 및 고혈압 치료를 위해 전통의약으로 사용된 기록이 있다.3) 최근 연구를 통해 선복화의 전통적 의약 용도의 과학적 근거가 마련되었고, 전통적 용도 외의 새로운 질환 치료 활성이 다양하게 보고되었다. 대표적으로 선복화의 추출물은 흰쥐에서 HCl/Ethanol로 유도한 위염을 억제하는 효과가 보고되었고,4) 페놀성 화합물을 함유한 선복화의 열수추출물은 3T3-L1세포에서 adipogenesis를 억제하였다.5) 또한, 선복화 추출물은 염증성 인자 조절을 통해 뇌신경세포 보호작용이 우수함이 보고되었는데,6) 선복화에 함유된 성분 중에서 sesquiterpene계열이 이에 기여하는 주요 생리활성물질임이 규명되었다.7)
선복화의 성분 연구는 1998년에 국내에서 최초로 보고된 것으로 확인되는데, 선복화의 chloroform 추출물로부터 분리한 4α,6α-dihydroxyeudesman-8β,12-olide이 세포독성을 가진 물질로 보고되었다.8) 그 이후 다양한 연구를 통해 선복화의 주요 성분으로서 sesquiterpene lactone, diterpenoid, flavonoid 계열의 물질이 보고되었다.9-13) 선복화로부터 유래한 sesquiterpenoid dimer는 human neutrophil elastase 억제를 통한 항염증효과가 확인되었고,14) 최신 연구를 통해 선복화로부터 sesquiterpenoid dimers계열의 신규물질이 추가로 규명되었다.15) 그 외에도 sesquiterpene의 항암활성,16) methoxy flavonoids 화합물의 SARS-CoV-2 3CLpro에 대한 저해활성 등이 보고되었다.17)
최근 신경세포 수준에서 스트레스 자극에 의한 손상 기전을 규명하기 위해 PC12 세포가 널리 활용되고 있다. 고농도의 글루코코르티코이드인 corticosterone 처리로 유도된 PC12 세포 손상 모델은 활성산소종(ROS) 증가, 지질과산화 및 NADPH oxidase 활성 증가, 염증매개인자(iNOS, COX-2, IL-6, TNF-α) 발현 증가 등을 동반하여 세포사멸을 촉진함이 보고된 바 있다.18) 또한 미토콘드리아 막전위의 저하, ATP 감소, 세포내 Ca2+ 증가, autophagy 및 ER 스트레스 마커 증가 등이 관찰되어 스트레스 자극 하에서 autophagy 이상 및 미토콘드리아·ER 기능 이상이 신경세포 손상의 핵심 경로로 제시되었다.19) 이 같은 연구들은 PC12 세포 모델이 스트레스 관련 신경독성 기전 규명 및 천연물 기반 신경보호 물질 탐색에 유용한 실험적 플랫폼임을 시사한다. 반면, corticosterone로 처리된 PC12세포에서 다양한 천연물 및 생리활성 물질들은 이러한 신호경로를 조절함으로써 산화·염증 반응을 억제하고 세포사멸을 저해하여 신경보호 효과를 나타내는 것으로 보고되었다. 대표적으로 paeoniflorin은 ROS 및 MDA 감소, NGF mRNA 증가 등을 통해 신경보호 효과를 나타냈고,20) 감초 유래 플라보노이드 배당체인 isoliquiritin은 미토콘드리아 막전위 붕괴, ROS 증가, [Ca2+]i 과부하 등을 억제하였다.21) Resveratrol은 세포사멸 관련 단백질(Bax, caspase-3) 감소 및 Bcl-2 증가를 통하여 뇌세포를 보호하였다.22) 특히 선복화와 동속 식물인 Inula helenium로부터 유래한 sesquiterpene lactone계열 costunolide는 PC12 세포에서 Nrf2 경로 활성화를 통해 산화손상에 대한 보호효과를 나타내었다.23)
최근 현대 사회에서 만성적 스트레스는 신체적 피로, 불안, 수면장애, 우울 등 다양한 정신생리적 이상을 유발하는 주요 원인으로 보고되고 있으며, 이에 따라 스트레스 완화 및 정서 안정에도 도움을 주는 기능성 식품에 대한 수요가 지속적으로 증가하고 있다.24,25) 국내에서도 건강기능식품 개별인정 제도의 확립으로 인체적용시험을 통한 과학적 근거 확보가 필수화되면서, 스트레스 관련 생리활성 소재의 표준화 및 안정성·기능성 평가에 대한 학문적, 산업적 관심이 증가하고 있다.26) 스트레스 완화 소재에 대한 시장의 수요를 바탕으로 corticosterone을 처리한 PC12세포를 검색계로 하여 천연물로부터 스트레스 저감 효과가 기대되는 신규 원료를 개발하고자 하였으며, 그 결과 선복화의 추출물이 corticosterone으로 유도한 독성으로부터 세포를 보호하는 효과가 매우 우수함을 확인하였다. 본 연구에서는 선복화 추출물의 스트레스 완화 작용 기전을 규명하기 위하여 corticosterone을 처리한 PC12 세포에서 스트레스 관련 인자인 BDNF와 NGF의 발현 및 CREB의 인산화, 염증조절 인자로서 ERK 및 p38의 인산화를 western blot assay를 통해 측정하였다. 또한 corticosterone으로 유도한 apoptosis 및 ROS 생성억제 활성을 flow cytometry를 이용해 평가하였다.
재료 및 방법
실험재료 – 본 연구에서 사용된 선복화(Inula britannica var. japonica)의 꽃은 (주)허브마을에서 구매하였다.
선복화 추출물의 제조 – 건조된 선복화를 믹서기로 분쇄하여 분말화한 후 두가지 조건으로 추출을 진행하였다. 건조 시료 1 g에 추출용매 30 mL을 혼합하여, 주정 추출물은 70℃ water bath에서, 열수 추출물은 100℃ water bath에서 각각 4시간씩 추출한 후 감압 농축하여 추출물을 제조하였다. 열수 추출물은 Phosphate-Buffered Saline (PBS)에, 주정 추출물은 dimethyl sulfoxide (DMSO)에 100 mg/mL 농도로 용해한 후 −20℃에서 보관하여 실험에 사용하였다.
세포배양 – 실험에 사용한 뇌신경세포주 PC12 세포는 ATCC (American Type Culture Collection, Rockefeller, MD, USA)으로부터 분양 받아 사용하였다. PC12 세포는 RPMI-1640 (Gibco BRL, Grand Island, NY, USA) 배지에 10% (v/v) HS (Horse serum, Sigma-Aldrich Inc, St. Louis, MO, USA), 5% (v/v) FBS (Gibco BRL, Grand Island, NY, USA) 및 1% (v/v) 항생제(100 U/mL penicillin and 100 μg/mL streptomycin, Sigma-Aldrich Inc, St. Louis, MO, USA)를 첨가하여 사용하고, incubator에서 37℃와 5% CO2를 유지하여 배양하였다.
세포 독성 측정 – PC12 세포에 대한 추출물의 무독성 농도를 확인하기 위하여 modified MTT (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide) assay를 실시하였다.27) PC12 세포를 96-well plate에 2 × 104 cells/well의 농도로 분주하고 24시간 동안 배양하였다. 배양한 PC12 세포에 선복화 추출물을 각각 50, 100, 200 μg/mL의 농도로 처리하여 다시 24시간 동안 배양하였다. 배양 후 다음 각 well에 10 μL씩 MTT 시약을 분주한 다음 4시간 배양 후 형성된 formazan을 DMSO 90 μL와 30% SDS (Sodium Dodecyl Sulfate) 용액 60 μL를 넣고 빛을 차단하여 15분간 shaking한 후 균질하게 녹여준 다음 550 nm에서 흡광도의 변화를 측정하여 대조군에 대한 세포 생존율을 백분율로 표시하였다.
단백질 발현 분석 – 선복화 추출물의 corticosterone 처리로 독성을 유발한 PC12 세포에서 단백질 발현에 미치는 영향은 western blot 분석을 통해 평가하였다. PC12 세포를 6-well plate에 4 × 105 cells/well의 농도로 분주하여 24시간 동안 배양하였다. 배양한 PC12 세포에 corticosterone 400 μM 처리한 다음 2시간 후에 추출물을 50 또는 100 μg/mL 농도별로 처리하여 24시간 배양하였다. 양성대조군으로 L-theanine과 fluoxetine 2가지를 사용하였고, L-theanine은 1000 μM, fluoxetine은 10 μM를 처리하였다. 각 well의 세포 배양액을 제거한 다음 PBS로 세척하고, protease inhibitor cocktail (Thermo Fisher Scientific, Waltham, MA, USA)을 넣은 lysis buffer (M-PERTM Mammalian Protein Extraction Reagent)를 사용하여 세포용해하고, 12,000 rpm에서 15분간 원심분리하여 상등액을 얻었다. 수거한 상등액은 BSA (bovine serum albumin)를 사용하여 단백질을 정량하여, 30 μg의 lysate를 5X sample buffer에 넣고 100℃에서 5분간 불활성화 시켰다. 10% SDS-PAGE (Sodium Dodecyl Sulfate-Polyacrylamide Gel Electrophoresis)를 통해 분리한 뒤, 단백질을 PVDF (polyvinylidence difluoride) membrane에 transfer한 후, 5% non-fat dry milk를 함유한 TBST에 상온에서 1시간 shaking한 후 비특이 단백질들에 대한 blocking을 을 실시한 후 TBST로 세척하였다. 준비된 membrane에 1차 항체를 반응시켰다. 1차 항체 반응은 p38, phosphorylation-p38, ERK, phospho-ERK (Cell Signaling Tech, Danvers, MA, USA), phosphorylation-CREB-1,CREB-1, BDNF, α-tublin (Santa Cruz Biotechnology, Califonia, USA)를 이용하여 4℃에서 overnight시킨 다음 TBST로 세척 한 후 1차 항체에 맞는 2차 항체는 HRP (Horse Radish Peroxidase)가 결합된 anti-rabbit IgG, anti-mouse IgG를 상온에서 1시간 동안 반응시켰다. 다시 TBST로 세척하고, ECL (enhanced chemilominescence) western blotting detection reagent (Bio-Rad)로 반응시킨 후 Chemidoc image 분석기(Vilber Fusion FX5, Germany)를 이용하여 특정 단백질의 발현량을 측정하였다. 단백질 밴드의 상대 밀도는 대조군으로 사용한 α-tublin의 발현과 비교하여 분석하였다.
mRNA 발현량 측정 – PC12 세포를 12-well plate에 2 × 105 cells/well의 농도로 분주하여 24시간 동안 배양하였다. 배양한 PC12 세포에 corticosterone 400 μM 처리한 다음 2시간 후에 각 추출물을 50 μg/mL 처리하여 24시간 배양하였다. 양성대조군으로 L-theanine과 fluoxetine 2가지를 사용하였고, theanine은 1000 μM, fluoxetine은 10 μM를 처리하였다. 배양된 세포를 인산염 완충 식염수(PBS)로 세척하고, RiboExreagent (GeneAllBiotechnology, Seoul, Korea)으로 총 RNA를 추출하고, 제조업체의 지침에 따라 역전사효소 키트(Bioneer, 한국)를 사용하여 역전사하였다. 첫 번째 가닥 상보적 DNA (cDNA)를 유전자 특이적 프라이머로 PCR 증폭하였다. 각 주기는 94℃에서 30초 동안 열 변성 단계, 57℃에서 30초 동안 어닐링 단계, 72℃에서 60초 동안 연장 단계로 구성되었다. 증폭된 cDNA 생성물을 ethidium bromide가 함유된 1% 아가로스 겔에서 전기영동하여 Chemidoc imaging System (Fusion FX5, VilberLourmat, France)을 사용하여 정량화하였다. GAPDH mRNA 발현에 대한 mRNA 발현을 분석하였다. 테스트에는 다음 프라이머가 사용되었다: Rat GAPDH forward, 5'-TATCGGACGCCTGGTTAC-3' and reverse, 5'-CTGTGCCGTTGAACTTGC-3'; rat NGF forward, 5'-TCATCCACCCACCCAGTCT-3' and reverse, 5'-CACGCAGGCTGTATCTATC-3'.
ROS 소거능 평가 – PC12 세포를 24-well plate에 1 × 105 cells/well의 농도가 되도록 분주하고 37℃, 5% CO2 Incubator에서 24시간 동안 배양한 후 추출물을 50 μg/mL 처리하고, 양성대조군으로 L-theanine은 1000 μM, fluoxetine은 10 μM를 처리하고 22시간 동안 재배양한 후 2시간 동안 1000 µM H2O2로 노출 시켰다. N-Acetylcysein (NAC, 5 mM)을 positive control로 2시간 동안 배양한 후 2시간 동안 1000 µM H2O2로 노출시켰다. 수거한 PC12 세포는 1X PBS로 washing 하여 Muse® Oxidative Stress Kit (MCH100111, EMD Millipore)로 37℃에서 30분간 배양 후 Guava® Muse® Cell Analyzer 및 Muse_Analysis_V1.9.0.2 소프트웨어(Luminex, Austin, TX, USA)를 이용하여 분석하였다.
세포자멸사 분석 – PC12 세포를 12-well plate에 2 × 105 cells/well의 농도로 분주하여 24시간 동안 배양하였다. 배양한 PC12 세포에 corticosterone 400 μM 처리한 다음 2시간 후에 각 추출물 50 μg/mL, L-theanine 1000 μM, fluoxetine 10 μM 처리하여 24시간 배양하였다. 세포를 수확한 후, 희석 완충액으로 배양배지에 5×105 cells/mL의 농도로 희석하였다. 다음으로, Annexin V/dead reagent 100 μL와 세포 현탁액 100 μL를 실온에서 20분 동안 어두운 곳에서 반응시켰다. 세포자멸사 단계별 세포분포는 Guava® Muse® Cell Analyzer 및 Muse_Analysis_V1.9.0.2 소프트웨어(Luminex, Austin, TX, USA)를 이용하여 분석하였다.
결과 및 고찰
선복화 추출물의 PC12세포 보호할성을 평가하기에 앞서, MTT assay를 통해 추출물의 세포독성 및 무독성 농도범위를 확인하고자 하였다. 건조한 선복화를 각각 열수 또는 50% 에탄올로 추출한 후 각 추출물을 50, 100, 200 μg/mL 농도로 PC12세포에 처리하였다. Fig. 1에서와 같이 200 μg/mL 농도까지 순차적으로 농도를 높여 처리하였을 때 열수 추출물과 주정추출물 모두 유의한 세포독성이 확인되지 않았다. 이러한 결과를 바탕으로, corticoid를 처리하여 독성을 유도한 PC12 세포에서 각 추출물의 보호효과를 측정하였다. 추출물의 우수성을 판단하기 위해 뇌신경세포보호 및 우울증 개선 효과가 확인된 녹차 유래 성분인 L-theanine과,28) 선택적 세로토닌 재흡수 억제제제로 우울증, 강박, 불안증 치료에 사용되는 fluoxetine을 양성대조군으로 사용하였다. Fig. 2에서와 같이 PC12세포에 corticoid 400 μM을 처리했을 때 무처리군 대비 세포생존율이 감소하였고, 선복화 추출물 처리에 의해 유의적으로 회복되는 것을 확인할 수 있다. 열수 추출물에 비해 주정 추출물의 보호효과가 더욱 우수하였고, 특히 선복화 주정 추출물 50 μg/mL 처리군에서 양성대조군에 준하는 우수한 효과가 확인되었다(Fig. 2).
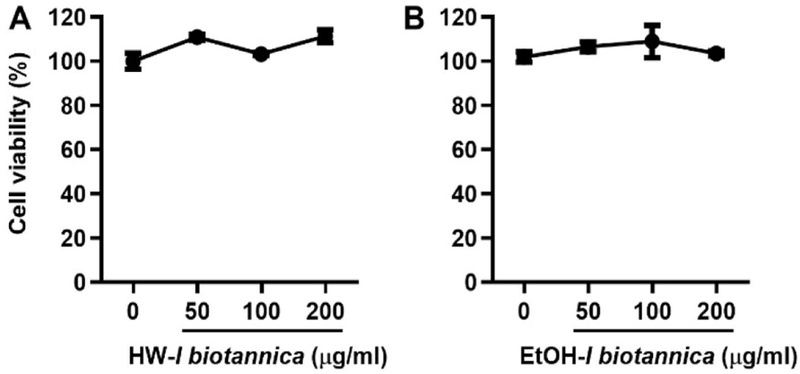
Cytotoxicity of hot water (A) and 50%-ethanolic (B) extracts of Inula britannica flowers in PC12 cells. PC12 cells were treated with various concentrations of the extracts (50, 100, 200 μg/mL) for 24 h. The cell viability was measured using an MTT assay. Results are presented as the mean ± S.D. of triplicate experiments. HW : Hot water.
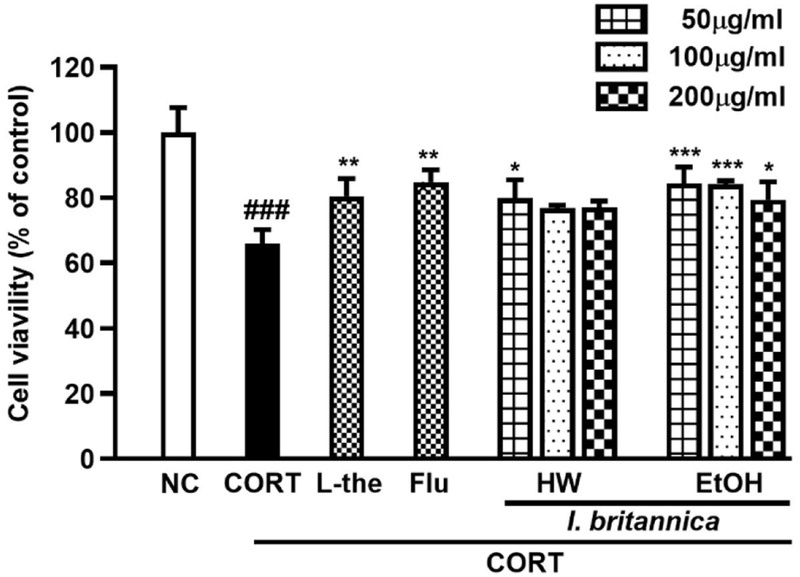
The protective effects of hot water and 50%-ethanolic extracts of Inula britannica flowers in corticosterone induced PC12 cells. PC12 cells were treated with corticosterone (400 μM) for 2 h. The cultures were then treated with various concentrations of Inula britannica extract (50, 100, 200 μg/mL), L-theanine (1000 μM), Fluoxetine (10 μM) for 24 h. The cell viability was measured using an MTT assay. Results are presented as the mean ± S.D. of triplicate experiments; ***p < 0.001 compared to CORT cells. *p < 0.05 and ***p < 0.001 compared to corticosterone induced PC12 cells. NC : non-treated control, L-the: L-theanine, Flu: Fluoxetine, CORT: Corticosterone, HW : Hot water.
PC12 세포를 이용한 다양한 연구보고를 통해 글루코코르티코이드(corticosterone, dexamethasone 등)에의 노출은 신경영양인자 및 전사인자의 발현을 억제하여 신경생존과 신경형성(neurite outgrowth)을 저해한다는 점이 확인되었다. Corticosterone를 처리했을 때 PC12 세포에서 BDNF 전사 및 단백질 수준이 감소되고, 이로 인해 세포생존과 시냅스가소성 관련 신호가 약화되었다.29) 또한 NGF mRNA 수준이 감소하고 NGF-유도 신경분화가 억제된다는 다수의 보고가 있어 NGF 경로의 저하가 스트레스 관련 신경형성 손상의 주요 기전임을 시사하였다.30) 특히 이러한 신경영양인자들의 저하는 주로 cAMP/PKA → CREB 신호의 억제 및 CREB 인산화 감소와 연계되어 있다. 즉, glucocorticoid receptor 매개 신호가 ERK/PKA/AKT 경로와 상호작용하여 CREB 활성을 저해함으로써 BDNF 및 기타 신경영양인자 전사를 억제하는 메커니즘이 보고되었다.31) 천연물 추출물 및 생리활성 물질의 PC12세포 보호효과를 규명한 다양한 연구보고에서도 이러한 주요 지표들의 조절을 통한 PC12 세포의 생존율이 향상되는 효과가 확인되었다.31-34)
본 연구에서는 선복화 추출물이 BDNF와 NGF의 발현, 그리고 CREB의 인산화에 미치는 효과를 western blot analysis과 RT-PCR을 통하여 조사하였다. 그 결과, Fig. 3와 같이 선복화의 열수 및 주정 추출물 처리에 의해 BDNF의 발현이 크게 증가하였고, 그 효과는 양성대조군 대비 월등히 우수하였다. 또한 CREB의 인산화 및 NGF의 발현은 각각 주정추출물 및 열수추출물 처리군에서 유의적인 증가가 확인되었다.
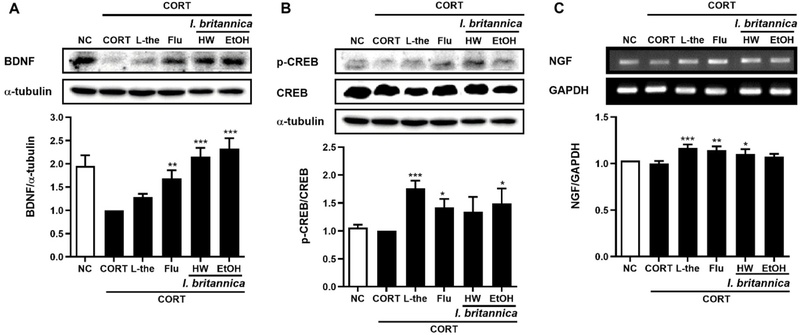
The effects of hot water and 50%-ethanolic extracts of Inula britannica flowers on the expression of BDNF (A), CREB (B) and NGF (C) in corticosterone-induced PC12 cells. PC12 cells were treated with corticosterone (400 μM) for 2 h. The cultures were then treated with Inula britannica (50 μg/mL), L-theanine (1000 μM), Fluoxetine (10 μM) for 24 h. The expression levels of BDNF and p-CREB in cells were analyzed by western blot. The NGF mRNA expression levels were analyzed by RT-PCR and normalized to GAPDH levels. Results are presented as the mean ± standard deviation of triplicate experiments. *p < 0.05, **p < 0.01 and ***p < 0.001 compared to corticosterone-treated cells. NC: non-treated control, CORT : Corticosterone, L-the: L-theanine, Flu: Fluoxetine, BDNF : Brain derived neurophic factor, CREB : cAMP response element binding protein, NGF : Nerve growth factor, HW : Hot water.
PC12세포에 대한 천연물의 보호효과를 보고한 기존 연구에서, CREB의 인산화와 BDNF/NGF 발현을 회복시키는 과정에서 산화∙염증 및 세포사멸(apoptosis)의 표지를 감소시킴으로써 신경세포를 보호함이 보고되었다.31-34) 선복화 추출물의 추가 작용기전을 규명하기 위하여 염증 지표로서 ERK 및 p38의 인산화를 western blot assay를 통해 확인하고, ROS 생성 및 apoptosis 억제 활성을 flow cytometry를 통해 측정하였다. 우선 선복화 추출물이 ERK와 p38 인산화에 미치는 영향을 평가하였고 그 결과를 Fig. 4에 나타내었다. Corticoid 처리에 의해 ERK와 p38의 인산화 레벨이 조금 상승하였으나 통계적으로 유의한 수준은 아니었으며, 양성대조군 중에서 L-theanine 처리에 의한 인산화가 크게 억제된 반면, fluoxetine 처리군에서는 유의적인 변화가 관찰되지 않았다. 선복화 추출물의 경우 ERK의 인산화에는 영향을 미치지 않는 반면, 열수와 주정 추출물 모두 p38의 인산화 억제하는 것으로 확인되었다. 선복화 추출물의 ROS 생성 저해능을 평가하기 위하여 PC12세포에 H2O2 (과산화수소) 처리로 산화적 스트레스를 유발한 후, flow cytometry를 이용하여 ROS+ 및 ROS–cell의 비율을 측정하였다. Fig. 5에서와 같이 H2O2를 처리에 의해 무처리군 대비 PC12 세포 내 ROS–cell의 비율이 유의적으로 감소하였고, 동시에 ROS+ cell의 비율은 유의적으로 증가하여 H2O2에 의한 산화적 스트레스가 유발된 것을 확인할 수 있다. 선복화 추출물 뿐만 아니라 양성대조군으로 사용한 N-Acetylcysein, L-theanine, fluoxetine 처리군에서 모두 H2O2 처리군 대비 ROS–cell의 비율이 증가하고, ROS+ cell의 비율은 감소하는 결과를 확인하였다. 양성대조군 중 N-Acetylcysein가 가장 우수한 ROS 생성 저해효과를 나타내었는데, 선복화의 열수 추출물의 경우 N-Acetylcysein에 준하는 ROS 생성 저해효과가 확인되어, 주정 추출물에 비해 열수 추출물의 항산화력이 더욱 우수하다는 것을 확인하였다. 선복화 추출물의 ROS 생성 억제능을 기반으로, 산화적 스트레스로 인해 촉진된다고 알려진 세포사멸에 보호효과를 평가하였다. Fig. 6과 같이, corticosterone 처리에 의해 PC12 세포 내 total apoptotic cell과 late apoptotic/dead cell의 비율이 무처리군 대비 큰 폭으로 증가하였다. 양성대조군인 L-theanine과 fluoxetine 처리군에서 late apoptotic/dead cell과 early apoptotic cell의 비율이 모두 감소한 반면, 선복화 추출물은 early apoptotic cell의 비율은 유의적인 변화가 관찰되지 않았으나 late apoptotic/dead cell의 비율이 크게 감소하였다. ROS 생성 억제능과 마찬가지로, 주정 추출물에 비해 열수추출물의 세포사멸 억제활성이 더욱 우수하였다. 이러한 결과는 선복화 추출물이 ROS 생성의 직접적인 저해뿐만 아니라 corticoid에 의해 유도된 산화적 스트레스 조건에서 신경세포의 세포사멸까지 효과적으로 보호하는 것을 시사한다.
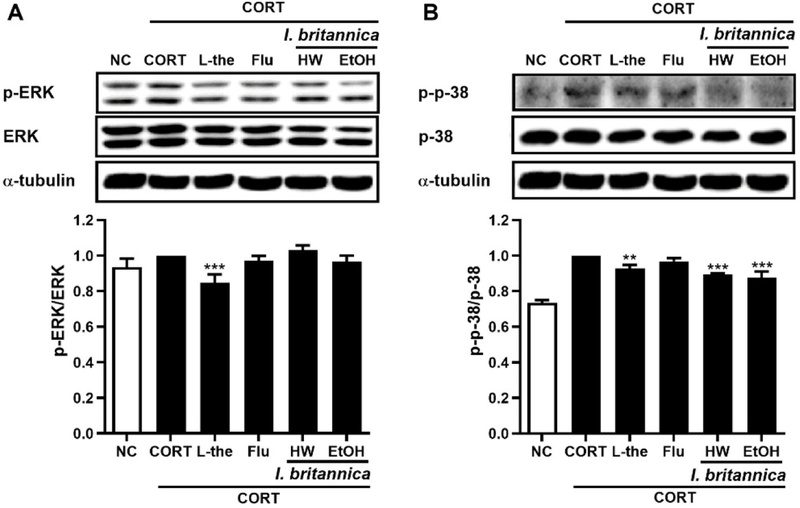
The effects of hot water and 50%-ethanolic extracts of Inula britannica flowers on the expression of p-ERK (A), p-p-38 (B) in corticosterone-induced PC12 cells. PC12 cells were treated with corticosterone (400 μM) for 2 h. The cultures were then treated with Inula britannica (100 μg/mL), L-theanine (1000 μM), Fluoxetine (10 μM) for 24 h. The expression levels of p-ERK (A), p-p-38 (B) in cells were analyzed by western blot. Results are presented as the mean ± standard deviation of triplicate experiments. **p < 0.01 and ***p < 0.001 compared to corticosterone-treated cells. NC: non-treated control, CORT : Corticosterone, L-the: L-theanine, Flu: Fluoxetine, HW : Hot water.
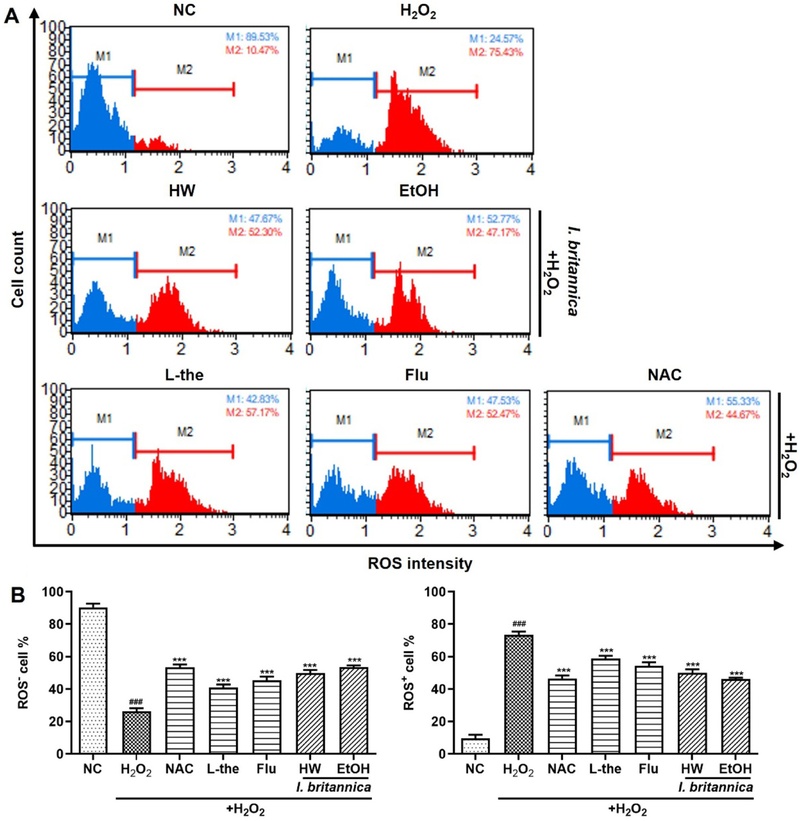
The effects of hot water and 50%-ethanolic extracts of Inula britannica flowers on H2O2-induced oxidative stress in PC12 cells. PC12 cells were seeded at a density of 1 × 105 cells/well and then stimulated with the 100 µg/mL under hot water and 50%-ethanolic of Inula britannica extracts for 22 h prior to treatment with 1000 µM H2O2 for 2 h. N-Acetylcysein (NAC, 5 mM) was used as the positive control. (A) Intracellular ROS generation was measured by flow cytometry using a Muse® Oxidative Stress Kit. Mean percentages of ROS− (M1; blue) and ROS+ (M2; red) populations are shown. (B) Percentage of ROS negative (ROS−) and ROS positive (ROS+) values observed for each treatment. Results are presented as the mean ± standard deviation from three independent experiments. ###p < 0.001 vs. the non-treated control (NC) ***p < 0.001 vs. H2O2 only–treated group.
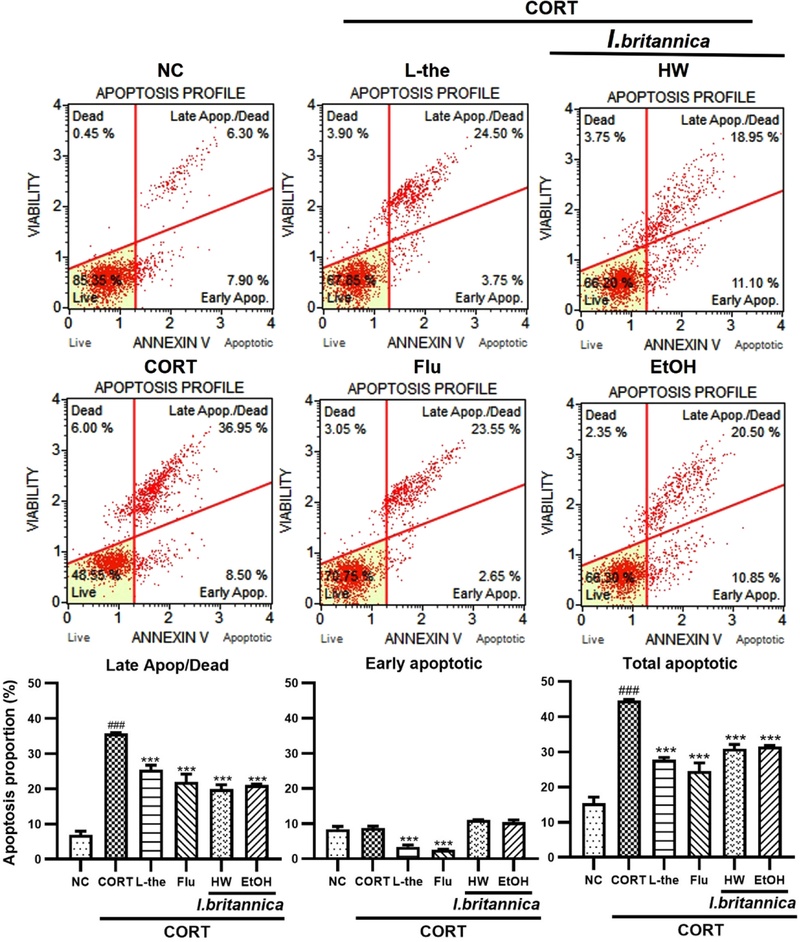
The effects of hot water and 50%-ethanolic extracts of Inula britannica flowers on the apoptosis in corticosterone-induced PC12 cells. PC12 cells were treated with corticosterone (400 μM) for 2 h. The cultures were then treated with Inula britannica (50 μg/mL), L-theanine (1000 μM), Fluoxetine (10 μM) for 24 h. The percentage of apoptotic cells was measured using Muse Annexin V and Dead Cell kit. Results are presented as the mean ± standard deviation of triplicate experiments. ###p < 0.001, vs. NC; ***p < 0.001, vs. CORT-treated cells. NC: non-treated control, CORT : Corticosterone, L-the: L-theanine, Flu: Fluoxetine, HW : Hot water.
결 론
현대 사회에서 스트레스로 인해 불안, 수면장애, 우울 등 다양한 정신생리적 이상이 유발됨에 따라 스트레스 완화 및 정서 안정에 도움을 주는 소재에 대한 수요가 지속적으로 증가하고 있다. 이러한 시장의 수요를 바탕으로 천연물로부터 스트레스 저감 및 이를 통한 뇌신경세포보호 효과가 우수한 신규 소재 발굴을 위하여 corticosterone을 처리한 PC12세포를 검색계로 하여 본 연구를 수행하였다. 그 결과, 선복화의 열수 및 주정 추출물은 corticoid 처리에 의한 독성에 대하여 PC12 세포를 보호하는 효과가 우수함이 확인되었다. 선복화 추출물은 CREB 인산화와 BDNF/NGF 발현을 회복시키고, ROS 생성억제, 염증지표 완화 및 세포사멸 표지를 감소시켰고 이를 통해 신경보호 작용을 나타내었다. 특히 선복화 추출물 처리에 의한 BDNF 발현 증가는 양성대조군인 L-theanine 및 fluoxetine 대비 월등히 우수하였다. 본 연구를 통해 선복화 추출물을 스트레스 저감 및 뇌신경세포 보호 소재로의 개발 가능성을 확인하였고, 추가적으로 유효성분과 작용기전에 대한 추가연구가 필요하다.
Acknowledgments
이 논문은 농촌진흥청 연구사업(과제번호: RS-2023-0023-1446)의 지원과 2025년도 경상국립대학교 연구년제 연구교수 연구지원비에 의하여 수행되었음.
References
- 배기환 (2019) 천연약물도감 I-II, 교학사, 한국.
-
Seca, A. M., Grigore, A., Pinto, D. C. and Silva, A. M. (2014) The genus Inula and their metabolites: From ethnopharmacological to medicinal uses. J. Ethnopharmacol. 154: 286-310.
[https://doi.org/10.1016/j.jep.2014.04.010]

- Editorial Committee of Chinese Pharmacopoeia (2010) Pharmacopoeia of the People's Republic of China, Volumes I-III. Shanghai People's Medical Publishing House, Shanghai.
-
Kim, Y. S., Lee, J. H., Song, J. and Kim, H. (2020) Gastroprotective effects of Inulae Flos on HCl/ethanol-induced gastric ulcers in rats. Molecules 25: 5623.
[https://doi.org/10.3390/molecules25235623]

-
Yu, H. S., Kim, W. J., Bae, W. Y., Lee, N. K. and Paik, H. D. (2020) Inula britannica inhibits adipogenesis of 3T3-L1 preadipocytes via modulation of mitotic clonal expansion involving ERK1/2 and Akt signaling pathways. Nutrients 12: 3037.
[https://doi.org/10.3390/nu12103037]

-
Yoon, H. J., Park, J. Y., Min, S. J., Lee, E. S., Lee, N. K. and Paik, H. D. (2025) Inula britannica exerts antioxidant and anti-inflammatory effects in SH-SY5Y cells through the Nrf2-Keap1 signaling pathway. Arch. Biochem. Biophys. 773: 110597.
[https://doi.org/10.1016/j.abb.2025.110597]

-
Tang, J. J., Guo, C., Peng, X. N., Guo, X. C., Zhang, Q., Tian, J. M. and Gao, J. M. (2021) Chemical characterization and multifunctional neuroprotective effects of sesquiterpenoid-enriched Inula britannica flowers extract. Bioorg. Chem. 116: 105389.
[https://doi.org/10.1016/j.bioorg.2021.105389]

-
Park, E. J. and Kim, J. (1998) Cytotoxic sesquiterpene lactones from Inula britannica. Planta Med. 64: 752-754.
[https://doi.org/10.1055/s-2006-957573]

-
Tang, S. A., Zhu, H., Qin, N., Zhou, J. Y., Lee, E., Kong, D. X., Jin, M. H. and Duan, H. Q. (2014) Anti-inflammatory terpenes from flowers of Inula japonica. Planta Med. 80: 583-589.
[https://doi.org/10.1055/s-0034-1368353]

-
Bai, N., Lai, C. S., He, K., Zhou, Z., Zhang, L., Quan, Z., Zhu, N., Zheng, Q. Y., Pan, M. H. and Ho, C. T. (2006) Sesquiterpene lactones from Inula britannica and their cytotoxic and apoptotic effects on human cancer cell lines. J. Nat. Prod. 69: 531-535.
[https://doi.org/10.1021/np050437q]

-
Park, E. J. and Kim, J. (1998) Cytotoxic sesquiterpene lactones from Inula britannica. Planta Med. 64: 752-754.
[https://doi.org/10.1055/s-2006-957573]

-
Park, E. J., Kim, Y. and Kim, J. (2000) Acylated flavonol glycosides from the flower of Inula britannica. J. Nat. Prod. 63: 34-36.
[https://doi.org/10.1021/np990271r]

-
Yang, J. L., Wang, R., Liu, L. L. and Shi, Y. P. (2011) Sesquiterpenoids from Inula britannica. Planta Med. 77: 362-367.
[https://doi.org/10.1055/s-0030-1250345]

-
Kim, K. C., Kim, D. J., Lee, M. S., Seo, J. Y., Yoo, I. D. and Lee, I. S. (2018) Inhibition of human neutrophil elastase by sesquiterpene lactone dimers from the flowers of Inula britannica. J. Microbiol. Biotechnol. 28: 1806-1813.
[https://doi.org/10.4014/jmb.1807.07039]

-
Zhang, J, Yan, J., Dong, H. J., Zhang, R., Chang, J., Feng, Y., Xu, X., Li, W., Qiu, F. and Chengpeng, S. (2025) Dimeric sesquiterpenoids with anti-inflammatory activities from Inula britannica. Chin. J. Nat. Med. 23: 961-971.
[https://doi.org/10.1016/S1875-5364(25)60931-9]

-
Qi, R. T., Guo, C., Peng, X. N. and Tang, J. J. (2022) Sesquiterpenoids from Inula britannica and their potential effects against triple-negative breast cancer cells. Molecules 27: 5230.
[https://doi.org/10.3390/molecules27165230]

-
Kim, J. H., Park, Y. I., Hur, M., Park, W. T., Moon, Y. H., Koo, S. C., Her, Y. C., Lee, I. S. and Park, J. S. (2022) The inhibitory activity of methoxyl flavonoids derived from Inula britannica flowers on SARS-CoV-2 3CLpro. Int. J. Biol. Macromol. 222: 2098-2104.
[https://doi.org/10.1016/j.ijbiomac.2022.10.008]

-
Tang, X. P., Guo, X. H., Geng, D. and Weng, L. J. (2019) d-Limonene protects PC12 cells against corticosterone-induced neurotoxicity by activating the AMPK pathway. Environ. Toxicol. Pharmacol. 70: 103192
[https://doi.org/10.1016/j.etap.2019.05.001]

-
Ma, R. D., Zhou, G. J., Qu, M., Yi, J. H., Tang, Y. L., Yang, X. Y., Nie, Y. X. and Gu, H. F. (2019) Corticosterone induces neurotoxicity in PC12 cells via disrupting autophagy flux mediated by AMPK/mTOR signaling. CNS Neurosci. Ther. 26: 167-176.
[https://doi.org/10.1111/cns.13212]

-
Mao, Q. Q., Zhong, X. M., Qiu, F. M., Li, Z. Y. and Huang, Z. (2012) Protective effects of paeoniflorin against corticosterone-induced neurotoxicity in PC12 cells. J. Ethnopharmacol. 135: 688-694.
[https://doi.org/10.1002/ptr.3673]

-
Zhou, Y., Li, X., Gong, W., Tian, J., Gao, X., Gao, L., Zhang, X., Du, G. and Qin, X. (2017) Protective effect of isoliquiritin against corticosterone-induced neurotoxicity in PC12 cells. Food Funct. 8: 1235-1244.
[https://doi.org/10.1039/C6FO01503D]

-
Zhang, Y., He, Y., Deng, N., Chen, Y., Huang, J. and Xie, W. (2019) Protective effect of resveratrol against corticosterone-induced neurotoxicity in PC12 cells. Transl. Neurosci. 10: 1-9.
[https://doi.org/10.1515/tnsci-2019-0038]

-
Peng, S., Hou, Y., Yao, J. and Fang, J. (2019) Activation of Nrf2 by costunolide provides neuroprotective effect in PC12 cells. Food Funct. 10: 4143-4152.
[https://doi.org/10.1039/C8FO02249F]

- Kim, S. H., Lee, D. H. and Kang, J. S. (2021) Natural products for stress-related disorders: neuroprotective potential and mechanisms. Arch. Pharm. Res. 44: 589-603.
- Park, J. H., Lee, M. J. and Kim, Y. S. (2023) Neuroprotective effects of flavonoids on corticosterone-induced stress in PC12 cells. Phytother. Res. 37: 1235-1245.
- 식품의약품안전처 (2023) 건강기능식품 개별인정 가이드라인, 식품의약품안전처, 한국.
-
Nga, N. T. H., Ngoc, T. T. B., Trinh, N. T. M., Thuoc, T. L. and Thao, D. T. P. (2020) Optimization and application of MTT assay in determining density of suspension cells. Anal. Biochem. 610: 113937.
[https://doi.org/10.1016/j.ab.2020.113937]

-
Xie, X., Wan, J., Zheng, X., Pan, W., Yuan, J., Hu, B., Feng, M., Liu, Z. and Cai, S. (2022) Synergistic effects of epigallocatechin gallate and L-theanine in nerve repair and regeneration by anti-amyloid damage, promoting metabolism, and nourishing nerve cells. Front. Nutr. 9: 951415.
[https://doi.org/10.3389/fnut.2022.951415]

-
Colucci-D’Amato, L., Speranza, L. and Volpicelli, F. (2020). Neurotrophic factor BDNF: physiological functions and therapeutic potential in neurodegenerative diseases.
[https://doi.org/10.3390/ijms21207777]

-
Terada, K., Kojima, Y., Watanabe, T., Izumo, N., Chiba, K. and Karube, Y. (2014) Inhibition of nerve growth factor-Induced neurite outgrowth from PC12 cells by dexamethasone: signaling pathways through the glucocorticoid receptor and phosphorylated Akt and ERK1/2. PLoS ONE 9: e93223.
[https://doi.org/10.1371/journal.pone.0093223]

-
He, D., Wang, N., Sai, X., Li, X. and Xu, Y. (2019). Camellia euphlebia protects against corticosterone-induced apoptosis in differentiated PC12 cells by regulating the mitochondrial apoptotic pathway and PKA/CREB/BDNF signaling pathway. Food Chem. Toxicol. 126: 211-222.
[https://doi.org/10.1016/j.fct.2019.02.028]

-
Mao, Q. Q., Zhong, X. M., Qiu, F. M., Li, Z. Y. and Huang, Z. (2011) Protective effects of paeoniflorin against corticosterone-induced neurotoxicity in PC12 cells. J. Ethnopharmacol. 135: 688-694.
[https://doi.org/10.1002/ptr.3673]

-
Gao, S., Li, W., Zou, W., Zhang, P., Tian, Y., Xiao, F., Gu, H. F. and Tang, X. (2015) H₂S protects PC12 cells against toxicity of corticosterone by modulation BDNF-TrkB pathway. Acta Biochim. Biophys. Sin. 47: 915-924.
[https://doi.org/10.1093/abbs/gmv098]

-
Chang, P. R., Liou, J. W., Chen, P. Y., Gao, W. Y., Wu, C. L., Wu, M. J. and Yen, J. H. (2023) The neuroprotective effects of flavonoid fisetin against corticosterone-induced cell death through modulation of ERK, p38, and PI3K/Akt/FOXO3a-dependent pathways in PC12 cells. Pharmaceutic. 15: 2376.
[https://doi.org/10.3390/pharmaceutics15102376]
