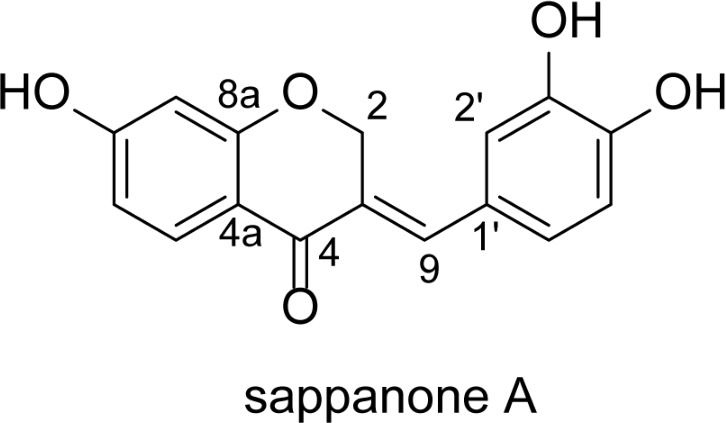
HPLC를 이용한 소목의 Sappanon A 분석법 확립
Abstract
In this experiment, we developed and validated the HPLC method for quantifying sappanone A from the heartwood of Caesalpinia sappan L. (Leguminosae). The extraction procedure based on sonication was established and the analysis method was optimized using a C18 column. Method validation was conducted in accordance with the KFDA validation guideline, evaluating linearity, accuracy, precision, repeatability, and limit of quantitation. All tested analytical parameters were within acceptable range, indicated that the developed HPLC method is reliable for the quantitative analysis of sappanone A of C. sappan heartwood.
Keywords:
Caesalpinia sappan L., Leguminosae, Sappanone A, HPLC method validation소목(Caesalpinia sappan L.)은 콩과(Leguminosae)에 속하는 상록 소교목으로, 주로 동남아시아 지역에 자생하며 우리나라에서는 한약재로 널리 사용되어 왔다. 전통적으로 소목의 심재는 어혈을 제거하고 혈액순환을 촉진하는 효능이 있어 한방에서 활혈(活血) 및 진통 등에 사용되었고, 항염, 항인플루엔자, 항알러지, 뇌신경보호효과 등이 보고되어 있다.2-4) 소목의 에탄올 추출물은 Streptococcus mutans에 항균 작용,5) 항염증과 상처치유작용,6) 위장보호효과 7) 등이 알려져 있고, 물 추출물은 항알러지성 비염효과가 8) 보고되어 있다. 소목의 성분으로 terpenoids, flavonoids, quinones, phenols, steroids, alkaloids 등이 알려져 있고,9) 소목은 페놀성 화합물이 주요 성분으로 보고되어 있으며 구조적으로 페놀릭 화합물은 brazilin 등의 homoisoflavonoid와 chalcone, protosappanin으로 나눈다.10) 분리된 화합물 중 brazilin은 항산화, 항염증, 항피부노화, 혈당상승, 혈관완화, 간보호, 피부보호, 항균작용 등이 알려져 있고,11,12) 소목의 chalcone류가 RAW264.7 cell의 LPS로 유도한 염증성 cytokine의 생성을 억제하였으며,13) 3-deoxysappanchalcone은 AKT/mTOR 경로로 oxygenase-1을 활성화하여 항염증효과가 알려져 있다.14) 소목의 성분들은 항산화, 항염증, 항균 및 항암작용 등 다양한 약리 활성을 나타내는 것으로 보고되어 있다.15)
Sappanone A는 소목 심재로부터 분리된 천연 homoisoflavanone 화합물로, 최근 다양한 질환 모델에서 항염증 및 항산화 작용이 보고되면서 생리활성 천연물로 주목받고 있다. Sappanone A는 인산디에스테라제-4 (PDE4) 및 NF-κB 신호 경로를 억제하고, Nrf2 경로를 활성화함으로써 세포 내 염증반응과 산화 스트레스를 완화하는 것으로 알려져 있다.16) Sappanone A 파골세포 분화를 억제하고 뼈 손실을 완화하는 효과가 확인되어, 염증성 질환 및 대사성 골질환의 치료 소재로서 잠재적 활용 가능성이 제시되고 있다.17)
최근 천연물 유래 기능성 소재를 건강기능식품 또는 의약품 원료로 개발하기 위한 연구가 활발히 진행되고 있으며, 이 과정에서 원료의 품질을 일관되게 평가할 수 있는 지표성분 (marker compound) 기반의 분석법 확립이 필수적이다. 그러나 현재까지 sappanone A에 대한 정량분석법은 주로 연구 목적에 따라 다양하게 보고되어 있어, 실질적인 품질 관리에 적용 가능한 표준화된 분석법은 확립되어 있지 않다. 특히, 각 연구에서 사용된 분석조건이나 밸리데이션 항목이 국제 가이드라인(ICH Q2(R1) 또는 식품의약품안전처고시 기준에 부합하지 않는 경우가 많아, 연구 결과의 신뢰성과 상호 비교 가능성에 한계가 존재한다.18)
이에 본 연구에서는 소목 화합물 중 주요 생리활성 성분인 sappanone A를 지표성분으로 설정하여, 식품의약품안전처(MFDS) 가이드라인에 준거한 HPLC 분석법을 확립하고 그 타당성을 검증하였다. 본 연구 결과는 향후 소목 유래 기능성 소재의 품질관리 및 건강기능식품 원료 개발 시 신뢰할 수 있는 시험법으로 활용될 수 있을 것으로 기대된다.
재료 및 방법
실험재료 – HPLC 밸리데이션 시험에 사용한 소목은 대구광역시 약령시에서 구입하여 사용하였다. 지표성분인 sappanone A 표준품은 소목에서 분리하여 사용하였다.10)
Sappanone A – 무정형 노란색 분말; C16H12O5; 1H NMR (400 MHz, CD3OD): δH 7.78 (1H, d, J=8.4 Hz, H-5), 7.64 (1H, brs, H-9), 6.86 (1H, d, J=8.4 Hz, H-5′), 6.82 (1H, d, J=2.0 Hz, H-2′), 6.76 (1H, dd, J=8.4, 2.0 Hz, H-6′), 6.52 (1H, dd, J=8.4, 2.0 Hz, H-6), 6.31 (1H, d, J=2.0 Hz, H-8), 5.34 (2H, d, J=1.6 Hz, H-2); 13C NMR (100 MHz, CD3OD): 183.1 (C-4),166.7 (C-7), 164.9 (C-8a), 148.8 (C-3′), 146.7 (C-4′), 138.6 (C-9), 130.8 (C-5), 129.6 (C-1′), 127.8 (C-3), 124.7 (C-6′), 118.5 (C-5′), 116.7 (C-2′), 116.0 (C-4a), 111.3 (C-6), 103.7 (C-8), 69.2 (C-2).
시약 및 기기 – HPLC system은 Waters사 binary pump controller Waters 1525, 717 auto-sampler, dual wavelength absorbance detector Waters 2487를 사용하였고, column은 CAPCELL PAK C18 (4.6 × 150 mm, 5 μm)를 사용하였다. 사용한 물은 Milli-Q로 처리한 물을 사용하였다.
표준용액의 조제 – Sappanone A 표준물질 약 10 mg을 정밀히 달아 50% 메탄올 10 mL에 녹여 농도가 1.0 mg/mL인 표준원액으로 하였으며, 밸리데이션 시험법 항목에 맞게 위 용액을 50% 메탄올로 적절히 희석하여 표준용액을 조제하였다.
시험용액의 조제 – 소목 분말 20 g을 취하여 50% 메탄올 100 mL을 가한 후 2시간 초음파 추출한 후 용액을 다시 50% 메탄올을 이용하여 희석하여 밸리데이션 시험법 항목에 적용하는 시험용액으로 하였다. 함량 측정용 시료는 10 g 소목 분말에 50% 메탄올 50 mL을 가한 후 2시간씩 2번 초음파 추출하여 100 mL로 만든 후 분석하였다.
HPLC 분석조건 – 이동상은 아세토니트릴과 H2O (0.1% TFA)를 사용하였고, 아세토니트릴 10→45% (60 min)의 농도로 조절하면서 분석하였다. 검출파장은 254 nm이며, 유속은 1.0 mL/min이었다. HPLC는 25℃를 유지하면서 분석하였다.
직선성 평가 – 1.0 mg/mL 농도의 sappanone A 표준원액을 50% 메탄올을 첨가하여 순차적으로 희석하여 1, 5, 20, 50, 100, 200 μg/mL의 총 6개 농도로 조제하였다. HPLC를 이용하여 측정 후 검량선을 구하였다.
정량한계 측정 – Sappanone A 표준원액을 50% 메탄올을 첨가하여 정량한계 측정농도와 같이 총 6개 농도로 조제하고, HPLC를 이용하여 측정하였으며 정량한계를 측정하였다. 상기 과정을 총 5회 반복하였으며 정량한계는 검량선 기울기 평균 (S) 및 y 절편의 표준편차(G)를 이용하여 계산하였다.
특이성(specificity) 평가 – 설정한 분석법으로 sappanone A를 첨가한 소목 추출용액의 HPLC 분석을 통해 sappanone A 피크 및 인근 물질 피크의 머무름 시간의 비교를 통해 시험법의 특이성을 판단하였다.
정확도(accuracy) 평가 – 3개 농도의 표준용액과 소목 추출물로 일정량 조제하고, 각 시험용액 농도 당 3회 반복 분석하여 판단하였다.
일내 정밀도(precision) 평가 – 일내 정밀도 시험은 3개 농도의 표준용액과 소목 추출물로 조제하고, 각 시험용액 농도 당 3회 반복 측정하였으며 상대 표준편차로 기준에 적합한지 평가하였다.
일간 정밀도(precision) 평가 – 일간 정밀도 시험은 3개 농도의 표준용액 조제와 소목 추출물로 조제하고, 각 시험용액 농도 당 3회 반복 측정하였으며 이 과정을 3일 반복 수행하였다.
추출 방법 검토 – 소목의 최적 추출 방법을 찾기 위하여 열수추출과 초음파추출 방법을 비교를 위해 시료 10 g과 50% 메탄올 50 mL을 사용하여 함량 비교를 하였고, 또한 추출 횟수, 추출 시간에 변수를 두어 최적의 추출방법을 검토하였다.
결과 및 고찰
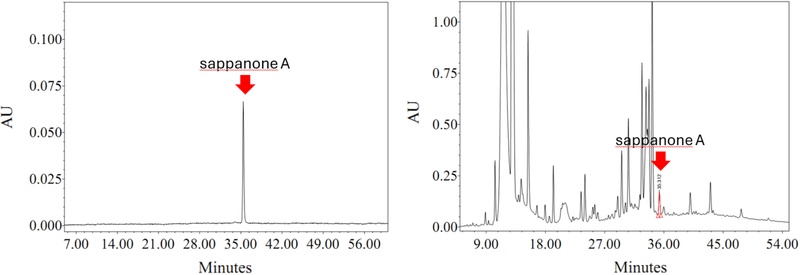
분석조건 설정 – 소목의 주요성분 sappanone A의 분석법을 확립하고자 유기용매와 산 조건을 변화하면서 분석조건을 검토하였다. Column은 CAPCELL PAK C18 (4.6×150 mm, 5 μm)을 이동상은 아세토니트릴과 H2O (0.1% TFA)를 이용하여 아세토니트릴 10→45% (60 min) 농도 변화와 UV 254 nm의 검출파장으로 설정하였다. 설정한 HPLC조건으로 분석한 결과 sappanone A는 35 분대의 머무름 시간으로 다른 피크와 겹치지 않아 소목의 sappanone A 분석방법으로 가능함을 확인하였다(Fig. 2).
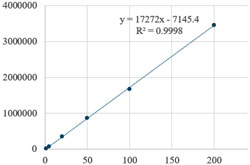
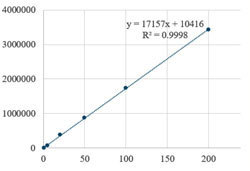
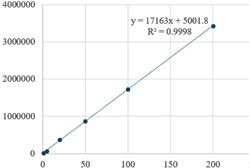
직선성 평가 – 표준용액을 6개 농도로 지정하여 1-200 μg/mL 범위에서 직선성을 확인하였다. 시험 시 발생할 수 있는 오차범위를 확인하기 위해 5회 반복 측정하였고 3개의 시험 모두 검량선의 상관계수(r2) 값이 0.9998로 6개의 농도범위에서 매우 우수한 직선성을 나타내었다(Table I).
정량한계 측정 – 6개 농도(1-200 mg/mL)로 희석한 표준용액을 5회 분석한 후, 검량선의 기울기와 y 절편 값을 이용하여 정량한계를 구하였다. 기울기 평균은 17197이며 y 절편의 표준편차는 2757로 이를 통해 정량한계는 0.038 μg/mL로 계산하였다(Table I).
특이성 평가 – HPLC 크로마토그램의 비교를 통해 sappanone A의 HPLC 분석조건에서 간섭물질의 영향이 없음을 확인하였고, sappanone A 표준용액과 소목 추출물 시험용액의 sappanone A 성분에 대한 머무름 시간 및 UV 스펙트럼이 일치함을 확인하였다.
정확도 평가 – 정확도 평가를 위하여 표준물질 첨가법을 이용하여 회수율로 확인하였고, 시료에 존재하는 참값과 가까운 농도를 시료에 추가하여 회수율을 측정하였다. 1.0, 5.0, 10.0 μg 농도의 sappanone A를 첨가하여 정확도 시험을 수행하였다. 시험결과 전체 회수율 평균은 99.63%였고, 회수율 구간은 96.90-100.36%이었다. 이는 식품의약품안전처 건강기능식품 지표물질 밸리데이션 가이드라인의 회수율시험 기준인 지표물질 0.1-1% 농도에 해당하는 회수율기준(90-108%)에 부합되는 결과이며, 따라서 본 시험법의 정확성을 확인하였다(Table II).
일내정밀도(반복성) 평가 – 표준물질 첨가법을 이용하여 회수율을 확인하였고, 시료에 존재하는 참값과 가까운 농도를 시료에 추가하여 농도 값을 측정하였다. 1.0, 5.0, 10.0 μg 농도의 sappanone A를 첨가하여 3회씩 반복 측정하였으며 상대표준편차(RSD)는 0.48-2.85%로, 이는 식품의약품안전처 건강기능식품 지표물질 밸리데이션 가이드라인에 부합하여 본 시험법의 일내정밀성이 있음을 확인하였다(Table III).
일간정밀도(재현성) 평가 – 실험일 간 반복정밀도를 확인하기 위해 표준물질 첨가법을 이용하여 회수율을 확인하였고, 시료에 존재하는 참값과 가까운 농도를 시료에 추가하여 농도 값을 측정하였다. 1.0, 5.0, 10.0 μg 농도의 sappanone A를 첨가하여 3회씩 반복 측정하였으며, 상대표준편차(RSD)는 1.95-3.19%로 이는 식품의약품안전처 건강기능식품 지표물질 밸리데이션 가이드라인에 부합하여 본 시험법의 일간 정밀성이 있음을 확인하였다(Table III).
추출방법 평가 – 소목에서 sappanone A 추출방법을 찾기 위하여 열수추출과 초음파추출 방법을 비교한 결과(열수추출물: 0.030 mg/g; 초음파추출물: 0.029 mg/g) 추출방법에는 차이가 적어 편리성이 높은 초음파추출 방법이 효과적으로 확인되었다. 추출 시간은 2 시간이 효과적이고, 횟수는 1에서 3회까지 차이가 없어 2회로 설정하였다(Table IV).
소목의 sappanone A 함량 측정 – 대구 약령시 4곳의 한약약업사에서 소목을 구입하여 상기의 HPLC 분석방법으로 sappanone A 함량을 측정하였다. 4종의 시료의 sappanone A 함량은 0.0251-0.0290 mg/g으로 일정한 함량으로 측정되어 설정한 실험법으로 분석이 가능함을 확인하였다.
결 론
소목의 주요성분 sappanone A의 함량측정을 위해 HPLC 분석법을 설정하였다. HPLC 분석법의 밸리데이션은 식품의약품안전처 고시에 따라 특이성, 정확도, 정밀도, 정량한계, 직선성 등을 평가하여 가이드라인에 부합함을 확인하였다.19) 이에 본 HPLC 분석법이 신뢰성이 있음을 검증하였으며 본 HPLC 분석법은 소목의 sappanone A의 분석을 수행하는 천연물 연구자들에게 참고가 될 것으로 사료된다.
Acknowledgments
본 연구는 2025년도 경상북도 RISE사업 연구개발비 지원에 의해 수행되었으며 이에 감사드립니다(2025-RISE-15-107).
References
- 배기환(2019) 천연약물도감, p 539 (I). 교학사, 서울.
-
Liu, A. L., Shu, S. H., Qin, H. L., Lee, S. M.; Wang, Y. T. and Du, G. H. (2009) In vitro anti-influenza viral activities of constituents from Caesalpinia sappan. Planta Medica 75: 337-339.
[https://doi.org/10.1055/s-0028-1112208]

-
Yodsaoue, O., Cheenpracha, S., Karalai, C., Ponglimanont, C. and Tewtrakul, S. (2009) Anti‐allergic activity of principles from the roots and heartwood of Caesalpinia sappan on antigen‐induced β‐hexosaminidase release. Phytotherapy Research 23: 1028-1031.
[https://doi.org/10.1002/ptr.2670]

-
Shen, J., Zhang, H., Lin, H., Su, H., Xing, D. and Du, L. (2007) Brazilein protects the brain against focal cerebral ischemia reperfusion injury correlating to inflammatory response suppression. European Journal of Pharmacology 558: 88-95.
[https://doi.org/10.1016/j.ejphar.2006.11.059]

-
Puttipan, R., Chansakaow, S., Khongkhunthian, S. and Okonogi, S. (2018) Caesalpinia sappan: A promising natural source of antimicrobial agent for inhibition of cariogenic bacteria. Drug Discoveries & Therapeutics 12: 197-205.
[https://doi.org/10.5582/ddt.2018.01035]

-
Tewtrakul, S., Tungcharoen, P., Sudsai, T., Karalai, C., Ponglimanont, C. and Yodsaoue, O. (2015) Antiinflammatory and wound healing effects of Caesalpinia sappan L. Phytotherapy Research 29: 850-856.
[https://doi.org/10.1002/ptr.5321]

-
Chellappan, D. R., Purushothaman, A. K. and Brindha, P. (2017) Gastroprotective potential of hydro-alcoholic extract of Pattanga (Caesalpinia sappan Linn.). Journal of Ethnopharmacology 197: 294-305.
[https://doi.org/10.1016/j.jep.2016.07.081]

-
Pyun, B. J., Jo, K, Lee, J. Y, Lee, A., Jung, M. A., Hwang, Y. H., Jung, D. H., Ji, K. Y., Choi, S., Kim, Y. H. and Kim, T. (2022) Caesalpinia sappan Linn. ameliorates allergic nasal inflammation by upregulating the Keap1/Nrf2/HO-1 pathway in an allergic rhinitis mouse model and nasal epithelial cells. Antioxidants (Basel) 11: 2256.
[https://doi.org/10.3390/antiox11112256]

-
Sun, Q., Wang, Q., Zhu, Y., Mao, M., Liao, R., Yan, X., Zhu, B. and Qin, L. (2025) Traditional uses and phytochemical and pharmacological analyses of Caesalpinia sappan Linn. Chemistry & Biodiversity 22: e202402681.
[https://doi.org/10.1002/cbdv.202402681]

-
Cuong, T. D., Tran, M. H., Kim, J. C., Kim, E. H., Woo, M. H., Choi, J. S., Lee, J. H. and Min, B. S. Phenolic compounds from Caesalpinia sappan Heartwood and their anti-inflammatory activity. Journal of Natural Products 75: 2069-2075.
[https://doi.org/10.1021/np3003673]

-
Nirmal, N. P., Rajput, M. S., Prasad, R. G. and Ahmad, M. (2015) Brazilin from Caesalpinia sappan heartwood and its pharmacological activities: A review. Asian Pacific Journal of Tropical Medicine 8: 421-430.
[https://doi.org/10.1016/j.apjtm.2015.05.014]

-
Park, J. I., Kim, S. J., Kim, Y. J. and Lee, S. J. (2022) Protective role of Caesalpinia sappan extract and its main component brazilin against blue light-induced damage in human fibroblasts. Journal of Cosmet. Dermatology 21: 7025-7034.
[https://doi.org/10.1111/jocd.15354]

-
Min, B. S., To, D. C., Tran, M. H., Min, B. K., Shin, B. S. and Woo, M. H. (2012) Compounds from the heartwood of Caesalpinia sappan and their anti-inflammatory activity. Bioorganic & Medicinal Chemistry Letters 22: 7436-7439.
[https://doi.org/10.1016/j.bmcl.2012.10.055]

-
Kim, J.-H., Choo, Y.-Y., Tae, N., Min, B. S. and Lee, J.-H. (2014) The anti-inflammatory effect of 3-deoxysappanchalcone is mediated by inducing heme oxygenase-1 via activating the AKT/mTOR pathway in murine macrophages. International Immunopharmacology 22: 420-6.
[https://doi.org/10.1016/j.intimp.2014.07.025]

-
Vij, T., Anil, P. P., Shams, R., Dash, K. K., Kalsi, R., Pandey, V. K., Harsányi, E., Kovács, B. and Shaikh, A. M. (2023) A comprehensive review on bioactive compounds found in Caesalpinia sappan. Molecules 28: 6247.
[https://doi.org/10.3390/molecules28176247]

-
Lee, S., Choi, S.-Y., Choo, Y.-Y., Kim, O., Tran, P. T., To, D. C., Min, B. S. and Lee, J.-H. (2015) Sappanone A exhibits anti-inflammatory effects via modulation of Nrf2 and NF-κB. International Immunopharmacology 28: 328-336.
[https://doi.org/10.1016/j.intimp.2015.06.015]

-
Choo, Y.-Y., Tran P. T., Min, B. S., Kim, O., Nguyen, H. D., Kwon, S.-H. and Lee, J.-H. (2017) Sappanone A inhibits RANKL-induced osteoclastogenesis in BMMs and prevents inflammation-mediated bone loss. International Immunopharmacology 52: 230-237.
[https://doi.org/10.1016/j.intimp.2017.09.018]

- Kim, S.-H. and Yoon, K. D. (2020) HPLC method validation for quantitative analysis of scopoletin from hot-water extract powder of Artemisia annua Linné. Korean Journal of Pharmacognosy 51: 78-85.
- 식품의약품안전처(2019) 건강기능식품 기능성 원료 및 기준규격 인정에 관한 규정(식품의약품안전처고시 제2024-79호, 2025. 08.).