
Cratoxylum formosum (Jack) Benth. & Hook.f. ex Dyer 줄기 메탄올 추출물이 아세틸콜린에스테라제 활성과 신경세포에서의 아밀로이드 전구 단백질 대사에 미치는 영향
Abstract
Cratoxylum formosum (Jack) Benth. & Hook.f. ex Dyer has been traditionally used in Asia to treat wounds, fever, cough, and food poisoning. This study aimed to evaluate the inhibitory effects of the methanol extract of Cratoxylum formosum stem (CFM) on amyloid-beta (Aβ) secretion, its potential modulation of amyloid precursor protein (APP) processing, and its acetylcholinesterase (AChE) inhibitory activity. CFM was tested on APPswe-transfected neuroblastoma cells. At a concentration of 100 μg/mL, CFM significantly reduced Aβ1-42 and Aβ1-40 secretion by 48.8% and 57.8%, respectively. Treatment with CFM also enhanced the secretion of soluble amyloid precursor protein-alpha (sAPPα), a metabolite of non-amyloidogenic APP processing pathway, suggesting the activation of α-secretase. Additionally, levels of α-carboxy-terminal fragments (CTFs) of APP were increased, suggesting a potential inhibition of β-secretase activity and consequent reduction in Aβ production. Moreover, CFM exhibited a significant acetylcholinesterase (AChE) inhibitory activity, with inhibition rates of 68.5% and 79.9% observed at concentrations of 25 and 50 μg/mL, respectively. These findings highlight the potential of CFM as a natural therapeutic agent for Alzheimer’s disease by suppressing Aβ production and AChE activity, thus mitigating two key pathological features of the disease.
Keywords:
Alzheimer’s disease, β-Amyloid, Amyloid precursor protein, Acetylcholinesterase, Cratoxylum formosum (Jack) Benth. & Hook.f. ex Dyer Aβ1-40, Aβ1-42알츠하이머 질환(Alzheimer’s disease; AD)은 기억력, 인지 능력을 저하시키는 신경 퇴행성 질환으로 가장 흔한 치매의 형태이며, 전체 치매 환자의 60∼80%를 차지하고 있다. AD의 두 가지 병리학적 마커인 베타아밀로이드(β-amyloid; Aβ)의 축적과 tau 단백질의 과인산화는 신경세포의 손상과 사멸을 초래하는데, Aβ 증가와 응집은 tau 단백질의 과인산화보다 먼저 진행되며 아세틸콜린에스테라제(acetylcholinesterase; AChE) 활성의 증가와도 연관성이 있다고 보고되었다.1-3)
Aβ는 알츠하이머 환자의 뇌에서 플라크의 형태로 발견되며 APP의 순차적 단백질 분해를 통해 생성된다.4) 한편, Aβ의 생성경로는 2가지로 나눌 수 있는데 첫째, 아밀로이드 전구 단백질(Amyloid precursor protein; APP)이 α-secretase에 의해 대사되어 sAPPα (soluble APP α)와 α-CTF (α-carboxyl-terminal fragment)로 분해되는 비아밀로이드 생성경로(non-amyloidogenic pathway), 두 번째로 β-secretase (APP 절단효소; BACE1)에 의해 절단되어 sAPPβ와 β-CTF (β-carboxyl-terminal fragment)로 대사되는 아밀로이드 생성경로(amyloidogenic pathway)로 구분된다.1,4) α-secretase는 APP 초기 대사과정에서 β-secretase와 경쟁적으로 작용하며 그 활성이 증가되면 P3 단편을 증가시키며, 그 결과 Aβ의 생성은 감소된다. 즉, 비아밀로이드 생성경로의 1차 대사물인 α-CTF는 γ-secretase에 의해 절단되어도 Aβ를 생성하지 않지만 β-secretase의 대사물인 β-CTF가 γ-secretase에 의해 절단되면 Aβ를 생성하게 된다.5)
현재까지 AD를 개선하기 위해 임상에서 주로 사용하고 있는 약물은 AChE 억제제이다. AChE는 중요 신경전달물질인 아세틸콜린(acetylcholine; ACh)을 acetate과 choline으로 가수분해한다. 알츠하이머 환자의 경우 ACh의 결핍으로 신경전달 기능이 손실되어 인지능력, 기억력 저하를 일으킨다.6,7) 뿐만 아니라, AChE는 Aβ의 응집에도 영향을 미치는데, AChE의 peripheral anionic site (PAS)를 통해 Aβ 단량체와 결합하여 Aβ의 응집과 섬유화를 촉진하며, 이는 알츠하이머 질환의 병리 진행과정에 관여한다.7,9,10) AChE 억제제인 갈란타민(galantamine) 및 리바스티그민(rivastigmine), 도네페질(donepezil) 등이 승인을 받아 주로 사용되고 있지만 모두 메스꺼움, 구토, 설사 등과 같은 부작용이 심해 독성이 낮고 AChE 억제 활성이 강한 새로운 약물 개발의 필요성이 대두되고 있다.11)
최근, 아두카누맙(aducanumab), 레카네맙(lecanemab), 그리고 도나네맙(donanemab)이 AD 치료제로서 FDA의 승인을 받았다.12) 이 약물들은 모두 Aβ 응집체와 결합하는 단클론항체(monoclonal antibody) 의약품으로서 초기 알츠하이머 질환의 인지능력 및 기억력 저하의 진행을 늦춘다.13) 이들 약물의 임상 적용의 의미는 Aβ가 알츠하이머 질환의 병리학적 바이오마커로서 유의미한 타깃임을 입증한 것이다.14)
한편, 천연물 추출물의 신경세포 손상 보호 및 인지능력 개선 효과에 대한 많은 연구들이 보고되고 있는데, 이러한 연구 결과를 통해 천연물 기반 치료법의 가능성을 제시하며, 신경 퇴행성 질환 예방 및 치료제 개발을 위한 중요한 과학적 근거를 제공하고 있다.15-17) 활성산소는 노화와 각종 질병, 암 뿐만 아니라 신경 퇴행성 질환을 유발하게 되는데, 산화 스트레스가 알츠하이머 질환에서도 뉴런의 소실과 치매로의 진행에 핵심적 역할을 한다는 것이 임상 연구를 통해 입증되었으며, Aβ의 생성을 직접 촉진한다고 보고하였다.18-20) 이와 같이 다양한 요인에 의해 복잡한 기전으로 발생하는 알츠하이머 질환의 치료제 개발을 위해서는 단일 표적보다는 다중 표적 약물에 대한 연구가 필요하며 이미 활발한 연구가 이루어지고 있다.21)
본 연구에 사용한 Cratoxylum formosum (Jack) Benth. & Hook.f. ex Dyer는 물레나무과(Hypericaceae)에 속하는 열대식물로 싱가포르와 베트남, 태국, 중국, 라오스 등 동남아시아에 주로 분포한다. 태국에서는 잎을 teaw라고 부르며 식용하고 있으며 전통적으로 피부에 발라 상처를 치료하고, 꽃은 기침을 완화시키는데 사용하고 있다.22) 또한 중국에서는 발열, 기침, 복통, 식중독, 설사, 소화성 궤양 치료에 사용한다고 알려졌다.23)
Cratoxylum formosum (Jack) Benth. & Hook.f. ex Dyer 잎에는 dicaffeoylquinic acid와 chlorogenic acid 등이 보고되었으며, 그 약리활성으로는 항산화 효과,22,24) 항염증 효과,24) 예쁜꼬마선충(Caenorhabditis elegans)에서의 Aβ의 독성 보호 효과,25) 그리고 항암 효과26) 등이 보고되었지만, APP의 대사과정을 비롯한 Aβ의 분비 또는 AChE 활성에 대한 효능연구는 보고된 적이 없다. 그리고 줄기의 약리활성 및 성분에 대한 연구는 거의 미미한 실정이다. 본 연구에서는 Aβ의 분비를 억제하고 AChE 활성을 억제하는 다중 약리활성을 가진 천연물 소재를 탐색하는 과정의 일환으로 라오스 자생 식물의 추출물을 스크리닝한 결과, C. formosum 줄기의 methanol (MeOH) 추출물이 Aβ 분비와 AChE 활성을 억제하며 항산화 활성을 나타내었기에 그 결과를 보고하고자 한다.
재료 및 방법
세포주 − APP Swedish 유전자가 과잉 발현되는 생쥐 유래 신경 세포주인 Neuro2a (APPswe)는 5% fetal bovine serum (FBS, SERENA Europe GmbH, Brandenburg, Germany), penicillin streptomycin (P/S, Lonza, Walkersville, MD, USA), L-glutamine (GE Healthcare Hyclone, Logan, UT, USA), hygromycin B (Invitrogen, Carlsbad, CA, USA)가 포함된 Dulbecco’s Modified Eagle’s Medium (DMEM, Lonza, Walkersville, MD, USA)와 Opti-MEM (Gibco, Grand Island, NY, USA)의 혼합 배지를 이용하여, 37℃, 5% CO2의 조건에서 배양하였다.
시험물질 및 시약 − Cratoxylum formosum MeOH 추출물(이하 CFM으로 약칭함)은 한국생명공학연구원 해외생물소재 연구센터(Daejeon, Republic of Korea)로부터 분양받아 DMSO에 100 mg/mL로 용해하여 각 농도로 희석하여 실험에 사용하였다. 식물은 라오스 캄무아네주 나카이 지역에서 채집하였으며, 건조된 줄기(86 g)를 99.9% (v/v) 메탄올 1 L로 15분 동안 반복 초음파 처리 후 2시간 정치를 반복하며 45℃에서 3일간 추출하였다. 수득한 추출액을 모아 감압 회전농축기(N-1000SWD, EYELA)로 농축하였으며 최종적으로 동결 건조하여 추출물 5.09 g을 얻었다. 실험에서 사용된 시약은 다음과 같다. β-secretase inhibitor IV (Calbiochem, Darmstadt, Germany), galantamine (Cayman Chemical, Ann Arbor, MI, USA), acetylcholinesterase from Electrophorus electricus, protease inhibitor (Sigma-Aldrich Co., St. Louis, MO, USA), anti-human sAPPα monoclonal antibody 2B3 (Immuno-Biological Laboratories, Gunma, Japan), rabbit anti-amyloid precursor protein polyclonal antibody CT20 (Calbiochem, Darmstadt, Germany), rabbit APP369 polyclonal antibody human amyloid β (1-40), human amyloid β assay kit (IBL, Gunma, Japan), cell viability EZ-cytox assay kit (CCK-8), acetylcholinesterase assay kit (Dogen bio Co., Ltd., Seoul, Korea), easy-spinTM total RNA extraction kit (iNtRON biotechnology, Seoul, Korea), primeScriptTM RT Master Mix, TB Green® Premix Ex TaqTM (Takara Korea Biomedical Inc., Seoul, Korea)를 사용하였다.
β-amyloid(Aβ)의 분비 억제 효과 검정 − APPswe 세포주에서 분비된 Aβ의 양을 정량하기 위해 sandwich ELISA를 활용하여 측정하였다. 6-well plate (SPL Life Science Inc., Pocheon, Korea)에 세포 농도가 1 × 106 cells/well이 되게 배양한 후 serum-free DMEM으로 희석한 CFM을 1, 10, 50, 100 μg/mL의 농도로 16시간 동안 처리한 후 배양액을 PMSF (phenylmethylsulfonyl fluoride)의 존재 하에 회수하여 시료로 사용하였으며 양성대조군으로 β-secretase inhibitor IV 10 μM를 사용하였다. Aβ (35-40) 특이적 monoclonal antibody 또는 Aβ (38-42) 특이적 polyclonal antibody로 코팅된 plate에 시료 100 μL를 첨가한 뒤, 4℃에서 16시간 동안 반응을 진행하였다. 이후 plate를 7회 세척한 후, horseradish peroxidase (HRP)로 결합된 Aβ (11-28) 특이적 monoclonal antibody를 추가하고 4℃에서 1시간 동안 반응시켰다. 그 다음 9회 세척 후, tetramethyl benzidine (TMB) 기질 용액을 넣고 실온에서 30분간 반응을 유도하였으며, 정지액 100 μL를 첨가하여 450 nm에서 microplate reader (Model 680, Bio-Rad, Hercules, CA, USA)를 통해 흡광도를 측정하였다.
세포독성 분석 − EZ-cytox kit를 사용하여 CFM의 APPswe 세포주와 RAW 264.7 세포주에 대한 세포독성을 측정하였다. 96-well plate (SPL Life Science Inc., Pocheon, Korea)에 5 × 103 cells/well이 되도록 배양한 후 CFM을 APPswe 세포주에는 1, 10, 50, 100 μg/mL, RAW 264.7 세포주에는 10, 25, 50, 100 μg/mL 의 농도로 24시간 처리하였다. Water-soluble tetrazolium 용액 10 μL를 첨가하여 1시간 배양한 후, 450 nm에서 microplate reader (Model 680, Bio-Rad, Hercules, CA, USA)를 이용하여 흡광도를 측정하였다.
단백질 발현 분석 − APPswe 세포주를 6-well plate (SPL Life Science Inc., Pocheon, Korea)에 1 × 106 cells/well이 되도록 배양한 후 serum-free DMEM으로 희석한 CFM 1, 10, 50, 100 μg/mL 또는 양성대조군인 β-secretase inhibitor IV 10 μM, γ-secretase inhibitor IX 10 μM을 24시간 처리하였다. Protease inhibitor (GenDEPOT, Katy, TX, USA)가 포함된 cell lysis buffer (150 mM NaCl, 50 mM Tris-HCl, pH 7.4, 0.5% sodium deoxycholate, 0.5% NP-40, 5 mM EDTA)를 넣고 초음파 분쇄하여 시료로 사용하였다. Bicinchonic acid (BCA) protein assay reagent (Thermo Fisher Inc., San Jose, CA, USA)를 사용하여 단백질 농도를 정량한 후, 50 μg의 단백질을 7%, 10% Tris-glycine 또는 16.5% Tris-Tricine SDS-PAGE로 분리하였다. 이후 immunoblotting을 통해 APP, sAPPα, APP carboxy-terminal fragment (CTF) 등의 단백질 발현을 분석하였으며, Azure C-600 (Azure Biosystems, Dublin, CA, USA)을 활용하여 결과를 확인하였다. 3회 반복 실험으로 얻어진 단백질 밴드를 ImageJ software (National Institutes of Health, Bethesda, MD, USA)에 의해 정량하였다.
Total RNA의 분리 및 real-time polymerase chain reaction (qPCR) 분석 − APPswe 세포주를 6-well plate (SPL Life Science Inc., Pocheon, Korea)에 1 × 106 cells/well이 되도록 배양한 후 serum-free DMEM으로 희석한 CFM 1, 10, 50, 100 μg/mL의 농도로 24시간 처리하였다. 배양액을 제거한 후 easy-spinTM total RNA extraction kit (iNtRON biotechnology, Seoul, Korea)를 사용하여 프로토콜 메뉴얼에 따라 total RNA를 분리하였다. 분리한 RNA는 260 nm, 280 nm에서 Nanodrop ND-1000 spectrophotometer (Thermo Fisher Inc., San Jose, CA, USA)을 사용하여 흡광도를 측정하고 total RNA양을 정량하였다. 각 시료는 50 ng/μL이 되도록 sterile water (RNase free)로 희석하여 사용하였으며 희석한 RNA; 8 μL, primeScriptTM RT Master Mix (Takara Korea Biomedical Inc., Seoul, Korea); 2 μL을 넣은 반응혼합물 10 μL으로 RT-qPCR 시행 전 cDNA 합성을 진행하였다. 반응은 reverse transcription 37℃에서 15분, heat inactivation of reverse transcriptase 85℃에서 5초로 설정하여 반응시켰다.
APP의 mRNA 발현을 알아보기 위한 RT-qPCR은 PCR tube에 TB Green®Premix Ex TaqTM (Takara Korea Biomedical Inc., Seoul, Korea); 12.5 μL, 10 pmol로 희석한 primer; 1 μL, cDNA 합성 RNA; 2 μL, sterile water (RNase free); 9.5 μL를 넣어 만든 25 μL 반응혼합물로 다음 분석을 진행하였다. 반응은 initial denaturation 95℃에서 30초, denaturation 95℃에서 5초, annealing & elongation 60℃에서 30초, cycle의 반복은 40회로 설정하여 CronoSTARTM 96 Real-Time PCR System (Takara Bio Inc., Kusatsu, Shiga, Japan)을 이용하여 분석하였다. 실험에 사용한 APP primer sequence는 forward가 TGG CCA ACA TGA TTA GTG ACC이며 reverse가 AAG ATG GCA TGA GAG CAT CGT이었다. GAPDH의 primer sequence는 forward가 AAC TTT GGC ATT GTG GAA GG이며 reverse가 GGA TGC AGG GAT GAT GTT CT이었다. Primer는 바이오니아(Bioneer, Daejeon, Korea)에 의뢰하여 제작하였다.
Acetylcholinesterase (AChE) 억제 활성 분석 − AChE의 억제 활성은 acetylcholinesterase activity colorimetric assay kit (Dogen bio Co. Ltd, Seoul, Korea)를 사용하여 측정하였다. 96-well plate에 DMSO 또는 CFM을 각각 1, 10, 25, 50 μg/mL의 농도로 처리한 뒤, acetylcholinesterase (from Electrophorus electricus) 30 μL와 10 μL를 추가하였다. 이후 반응 혼합물 (AChE assay buffer 45 μL, AChE enzyme mix 2 μL, AChE probe 2 μL, AChE substrate 1 μL; 1 assay 기준)을 50 μL씩 첨가하고, 차광하여 실온에서 20분 동안 반응을 진행하였다. 최종적으로 microplate reader (Model 680, Bio-Rad, Hercules, CA, USA)를 이용하여 570 nm에서 흡광도를 측정하였다. 10 μM galantamine을 대조 약물로 사용하였으며, 시료가 첨가되지 않은 대조군의 흡광도를 AChE 활성의 100%로 설정하였다. 이후 각 시료의 억제 활성을 백분율로 환산한 후, 3회 반복 분석하여 통계 분석을 수행하였다.
DPPH radical 소거능에 의한 항산화 활성 분석 − 96-well plate에 CFM을 최종농도가 1, 10, 50, 100 μg/mL이 되도록 99% EtOH로 희석하여 100 μL씩 첨가하고, 99% EtOH로 희석한 DPPH 100 μM working solution을 100 μL씩 넣고 차광하여 15분 반응 진행 후, microplate reader (Model 680, Bio-Rad, Hercules, CA, USA)를 이용하여 517 nm에서 흡광도를 측정하였다. 대조 약물로 L-ascorbic acid (Vit.C)를 CFM과 동일한 농도로 희석하여 사용하였다. 무첨가군과 첨가군의 값을 비교하여 DPPH radical scavenging activity (%)로 나타내었다.
통계처리 − 모든 생리활성 실험은 3회 반복 수행되었으며, 결과는 mean ± standard error of the mean (SEM)로 표시하였다. 통계 분석은 Student’s t-test와 one-way ANOVA를 활용하였으며(GraphPad Prism 5 software, La Jolla, CA, USA), 유의수준은 0.1%, 1%, 5%로 설정하여 검정하였다. 통계적 유의성은 *p < 0.05, **p < 0.01, ***p < 0.001로 나타내었다.
결과 및 고찰
C. formosum MeOH 추출물(CFM)의 세포독성 및 β-amyloid(Aβ) 분비억제 효과 − CFM의 APPswe 세포주에 대한 독성을 분석하였다. CFM 1, 10, 50 또는 100 μg/mL 처리 세포의 생존율은 각각 대조군의 세포 생존율과 비교 정량한 결과, 96.49 ± 3.7, 85.57 ± 2.4, 86.58 ± 3.3, 54.96 ± 6.3%를 나타내었다. CFM은 50, 100 μg/mL의 농도에서 APPswe 세포주에 대해 각각 13, 45%의 세포독성을 나타내었다(Fig. 1A).
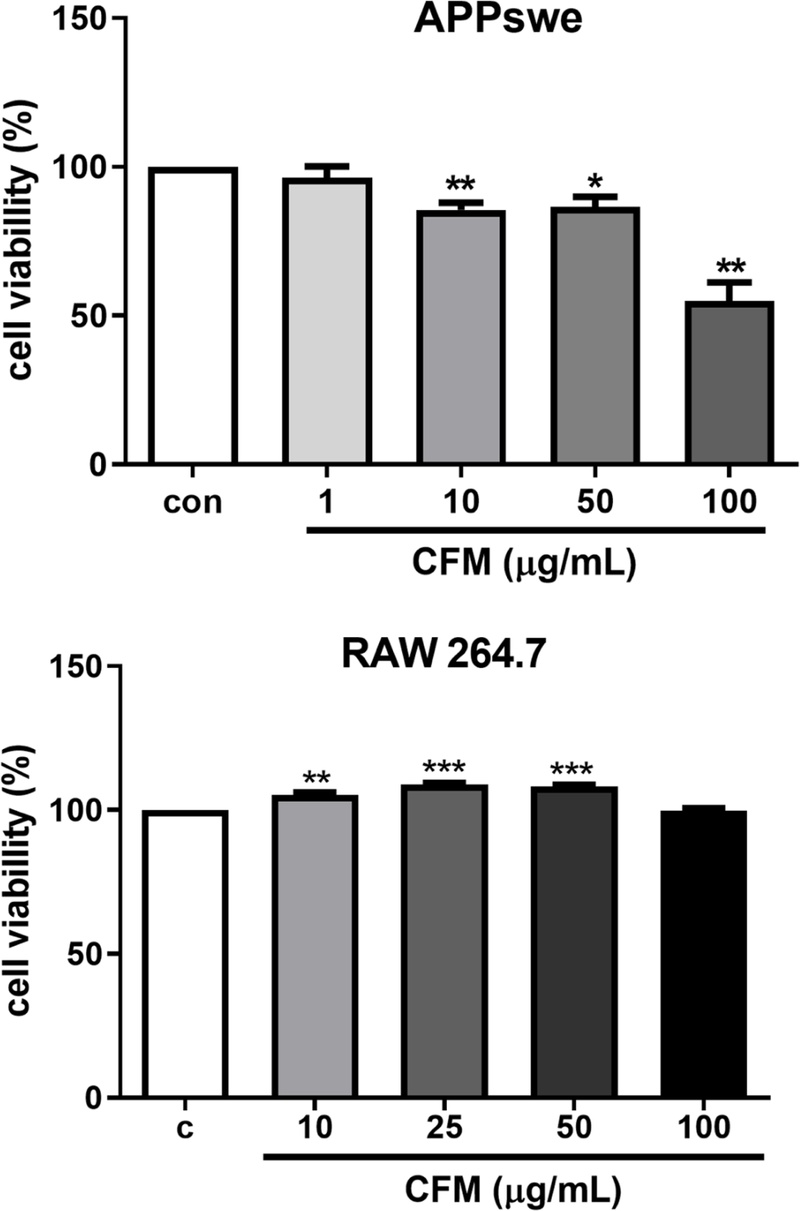
Effects of Methanol extract of Cratoxylum formosum on cell viability. APPswe cells and RAW 264.7 cells were cultured at confluency in a 96-well plate and treated with various concentrations (1, 10, 25, 50, or 100 μg/mL) of the methanol extract from the stem of Cratoxylum formosum (CFM) for 24 hours. Following treatment, the EZ-Cytox reagent was added to each well, and cells were incubated for an additional hour. Absorbance at 450 nm was measured using a microplate reader (Bio-Rad, Hercules, CA). Data are expressed as the mean ± standard error (SE) from three independent experiments (*p < 0.05, **p < 0.01 compared to control cells, analyzed using one-way ANOVA with GraphPad Prism 5 software. C; negative control, treatment with 0.1% dimethyl sulfoxide (DMSO)).
또한 CFM의 RAW 264.7 세포주에 대한 독성을 분석한 결과, CFM 10, 25, 50 또는 100 μg/mL 처리 세포의 생존율은 각각 대조군의 세포 생존율과 비교 정량한 결과, 105.23 ± 0.99%, 108.98 ± 0.5%, 108.16 ± 0.66%, 99.64 ± 1.06%를 나타내어 100 μg/mL의 농도에서 RAW 264.7 세포주에 대해 약 1% 미만의 세포독성을 나타내었다(Fig. 1B).
APPswe 세포주에 CFM을 농도별로 처리한 후 세포 배양액으로 분비된 Aβ의 양을 sandwich ELISA 방법으로 측정하였다. DMSO를 처리한 음성대조군(C)의 Aβ의 분비량과 비교하여 백분율로 표시하였다. CFM 1, 10, 50, 또는 100 μg/mL 처리 시 Aβ1-40의 분비량은 각각 음성대조군의 202.05 ± 1%, 152.18 ± 45.1%, 48.44 ± 7.2%, 42.60 ± 16.6%이었으며, Aβ1-42의 분비량은 각각 음성대조군의 171.11 ± 48%, 123.46 ± 29.5%, 60.78 ± 13.6%, 51.20 ± 19.2%이었다. 즉, CFM 100 μg/mL 처리는 Aβ1-40의 분비를 약 57% 억제하였으며 Aβ1-42의 분비는 약 50% 억제하였다. 한편, 양성대조군으로 사용한 10 μM의 β-SI (β-secretase inhibitor IV)는 Aβ1-40와 Aβ1-42의 분비를 각각 약 75%, 55% 억제하였다(Fig. 2).
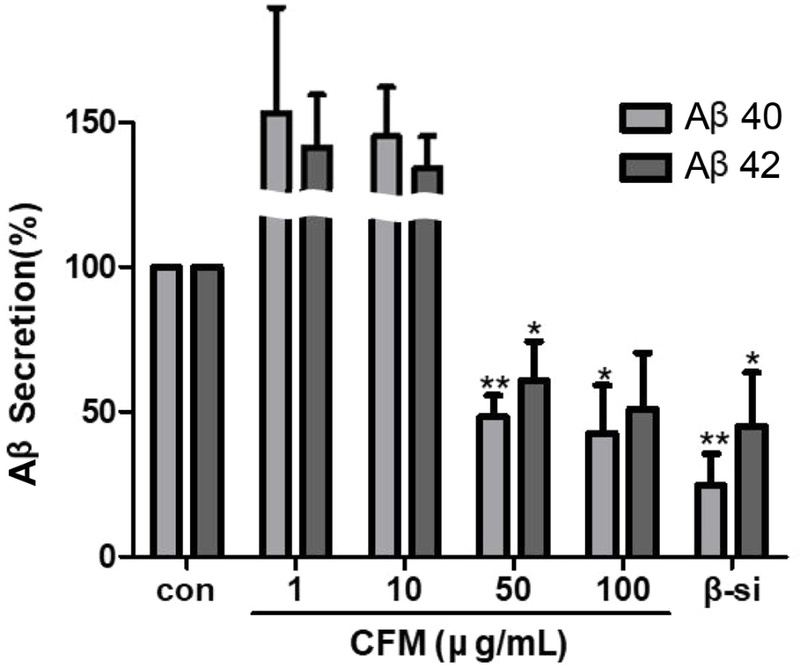
Effects of the methanol extract of Cratoxylum formosum on the secretion of β-amyloid. APPswe cells were treated with DMSO (Control) or various concentrations (1, 10, 50, or 100 μg/mL) of the methanol extract from the stem of Cratoxylum formosum (CFM) for 24 hours. The conditioned media were collected and analyzed using Aβ40/42 ELISA. Data are expressed as the mean ± standard error (SE) from three independent experiments (*p < 0.05, **p < 0.01 compared to control cells, analyzed using one-way ANOVA with Graph-Pad Prism 5 software. C; negative control, treatment with 0.1% dimethyl sulfoxide (DMSO); β-si: positive control, treatment of 10 μM of β-secretase inhibitor; Aβ40: β-amyloid 40; Aβ42: β-amyloid 42).
CFM 100 μg/mL에서 Aβ1-40와 Aβ1-42가 각각 57%, 50%가 감소한 것이 동일 농도에서의 45%의 세포 독성에 의해 Aβ의 분비 억제 활성에 영향을 받았을 수 있으나, 약 13%의 세포독성을 보이는 50 μg/mL에서 Aβ1-40, Aβ1-42가 각각 52%, 40% 감소하였으므로, 세포독성에 비해 현저한 Aβ 분비 억제 활성을 나타내었다. 따라서 CFM이 Aβ의 분비를 억제하는 주된 기전은 CFM의 세포독성에 의한 것이 아님을 의미한다.
C. formosum M eOH 추출물(CFM)의 APP(amyloid precursor protein)와 관련 단백질 발현 및 mRNA 발현에 미치는 양상 CFM의 Aβ 분비 억제효과의 작용 메커니즘을 규명하기 위해 CFM을 1, 10, 50 또는 100 μg/mL 농도로 처리한 APPswe 세포주로부터 세포 분획을 회수하여 Western blot에 의해 단백질의 양상을 분석하였다. 그 결과 APP 단백질의 발현은 음성대조군(DMSO 처리군)에 비해 각각 81.97 ± 4.11%, 72.8 ± 5.67%, 66.90 ± 8.79%, 109.97 ± 0.89%를 나타내며 CFM의 농도가 높아짐에 따라 APP 단백질의 발현이 증가하는 경향을 보였다. 한편, APP 단백질이 α-secretase에 의해 절단되어 배양액으로 분비된 sAPPα의 경우 음성대조군 대비 각각 122.11 ± 4.11%, 136.80 ± 22.59%, 360.12 ± 30.86%, 403.00 ± 45.55%을 나타내며 sAPPα 분비량을 현저하게 증가시켰다(Fig. 3A-C). 이는 α-secretase의 활성이 증가하였음을 의미하며 경쟁적으로 작용하는 β-secretase의 활성을 억제시켜 Fig. 1과 같이 Aβ의 분비량을 감소시켰음을 간접적으로 시사한다.
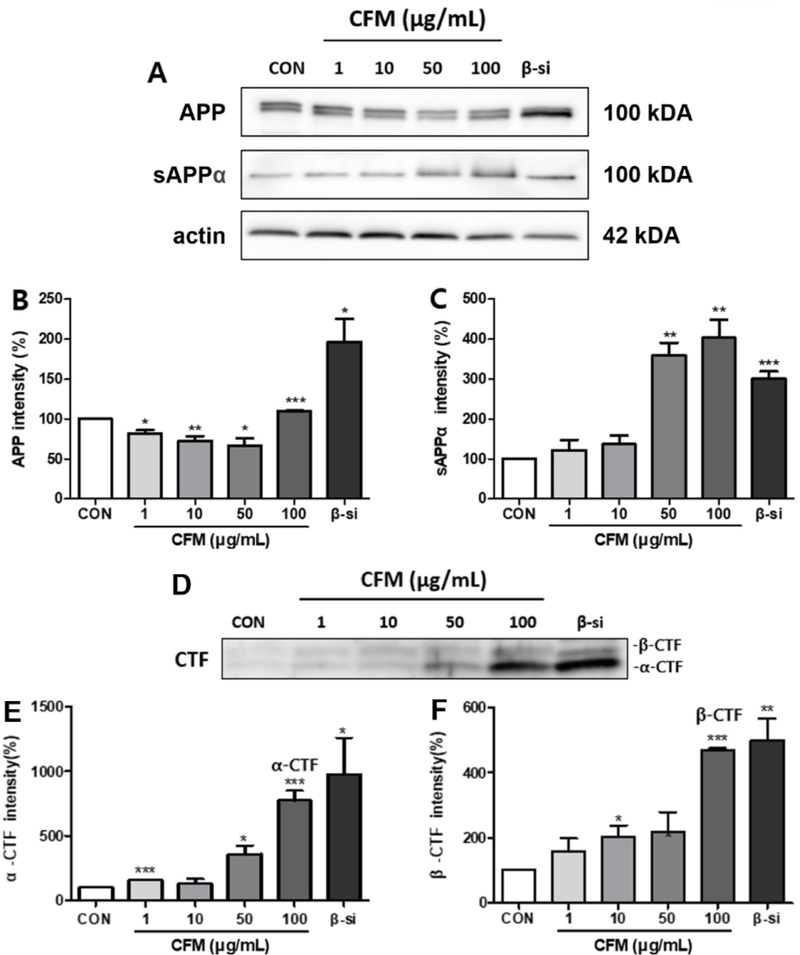
Effects of methanol extract of Cratoxylum formosum on the metabolism of amyloid precursor protein (APP). APPswe cells were exposed to DMSO (control) or varying concentrations of the methanol extract derived from the stem of Cratoxylum formosum (CFM) for 24 hours, followed by lysis with cell lysis buffer. The cell lysates and conditioned media were separated on 7% Tris-glycine SDS-PAGE or 16.5% Tris-tricine gels and analyzed by immunoblotting. (A, C): Mouse anti-sAPPα (2B3) monoclonal antibody (1:500); (B): Rabbit anti-APP polyclonal antibody (1:1,000); (D, E, F): Rabbit APP369 polyclonal antibody (1:1,000). Actin was used as a loading control. Protein levels were quantified relative to actin expression using Image J 1.37 software. Data are presented as the mean ± standard error (SE) from three independent experiments (*p < 0.05, **p < 0.01, ***p < 0.001 compared to control cells, analyzed using one-way ANOVA with GraphPad Prism 5 software. C: control, treatment with 0.1% dimethyl sulfoxide (DMSO); γ-si: positive control, treatment with 10 μM γ-secretase inhibitor; APP: amyloid precursor protein; sAPPα: soluble APPα; CTF-α: APP carboxy terminal fragment α; CTF-β: APP carboxy terminal fragment β).
다음으로, CFM의 β-secretase에 대한 영향을 규명하고자 Tris-Tricine gel로 CTF 발현 양상을 확인하였을 때, α-CTF 단백질은 음성대조군 대비 각각 155.11 ± 3.90%, 132.12 ± 36.34%, 360.99 ± 63.21%, 774.24 ± 76.41%를 나타냈다. β-CTF 단백질은 음성대조군 대비 각각 158.28 ± 39.78%, 201.66 ± 35.84%, 216.45 ± 61.88%, 470.14 ± 4.63%를 나타내 CFM의 농도가 높아질수록 α-CTF와 β-CTF 모두 증가시키는 경향을 보였으며, 이는 양성대조군으로 사용한 β-SI와 동일하게 세포 내에 상대적으로 많은 양의 α-CTF와 비교적 적은 양의 β-CTF가 축적되는 양상을 나타내었다(Fig. 3D-F).
또한, CFM이 APPswe 세포주에서 APP mRNA 발현에 미치는 영향을 검정하기 위하여 CFM을 1, 10, 50 또는 100 μg/mL 농도로 24시간 처리한 후 APPswe 세포주로부터 RNA를 분리하여 RT-qPCR (Reverse transcription quantitative real-time polymerase chain reaction)을 진행하였다. 기준 유전자는 housekeeping gene인 GAPDH를 사용하였다. 그 결과 CFM을 1, 10, 50 또는 100 μg/mL 농도로 처리 시 APP mRNA 발현량은 음성대조군과 비교하여 각각 124.14 ± 40.12%, 97.48 ± 23.91%, 41.94 ± 5.57%, 33.94 ± 7.68%을 나타냈다. CFM은 농도 1 μg/mL에서는 mRNA의 발현량을 증가시켰으나 50, 100 μg/mL에서는 현저하게 감소시켰다(Fig. 4). APP 단백질 발현량(Fig. 3A, B)이 증가하는 양상과는 상이한 결과를 보인다.
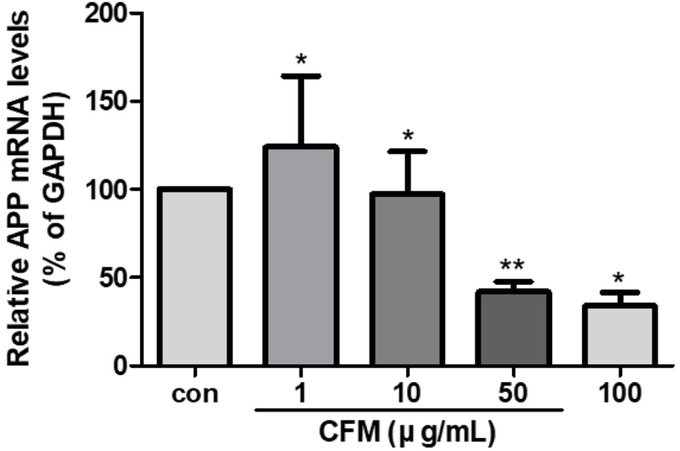
Effects of the methanol extract of Cratoxylum formosum on the inhibition of APP mRNA expression. APPswe cell lines were cultured in 6-well plates (SPL life science Inc., Pocheon, Korea) at a density of 1 × 106 cells/well and treated with serum-free DMEM containing various concentrations of Cratoxylum formosum methanol extract (CFM; 1, 10, 50, or 100 μg/mL) for 24 hours. The relative expression levels of APP mRNA were quantified by real-time PCR using primers specific for APP and GAPDH. The primers were synthesized by Bioneer (Daejeon, Korea), with the following sequence: GAPDH forward: 5’ AAC TTT GGC ATT GTG GAA GG 3’ (20-mer); GAPDH reverse: 5’ GGA TGC AGG GAT GAT GTT CT 3’ (20-mer); APP forward: 5’ TGG CCA ACA TGA TTA GTG ACC 3’ (21-mer); APP reverse: 5’ AAG ATG GCA TGA GAG CAT CGT 3’ (21-mer). Data are expressed as the mean ± standard error (SE) from three independent experiments. CON: control.
즉, CFM 50, 100 μg/mL을 처리한 APPswe 세포주에서 APP mRNA 발현량을 감소시키지만, 이미 번역되어 세포 내에 축적된 APP 단백질의 존재로 인해 APP 단백질의 총량은 APP mRNA 감소량에 비해 증가한 것으로 사료된다. 한편, mRNA로부터 단백질 합성까지의 과정은 최소 20초에서 최대 몇 분 이내의 짧은 시간 안에 진행된다.27) 향후, CFM이 APP mRNA 발현을 타겟팅 하는 시작 시점을 명확히 규명하기 위해 다양한 처리 시간 조건을 적용하여 RT-qPCR을 진행할 예정이다.
C. formosum M eOH 추출물(CFM)의 AChE (acetylcholinesterase) 억제 활성 CFM의 AChE 활성에 미치는 영향을 평가하기 위해 CFM을 10, 25, 50 μg/mL 농도로 처리하여 시험관 내 AChE 효소 활성을 측정하였다. 본 실험은 세포를 사용하지 않고 시험관 내에서 직접적으로 효소에 미치는 영향을 분석한 것으로, 세포독성의 영향을 배제하고 추출물의 고유한 억제 활성을 확인하였다. CFM의 농도를 50 μg/mL까지 사용하였으며, 양성대조군으로 galantamine을 사용하였다. 그 결과, 음성대조군과 비교하여 CFM 10 μg/mL 농도에서는 억제 활성을 보이지 않았으나 25, 50 μg/mL 농도에서는 각각 68.5 ± 1.9, 79.9 ± 0.7%의 억제 활성을 나타냈다(Fig. 5). 한편 galantamine 10 μM은 61.5 ± 1.1%의 억제 활성을 나타냈다(Fig. 5). 한편 Cratoxylum formosum의 잎에는 dicaffeoylquinic acid, chlorogenic acid 등의 성분을 가지고 있다고 보고되었으며,22,24) dicaffeoylquinic acid는 AChE를 억제하고,28) Aβ의 응집을 억제하며,29) Aβ에 의한 신경독성에 대해 보호 작용을 나타낼 뿐 아니라30) trimethyltin(TMT)에 의해 유도된 인지 기능 장애를 개선한다고 보고하였다.28) CFM은 줄기 부위를 사용한 것이지만 Aβ 분비 억제와 AChE 억제 활성은 이러한 활성 성분들이 직접 또는 간접적으로 영향을 미쳤을 것으로 추정되며, 추후 유효성분의 규명이 필요하다.
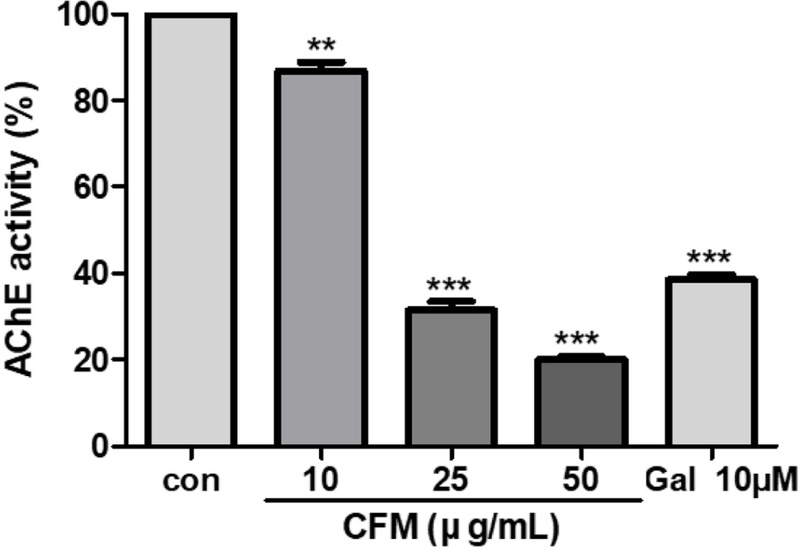
Effects of the methanol extract of Cratoxylum formosum on acetylcholinesterase (AChE) activity. The methanol extract from the stem of Cratoxylum formosum (CFM) was prepared at final concentrations of 10, 25, and 50 μg/mL using acetylcholinesterase (AChE) assay buffer. Galantamine (10 μM) was used as the positive control. AChE activity was measured, and data are expressed as the mean ± standard error (SE) from three independent experiments (**p < 0.01, ***p < 0.001 compared to control cells, analyzed using one-way ANOVA with GraphPad Prism 5 software. C: negative control, treatment with 0.1% dimethyl sulfoxide (DMSO); GAl: positive control, treatment with 10 μM galantamine (AChE inhibitor).
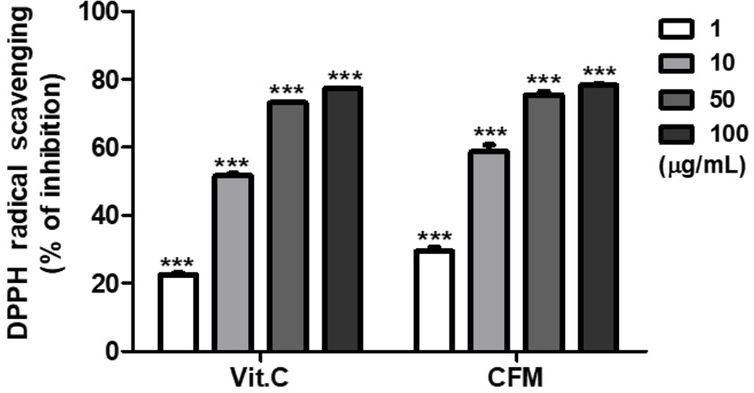
Effects of the methanol extract of Cratoxylum formosum on DPPH radical scavenging activity. The methanol extract from the stem of Cratoxylum formosum (CFM) was prepared at final concentrations of 1, 10, 50, 100 μg/mL using distilled EtOH. L-ascorbic acid (Vitamin C) was used as the positive control. The DPPH radical scavenging activity was measured, and data are expressed as the mean ± standard error (SE) from three independent experiments (*p < 0.05, **p < 0.01, ***p < 0.001 compared to control, analyzed using one-way ANOVA with GraphPad Prism 5 software.) Vit. C: positive control (L-ascorbic-acid).
C. formosum M eOH 추출물(CFM)의 DPPH radical scavenging 활성 − DPPH (2,2-diphenyl-1-picrylhydrazyl)가 지닌 free radical이 항산화 물질과 반응하여 자색의 혼합물이 노란색으로 환원되는 성질을 이용하여 CFM을 1, 10, 50 또는 100 μg/mL의 농도로 처리한 후 시험관 내 항산화 활성을 측정하였다. 그 결과 CFM의 DPPH 소거 활성은 각각 29.44 ± 1.08%, 58.70 ± 2.04%, 75.42 ± 0.98%, 78.20 ± 0.42%로 나타났으며, 농도의존적으로 DPPH free radical소거활성이 증가하였다. 한편, 양성대조군 Vit. C는 각각 22.50 ± 0.43%, 51.61 ± 0.68%, 73.11 ± 0.19%, 77.19 ± 0.29%의 항산화 활성을 나타냈다. CFM 10 μg/mL은 양성대조군인 Vit. C와 비교하여 약 7.1% 더 높은 항산화 활성을 보였다. 활성산소는 노화가 진행될수록 미토콘드리아, 핵 DNA 단백질에 손상을 초래한다. 그 손상이 AD 환자의 측두엽에서는 더 두드러지게 관찰되는 것으로 보고되었다.9) 또한 Aβ는 활성산소의 작용에 의해 응집이 촉진되는데, 활성산소를 감소시키는 항산화제는 Aβ의 독성으로부터 신경세포를 보호한다고 보고되어 있다.18,31,32)
결 론
CFM은 AD에 대한 다중 표적인 Aβ, AChE 모두 유효한 활성을 나타내었으며, 또한 강한 항산화 활성에 의해 활성산소를 억제함으로써 산화 스트레스에 의해 유발될 수 있는 Aβ 응집을 억제할 수 있을 것으로 사료된다. 향후 CFM의 유효성분의 규명과 in vitro에서의 항염증 활성과 in vivo 활성을 검정할 예정이다. 이러한 연구결과를 종합해 보면, C. formosum은 AChE와 Aβ를 이중 표적으로 하는 후보 자원으로서 치매 치료를 위한 천연물 의약품 개발에 기여할 것으로 사료된다.
Acknowledgments
본 연구는 2025년도 교육부 및 전북특별자치도의 재원으로 전북RISE센터의 지원을 받아 수행된 지역혁신중심 대학지원체계(RISE)의 결과입니다(2025-RISE-13-WSU).
References
-
Busche, M. A. and Hyman, B. T. (2020) Synergy between amyloid-β and tau in Alzheimer’s disease. Nat. Neurosci. 23: 1183-1193.
[https://doi.org/10.1038/s41593-020-0687-6]

-
Wiley, J. (2023) Alzheimer’s disease facts and figures. Alzheimer’s Dement. 17: 327-406.
[https://doi.org/10.1002/alz.12328]

- Lee, E. H., Yoon, Y. C., Park, K. Y., Min, J. H, Kwon, O. S, Lee, H. O. and Hong, H. J. (2008) The effect of acetylcholine esterase inhibitor on cerebrospinal fluid β-amyloid 1-42 and phosphorylated tau protein in Korean Alzheimer’s disease patients: Preliminary study. J. Korean Neurol. Assoc. 26: 224-230.
-
Nguyen, K. V. (2019) β-Amyloid precursor protein (APP) and the human diseases. AIMS Neurosci. 6: 273-281.
[https://doi.org/10.3934/Neuroscience.2019.4.273]

-
Castro, M. A., Hadziselimovic, A. and Sanders, C. R. (2019). The vexing complexity of the amyloidogenic pathway. Protein Sci. 28: 1177-1193.
[https://doi.org/10.1002/pro.3606]

-
Talesa, V. N. (2001) Acetylcholinesterase in Alzheimer’s disease. Mechanisms of ageing and development. Mech. Ageing Dev. 122: 1961-1969.
[https://doi.org/10.1016/S0047-6374(01)00309-8]

-
Singh, M., Kaur, M., Kukreja, H., Chugh, R., Silakari, O. and Singh, D. (2013) Acetylcholinesterase inhibitors as Alzheimer therapy: from nerve toxins to neuroprotection. Eur. J. Med. Chem. 70: 165-188.
[https://doi.org/10.1016/j.ejmech.2013.09.050]

-
Alvarez, A., Alarcon, R., Opazo, C., Campos, E. O., Munoz, F. J., Calderon, F. H. and Inestrosa, N. C. (1998) Stable complexes involving acetylcholinesterase and amyloid-β peptide change the biochemical properties of the enzyme and increase the neurotoxicity of Alzheimer’s fibrils. J. Neurosci. 18: 3213-3223.
[https://doi.org/10.1523/JNEUROSCI.18-09-03213.1998]

-
Nordberg, A., Ballard, C., Bullock, R., Darreh-Shori, T. and Somogyi, M. (2013) A review of butyrylcholinesterase as a therapeutic target in the treatment of Alzheimer’s disease. Prim. Care Companion CNS Disord. 15: 26731.
[https://doi.org/10.4088/PCC.12r01412]

-
Inestrosa, N. C., Alarcon, R., Arriagada, J., Donoso, A., Alvarez, J. and Campos, E. O. (1994) Blood markers in Alzheimer disease: subnormal acetylcholinesterase and butyrylcholinesterase in lymphocytes and erythrocytes. J. Neurol. Sci. 122: 1-5.
[https://doi.org/10.1016/0022-510X(94)90044-2]

-
Mullard, A. (2024) FDA approves third anti-amyloid antibody for Alzheimer disease. Nat. Rev. Drug Discov. 23: 571.
[https://doi.org/10.1038/d41573-024-00116-1]

-
Mintun, M. A., Lo, A. C., Duggan Evans, C., Wessels, A. M., Ardayfio, P. A., Andersen, S. W. and Skovronsky, D. M. (2021) Donanemab in early Alzheimer’s disease. N. Engl. J. Med. 384: 1691-1704.
[https://doi.org/10.1056/NEJMoa2100708]

-
van Dyck, C. H., Swanson, C. J., Aisen, P., Bateman, R. J., Chen, C., Gee, M., Kanekiyo, M., Li, D., Reyderman, L., Cohen, S., Froelich, L., Katayama, S., Sabbagh, M., Vellas, B., Watson, D., Dhadda, S., Irizarry, M., Kramer, L. D. and Iwatsubo, T. (2023) Lecanemab in early Alzheimer’s disease. N. Engl. J. Med. 388: 9-21.
[https://doi.org/10.1056/NEJMoa2212948]

-
Kim, J. H., Kim, M. J., Park, C. H., Lee, J. Y., Shin, Y. S. and Jo, E. J. (2020) Protective effects of a composite of safflower seeds (Carthamus tinctorius L.) and white dandelion (Taraxacum coreanum) on scopolamine-induced memory impairment. J. Korean Soc. Med. Crop Sci. 28: 85-94.
[https://doi.org/10.7783/KJMCS.2020.28.2.85]

-
Lee, J. W., Lee, Y. S., Lee, S. E., Lee, D. Y., Ahn, Y. S., Park, C. G and Kim, G. S. (2016) A study on the preparation of white ginseng extract for enhancing cognitive function. J. Korean Soc. Med. Crop Sci. 24: 375-385.
[https://doi.org/10.7783/KJMCS.2016.24.5.375]

-
Kim, J. Y. and Leem, J. Y. (2021) Acetylcholinesterase inhibitory activity and anti-amyloid effects of an ethanol extract from the seeds of Cercis chinensis Bunge. J. Korean Soc. Med. Crop Sci. 29: 337-344.
[https://doi.org/10.7783/KJMCS.2021.29.5.337]

- Choi, H. Y., Kim, J. Y., Ma, S. Y., Jo, H. G., Kim, D. S. and Leem, J. Y. (2022) Effects of an ethanol extract of Campbell Early (Vitis labruscana B.) leaves on amyloid precursor protein expression and acetylcholinesterase activity in neuronal cells. J. Korean Soc. Pharmacogn. 53: 102-110.
-
Christen, Y. (2000) Oxidative stress and Alzheimer disease. Am. J. Clin. Nutr. 71: 621S-629S.
[https://doi.org/10.1093/ajcn/71.2.621s]

-
Floyd, R. A. and Hensley, K. (2002) Oxidative stress in brain aging: implications for therapeutics of neurodegenerative diseases. Neurobiol. Aging 23: 795-807.
[https://doi.org/10.1016/S0197-4580(02)00019-2]

-
Pham-Huy, L. A., He, H. and Pham-Huy, C. (2008) Free radicals, antioxidants in disease and health. Int. J. Biomed. Sci. 4: 89-96.
[https://doi.org/10.59566/IJBS.2008.4089]

-
Wang, T., Liu, X. H., Guan, J., Ge, S., Wu, M. B., Lin, J. P. and Yang, L. R. (2019) Advancement of multi-target drug discoveries and promising applications in the field of Alzheimer’s disease. Eur. J. Med. Chem. 169: 200-223.
[https://doi.org/10.1016/j.ejmech.2019.02.076]

-
Maisuthisakul, P., Pongsawatmanit, R. and Gordon, M. H. (2007) Characterization of the phytochemicals and antioxidant properties of extracts from Teaw (Cratoxylum formosum Dyer). Food Chem. 100: 1620-1629.
[https://doi.org/10.1016/j.foodchem.2005.12.044]

- Jan, W. H., Tai, V. H., Yang, S. Y. and Kim, Y. H. (2017) Cholinesterase inhibitory compounds derived from the leaves of Cratoxylum formosum Dyer. Collect. Pap. Pharm. Sci. (Chungnam National University). 32: 55-60.
-
Choi, S. J., Tai, B. H., Cuong, N. M., Kim, Y. H. and Jang, H. D. (2012) Antioxidative and anti-inflammatory effect of quercetin and its glycosides isolated from mampat (Cratoxylum formosum). Food Sci. Biotechnol. 21: 587-595.
[https://doi.org/10.1007/s10068-012-0075-4]

-
Keowkase, R. and Weerapreeyakul, N. (2016) Cratoxylum formosum extract protects against amyloid-beta toxicity in a Caenorhabditis elegans model of Alzheimerʼs disease. Planta Med. 82: 516-523.
[https://doi.org/10.1055/s-0041-111621]

-
Senggunprai, L., Thammaniwit, W., Kukongviriyapan, V., Prawan, A., Kaewseejan, N. and Siriamornun, S. (2016) Cratoxylum formosum extracts inhibit growth and metastasis of cholangiocarcinoma cells by modulating the NF-kB and STAT3 pathways. Nutr. Cancer. 68: 328-341.
[https://doi.org/10.1080/01635581.2016.1142580]

- Alberts, B., Johnson, A., Lewis, J., Raff, M., Roberts, K. and Walter, P. (2002) Molecular biology of the cell, p833, Garland Science, New York.
-
Kang, J. Y., Park, S. K., Guo, T. J., Ha, J. S., Lee, D. S., Kim, J. M. and Heo, H. J. (2016) Reversal of trimethyltin-induced learning and memory deficits by 3, 5-dicaffeoylquinic acid. Oxid. Med. Cell Longev. 2016: 6981595.
[https://doi.org/10.1155/2016/6981595]

-
Sun, Y., Wang, X., Zhang, X., Li, Y., Wang, D., Sun, F. and Qing, G. (2024) Dicaffeoylquinic acid: a potential inhibitor for amyloid-beta aggregation. J. Nat. Med. 78: 1029-1043.
[https://doi.org/10.1007/s11418-024-01825-y]

- Xiao, H. B., Cao, X., Wang, L., Run, X. Q., Su, Y., Tian, C., Sun, S. G. and Liang, Z. H. (2011) 1, 5-dicaffeoylquinic acid protects primary neurons from amyloid β1-42-induced apoptosis via PI3K/Akt signaling pathway. Chin. Med. J. 124: 2628-2635.
-
Behl, C., Davis, J., Cole, G. M. and Schubert, D. (1992) Vitamin E protects nerve cells from amyloid β protein toxicity. Biochem. Biophys. Res. Commun. 186: 944-950.
[https://doi.org/10.1016/0006-291X(92)90837-B]

-
Butterfield, D. A. (2002) Amyloid β-peptide (1-42)-induced oxidative stress and neurotoxicity: implications for neurodegeneration in Alzheimer’s disease brain. A review. Free Radic. Res. 36: 1307-1313.
[https://doi.org/10.1080/1071576021000049890]
