
글루타메이트로 유발한 과흥분독성에 대한 청위산의 신경세포보호 및 항산화 효과
Abstract
Oxidative stress contributes to neuronal damage and neurodegenerative disease as Alzheimer’s disease (AD). While glutamate, a key neurotransmitter in the central nervous system, is fundamental to neuronal viability and normal brain function, its excessive accumulation leads to oxidative stress. In this study, we investigated the effect of Cheongwisan (CWS), as Korean medicine consist in 5 nature herbs, on glutamate-induced injury in HT22 cells and explored the underlying mechanism involved. Our results show that CWS significantly reduced neuronal cell death and apoptotic marker. Also, CWS has antioxidant effect, reducing reactive oxygen species (ROS) level and increasing antioxidant molecules as heme oxygenase-1 (HO1), NAD(P)H: quinone oxidoreductase 1 (NQO1). Western blot analysis revealed that CWS upregulated brain-derived neurotrophic factor (BDNF) and promoted the extracellular signal-regulated kinase (ERK), and cAMP response element binding protein (CREB), which were downregulated by glutamate. Furthermore, CWS promoted the translocation of nuclear factor erythroid 2-related factor 2 (NRF2) into the nuclear. Thus, CWS may protect hippocampal cells against glutamate-induced oxidative stress by activating the BDNF/ERK/CREB and ERK/NRF2 signaling pathways, suggesting its therapeutic potential for AD.
Keywords:
Cheongwisan, Excitotoxicity, Neuroprotect, Antioxidant, HT22 cell중추신경계(Central Nerve System) 내 주요 흥분성 신경전달물질인 글루타메이트는 신경세포의 생존과 정상적인 뇌기능에 필수적이다.1,2) 하지만 글루타메이트가 과다 분비될 경우 산화적 스트레스가 증가되어 신경흥분독성이 나타나 뇌신경세포 사멸로 이어질 수 있다.3) 산화적 스트레스의 증가는 체내 활성산소종의 과다 생성 및 항산화 시스템의 기능 저하에 의해 나타나며, 이는 알츠하이머병 등과 같은 중추신경계의 퇴행성 뇌질환이나 뇌졸중 등과 같은 뇌질환을 유발하는 중요한 요인으로 알려져 있다. 따라서 산화스트레스를 억제하는 것이 신경퇴행성 질환의 예방 및 치료에 유망한 전략이 될 수 있다.4)
HT22 세포주는 마우스 유래 해마조직 세포주로, 글루타메이트에 의한 과흥분독성을 유도하여 산화적 스트레스에 대한 연구를 하기 적합하다고 알려져 있다.5) 산화스트레스에 대한 방어 기전이 BDNF와 NRF2가 관여한다고 알려져 있다.6,7) 신경세포의 생존과 성장을 촉진하는 BDNF의 발현은 ERK/CREB의 신호전달에 의해 유도되며, BDNF 발현 증가하면 산화스트레스로부터 신경세포를 보호하여 신경퇴행성 질환의 위험을 완화하는 것으로 나타났다.8) 또한 NRF2는 HO-1, NQO1와 같은 다양한 항산화효소의 발현을 조절함으로써 산화스트레스로부터 세포를 보호한다.9) HT22 세포에도 HO-1의 상향 조절이 글루타메이트 유발 산화스트레스를 효과적으로 완화시킨다는 연구가 보고되었다.10,11)
청위산(Cheongwisan, CWS)은 승마, 목단피, 당귀, 생지황, 황련의 5종 한약재로 구성되었으며 구강 질환 치료에 흔히 사용되어지고 있는 기허가 한약제제이다. 청위산은 청위양혈(淸胃凉血)의 효능으로 위열(胃熱)에 의한 극심한 치통(齒痛)을 치료하며, 특히 잇몸이 붓고 아프며 피가 나는 증상인 치은염 및 출혈을 치료하기 위해 사용되어졌다.12,13) 또한, 청위산은 당뇨병성 구강통증 환자의 치료에 효과가 있다고 보고되었으며, 위장관, 피부, 해열 및 항염 등 다양한 계통에서 치료 효능을 가진다고 보고되었다.14-16) 최근 연구에서 이 청위산이 신경보호효과가 있을 수 있다는 논문이 보고되었지만,17) 알츠하이머 세포 모델에서의 효과와 그 분자적 기전을 아직 규명되지 않았다.
따라서, 본 연구에서는 HT22 세포주에서 청위산이 글루타메이트 유발 산화 스트레스에 대한 신경 보호 효과와 그 기저 메커니즘을 규명하고자 하였다.
재료 및 방법
청위산(CWS) 추출물 재료 준비 − 본연구에사용된청위산은 승마, 목단피, 당귀, 생지황, 황련의 5종 한약재로 구성되었으며, 모든 한약재는 휴먼허브(Human Herb, Daegu, Korea)에서 구입하였다. 대한민국 보건복지부 및 건강보험심사평가원(HIRA)에서 고시하는 건강보험 급여 한약제제의 표준 처방 규격을 따라 청위산 처방을 구성 및 배합하였다. 본 규격은 한국의 전통 임상 의서인 『방약합편(方藥合編)』에 근거하였다.18,19) 각 한약재는 배합 비율에 따라 혼합하여 총 중량이 130 g이 되도록 하였다. 준비된 혼합물에 10배량의 생수(1.3 L)를 가하여 상온에서 1시간 동안 침출시킨 후, 약탕기를 이용하여 약 100℃에서 3시간 동안 전탕추출을 수행하였다. 추출액은 여과지를 사용하여 여과한 후, 얻어진 여과액을 -80℃에서 냉동하였다. 이후 동결건조기를 이용하여 72시간 동안 감압 동결 건조를 실시하였다. 건조된 추출물은 분쇄하여미세분말형태로제조한후실험에사용하였다. 최종적으로 수득한 추출물의 중량은 13.82 g이었으며, 수득률은 10.63%로 산출되었다. 본 연구에 사용된 표본(KIOMAP-MH-021)은 한국한의학연구원 한의기술응용센터에서 보관 및 관리되고 있다. 청위산 구성 약재의 생약명, 생약 라틴명 및 배합비를 Table I에 제시하였다(Table I).
세포 배양 및 추출물 처리(Cell culture and drug treatment) − HT-22 세포는 L-글루타메이트가 배제된 Dulbecco’s Modified Eagle's Medium (DMEM, Hyclone)에서 배양되었으며, 10% 소태아혈청(fetal bovine serum), 스트렙토마이신(streptomycin, 100 µg/ml), 페니실린(penicillin, 100 unit/ml)를 배지에 혼합하여 사용하였다. 세포는 37℃와 CO2 농도가 5%로 일정하게 유지되는 배양기(incubator)에서 배양되었다. 추출물 처리는 세포에 24시간동안전처리하고, 그 후 5 mM 글루타메이트를 처리하여 실험은 대조군, 글루타메이트처리군, 청위산과 글루타메이트 혼합 처리군, 청위산 처리군으로 나누어 실시하였다. 글루타메이트는 멸균된 증류수에 녹여 사용하였다. 청위산은 글루타메이트 처리 24시간 전에 배지에 혼합하여 처리하였으며, 세포는 글루타메이트 처리 후 24시간 후에 수거하였다.
세포 생존율 측정(Measurements of of cell viability) − 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide (MTT) 시약을 사용하여 세포 생존율 분석을 수행하였다. 세포는 24시간 동안 96 well plate에서 배양되었으며, 청위산 처리 24시간 뒤, 글루타메이트(5 mM)를 처리하여 24시간 동안 배양하였다. MTT 용액(5 mg/ml)을 각 well에 첨가하여 빛이 차단된 상태에서 2시간 동안 MTT 용액으로 반응시킨 후 MTT 용액을 제거하였으며, DMSO (100 ul)를 첨가하여 용해시켰다. 용해된 현탁액은 ELISA 판독기를 사용하여 550 nm 파장에서 흡광도를 측정하였다. 세포 생존율은 대조군의 흡광도 값에 대한 각 실험군의 흡광도 값의 백분율로 평가되었다.
활성 산소종 분석(Reactive oxygen species assay) − 각 실험군의 ROS 값을 측정하기 위하여 세포를 37℃에서 1시간 동안 2′,7′-dichlorodihydrofluorescein diacetate (DCFH-DA, 5 mM)로 반응시켜 DCFH-DA를 형광산물 2′7′-dichlorofluorescein (DCF) 물로 전환하였고, 형광 DCF 수준을 484/530 nm의 파장에서 ELISA 판독기를 이용하여 흡광도를 측정하였다. 측정값은 대조군의 흡광도 값으로 나누어 백분율로 평가되었다.
Western blot 분석 − 수거한 세포는 RIPA buffer와 프로테아제 저해 칵테일을 함께 처리하여 균질화하였다. 동일한 양의 단백질을 10% SDS-PAGE를 이용해 분리하고, PVDF membrane에 transfer시켜 5% BSA를 사용하여 1시간 동안 blocking 시켰다. 그 후, 적합한항체들로 overnight시키고 PBST로 씻고 horseradish peroxidase로 이루어진 이차항체를 1시간 동안 배양시켰다. 단백질 밴드는 enhanced chemiluminescence system을 사용하여 사진을 찍었다. 결과는 β-actin으로 정량하여 대조군의 값으로 나누어 나타내었다.
통계 분석 − 각 실험 데이터는 평균 ± 표준 평균 오차 (S.E.M.)로 나타내었다. 실험자료의 분석은 Graph Pad 프로그램을 사용하였고, 정규성 검정은 One-way ANOVA를 실시하여 Turkey’s pos-hoc을 이용하여 유의성을 검증하였다. 통계적 유의 수준은 p<0.05로 하였다.
결 과
글루타메이트 처리에 의한 세포 손상에 대한 청위산의 신경세포 보호효과 − 청위산의 글루타메이트 유발 신경 독성에 대한 신경보호 효과를 알아보기 위해 세포생존율을 평가하였다. 먼저, Fig. 1A와 같이 청위산에 독성을 확인했을 때 청위산 1~25 μg/ml 농도에서 독성이 없음을 확인하였다. Fig. 1B와 같이 글루타메이트로 처리한 HT22 세포는 대조군에 비해 세포생존율이 유의성 있게 감소하였다. 청위산을 10~50 μg/ml 농도로 처리하였을때 세포생존율이 유의하게 개선되었다. 우리는 세포독성이 없고 세포생존율이 높아지는 10, 25 μg/ml 농도를 선택하여 Fig. 1C와 같이 세포 형태학적 관찰을 했을 때, 글루타메이트의 처리는 세포 모양의 수축, 수상돌기 손실, 핵 응축을 나타내었으며 세포의 수도 현저히 감소시켰다. 청위산의 투여는 글루타메이트로 인해 유발된 형태학적 변화를 완화시킴을 확인하였다. 이후 실험은 이 두 농도로 선택하여 실험하였다.
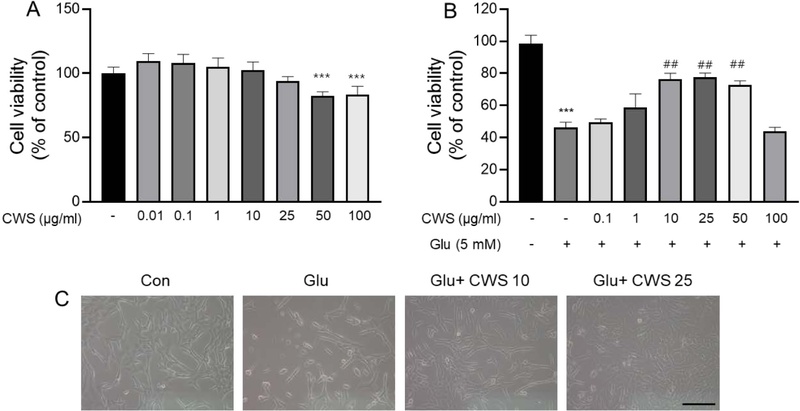
Neuroprotective effect of CWS on glutamate-induced cytotoxicity in HT22 cells. (A) HT-22 cells were treated with CWS for 24 h. (B) HT-22 cells were treated with CWS (0.1~100 μg) was treated 24 h before glutamate exposure. (C) Morphology of cells. CWS dose-dependently protects neural cells from glutamate toxicity. Data (n = ) are presented as means ± standard error of the means. Scale bars = 100 µm. ***p < 0.001, vs. Contol group; ##p < 0.01, vs. Glutamate group. CWS, Cheongwisan; Con, control; Glu, glutamate.
글루타메이트에 의한 아폽토시스(apoptosis) 대한 청위산의 보호 효과 − HT22 세포에 글루타메이트를 처리하면 아폽토시스가 증가한다고 알려져 있다. 이에 아폽토시스 관련 단백질인 caspase3, Bax, Bcl2의 발현을 확인하였다. Fig. 2와 같이 글루타메이트로 처리한 HT22 세포는 대조군에 비해 cleaved caspase3와 Bax의 발현은 증가하고 청위산 25 μg/ml을 처리하였을 때 유의적으로 감소시켰다. 또한, Bcl2의 발현은 글루타메이트를 처리에 의해 감소한 Bcl2 발현은 청위산 25 μg/ml 처리에 의해 유의적으로 증가하였다. 이상의 결과는 청위산이 글루타메이트에 의한 아폽토시스 세포사멸을 감소시켜 신경세포 보호효과를 나타냄을 확인할 수 있었다.
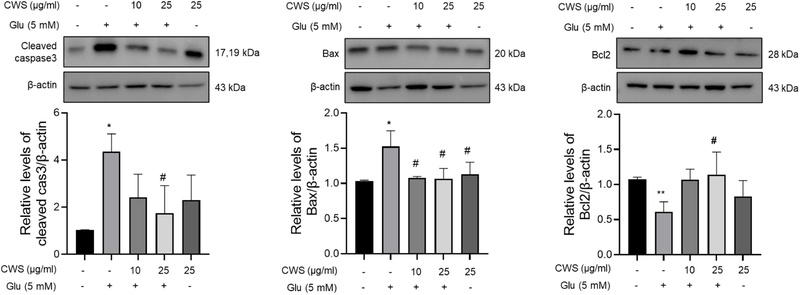
Antiapoptotic effects of CWS in glutamate-induced HT22 cells. Western blot of cleaved caspase3, Bax and Bcl2 in cells and results were normalized to β-actin. Data (n = 3) are presented as means ± standard error of the means. *p < 0.05, **p < 0.01, vs. Contol group; #p < 0.05, vs. Glutamate group. CWS, Cheongwisan; Con, control; Glu, glutamate.
글루타메이트에 의한 산화스트레스에 대한 청위산의 HO1, NQO1 발현 조절을 통한 항산화 효과 − 글루타메이트에 노출된 HT22 세포에서 청위산의 항산화 효과를 확인하기 위해서 활성산소종(ROS)를 확인하였다. Fig. 3A와 같이 글루타메이트에 노출된 세포는 ROS 발현을 증가시켰고, 청위산 처리는 농도의존적으로 증가된 ROS를 감소시켰다. 또한, 청위산의 항산화효과가 있다고 알려진 HO1, NQO1 발현에 미치는 영향을 조사했다. Fig. 3B와 같이 글루타메이트에 노출된 세포는 대조군에 비해 HO1, NQO1 발현이 유의적으로 증가하였다. 이상의 결과는 청위산이 글루타메이트에 의한 산화스트레스를 감소시키는 항산화효과가 있음을 확인할 수 있었다.
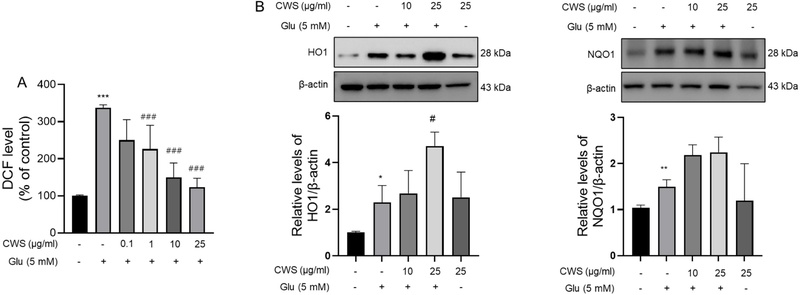
Antioxidant effects of CWS in glutamate-induced HT22 cells. (A) H2DCFDA fluorescence intensity. (B) Western blot of HO1 and NQO1 in cells and results were normalized to β-actin. Data (n = 3) are presented as means ± standard error of the means. *p < 0.05, **p < 0.01, ***p < 0.001 vs. Contol group; #p < 0.05, ###p < 0.001 vs. Glutamate group. CWS, Cheongwisan; Con, control; Glu, glutamate.
글루타메이트에 의한 신경 손상에 대한 청위산의 시냅스 가소성 향상 효과 − 글루타메이트에 의한 신경 손상에서 청위산의 신경 보호 효과에 BDNF/CREB/ERK 신호 전달 분자가 기여하는지 여부를 확인하기 위해 관련 단백질의 발현 및 인산화 수준을 조사했다. Fig. 4와 같이 글루타메이트 처리는 BDNF 발현와 CREB, ERK 인산화를 감소시켰다. 이에 청위산의 처리는 유의적으로 이를 향상시킴을 확인하였다. 이러한 결과는 청위산이 BDNF/CREB/ERK 신호 전달 분자의 활성화를 조절함으로써 신경보호효과를 가짐을 시사한다.
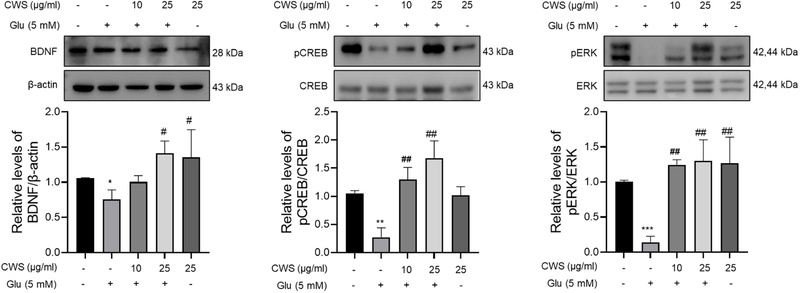
Effect of CWS on BDNF expression and the phosphorylation of CREB and ERK. Western blot and the expression levels of BDNF/β-actin, pCREB/CREB and pERK/ERK. Results were normalized to β-actin. Data (n = 3) are presented as means ± standard error of the means. *p < 0.05, **p < 0.01, ***p < 0.001 vs. Contol group; #p < 0.05, ##p < 0.01 vs. Glutamate group. CWS, Cheongwisan; Con, control; Glu, glutamate.
글루타메이트에 의한 신경 세포 손상에 대한 청위산의 NRF2 및 HO-1 효소 발현 조절 효과 − 글루타메이트에 노출된 HT22 세포에서 청위산의 항산화 효과가 NRF2, KEAP1 발현과 관련있음을 조사했다. Fig. 5A와 같이 전체 NRF2의 발현이 글루타메이트에 노출된 세포에서 대조군에 비해 증가하였고, 청위산 처리가 글루타메이트 노출된 세포보다 더 유의적으로 높게 증가하였다. Fig. 5B와 같이 핵 내 NRF2 발현도 글루타메이트 노출된 세포에서 대조군에 비해 핵 내 NRF2 발현이 증가하였고, 청위산 처리가 이보다 유의성 높게 증가하였다. 이러한 결과는 청위산은 NRF2의 핵 내 이동을 촉진하여 글루타메이트 유발 산화 스트레스를 억제함을 시사한다.
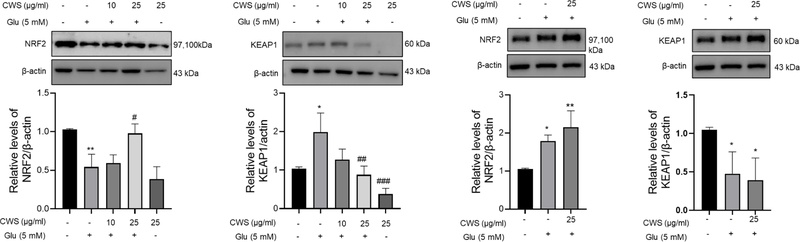
Effect of CWS on NRF2 and KEAP1 expression. Western blot and the expression levels of NRF2 and KEAP1 and results were normalized to β-actin. Data (n = 3) are presented as means ± standard error of the means. *p < 0.05, **p < 0.01 vs. Contol group; #p < 0.05, ##p < 0.01, ###p < 0.001 vs. Glutamate group. CWS, Cheongwisan; Con, control; Glu, glutamate.
고 찰
본 연구는 청위산(CWS)의 산화 스트레스에 의한 신경세포 보호 효과를 규명하였으며, 이러한 효과가 BDNF/ERK/CREB 및 NRF2/HO1, NQO1 신호전달 경로의 활성화를 통해 나타남을 확인하였다.
청위산은 위열(胃熱)을 내리고 혈액을 식히는 효능이 있어, 임상적으로 위열증후군으로 인한 구강궤양, 치주염, 구취 치료에 널리 사용되어 왔다.12-16) 그러나 청위산의 신경 보호 효과 및 그 기전에 관한 연구는 아직 보고된 바 없다.17) 글루타메이트(Glutamate)는 중추신경계의 주요 내인성 흥분성 신경전달물질로서 세포의 성장과 분화에 필수적이지만, 과도하게 증가할 경우 흥분 독성(Excitotoxicity)을 유발하여 신경세포 손상을 초래한다.5,20) 본 연구에서는 글루타메이트 유도 세포독성 및 산화 스트레스 연구에 널리 사용되는 생쥐 해마 신경세포주인 HT22 세포를 이용하여 청위산의 신경 보호 기전을 확인하고자 하였다.20) 실험 결과, 청위산은 글루타메이트에 의해 감소된 세포 생존율을 농도 의존적으로 회복시켰으며, 특히 25 ug과 50 ug 농도에서 가장 유의미한 효과를 나타냈다(Fig. 1). 또한, 형태학적 관찰에서 글루타메이트 처리는 세포 수축, 수상돌기 손실, 핵 응축을 유발했으나, 청위산 투여는 이러한 변화를 현저히 완화시켰다.
HT22 세포에 대한 글루타메이트 처리는 산화 스트레스를 유발하여 아팝토시스(Apoptosis)에 의한 세포사멸을 일으킨다.21) 이는 신경 손상의 주요 원인이며, 알츠하이머병 환자의 뇌에서도 증가된 산화 스트레스 수치가 관찰된다.22) 본 연구 결과, 청위산은 아팝토시스 관련 마커인 caspase-3, Bcl-2, Bax의 발현을 조절하고, ROS 생성을 억제하는 동시에 항산화 효소의 발현을 증가시켰다(Fig. 2, 3).
청위산의 신경 보호 효과를 뒷받침하는 주요 기전 중 하나는 ERK/CREB/BDNF 경로의 활성화이다. BDNF는 중추신경계 전반에서 신경세포의 생존을 촉진하는 핵심 신경영양인자로, 신경퇴행성 질환에서 보호적 역할을 수행하는 것으로 알려져 있다.23) BDNF는 MAPK 경로의 ERK를 활성화하고, 이는 다시 CREB의 인산화를 촉진하여 세포 생존 및 복구에 관여하는 다양한 유전자의 발현을 조절한다.24) 이전 연구에서는 ERK 매개 인산화가 CREB 활성화를 통해 BDNF 발현을 조절함이 밝혀진 바 있다.25) 본 연구 결과는 청위산이 글루타메이트에 노출된 HT22 세포에서 감소된 BDNF 수준을 회복시키고 ERK 및 CREB의 인산화를 증가시킴으로써, 산화 스트레스로부터 해마 신경세포를 보호함을 시사한다.
또한, 청위산은 ERK/NRF2 경로 활성화를 통해 HO1 및 NQO1과 같은 항산화 효소의 발현을 유도하였다. NRF2는 세포 내 산화환원 항상성 유지를 담당하는 전사 인자로, 산화 손상 방어 기전의 핵심이다.26) NRF2의 활성화는 하위 표적 유전자인 HO1과 NQO1의 발현을 직접 조절하여 활성산소를 제거하고 신경세포를 보호한다.3,27) 본 연구에서도 청위산이 NRF2의 핵 내 이동을 촉진하고 HO1, NQO1 발현을 증가시킴을 확인하였다.
결론적으로, 청위산은 ERK/CREB/BDNF 및 NRF2/HO1 신호전달 경로를 활성화함으로써 글루타메이트 유발 산화 스트레스 조건 하의 신경세포를 보호한다. 이러한 결과는 청위산이 신경퇴행성 질환의 진행을 예방하거나 완화할 수 있는 유망한 치료 후보 물질이 될 수 있음을 시사한다. 향후 생체 내(in vivo) 모델을 통한 추가적인 검증 연구가 필요할 것으로 판단된다.
Acknowledgments
이 논문은 정부(과학기술정보통신부, 보건복지부)의 재원으로 지원을 받아 수행된 연구결과임(KSN2413012, KSN2413011, HI23C1368).
References
-
Esposito, Z., Belli, L., Toniolo, S., Sancesario, G., Bianconi, C. and Martorana, A. (2013) Amyloid β, glutamate, excitotoxicity in Alzheimer's disease: are we on the right track?. CNS Neurosci. Ther. 19: 549-555.
[https://doi.org/10.1111/cns.12095]

-
Al-Nasser, M. N., Mellor, I. R. and Carter, W. G. (2022) Is L-Glutamate toxic to neurons and thereby contributes to neuronal loss and neurodegeneration? A Systematic Review. Brain Sci. 12: 577.
[https://doi.org/10.3390/brainsci12050577]

-
Song, J. H., Lee, H. J. and Kang, K. S. (2019) Procyanidin C1 activates the Nrf2/HO-1 signaling pathway to prevent glutamate-induced apoptotic HT22 cell death. Int. J. Mol. Sci. 20: 142.
[https://doi.org/10.3390/ijms20010142]

-
Lee, H. R., Jee, J. J. and Jung, Y. (2025) Neuroprotective effect of β-lapachone against glutamate-induced injury in HT22 cells. Biomol. Ther. 332: 286-296.
[https://doi.org/10.4062/biomolther.2024.241]

-
Fukui, M., Song, J. H., Choi, J., Choi, H. J. and Zhu, B. T. (2009). Mechanism of glutamate-induced neurotoxicity in HT22 mouse hippocampal cells. Eur. J. Pharmacol. 617: 1-11.
[https://doi.org/10.1016/j.ejphar.2009.06.059]

-
Johnson, J. A., Johnson, D. A., Kraft, A. D., Calkins, M. J., Jakel, R. J., Vargas, M. R. and Chen, P. C. (2008) The Nrf2-ARE pathway: an indicator and modulator of oxidative stress in neurodegeneration. Ann. N. Y. Acad. Sci. 1147: 61-69.
[https://doi.org/10.1196/annals.1427.036]

-
Yan, T., Mao, Q., Zhang, X., Wu, B., Bi, K., He, B. and Jia, Y. (2021) Schisandra chinensis protects against dopaminergic neuronal oxidative stress, neuroinflammation and apoptosis via the BDNF/Nrf2/NF-κB pathway in 6-OHDA-induced Parkinson’s disease mice. Food Funct. 12: 4079-4091.
[https://doi.org/10.1039/D0FO02836C]

-
Gao, L., Zhang, Y., Sterling, K. and Song, W. (2022) Brain-derived neurotrophic factor in Alzheimer’s disease and its pharmaceutical potential. Transl. Neurodegener. 11: 4.
[https://doi.org/10.1186/s40035-022-00279-0]

-
Alonso-Piñeiro, J. A., Gonzalez-Rovira, A., Sánchez-Gomar, I., Moreno, J. A. and Durán-Ruiz, M. C. (2021) Nrf2 and heme oxygenase-1 involvement in atherosclerosis related oxidative stress. Antioxidants (Basel) 10: 1463.
[https://doi.org/10.3390/antiox10091463]

-
Kim, H. J., Lim, S. S., Park, I. S., Lim, J. S., Seo, J. Y. and Kim, J. S. (2012) Neuroprotective effects of dehydroglyasperin C through activation of heme oxygenase-1 in mouse hippocampal cells. J. Agric. Food Chem. 60: 5583-5589.
[https://doi.org/10.1021/jf300548b]

-
Tang, G. H., Chen, Z. W., Lin, T. T., Tan, M., Gao, X. Y., Bao, J. M., Cheng, Z. B., Sun, Z. H., Huang, G. and Yin, S. (2015) Neolignans from Aristolochia fordiana prevent oxidative stress-induced neuronal death through maintaining the Nrf2/HO-1 pathway in HT22 cells. J. Nat. Prod. 78: 1894-1903.
[https://doi.org/10.1021/acs.jnatprod.5b00220]

- Heo, J. (2005) Donguibogam (Humanist Ed. & Trans.). Seoul, Korea: Humanist. (Original work published 1613).
- Xu GZ. (2010) Textual research on dose conversion of ancient and modern Chinese medicine. J. Tradit. Chin. Med. Lit. 28: 23-24.
-
Shi, L., An, Y., Cheng, L., Li, Y., Li, H., Wang, C., Lv, Y., Duan, Y., Dai, H., He, C., Zhang, H., Huang, Y., Fu, W., Wang, S., Zhao, B., Wang, Y. and Zhao, Y. (2022) Qingwei San treats oral ulcer subjected to stomach heat syndrome in db/db mice by targeting TLR4/MyD88/NF-κB pathway. Chin. Med. 17: 1.
[https://doi.org/10.1186/s13020-021-00565-5]

-
Li, H., Wang, C., Lyu, Y., Shi, L., He, C., An, Y., Zhang, H., Zhao, Y. and Zhao, B. (2023) Metabolomics characterization of Qingwei San on oral ulcer in db/db mice with stomach heat pattern. J. Tradit. Chin. Med. Sci. 10: 267-279.
[https://doi.org/10.1016/j.jtcms.2023.06.002]

- Meng, Y., Jiang, Z. T., Yan, G. J., Shen, J., Sun, K. P., Wang, Y. Y., Cao, J. N., Xia, M. Y. and Pan, J. H. (2022) Mechanism of Qingwei Powder in treatment of periodontitis based on UPLC-Q-TOF-MS, GC-MS, network pharmacology and molecular docking. China journal of Chinese materia medica 47: 2778-2787.
-
Seo, Y. K., Lee, J. Y., Oh, Y. C., Lee, J. J., Li, W., Jeong, Y. H., Lee, S. J., Go, Y. H. and Jung, I. C. (2019) Exploring the effective herbal prescription for cognitive disorder treatment among licensed herbal medicines in Korea - A preliminary study for clinical trial of cognitive disorders. J. Physiol. & Pathol. Korean Med. 33: 207-218.
[https://doi.org/10.15188/kjopp.2019.08.33.4.207]

- Hwang, D. Y. (1993) Bangyak-hapyeon [Formula and medicine combined] (M. G. Kang, Ed.). Namsandang.
- Ministry of Health and Welfare (2025) List of reimbursable herbal medicine preparations and upper limit prices. Ministry of Health and Welfare Notification No. 2025-175, Ministry of Health and Welfare, Sejong, Republic of Korea.
-
Nishizawa Y. (2001) Glutamate release and neuronal damage in ischemia. Life Sci. 69: 369-381.
[https://doi.org/10.1016/S0024-3205(01)01142-0]

-
Nicholls D. G. (2004) Mitochondrial dysfunction and glutamate excitotoxicity studied in primary neuronal cultures. Curr. Mol. Med. 4: 149-177.
[https://doi.org/10.2174/1566524043479239]

-
Huang, D., Chen, L., Ji, Q., Xiang, Y., Zhou, Q., Chen, K., Zhang, X., Zou, F., Zhang, X., Zhao, Z., Wang, T., Zheng, G. and Meng, X. (2024) Lead aggravates Alzheimer's disease pathology via mitochondrial copper accumulation regulated by COX17. Redox Biol. 69: 102990.
[https://doi.org/10.1016/j.redox.2023.102990]

-
Ibrahim, A. M., Chauhan, L., Bhardwaj, A., Sharma, A., Fayaz, F., Kumar, B., Alhashmi, M., AlHajri, N., Alam, M. S. and Pottoo, F. H. (2022) Brain-derived neurotropic factor in neurodegenerative disorders. Biomedicines 10: 1143.
[https://doi.org/10.3390/biomedicines10051143]

-
Zhen, W., Zhen, H., Wang, Y., Chen, L., Niu, X., Zhang, B., Yang, Z. and Peng, D. (2023) Mechanism of ERK/CREB pathway in pain and analgesia. Front. Mol. Neurosci. 16: 1156674.
[https://doi.org/10.3389/fnmol.2023.1156674]

-
Mao, X. Y., Cao, Y. G., Ji, Z., Zhou, H. H., Liu, Z. Q. and Sun, H. L. (2015) Topiramate protects against glutamate excitotoxicity via activating BDNF/TrkB-dependent ERK pathway in rodent hippocampal neurons. Prog. Neuropsychopharmacol. Biol. Psychiatry 60: 11-17.
[https://doi.org/10.1016/j.pnpbp.2015.01.015]

-
Bellezza, I., Giambanco, I., Minelli, A. and Donato, R. (2018) Nrf2-Keap1 signaling in oxidative and reductive stress. Biochim. Biophys. Acta Mol. Cell Res. 1865: 721-733.
[https://doi.org/10.1016/j.bbamcr.2018.02.010]

-
Baek, S. Y. and Kim, M. R. (2020) Neuroprotective effect of carotenoidrich enteromorpha prolifera extract via TrkB/Akt pathway against oxidative stress in hippocampal neuronal cells. Mar. Drugs 18: 372.
[https://doi.org/10.3390/md18070372]

