
Lucidenic acid A 고함량 녹각영지버섯 추출물의 피부 장벽 보호 및 Staphylococcus aureus 감염 억제 효과
Abstract
This study was conducted to evaluate the skin barrier enhancing effects and the potential to alleviate Staphylococcus aureus–associated skin disorders of an antler-shaped Ganoderma lucidum extract (AGL-E) enriched in lucidenic acid A (LAA). HPLC analysis revealed that the LAA content of AGL-E was 1.29%, approximately 14-fold higher than that of a conventional G. lucidum extract (0.09%). In HaCaT cells, MTT assays showed that AGL-E exhibited no cytotoxicity at concentrations up to 100 μg/mL, while LAA was non-cytotoxic at concentrations up to 50 μg/mL. Analysis of mRNA expression of skin barrier–related markers, including filaggrin (FLG), loricrin (LOR), and involucrin (IVL), demonstrated that AGL-E significantly upregulated FLG and LOR expression, suggesting its potential to enhance epidermal barrier formation through modulation of keratinocyte differentiation. In contrast, LAA significantly increased the expression of FLG and IVL, indicating its contribution to barrier-related functional enhancement. Furthermore, both AGL-E and LAA significantly suppressed S. aureus–induced secretion of pro-inflammatory cytokines, including IL-1β and TNF-α. In a S. aureus infection model labeled with CellTraceTM Far-red, treatment with AGL-E or LAA markedly reduced S. aureus-associated infection levels in keratinocytes, confirming their infection-inhibitory effects. Collectively, these findings suggest that AGL-E exerts multifunctional protective effects in skin environments characterized by barrier disruption and microbe-associated inflammation by modulating barrier-related differentiation markers and suppressing S. aureus–induced inflammatory and infectious responses, with LAA suggested as a contributing bioactive constituent.
Keywords:
Antler-type Ganoderma lucidum, Lucidenic acid A, Skin barrier, Anti-inflammatory, Anti-infection표피의 각질형성세포(keratinocyte)는 분화 과정을 거치며 장벽을 구성하는 핵심 인자의 발현을 조절함으로써 피부 항상성을 유지한다. 분화의 최종 단계에서 형성되는 각질층(stratum corneum)은 각질세포(corneocyte)와 세라마이드, 콜레스테롤, 유리 지방산 등으로 이루어진 층상 지질(lamellar lipid) 구조를 가지며, ‘벽돌과 시멘트(brick-and-mortar)’ 모델에 비유되는 견고한 장벽을 형성한다.1) 이와 같은 장벽 구조가 손상되면 transepidermal water loss (TEWL)가 증가하고, 외부 유해물질이나 미생물의 침입이 용이해져 피부염, 건조증, 아토피피부염 등의 피부 질환이 발생한다.2,3)
각질형성세포의 단계적 분화는 장벽 무결성(integrity)을 좌우한다. 특히 분화의 말기에 cornified envelope (CE)을 구성하는 대표 단백질인 filaggrin (FLG), loricrin (LOR), involucrin (IVL)이 발현·가교되어 각질층의 기계적 강도와 밀폐성을 확립한다.4,5) 이들 단백질은 상호 보완적으로 작용하며, 특히 FLG는 케라틴 필라멘트의 결합을 촉진하고 분해 산물이 천연보습인자의 전구체로 기능하여 수분 항상성을 유지한다.2,6,7) 더불어 LOR은 분화 말기에 대량 발현되는 CE의 주성분으로, transglutaminase 매개 교차결합과 이황화 결합을 통해 단단한 단백질 외막을 형성하여 각질층의 기계적 강도와 밀폐성을 높인다.4,5) 이러한 단백질 네트워크는 각질층의 기계적 안정성과 저투과성을 동시에 확보함으로써 피부 장벽 무결성을 유지한다.4-6,8,9) 한편 IVL은 분화 초기에 원형질막 내측에 먼저 축적되어 CE 형성의 기질(scaffold)로 작용하고, transglutaminase-1에 의해 교차 결합되어 견고한 단백질 외막의 토대를 마련한다.4,5) 그 결과 단백질 외막과 지질 라멜라가 연속된 저투과성 장벽 구조가 확립되며, 장벽 무결성과 내구성 향상에 기여한다.4-6) 따라서 FLG·LOR·IVL의 균형있는 상향은 장벽 구조의 안정화와 기능 회복에 핵심적이다.
장벽 손상은 단순한 수분 손실뿐 아니라 면역학적 방어 약화로 이어진다. 특히 손상된 장벽은 병원성 세균의 부착과 증식을 용이하게 하며, 그 중에서도 Staphylococcus aureus는 아토피피부염 환자의 피부에서 가장 흔하게 검출되는 병원균으로 알려져 있다.10,19) S. aureus는 각질세포에 부착하여 독소와 효소를 분비하고, IL-1β, IL-6, TNF-α 등 전염증성 사이토카인의 분비를 촉진해 피부 염증 반응을 증폭시킨다.10,13,14) 이러한 염증의 악순환은 장벽을 추가로 손상시키고,20) 재감염과 만성화로 이어질 수 있다. 또한 최근 연구들은 아토피피부염 환자에서 S. aureus의 과증식과 피부 마이크로바이옴 불균형이 질환의 악화와 밀접하게 연관됨을 보고하고 있다.11,12) 따라서 FLG, LOR, IVL과 같은 장벽 핵심 단백질의 발현을 강화하여 장벽의 구조적 무결성을 회복하는 것은, S. aureus의 부착·침입을 차단하고 후속 염증 반응을 근본적으로 억제하는 전략이 될 수 있다. 즉, “장벽 강화 → 세균 부착 감소 → 염증 완화”라는 인과적 기전은 피부 항상성 유지의 핵심 축이라 할 수 있으며, 이에 따라 장벽 강화 효능을 갖는 소재는 곧 항감염 및 항염 기능을 동반한 다기능성 후보로 평가될 수 있다.
동아시아 전통의학에서 영지버섯(Ganoderma lucidum)은 오래전부터 면역조절·항염·항산화 효능으로 활용되어 왔으며, 현대 연구에서도 triterpenoid와 polysaccharide 등 다양한 생리활성 성분이 보고되고 있다.15) 이 가운데 triterpenoid 계열 lucidenic acid는 NF-κB 신호 억제를 통한 항염 작용으로 주목받고 있으며16,17), 피부 염증 완화 소재로의 응용 가능성이 제시되고 있다. 특히 녹각영지버섯(antler-shaped Ganoderma lucidum)은 자실체가 뿔 모양을 이루는 변종으로, 일반 영지버섯과는 triterpenoid 조성 및 함량에서 차이를 보이는 것으로 알려져 있다.18) 그러나 현재까지 녹각영지버섯 추출물과 lucidenic acid A (LAA)가 각질형성세포의 장벽 단백질 발현 조절과 S. aureus 연관 염증·감염 반응에 미치는 영향을 통합적으로 분석한 연구는 거의 보고되지 않았다.
이에 본 연구에서는 lucidenic acid A를 고함량으로 함유한 녹각영지버섯 추출물을 이용하여 각질형성세포의 장벽 강화 효과를 평가하고, S. aureus 유도 염증 반응 및 감염 억제 효과를 종합적으로 분석하고자 하였다. 또한 순수 LAA를 병행 분석함으로써, 추출물 내 복합 성분의 시너지 효과와 단일 활성 성분의 기여도를 비교·검증하고자 하였다.
재료 및 방법
영지버섯 추출물 제조 − 본 실험에 사용한 일반 영지버섯과 녹각영지버섯은 각각 Geongangjungsim Co. Ltd. (Korea)와 ㈜위더스(Korea)에서 구입하여 사용하였다. 각 시료는 동일한 방법으로 추출하였다. 즉, 건조된 버섯에 70% 에탄올을 첨가하여 80℃에서 3 h 동안 가열 추출한 후, 여과를 통해 추출액을 회수하였다. 이후 잔사는 건조한 뒤 증류수를 첨가하여 80℃에서 3 h 동안 추가로 열수 추출하였다. 얻어진 추출액은 여과하여 잔사를 제거한 후 감압 농축기(Rotavapor® R-215, Switzerland)를 사용하여 농축하였고, 동결 건조기(TF-10D, Tefic Biotech Co., Ltd., China)로 분말화하였다. 이렇게 제조한 일반 영지버섯 추출물은 conventional Ganoderma lucidum extract (CGL-E)로, 녹각영지버섯 추출물은 antler-shaped Ganoderma lucidum extract (AGL-E)로 명명하여 실험에 사용하였다.
HPLC 분석 − AGL-E에 함유된 LAA를 정량분석하기 위해 HPLC (Waters 2695, Waters, USA)를 이용하였다. AGL-E와 CGL-E는 50 mg/mL 농도로 제조한 후 0.22 µm filter (Hyundai Micro, Korea)로 여과하여 분석에 사용하였다. 분리는 C18 column (Phenomenex Luna C18, 250 × 4.6 mm, 5.0 μm, Phenomenex, USA)을 사용하였으며, 이동상은 water (0.1% TFA) (A)와 acetonitrile (B)로 구성하였고, 검출은 255 nm에서 측정하였다. HPLC 분석은 이동상 B를 기준으로 한 구배 조건에서 수행하였으며, 구배 조건은 다음과 같다. 0 min: B (10%), 0~5 min: B (10%), 5~30 min: B (30%), 30~50 min: B (50%), 50~52 min: B (90%), 52~55 min: B (90%), 55~57 min: B (10%), 57~70 min: B (10%). 시료 주입량은 10 μL였으며, 표준물질로는 LAA (Sigma-Aldrich, USA)를 사용하였다.
세포주 및 세포 배양 − 인간 각질형성세포주인 HaCaT 세포(CLS Cell Lines Service GmbH, Germany)는 10% FBS (fetal bovine serum, Welgene, Korea)와 1% P/S (penicillin/streptomycin, Welgene)이 첨가된 DMEM (Welgene) 배지에 37℃, 5% CO2 incubator에서 배양하였다.
S. aureus 배양 − Staphylococcus aureus ATCC 12600 (American Type Culture Collection, USA)는 BHI (Brain Heart Infusion, Difco, USA) 배지에 접종 후 37℃, 24 h 동안 진탕 배양하여 종배양액으로 사용하였다. 이후 1% 종배양액을 본 배양 액체 배지에 접종하였고, 37℃에서 24 h 배양하였다.
세포생존율 평가 − 세포생존율은 3-(4,5-dimethylthiazil-2-yl)-2,5 diphenyltetrazolium bromide (MTT, Sigma-Aldrich) assay를 이용하여 확인하였다. 96-well plate에 HaCaT 세포를 2 × 104 cells/well이 되도록 seeding하고 37℃로 설정된 5% CO2 incubator에서 24 h 배양하였다. 이후 PBS (phosphate-buffered saline, Welgene)로 세척한 후, 새로운 DMEM 배지를 각 well에 100 μL를 넣고 AGL-E와 LAA를 농도별로 처리하여 37℃의 5% CO2 incubator에서 24 h 배양하였다. 배양 후 PBS를 이용해 2회 washing한 뒤, MTT를 처리하여 37℃에서 4 h 반응하였다. 생성된 MTT formazan dye를 DMSO (dimethyl sulfoxide, Deajung Chemicals & Metals Co. Ltd., Korea)로 녹인 뒤, microplate reader (Epoch, BioTek, USA)를 이용하여 흡광도 570 nm를 측정하였으며, control (medium only)의 흡광도 값을 기준으로 세포생존율을 비교하였다.
피부 장벽 관련 인자 발현 측정 − 6-well plate에 HaCaT 세포를 5 × 105 cells/well이 되도록 seeding하고 37℃로 설정된 5% CO2 incubator에서 24 h 배양하였다. 1% FBS가 포함된 DMEM 배지로 희석한 AGL-E와 LAA를 농도별로 첨가하여 24 h 동안 추가 배양하였다. 배양한 세포를 회수하여 TRIzolTM Reagent (Invitrogen, USA)를 이용하여 total RNA를 추출한 후, AccuPower® CycleScriptTM RT PreMix & Master Mix (Bioneer, Korea)를 이용하여 complementary DNA (cDNA)를 합성하였다. 합성한 cDNA로 AccuPower® 2 × GreenStarTM qPCR Master Mix (Bioneer)를 이용하여 실시간 중합효소연쇄반응(quantitative real-time polymerase chain reaction, qRT-PCR)을 수행하여 FLG, LOR, IVL mRNA 발현 정도를 측정하였다. qRT-PCR에 사용한 프라이머 서열은 다음과 같다 (Table I).
S. aureus 유도 염증 반응 억제 분석 − S. aureus로부터 유도된 사이토카인을 측정하기 위하여 12-well plate에 HaCaT 세포를 2.5 × 105 cells/well이 되도록 seeding하고 37℃로 설정된 5% CO2 incubator에서 24 h 배양하여 사용하였다. 이후 PBS를 이용해 2회 washing을 실시하였다. FBS와 P/S가 포함되지 않은 DMEM 배지를 사용하여 AGL-E와 LAA를 농도별로 희석한 뒤 S. aureus 100 MOI와 동시 처리하였다. 24 h 동안 배양한 후, 배양액을 수거하여 16,200 × g에서 10 min 원심분리 하였다. 분리된 상층액 내 사이토카인 함량은 ELISA kit (R&D system, USA)을 사용하여 측정하였으며, 이때 사이토카인의 농도는 kit에 포함되어 있는 표준용액으로부터 산출된 표준곡선으로부터 계산되었다.
형광 분석법을 이용한 S. aureus 억제 효능 분석 − HaCaT 세포와 S. aureus 공동 배양 환경에서 HaCaT 세포의 S. aureus 감염 억제 효과를 확인하기 위해 각각의 세포를 형광 염색을 실시하여 평가하였다. HaCaT 세포를 12-well plate에 2.5 × 105 cells/well이 되도록 seeding하고 24 h 배양 후 AGL-E와 LAA를 농도별로 처리하고 24 h 추가 배양하였다. 이후, CellTraceTM Far-red (C34572, Invitrogen)로 형광 표지한 S. aureus를 100 MOI로 처리하고 2 h 추가 배양한 후 Hoechst 33342 (H3570, Invitrogen) 형광 염색을 통해 HaCaT 세포의 핵을 염색하고 형광 현미경을 통해 세포 밀도 및 감염 정도를 확인하였다. 1 N NaOH로 HaCaT 세포를 회수하여 형광 광도계(Infinite 200 PRO, TECAN, Switzerland)를 이용하여 Far-red (Excitation: 620 nm, Emission: 665 nm) 및 Hoechst 33342 (Excitation: 320 nm, Emission: 535 nm)의 형광 정도를 측정하였다. Far-red 형광 신호는 Hoechst 33342 형광 신호를 이용하여 세포 수에 따른 보정을 진행하였고, 이를 통해 최종적인 감염 억제 효과를 평가하였다.
공초점 레이저 주사 현미경을 이용한 S. aureus 감염 억제 효능 분석 − 시료 처리에 따른 S. aureus의 감염 억제 효능을 공초점 레이저 주사 현미경(confocal laser scanning microscope, K1-Fluo, Nanoscope Systems, Korea)을 통한 형광 이미지로 분석하였다. 각 농도별로 시료가 전처리된 HaCaT 세포에 CellTraceTM Far-red로 표지된 S. aureus를 100 MOI로 처리하고 2 h 동안 감염을 유도하였다. 감염 종료 후 PBS로 3회 세척하여 감염 또는 부착되지 않은 균을 제거하였다. 이후 4% paraformaldehyde를 이용해 15 min간 고정한 뒤, Hoechst 33342로 HaCaT 세포의 핵을 염색하였다. 모든 시료는 동일한 레이저 출력 및 Gain 조건에서 이미지를 획득하였으며, Far-red 신호의 강도 및 분포를 기준으로 시료의 S. aureus 감염 억제 효과를 비교 분석하였다.
통계 분석 − 모든 실험은 3회 이상 반복 실시하였으며, 사용된 모든 데이터는 평균 ± 표준편차(mean ± standard deviation)로 나타내었다. 통계 분석은 GraphPad Prism software (version 9.x, GraphPad Software, San Diego, CA, USA)를 사용하여 수행하였다. 두 군 간 비교는 unpaired two-tailed Student’s t-test를 이용하여 분석하였으며, p < 0.05 일 때 통계적으로 유의한 것으로 판단하였다.
결과 및 고찰
지표성분 함량 분석 − AGL-E와 CGL-E의 LAA 함량을 비교하기 위하여 HPLC 정량분석을 수행하였다. Ganoderma 속 버섯에는 triterpenoids를 포함한 다양한 triterpenoid 대사산물이 존재하며, 이들 성분은 생리활성과 함께 주요 품질지표로 활용될 수 있음이 보고되어 있다.17) 본 연구에서는 AGL-E와 CGL-E 내 LAA를 지표성분으로 설정하고 그 함량을 정량적으로 비교하였다. 표준물질 반복 분석 결과 상대표준편차(% RSD)는 0.69%로 나타나 분석법의 정밀도가 확보되었음을 확인하였다. 또한 시료에 대한 3회 반복 분석(n = 3)을 수행한 결과, AGL-E와 CGL-E 모두에서 LAA 표준물질과 동일한 유지시간의 피크가 검출되었다(Fig. 1A-C). LAA 함량은 AGL-E에서 1.290 ± 0.007%, CGL-E에서 0.090 ± 0.001%로 나타나, AGL-E가 CGL-E보다 약 14배 높은 LAA 함량을 갖는 것으로 확인되었다(Fig. 1D).
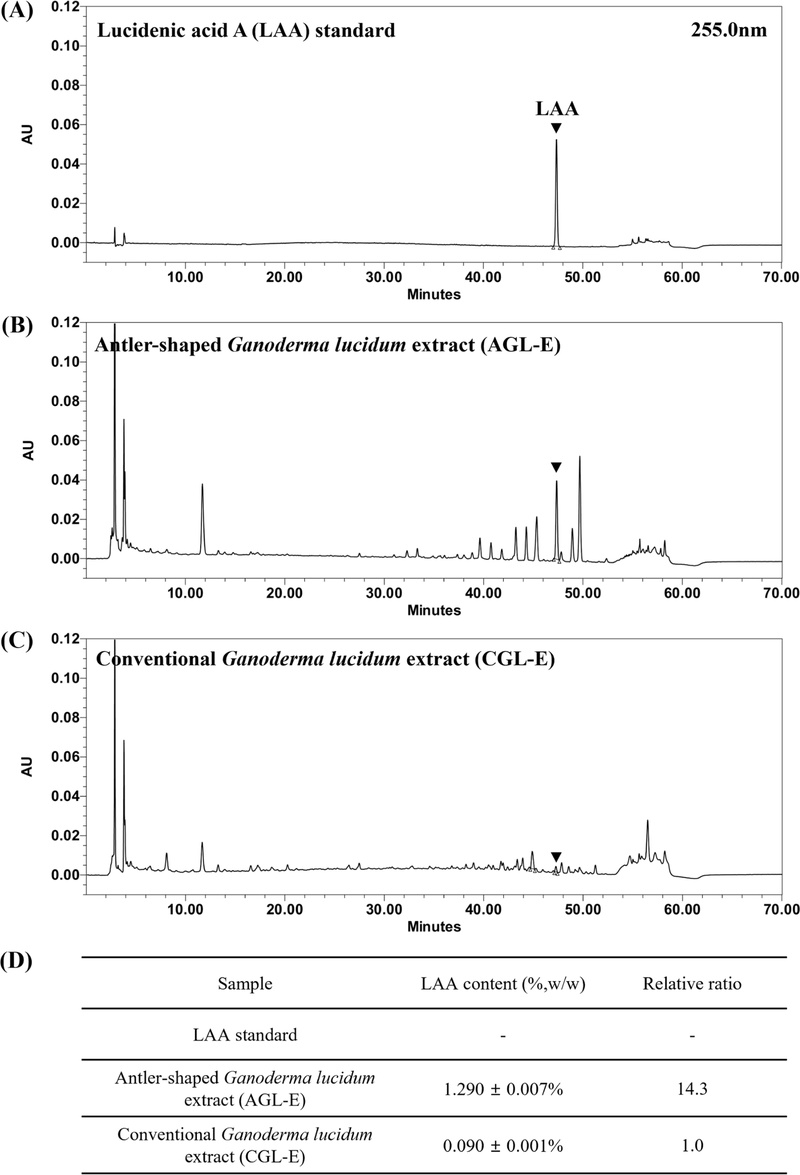
HPLC chromatograms of (A) LAA standard, (B) AGL-E, and (C) CGL-E, and (D) quantitative analysis of LAA content in AGL-E and CGL-E by HPLC (n=3). The major peak corresponding to LAA was identified based on its retention time and UV spectral pattern compared with the reference standard. HPLC, high-performance liquid chromatography; LAA, lucidenic acid A; AGL-E, antler-shaped Ganoderma lucidum extract; CGL-E, conventional Ganoderma lucidum extract.
AGL-E 및 LAA의 세포 생존에 미치는 영향 − 피부 생리 활성 평가를 위한 적정 처리 농도를 설정하기 위해 HaCaT 세포에서 MTT assay를 수행하였다. AGL-E를 10, 20, 50, 및 100 μg/mL 처리한 결과, 세포 생존율은 각각 98 ± 1.18%, 97 ± 1.10%, 96 ± 1.25%, 및 94 ± 2.22%로 나타났으며, 대조군(100 ± 1.05%) 대비 전 농도에서 유의한 세포독성은 관찰되지 않았다(Fig. 2A). 반면, LAA 처리군에서는 동일 농도에서 각각 87 ± 1.50%, 85 ± 0.70%, 82 ± 1.70%, 및 75 ± 1.50%의 세포 생존율을 보였다. 50 μg/mL까지는 세포 생존율이 80% 이상으로 유지되었으나, 100 μg/mL에서는 80% 이하로 감소하여 경미한 세포독성이 확인되었다(Fig. 2B). 이에 따라 후속 실험은 LAA의 경우 50 μg /mL 이하, AGL-E의 경우 100 μg/mL 이하의 농도 범위에서 수행하였다.
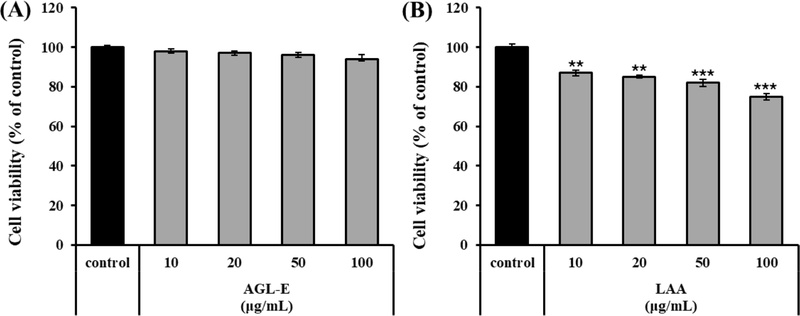
Cell viability of AGL-E and LAA in HaCaT cells. Cells were exposed to (A) AGL-E (10, 20, 50, and 100 μg/mL) or (B) LAA (10, 20, 50, and 100 μg/mL) for 24 h, and cell viability was determined using an MTT assay. All results are expressed as the mean ± standard deviation of triplicate experiments. AGL-E, antler-shaped Ganoderma lucidum extract; LAA, lucidenic acid A; MTT, 3-(4,5-dimethylthiazolyl-2-yl)-2,5-diphenyltetrazolium bromide.
AGL-E 및 LAA가 각질형성세포에서 피부 장벽 관련 인자의 mRNA 발현에 미치는 영향 − 본 연구에서 HaCaT 세포에 AGL-E와 그 지표 성분인 LAA를 농도별로 처리한 후, 피부 장벽 관련 인자인 FLG, LOR, IVL mRNA 발현에 미치는 영향을 분석하였다(Fig. 3). 이들은 각질세포의 분화 및 cornified envelope 형성에 필수적인 핵심 마커로서, 이들의 감소는 건조증·장벽 손상·염증 악화를 초래하는 것으로 알려져 있어1-3) 장벽 개선 기능성 평가의 중요한 기준이 된다. HaCaT 세포에 AGL-E를 처리한 결과, FLG 발현은 100 μg/mL에서 대조군 대비 3.67배로 통계적으로 유의하게 증가하였으며(Fig. 3A), LOR 발현 또한 동일 농도에서 3.50배로 유의한 증가를 나타냈다(Fig. 3B). 반면, IVL 발현에서는 AGL-E 처리에 따른 통계적으로 유의한 변화가 관찰되지 않았다(Fig. 3C). 이 결과는 AGL-E가 100 μg/mL에서 FLG와 LOR 발현을 선택적으로 증강시켜, keratinocyte 분화 후반부의 CE 형성과 피부 장벽 강화에 기여할 수 있음을 시사한다. LAA 처리군에서는 FLG 발현이 50 μg/mL에서 대조군 대비 2.42배로 증가하였으며(Fig. 3D), IVL 발현 역시 동일 농도에서 1.66배로 통계적으로 유의한 증가를 보였다(Fig. 3F). 그러나 LOR 발현에서는 LAA 처리에 따른 유의한 변화가 확인되지 않았다(Fig. 3E). 이러한 결과는 LAA가 각질형성세포 분화와 관련된 일부 장벽 유전자 발현을 조절할 수 있음을 보여준다. 한편, 본 연구에서 사용된 LAA의 처리 농도는 AGL-E 내 LAA 함량 (약 1.26% w/w)을 고려할 때 상대적으로 높은 수준으로, AGL-E와 LAA 간의 정량적 비교에는 제한이 있다. 따라서 본 결과는 LAA가 AGL-E의 생리활성에 부분적으로 기여할 가능성을 시사하는 것으로 해석된다.
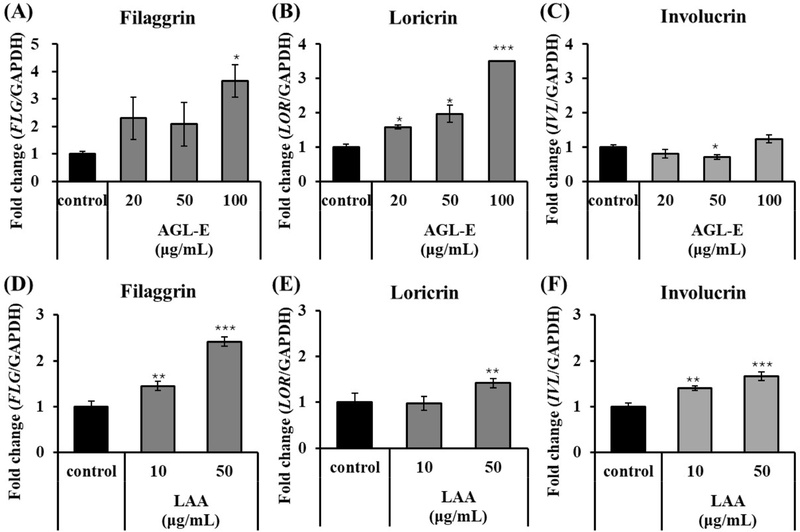
Effects of AGL-E and LAA on skin barrier-related gene expression in HaCaT cells. Cells were treated with AGL-E (20, 50, and 100 μg/mL) (A–C) or LAA (10 and 50 μg/mL) (D–F) for 24 h. The mRNA expression levels of FLG, LOR, and IVL were analyzed by qRT-PCR. All results are expressed as the mean ± standard deviation of triplicate experiments. AGL-E, antler-shaped Ganoderma lucidum extract; LAA, lucidenic acid A; FLG, filaggrin; LOR, loricrin; IVL, involucrin; qRT-PCR, quantitative real-time polymerase chain reaction. *p<0.05, **p<0.01, ***p<0.001 versus control.
AGL-E 및 LAA의 S. aureus 유도염증반응억제효과 − S. aureus 자극은 HaCaT 세포에서 IL-1β 및 TNF-α 분비를 유의하게 증가시켜, 세균성 자극에 의한 keratinocyte의 선천면 역반응 활성화를 확인하였다(Fig. 4). S. aureus 단독 처리군을 100%로 설정하여 비교한 결과, AGL-E 처리 시 IL-1β 생성은 20, 50, 100 μg/mL에서 각각 56.48 ± 1.02%, 59.95 ± 1.59%, 61.56 ± 1.26% 감소하여 모든 농도에서 유의한 억제 효과를 나타냈다(Fig. 4A). TNF-α 또한 AGL-E 20, 50, 100 μg/mL에서 각각 34.38 ± 5.82%, 67.54 ± 3.22%, 74.45 ± 4.03% 감소하여 농도 의존적인 억제 경향을 보였다(Fig. 4B). LAA 단독 처리에서도 IL-1β 생성은 10 및 50 μg/mL에서 각각 66.87 ± 3.27% 및 72.87 ± 4.85% 감소하여 뚜렷한 억제 효과가 확인되었다(Fig. 4C). 반면 TNF-α의 경우, 50 μg/mL에서만 35.09 ± 0.75% 감소가 관찰되어 AGL-E 대비 상대적으로 제한적인 억제 효과를 나타냈다(Fig. 4D). 이러한 결과는 LAA가 AGL-E의 항염 효과를 부분적으로 설명할 수 있는 bioactive marker임을 시사하며, 특히 IL-1β 억제에서 유의한 기여를 하는 것으로 판단된다. 나아가 AGL-E에서 TNF-α 억제 효과가 보다 두드러지게 나타난 점은, LAA 외에도 triterpenoid 계열의 공존 성분들이 복합적으로 작용하여 전체 추출물 수준에서의 항염 활성을 강화했을 가능성을 제시한다.10,21) 이는 AGL-E가 S. aureus 유도 keratinocyte 염증 반응을 조절하는 데 유효한 천연 유래 소재가 될 수 있음을 뒷받침한다.
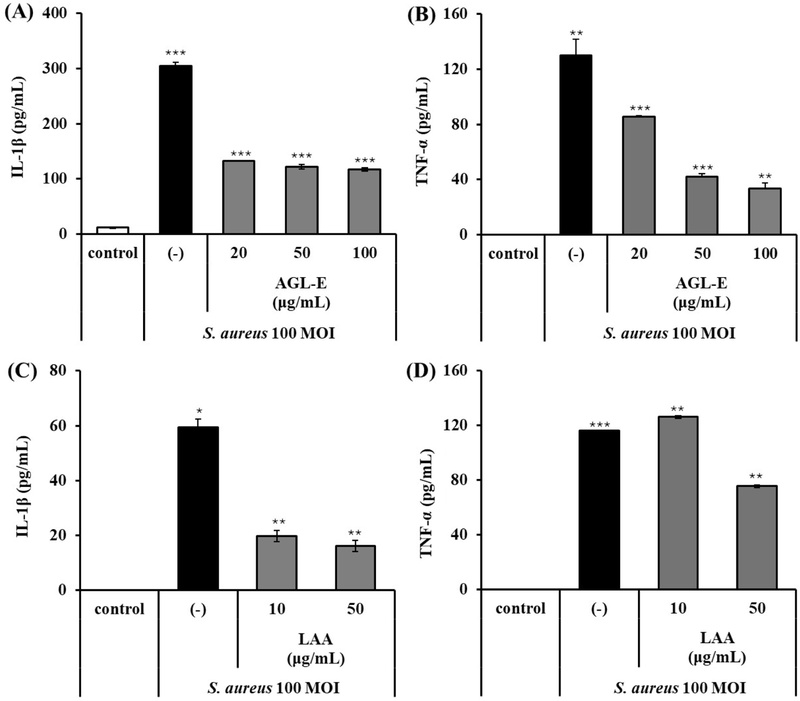
Inhibitory effects of AGL-E and LAA on S. aureus-induced pro-inflammatory cytokine production in HaCaT cells. Cells were stimulated with S. aureus (MOI=100) for 24 h in the absence or presence of AGL-E (20, 50, 100 μg/mL) or LAA (10, 50 μg/mL). Levels of IL-1β and TNF-α in culture supernatants were measured by ELISA. (A) IL-1β and (B) TNF-α levels following AGL-E treatment; (C) IL-1β and (D) TNF-α levels following LAA treatment. All results are expressed as the mean ± standard deviation of triplicate experiments. “control” indicates cells not infected with S. aureus, whereas “(–)” indicates S. aureus-treated cells without sample treatment. AGL-E, antler-shaped Ganoderma lucidum extract; LAA, lucidenic acid A; ELISA, enzyme-linked immunosorbent assay. *p<0.05, **p<0.01, ***p<0.001 versus S. aureus-treated control.
AGL-E 및 LAA의 S. aureus 감염 억제 효과 − Far-red로 표지된 S. aureus (MOI = 100)를 HaCaT 세포에 감염시킨 결과, 무처리 대조군 대비 Far-red/Hoechst 33342 비율이 현저히 증가하여 각질형성세포에 대한 감염이 효과적으로 유도됨을 확인하였다(Fig. 5). 이러한 결과는 S. aureus가 피부에서 감염 및 염증 반응을 유도한다는 기존 보고와 일치한다.10,12) S. aureus 단독 처리군을 100%로 설정하여 비교한 결과, AGL-E 처리 시 감염 수준은 20, 50, 100 μg/mL에서 각각 82.37 ± 1.08%, 76.22 ± 1.61%, 74.63 ± 7.16%로 유의하게 감소하여 농도 의존적인 억제 경향을 나타냈다(Fig. 5A). LAA 처리군에서도 10 및 50 μg/mL에서 각각 79.95 ± 0.11% 및 75.70 ± 2.03%로 감소하여 단일 성분으로도 감염 억제 효과가 확인되었다(Fig. 5B). 공초점 레이저 주사 현미경 분석 결과, 무처리 대조군(Fig. 6A)에서는 Far-red 신호가 거의 관찰되지 않은 반면, S. aureus 감염군(Fig. 6B)에서는 HaCaT 세포 주변에 Far-red 신호가 뚜렷하게 증가하여 세균의 부착 및 분포가 현저히 증가한 양상이 확인되었다. AGL-E 처리군에서는 20, 50, 100 μg/mL에서 각각 Far-red 신호가 점차 감소하는 경향을 보였으며(Fig. 6C–E), 특히 100 μg/mL 처리군(Fig. 6E)에서 가장 뚜렷한 감소가 관찰되었다. 또한 LAA 50 μg/mL 처리군(Fig. 6F)에서도 감염군 대비 Far-red 신호의 강도와 분포가 감소하여 S. aureus 감염 억제 효과가 시각적으로 확인되었다. 이러한 결과는 Fig. 5의 정량적 형광 분석 결과를 시각적으로 뒷받침하며, AGL-E 및 LAA가 S. aureus의 keratinocyte 부착 또는 초기 감염 과정에 영향을 미쳐 세포와의 상호작용을 감소시켰을 가능성을 시사한다. 특히 AGL-E에서 보다 일관된 억제 경향이 관찰된 점은, 단일 성분 대비 복합 성분 조합에 의해 감염 억제 효과가 확장 될 수 있음을 보여준다. 나아가 이러한 감염 억제 양상은, 앞서 확인된 염증성 사이토카인 감소 결과와 함께 고려할 때, S. aureus에 의해 유도되는 피부 염증 반응의 완화와 연관될 가능성을 뒷받침한다.10-13)
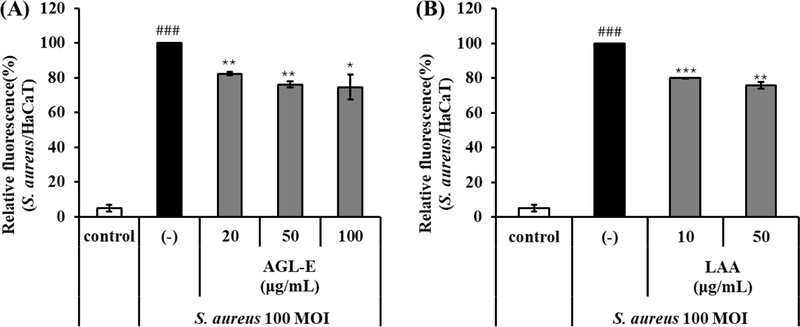
Inhibitory effects of AGL-E and LAA on S. aureus infection in HaCaT cells. Cells were infected with Far-red-labeled S. aureus (MOI=100) and treated with (A) AGL-E (20, 50, 100 μg/mL) or (B) LAA (10, 50 μg/mL) for 24 h. Cell nuclei were stained with Hoechst 33342, and infection levels were quantified as the ratio of Far-red fluorescence to Hoechst 33342 fluorescence. All results are expressed as the mean ± standard deviation of triplicate experiments. “control” indicates S. aureus-untreated cells, and “(–)” indicates S. aureus-treated cells without sample treatment. AGL-E, antler-shaped Ganoderma lucidum extract; LAA, lucidenic acid A. ###p<0.001 versus S. aureus-untreated control. *p<0.05, **p<0.01, ***p<0.001 versus S. aureus-treated control.
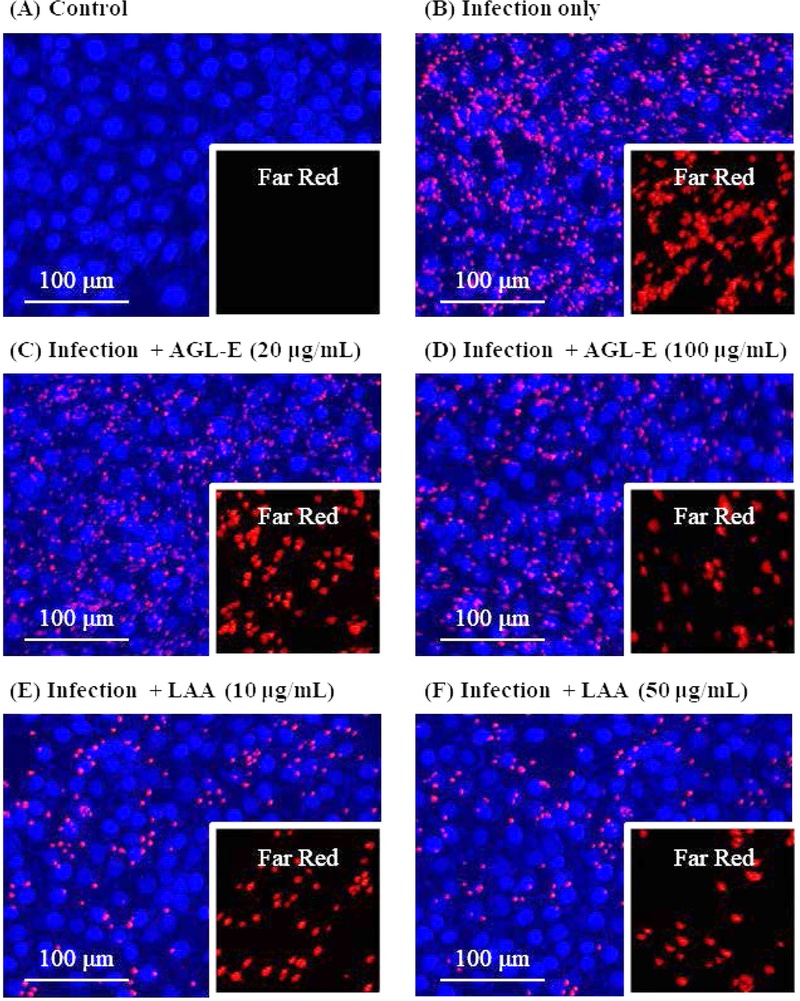
Confocal microscopy analysis of the inhibitory effects of AGL-E and LAA on S. aureus infection in HaCaT cells. (A) control (uninfected). (B) S. aureus-infected HaCaT cells (MOI = 100). (C, D) S. aureus-infected HaCaT cells treated with AGL-E at 20 μg/mL and 100 μg/mL. (E, F) S. aureus-infected HaCaT cells treated with LAA at 10 μg/mL and 50 μg/mL. Scale bar = 100 μm.
결 론
본 연구는 LAA를 고함량으로 함유한 AGL-E의 피부 장벽 보호 및 S. aureus 관련 피부 문제 개선 가능성을 종합적으로 평가하고, 이를 통해 복합 피부 개선 기능성 소재로서의 활용 가능성을 검토하고자 수행되었다. 그 결과, AGL-E는 HaCaT 세포에서 피부 장벽 형성과 밀접하게 연관된 분화 인자의 발현을 조절함으로써 장벽 강화에 기여할 수 있음을 확인하였다. 또한 S. aureus에 의해 유도되는 염증성 사이토카인 반응을 효과적으로 억제하였으며, 세균 감염 수준을 유의하게 감소시켜 병원성 미생물에 의한 피부 손상 완화 가능성을 제시하였다. 종합적으로, AGL-E는 피부 장벽 약화, 미생물 감염 및 염증 반응이 상호 연관되어 악화되는 피부 환경에서 장벽 보호와 염증·감염 조절을 동시에 수행할 수 있는 잠재력을 지닌 소재로 판단된다. 한편, 본 연구에서 확인된 LAA의 생리활성은 AGL-E의 효능에 부분적으로 기여할 가능성을 시사하나, 단독 처리에 사용된 농도는 AGL-E 내 실제 함량 범위를 초과하므로 추출물 내 역할을 정량적으로 직접 반영하는 것으로 해석하는 데에는 한계가 있다. 따라서 본 결과는 LAA를 AGL-E의 활성에 기여할 수 있는 지표 성분 중 하나로 제시하는 수준에서 이해하는 것이 타당하며, AGL-E의 전체 효능은 공존하는 다양한 성분들의 복합적 작용에 의해 발현될 가능성이 높다. 향후에는 AGL-E 내 실제 LAA 함량 범위에 상응하는 농도 조건에서 추가 검증과 함께, 주요 공존 성분들의 기여도 및 세포 내 신호전달 기전을 보다 정밀하게 규명할 필요가 있다. 또한 3차원 피부 모델 및 인체적용시험을 통해 실제 피부 환경에서의 유효성과 안전성을 검증한다면, AGL-E는 S. aureus 연관 피부 염증, 장벽 손상 피부 및 민감성 피부 개선을 위한 복합 기능성 화장품 소재로 활용될 수 있을 것으로 판단된다.
Acknowledgments
이 논문은 2025년도 중소벤처기업부의 기술개발사업 지원에 의한 연구입니다(S3275648).
References
-
Elias, P. M. (2005) Stratum corneum defensive functions: an integrated view. J. Invest. Dermatol. 125: 183-200.
[https://doi.org/10.1111/j.0022-202X.2005.23668.x]

-
Kezić, S. and Jakasa, I. (2016) Filaggrin and skin barrier function. Curr. Probl. Dermatol. 49: 1-7.
[https://doi.org/10.1159/000441539]

-
Engebretsen, K. A. and Thyssen, J. P. (2016) Skin barrier function and allergens. Curr. Probl. Dermatol. 49: 90-102.
[https://doi.org/10.1159/000441548]

-
Kalinin, A., Marekov, L. N. and Steinert, P. M. (2001) Assembly of the epidermal cornified cell envelope. J. Cell Sci. 114: 3069-3070.
[https://doi.org/10.1242/jcs.114.17.3069]

-
Candi, E., Schmidt, R. and Melino, G. (2005) The cornified envelope: a model of cell death in the skin. Nat. Rev. Mol. Cell Biol. 6: 328-340.
[https://doi.org/10.1038/nrm1619]

-
Dębińska, A. (2021) New treatments for atopic dermatitis targeting skin barrier repair via the regulation of FLG expression. J. Clin. Med. 10: 2506.
[https://doi.org/10.3390/jcm10112506]

-
Sandilands, A., Sutherland, C., Irvine, A. D. and McLean, W. H. I. (2009) Filaggrin in the frontline: role in skin barrier function and disease. J. Cell Sci. 122: 1285-1294.
[https://doi.org/10.1242/jcs.033969]

-
Furue, M., Tsuji, G., Mitoma, C., Nakahara, T., Chiba, T., Morino-Koga, S. and Uchi, H. (2015) Gene regulation of filaggrin and other skin barrier proteins via aryl hydrocarbon receptor. J. Dermatol. Sci. 80: 83-88.
[https://doi.org/10.1016/j.jdermsci.2015.07.011]

-
Furue, M. (2020) Regulation of filaggrin, loricrin, and involucrin by IL-4, IL-13, IL-17A, IL-22, aryl hydrocarbon receptor, and NRF2: pathogenic implications in atopic dermatitis. Int. J. Mol. Sci. 21: 5382.
[https://doi.org/10.3390/ijms21155382]

-
Miller, L. S. and Cho, J. S. (2011) Immunity against Staphylococcus aureus cutaneous infections. Nat. Rev. Immunol. 11: 505-518.
[https://doi.org/10.1038/nri3010]

-
Kong, H. H., Oh, J., Deming, C., Conlan, S., Grice, E. A., Beatson, M. A., Nomicos, E., Polley, E. C., Komarow, H. D., Murray, P. R., Turner, M. L. and Segre, J. A. (2012) Temporal shifts in the skin microbiome associated with disease flares and treatment in children with atopic dermatitis. Genome Res. 22: 850-859.
[https://doi.org/10.1101/gr.131029.111]

-
Nakamura, Y., Oscherwitz, J., Cease, K. B., Chan, S. M., Muñoz-Planillo, R., Hasegawa, M., Villaruz, A. E., Cheung, G. Y., McGavin, M. J., Travers, J. B., Otto, M., Inohara, N. and Núñez, G. (2013) Staphylococcus δ-toxin induces allergic skin disease by activating mast cells. Nature 503: 397-401.
[https://doi.org/10.1038/nature12655]

-
Olaru, F. and Jensen, L. E. (2010) Chemokine expression by human keratinocyte cell lines after activation of Toll-like receptors. Exp. Dermatol. 19: e314-e316.
[https://doi.org/10.1111/j.1600-0625.2009.01026.x]

-
Lowes, M. A., Bowcock, A. M. and Krueger, J. G. (2007) Pathogenesis and therapy of psoriasis. Nature 445: 866-873.
[https://doi.org/10.1038/nature05663]

- Lin, Z. B. and Zhang, H. N. (2004) Anti-tumor and immunoregulatory activities of Ganoderma lucidum and its possible mechanisms. Acta Pharmacol. Sin. 25: 1387-1395.
-
Xu, J. W., Zhao, W. and Zhong, J. J. (2010) Biotechnological production and application of ganoderic acids. Appl. Microbiol. Biotechnol. 87: 457-466.
[https://doi.org/10.1007/s00253-010-2576-5]

-
Galappaththi, M. C. A., Patabendige, N. M., Premarathne, B. M., Hapuarachchi, K. K., Tibpromma, S., Dai, D.-Q., Suwannarach, N., Rapior, S. and Karunarathna, S. C. (2023) A review of Ganoderma triterpenoids and their bioactivities. Biomolecules 13: 24.
[https://doi.org/10.3390/biom13010024]

-
Watanabe, K., Shuto, T., Sato, M., Onuki, K., Mizunoe, S., Suzuki, S., Sato, T., Koga, T., Suico, M. A., Kai, H. and Ikeda, T. (2011) Lucidenic acids-rich extract from antlered form of Ganoderma lucidum enhances TNF-α induction in THP-1 monocytic cells possibly via its modulation of MAP kinases p38 and JNK. Biochem. Biophys. Res. Commun. 408: 18-24.
[https://doi.org/10.1016/j.bbrc.2011.03.108]

-
Ngo, Q. V., Faass, L., Sähr, A., Hildebrand, D., Eigenbrod, T., Heeg, K. and Nurjadi, D. (2022) Inflammatory response against Staphylococcus aureus via intracellular sensing of nucleic acids in keratinocytes. Front. Immunol. 13: 828626.
[https://doi.org/10.3389/fimmu.2022.828626]

-
Kim, J., Kim, B. E., Berdyshev, E., Bronova, I., Bin, L., Bae, J., Kim, S., Kim, H.-Y., Lee, U. H., Kim, M. S., Kim, H., Lee, J., Hall, C. F., Hui-Beckman, J., Chang, Y., Bronoff, A. S., Hwang, D., Lee, H.-Y., Goleva, E., Ahn, K. and Leung, D. Y. M. (2023) Staphylococcus aureus causes aberrant epidermal lipid composition and skin barrier dysfunction. Allergy 78: 1292-1306.
[https://doi.org/10.1111/all.15640]

-
Bauernfried, S., Komar, T., Sterle, K., Tanzer, M. C., Horswill, A. R., Mann, M. and Hornung, V. (2025) Inflammasome-independent IL-1β activation via staphopain A protease of Staphylococcus aureus. J. Biol. Chem. 301: 110574.
[https://doi.org/10.1016/j.jbc.2025.110574]

