외대쇠치기아재비 추출물의 주요성분 분석을 위한 HPLC 분석 밸리데이션
Abstract
This study aimed to develop and validate a high-performance liquid chromatography (HPLC) method for the quantitative analysis of maysin, a major bioactive flavonoid in Eremochloa ophiuroides extract. The analytical method was validated in accordance with the guidelines of the Ministry of Food and Drug Safety and AOAC with respect to specificity, linearity, accuracy, precision, and sensitivity. Specificity was confirmed by comparing the retention times and UV spectra of maysin in standard and extract samples, demonstrating identical retention times and no interference from coexisting compounds at the maysin peak. Excellent linearity was achieved over a concentration range of 2.5–50 mg/L, with correlation coefficients (R2) of 0.9999 for all three calibration curves. The mean regression equation was determined as y = 3687.8x − 1434.8. Accuracy, evaluated using the standard addition method, showed recoveries ranging from 99.2% to 101.7%, with relative standard deviations (RSDs) of 0.2–1.0%, satisfying AOAC acceptance criteria. Precision was assessed at three concentration levels (50%, 100%, and 150%). Intra-day precision results obtained by two analysts over five consecutive days showed RSD values ranging from 0.10% to 1.43%. Inter-day and inter-analyst precision results demonstrated RSD values ranging from 0.92% to 1.50%, meeting the AOAC acceptance criterion for reproducibility (RSD ≤ 4.0%). The limit of detection (LOD) and limit of quantitation (LOQ) were calculated as 1.28 μg/mL and 3.89 μg/mL, respectively. Using the validated method, the maysin content of E. ophiuroides extract was consistently determined to be approximately 11.60–12.30 mg/g across different sample loading levels (50%, 100%, and 150%) evaluated during precision validation. Collectively, these results demonstrate that the validated HPLC method provides sufficient specificity, linearity, accuracy, precision, and sensitivity, and is suitable for the reliable quantitative analysis and quality control of maysin in E. ophiuroides extracts.
Keywords:
Eremochloa ophiuroides, Maysin, HPLC, Validation외대쇠치기아재비(Eremochloa ophiuroides (Munro) Hack.)는 벼과에 속하는 다년생 식물로 센티페드그라스라는 이명으로 사용된다. 외대쇠치기아재비는 생육이 늦은 난지형 잔디로서 주로 중국이나 동아시아, 인도차이나, 미국 북동부 지역에 서식하며 국내에는 1996년 이전에 유입되어 귀화종으로 분류되어 제주도와 남부 내륙 및 해안가 지방에 분포하고 있다. 외대쇠치기아재비는 주로 잔디밭 또는 뗏장 잔디로 사용되며 높은 잎의 비율과 좋은 맛 때문에 동물용 조사료로 이용되며, 곤충 및 질병 감염에 대한 저항성과 뛰어난 내열성을 가지고 있다.1,2) 외대쇠치기아재비에는 maysin을 비롯하여 chlorogenic acid, isoorientin 및 derhamnosylmaysin 등 다양한 페놀성 및 플라보노이드 계열 화합물이 존재하는 것으로 보고된 바 있다.3-5) 이러한 성분들은 항산화 활성 등 다양한 생리활성과 관련된 천연물 유래 기능성 성분으로 보고되어 있으며, 외대쇠치기아재비의 생리활성과 밀접하게 관련되어 있는 것으로 알려져 있다.3) 그 중 maysin은 외대쇠치기아재비 및 옥수수수염에서 대표적으로 보고된 생리활성물질로 표준물질 확보가 가능하여 분석법 확립 및 정량 분석에 적합한 지표성분으로 활용될 수 있다.
Maysin (Fig. 1)은 1980년대 초 옥수수수염(Zea mays L.)에서 처음으로 발견되었으며, 논문에 최초로 언급된 시기는 1982년이다. Maysin은 플라보노이드 계열의 물질로 항산화, 항암 활성이 뛰어난 물질로 알려져 있으며, 세포독성 효과와 생육 억제 활성, radical 소거 활성 등이 보고되어 있다.6,7) Maysin은 phenylpropanoid-flavonoid 생합성 경로를 통해 생성되는 C-glycosyl flavone 계열 화합물로, luteolin 유도체로부터 효소적 hydroxylation 및 glycosylation 과정을 거쳐 형성되는 것으로 알려져 있다. 이러한 flavonoid 계열 2차 대사산물은 식물에서 자외선 차단, 병원균에 대한 방어, 환경 스트레스 대응 등과 밀접하게 관련된 것으로 보고되어 있으며, 외대쇠치기아재비 또한 이러한 flavonoid 대사를 통해 maysin 및 그 유도체를 생성 · 축적하는 것으로 보고되어 있다.8,9)
Maysin이 산화적 스트레스를 유발시킨 SK-N-SH 세포의 항산화 효소(catalase, SOD-1, SOD-2)의 활성을 증가시켜 산화적 스트레스에 대한 방어 작용으로 인해 뇌 신경세포를 보호한다고 보고된 바 있으며, 종양 세포주에 대한 세포독성 활성 등 maysin에 관한 다양한 생리활성에 대한 연구가 보고되어 있다.6,10,11) 하지만, 옥수수수염에 존재하는 maysin은 옥수수수염이 수정된 후에는 조직의 생장이 정지되고 노화 및 퇴화가 진행되면서 함량이 급격하게 감소한다는 단점과 옥수수의 품종마다 수염에 함유된 maysin의 함량에 차이가 있을 수 있으며, 모든 옥수수 품종에서 maysin이 존재하지 않는다는 단점이 있다.12,13)
이전의 연구에서는 외대쇠치기아재비의 감마선 조사에 의한 생물학적 활성, maysin 함량의 증가, 내염성과 항산화 활성 등 외대쇠치기아재비에 대한 연구가 이루어져 왔으며, ethyl acetate 분획물 내 maysin 및 그 유도체 화합물이 알츠하이머 환자의 체액성 및 세포성 면역 반응과 항염증을 증가시킬 수 있는 보조제에 대한 치료 또는 대체 예방 조치가 될 수 있음을 시사한 바 있다.8,14-16) 또한, 외대쇠치기아재비의 NIH-3T3 섬유아세포에 대한 방사선 보호 효과,17) lipopolysaccharide (LPS)로 유도된 NO 생성 억제 활성,18) Receptor Activator of Nuclear Factor Kappa B Ligand (RANKL)에 의해 유도된 Nuclear Factor of Activated T-cells, cytoplasmic 1 (NFATc1)의 발현 감소 19) 등 외대쇠치기아재비의 효능에 대한 다양한 연구가 보고되어 있다.
천연물을 활용한 건강기능식품, 신약의 개발 및 생산을 위해서는 원료의 표준화와 규격화가 중요한 부분을 차지하며, 기능성 원료의 인정을 위해서는 안전성, 기준과 규격 설정을 위한 과학적인 근거를 제시하여 기능 및 지표성분의 표준화, 원료에 대한 제조 공정의 표준화 등 기준 규격을 설정하는 것이 중요하다. 따라서, 분석방법의 신뢰성을 확보하기 위해 밸리데이션 시험법이 필요하다. 외대쇠치기아재비 추출물을 기능성 소재로 활용하기 위한 연구는 현재까지도 활발하고 진행되고 있으며, 주요 성분인 maysin에 대한 정량 분석법을 개발하는 것은 매우 중요하다. 하지만, 아직까지 외대쇠치기아재비 유래 maysin에 대한 정량 분석법 밸리데이션을 수행한 연구는 보고된 바 없다. 식품의약품안전처의 규정에 따르면 건강기능식품의 기능성 성분 또는 지표성분의 시험법은 ‘건강기능식품의 기준 및 규격’, ‘식품첨가물의 기준 및 규격’ 및 Codex Alimentarius Commission와 AOAC 등의 공인된 방법에 따라 설정되어야 한다고 기술되어 있다. 따라서, 본 연구에서는 생리학적 기능성이 있는 외대쇠치기아재비 추출물의 주요 성분인 maysin의 HPLC 분석법을 국제적 기준에 부합하게 확립하고, 외대쇠치기아재비에 적합한 maysin 정량 분석법을 개발하고자 한다.
재료 및 방법
외대쇠치기아재비 추출물 제조 − 본 실험에 사용된 외대쇠치기아재비는 전용 재배농지(전북특별자치도 익산 소재)에서 수확하였으며, 전용 추출 및 농축 시스템을 이용하여 진행하였다. 외대쇠치기아재비 4 kg을 20배수의 에탄올을 용매로 5일간 침지추출 후 동일 과정을 3일간 반복하였다. 이후, 추출물은 100 mesh 필터를 거쳐 여과한 후 회전감압 농축(40℃)하여 380 g (9.5%)의 추출물을 확보하였다. 실험에 사용된 추출물은 소분하여 냉동(-20℃) 보관하면서 실험에 사용하였다.
시약 및 분석 기기 − 지표성분인 maysin 표준물질은 외대쇠치기아재비로부터 반복적인 컬럼크로마토그래피를 수행하여 순수한 단일물질로 분리정제하고 NMR 및 high-resolution electrospray ionization mass spectrometry 등 분광학적 분석을 수행하여 화합물의 구조를 동정하였다. HPLC 분석 및 시료의 조제에 사용된 용매 및 이동상은 모두 J. T. Baker (Phillipsburg, NJ, USA)사의 제품을 사용하였다. 분석조건은 Table I에 따라 분석되었으며, HPLC 장비는 SPD-20A detector가 장착된 Shimadzu 장비를 사용하였다. 컬럼은 YMC-Pack-ODS-A 302컬럼(4.6 mm I.D. × 150 mm; particle size 5 μm)을 사용하였으며, 컬럼의 온도는 40℃를 유지하였다. Mobile phase는 용매A (0.1% formic acid가 포함된 물)와 B (Acetonitrile)를 분당 1 mL의 유속으로 흘려주었으며, 0분에서 5분까지는 이동상 A와 B를 초기 조건으로 시작하여 Table I에 따라 분석되었다.
시험방법 밸리데이션 항목 및 내용 − HPLC를 이용한 외대쇠치기아재비 추출물의 분석법 밸리데이션은 식품의약품안전처에서 제시한 분석법 검증 가이드라인에 준수하여 수행하였다.
20) 분석법 검증은 특이성, 직선성, 정확성, 정밀성, 검출한계 및 정량한계 항목을 기준으로 진행하였으며, 실제 분석 대상 시료로는 외대쇠치기아재비 추출물을 사용하였다. 검체 투입량에 따른 지표성분(maysin)의 정량 결과를 비교하여 상대표준편차(RSD)를 산출하였다. 이를 통해 단순 표준물질 중심의 분석법 검증을 넘어, 실제 시료 중 지표성분 정량에 대한 분석법의 신뢰성을 검증하였다.
표준용액의 조제 − Maysin 표준물질 1.5 mg을 정밀저울로 정밀하게계량후 2.0 mL 유리바이알에넣고 50% 메탄올을 넣어 초음파 분산시킨 후 정확하게 1.0 mL로 맞춘 후 여과한 액을 표준용액(농도 1.5 mg/mL)으로 조제하였다.
시험용액의 조제 − 외대쇠치기아재비 추출물(Eremochloa ophiuroides extract) 50, 100 및 150 mg을 정밀저울로 정밀하게 계량 후 50% 메탄올을 넣어 초음파 추출하여 분산시킨 후정확하게 10 mL 맞춘후여과한액을 50 (50%), 100 (100%) 및 150 (150%) mg/mL로 시험용액을 조제하였다.
특이성평가 − 외대쇠치기아재비추출물의특이성은 maysin을 선택적으로 정확하게 측정할 수 있는 방법을 의미하며, 특이성을 검증하기 위해 표준용액(Maysin; 1.5 mg/mL)과 시험용액(외대쇠치기아재비 추출물; 5 mg/mL)의 HPL C 크로마토그램을 maysin peak 및 인근 물질 peak의 머무름 시간과 UV 스펙트럼을 비교하여 특이성을 확인하였다.
직선성 평가 − 외대쇠치기아재비 추출물 내 maysin의 농도에 대한 측정값을 검증하기 위해 maysin 표준원액에 50% 메탄올을 첨가하여 2.5, 5, 10, 25 및 50 mg/L 농도의 표준용액을 제조하여 HPL C를 이용하여 측정하였으며 농도별 면적을 구하여 검량선을 작성하였다. 표준용액 제조를 총 3회 반복하여 측정하였으며 결정계수(R2) 값이 0.990 이상인지 여부를 확인하였다.
정확도(회수율) 평가 − 외대쇠치기아재비 추출물 100 mg을 정밀하게 계량 후 50% 메탄올 10 mL을 첨가하여 초음파 추출하여 분산시킨 후 1 mL을 취해 50% 메탄올 9 mL을 가하여 10배 희석한 후 0.45 μm membrane filter로 여과하였다. 이 용액에 표준용액(500 mg/L)을 0.012, 0.024 및 0.036 mL 첨가하여 시험용액을 제조하였다. 해당 시험은 표준용액 제조를 포함하여 일련의 과정을 총 3회 반복하였다.
정밀도(반복성, 재현성) 평가 − 외대쇠치기아재비 추출물의 정밀도 평가를 위해 검체 약 50, 100, 150 mg을 정밀하게 계량하여 50% 메탄올을 넣어 초음파 추출하여 분산시킨 후 정확하게 10 mL로 맞춘 용액을 시험원액으로 하였으며, 이 액 1 mL에 50% 메탄올 9 mL을 가하여 정확하게 10 mL로 맞춘 용액을 시험용액으로 하였다. 검액을 각 농도별로 6회 제조하여 분석 조건에 따라 측정하였으며 6회 측정한 결과값에 대한 함량의 상대표준편차(RSD%)를 구하였다.
정량한계 및 검출한계 측정 − 직선성 시험용액 3 그룹에 대한 검량선을 작성하여 각각의 검량선의 기울기와 y절편을 구한 후 각 검량선에서 기울기의 평균값과 y절편에 대한 표준편차를 구하여 ICH의 규정대로 검출한계 및 정량한계를 구하였다.
결과 및 고찰
특이성 평가 − 외대쇠치기아재비 추출물에서 maysin을 선택적으로 정확하게 측정할 수 있는지 확인하기 위해 특이성 평가를 실시하였다. HPLC를 이용하여 분석한 결과 표준용액(maysin)의 머무름 시간(21.122 min)과 시험용액의 머무름 시간(21.128 min)이 서로 일치함을 확인하였으며, maysin peak 검출 시간에 영향을 미치는 peak가 검출되지 않음을 확인하였다. 따라서, 다른 화합물의 영향을 받지 않고 대상 물질을 선택적으로 정확하게 측정할 수 있음을 확인할 수 있었다(Fig. 2).
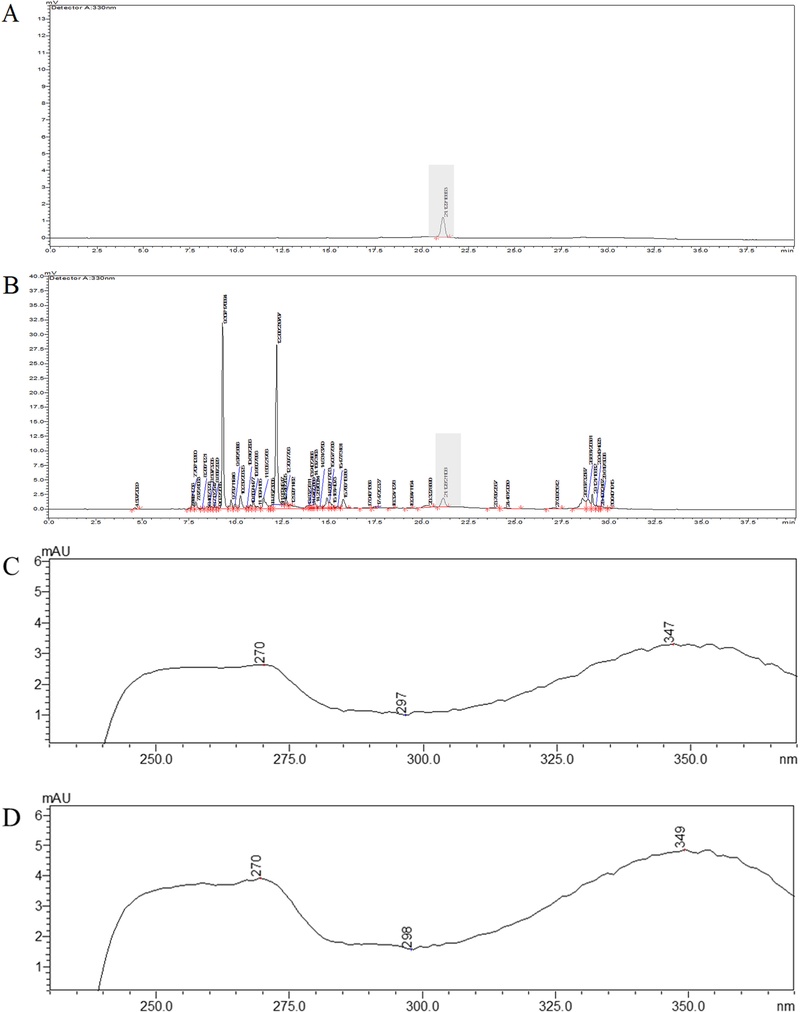
The HPLC chromatograms of maysin standards (A) and Eremochloa ophiuroides extract (B). UV spectrum of maysin (C) and Eremochloa ophiuroides extract (D).
직선성 평가 − 직선성을 입증하기 위해 2.5, 5, 10, 25 및 50 mg/L 농도에서 각 3회 반복 분석하여 평가하였다. 피크 면적을 농도에 대한 함수로 하여 선형 회귀분석을 수행한 결과, 3회 모두 결정계수(R2)가 0.9999 이상으로 나타났으며, 평균 회귀식은 y = 3687.8x − 1434.8로 확인되었다. 또한 기울기의 표준편차는 5.5로 측정 간 변동이 미미함을 확인하였다(Table II). 이상의 결과는 본 HPLC 분석법이 설정된 농도 범위에서 우수한 직선성을 확보하고 있음을 의미한다.
정확도(회수율) 평가 − 외대쇠치기아재비 추출물 내 함유된 maysin의 참값과 가까운 농도의 maysin을 시료에 추가하여 분석하는 표준물질 첨가법을 이용하여 정확도(회수율)를 측정하였다. 그 결과, 평균 회수율은 99.2~101.7% 범위로 나타났으며, 상대표준편차(RSD)는 0.2~1.0%로 확인되었다(Table III). 이는 AOAC 기준(92~105%)을 충분히 만족하는 값으로, 본 HPLC 분석법이 외대쇠치기아재비 추출물 내 maysin의 정량에 대해 우수한 정확도를 갖는 것을 의미한다.
정밀성 평가 − 실험자 A와 B의 외대쇠치기아재비 추출물의 정밀성은 3가지 농도(50%, 100% 및 150%)에서 6회 반복 측정한 일내 정밀도(Intra-day, 반복성)와 측정한 일간 정밀도(inter-day, 실험실 내 정밀도)를 분석하였다. 실험자 A가 5일간 수행한 일내 정밀도 측정 결과 50%, 100% 및 150% 농도에서 일자별 평균 maysin 함량은 12.06~12.30 mg/g (RSD 0.49~1.43%), 11.60~12.02 mg/g (RSD 0.13~1.14%) 및 11.61~11.87 mg/g (RSD 0.10~0.91%)범위로 산출되었다. 실험자 B가 5일간 수행한 일내 정밀도 측정 결과는 11.81~12.11 mg/g (RSD 0.11~0.64%), 11.74~11.99 mg/g (RSD 0.15~0.80%) 및 11.61~11.94 mg/g (RSD 0.27~0.89%)범위로 산출되었다(Table IV). 모든 농도 구간에서 AOAC 기준인 2% 이하를 충족하였다. 실험자 A의 일간 정밀도 측정 결과는 각 농도에서 12.17 ± 0.13 mg/g (RSD 1.09%), 11.88±0.11 mg/g (RSD 1.50%), 11.73±0.13 mg/g (RSD 1.11%)를 나타내었으며, 실험자 B의 일간 정밀도 측정 결과는 각 농도에서 12.02 ± 0.12 mg/g (RSD 1.00%), 11.86±0.11 mg/g (RSD 0.92%), 11.74±0.14 mg/g (RSD 1.21%) 구간을 나타내어 모든 농도 구간에서 AOAC 기준인 4% 이하를 충족하였다(Table V). 재현성은 실험자 A와 B의 측정 결과값을 이용하여 두 실험자의 전체 maysin 평균 함량 차이와 통합 RSD를 통합하여 분석하였다. 50% 농도에서는 각각 12.17 mg/g (RSD 1.09%), 12.02 mg/g (RSD 1.00%)로 산출되었으며, 분석자 간의 상대 평균 maysin 함량 분석 값은 12.09 ± 0.15 mg/g (RSD 1.22%)로 나타났다. 100% 농도에서는 11.88 mg/g (RSD 1.50%), 11.86 mg/g (RSD 0.92%)로 산출되었으며, 상대평균 maysin 함량분석값은 11.87 ± 0.15 mg/g (RSD 1.24%)로 나타났다. 150% 농도에서는 11.73 mg/g (RSD 1.12%), 11.74 mg/g (RSD 1.21%)로 산출되었으며, 상대 평균 maysin 함량 분석 값은 11.73 ± 0.13 mg/g (RSD 1.15%)로 나타났다(Table V). 두 실험자 간 재현성은 모든 농도에서 AOAC 기준인 4% 이하를 충족하였다.
정량한계및검출한계 − Maysin의검출한계(limit of detection, LOD)와 정량한계(limit of quantitation, LOQ)는검량선의기울기와 표준편차를 이용하여 각각 3.3σ/slope 및 10σ/slope에 따라 산출하였다. 그 결과, maysin의 L OD와 L OQ는 각각 1.28 μg/mL과 3.89 μg/mL로 확인되었다. 이는 본 분석법이 외대쇠치기아재비 추출물 내 maysin을 미량 수준에서도 검출 및 정량할 수 있는 충분한 민감도를 보유하고 있음을 나타낸다(Table VI).
결 론
본 연구에서는 외대쇠치기아재비 추출물 내 주요 지표 성분인 maysin의 정량 분석을 위한 HPLC 분석법을 확립하고, 밸리데이션을통해그신뢰성을검증하였다. 특이성평가결과, 표준용액과시험용액의머무름시간이일치하였으며 maysin의 peak 검출에 영향을 미치는 간접 성분이 관찰되지 않아 선택성이 확보됨을 확인하였다. 직선성 평가에서는 2.5~50 mg/L 농도 범위에서 결정계수(R2) 0.9999 이상의 우수한 직선성을 나타내었다. 또한, 정확도(회수율)는 99.2~101.7% 범위로 AOAC 기준을 만족하였으며, 상대표준편차는 0.2~1.0%로 양호한 정확도를 나타내었다. 정밀성 평가 결과, 일내 정밀도(intra-day precision, 반복성)의 RSD는 0.10~1.43% 범위로 나타났으며, 일간 정밀도(inter-day precision) 및 분석자 간 재현성(inter-analyst reproducibility)의 RSD는각각 0.92~1.50% 및 1.00~1.24% 범위로 확인되어 AOAC에서 제시하는 일반적인 허용 기준을 충족하는 우수한 정밀성을 나타내었다. 검출한계(LOD)와 정량한계(LOQ)는 각각 1.28 μg/mL 및 3.89 μg/mL로산출되어본분석법이미량수준의 maysin까지신뢰성 있게검출및정량할수있는충분한민감도를확보하고있음을 확인하였다. 이상의 결과를 종합하였을 때 본 연구에서 확립한 HPLC 분석법은 외대쇠치기아재비 추출물 내 maysin 분석에있어정확성, 정밀성, 민감도및선택성을모두충족하는 신뢰성 높은 분석법으로 판단되며, 향후 기능성 원료의 품질 관리 및 표준화 분석에 유용한 기초 자료로 활용될 수 있을 것으로 사료된다.
Acknowledgments
이 논문은 과학기술정보통신부의 재원으로 연구개발특구진흥재단(메이신-한방 천연물 복합소재 기반 탈모 완화 기능성 화장품 사업화 실증)의 지원을 받아 연구되었음(RS-2024-00416870).
References
-
Reese, J. C., Chan, B. G. and Waiss, A. C. (1982) Effects of cotton condensed tannin, maysin (corn) and pinitol (soybeans) on Heliothis zea growth and development. J. Chem. Ecol. 8: 1429-1436.
[https://doi.org/10.1007/BF00989100]

- Ku, K. M., Kim, S. K. and Kang, Y. H. (2009) Antioxidant activity and functional components of corn silk (Zea mays L.). KJPR 22: 323-329.
- Kang, S. H., Lee, H., Kim, M. Y., Kang, C. W. and Lee, S. S. (2025) Comprehensive Photoprotective Effects of Centipedegrass (Eremochloa ophiuroides) Extract Against Ultraviolet-Induced Skin Damage. Journal of Radiation Industry 19: 173-183.
-
Lee, E. M., Lee, S. S., Chung, B. Y., Cho, J. Y., Lee, I. C., Ahn, S. R. and Kim, T. H. (2010) Pancreatic lipase inhibition by C-glycosidic flavones isolated from Eremochloa ophiuroides. Molecules 15: 8251-8259.
[https://doi.org/10.3390/molecules15118251]

-
Lee, E. M., Bai, H. W., Lee, S. S., Hong, S. H., Cho, J. Y., Lee, I. C. and Chung, B. Y. (2012) Stress-induced increase in the amounts of maysin and maysin derivatives in world premium natural compounds from centipedegrass. Radiation Physics and Chemistry 81: 1055-1058.
[https://doi.org/10.1016/j.radphyschem.2012.01.002]

-
Choi, D. J., Kim, S.L., Choi, J.W. and Park, Y. I. (2014) Neuroprotective effects of corn silk maysin via inhibition of H2O2-induced apoptotic cell death in SK-N-MC cells. Life Sci. 109: 57-64.
[https://doi.org/10.1016/j.lfs.2014.05.020]

-
Lee, E. A., Byrne, P. F., McMullen, M. D., Snook, M. E., Wiseman, B. R., Widstrom, N. W. and Coe, E. H. (1998) Genetic mechanisms underlying apimaysin and maysin synthesis and corn earworm antibiosis in maize (Zea mays L.). Genetics 149: 1997-2006.
[https://doi.org/10.1093/genetics/149.4.1997]

-
Song, Y., Kim, H. D., Lee, M. K., Hong, I. H., Won, C. K., Bai, H. W., and Cho, J. H. (2017) Maysin and its flavonoid derivative from centipedegrass attenuates amyloid plaques by inducting humoral immune response with Th2 skewed cytokine response in the Tg (APPswe, PS1dE9) Alzheimer’s mouse model. PLoS One 12: e0169509.
[https://doi.org/10.1371/journal.pone.0169509]

-
Byrne, P. F., McMullen, M. D., Wiseman, B. R., Snook, M. E., Musket, T. A., Theuri, J. M., and Coe, E. H. (1998) Maize silk maysin concentration and corn earworm antibiosis: QTLs and genetic mechanisms. Crop Science 38: 461-471.
[https://doi.org/10.2135/cropsci1998.0011183X003800020032x]

- Kim, S. L., Snook, M. E. and Lee, J. O. (2003) Radical scavenging activity and cytotoxicity of maysin (C-glycosylflavone) isolated from silks of Zea mays L. KJCS 48: 392-396.
- Kim, S. L., M. E. Snook, E. H. Kim. and C. H. Park. (2000) Identification of maysin and related flavonoid analogues in corn silks. KJCS 45: 151-157.
-
Hanna, W. W. and Burton, G. W. (1978) Cytology, reproductive behavior, and fertility characteristics of centipedegrass 1. Crop Sci. 18: 835-837.
[https://doi.org/10.2135/cropsci1978.0011183X001800050038x]

-
Hanna, W. W. (1995) Centipedegrass diversity and vulnerability. Crop Sci. 35: 332-334.
[https://doi.org/10.2135/cropsci1995.0011183X003500020007x]

- Lee, E. M., Lee, S. S., Hong, S. H., Cho, J. Y., Lee, I. C., and Chung, B. Y. (2011) The remarkable increase of maysin and maysin derivatives contents from Eremochloa ophiuroides by various stresses. Proceedings of the KNS Autumn Meeting. p. 2-2.
-
Lee, E. M., Lee, S. S., Bai, H. W., Cho, J. Y., Kim, T. H. and Chung, B. Y. (2013) Effect of gamma irradiation on the pigments and the biological activities of methanolic extracts from leaves of centipedegrass (Eremochloa ophiuroides Munro). Radiat. Phys. Chem. 91: 108-113.
[https://doi.org/10.1016/j.radphyschem.2013.06.010]

-
Maeda, Y., Nagasawa, T., Tsurumi, T., Iida, K., Nakazawa, R. and Tadano, T. (2011) Physiological characteristics of salt tolerance in centipedegrass (Eremochloa ophiuroides (Munro) Hack. cv. TifBlair). Grassl. Sci. 57: 65-71.
[https://doi.org/10.1111/j.1744-697X.2011.00210.x]

-
Kang, S. H., Bak, D. H., Lee, S. S., Bai, H. W., Chung, B. Y. and Kang, B. S. (2021) Radioprotective effects of centipedegrass extract on NIH-3T3 fibroblasts via anti-oxidative activity. Exp. Ther. Med. 21: 1-10.
[https://doi.org/10.3892/etm.2021.9863]

-
Bai, H. W., Park, C. H., Jang, D. M., Kawala, R. A., Lee, S. S., and Chung, B. Y. (2019) Centipedegrass extracts regulate LPS-mediated aberrant immune responses by inhibiting Janus kinase. Phytomedicine 55: 172-178.
[https://doi.org/10.1016/j.phymed.2018.06.039]

-
Choi, B. Y., Park, C. H., Na, Y. H., Bai, H. W., Cho, J. Y. and Chung, B. Y. (2016) Inhibition of RANKL-induced osteoclast differentiation through the downregulation of c-Fos and NFATc1 by Eremochloa ophiuroides (centipedegrass) extract. Mol. Med. Rep. 13: 4014-4022.
[https://doi.org/10.3892/mmr.2016.5015]

- Korea Food & Drug Administration (2021) Guideline for Recognition of Functional Ingredients for Health Functional Foods. Cheongju.