주목나무 Ethyl acetate 분획의 예쁜꼬마선충 체내의 Lipofuscin 축적억제 효과
Abstract
Lipofuscin is known as an aging pigment observed when aging proceeds in organic organisms. The intestinal lipofuscin value of Caenorhabditis elegans decreased in the experimental group treated with the ethyl acetate fraction of interest compared to the control group. Among several factors related to aging, movement, body length, and exercise of the pharynx were measured to determine the effect of treatment with the Taxus cuspidata S. et Z. ethyl acetate fraction on nematode intake or growth and motility, respectively. The increase in food intake or body length showed no significant change compared to the control group, but the exercise amount showed a significant increase compared to the control group.
Keywords:
Lipofuscin, Taxus cuspidata S. et Z., Caenorhabditis elegans세포는 고분자를 저분자 성분으로 분해하여 지속적으로 재구성하며 calpain, proteasome, lysosome 등을 포함한 여러 분해 시스템을 가지고 있다.1) Lysosome의 결함은 천천히 lipofuscin 형성을 초래한다. Lipofuscin은 생체 내의 산화된 단백질과 지질의 복합물로써 세포 내에서 분해되지 않고 점차 축적되는 물질이다.1,2) Lipofuscin은 산화된 단백질, 지질, Al3+, Ca2+, Cu2+, Fe3+, Zn2+, Mn2+과 같은 금속 이온 등으로 이루어져 있고 주로 노화된 세포에서 관찰되는 노화의 biomarker로서 형광을 발하는 물질이다.3,4) 축적된 lipofuscin은 세포의 기능장애를 일으키고 cell 생존에 문제가 되고 노화를 유도하는 것으로 알려져 있다.1,4) Lipofuscin은 세포 내에서 주로 mitochondria에서 생성된 reactive oxygen species(ROS)에 의해서 lysosome 내에서 분해될 단백질 등이 산화적 손상을 받아 분해가 이루어지지 않고 lysosome 내에 granule로 축적되고 관찰되는 것으로 알려져 있다.5)
주목(Taxus cuspidata S. et Z., Taxaceae)은 한국, 일본, 러시아 남동쪽에 자생하는 상록수 목질 식물로, 전 세계적으로 항종양 활성이 있는 생약으로 잘 알려져 있다.6) T. cuspidata는 Taxus 속 식물들이 주로 생산하는 diterpenoid인 항종양 화합물인 taxol이 알려져 있다.7) T. cuspidata에 대한 연구는 항진균,8) 항암,9) 항당뇨,10) 항산화11) 및 이뇨 효과가 보고되어 있다.12)
본 연구는 항노화 활성 물질을 찾는 과정 중 항암 식물인 주목을 대상으로 노화색소인 lipofuscin의 축적을 억제하는 효능이 있는지를 확인하고자 주목의 메탄올 추출물을 제조하여 예쁜꼬마선충 모델을 이용하여 실험을 진행하였다. 주목 메탄올 추출물의 용매 계통 분획물을 제조하여 가장 강한 DPPH radical 소거 활성을 보인 ethyl acetate 분획을 예쁜꼬마선충을 이용하여 lipofuscin 축적에 미치는 영향을 확인하였으며, 노화와 관련된 선충의 먹이 섭취양과 성장 및 운동성에 미치는 영향을 실험한 결과 몇 가지 효능을 확인하였다.
재료 및 방법
실험재료 – 실험재료인 주목은 완주군에서 재배하는 것을 채집하여 우석대 김대근 교수가 검증한 후에 건조하여 사용하였으며, 표준품은 국산축산과학원에 보관하고 있다(NI25-001).
추출 및 분획 – 건조한 주목 150 g을 50℃에서 메탄올로 5시간씩 2회 추출한 후 수욕상에서 감압농축하여 메탄올 추출물 약 2.7 g을 얻었다. 증류수로 용해하여 methylene chloride (5.7 g), ethyl acetate (1.7 g)과 n-butanol (5.1 g)으로 분획하여 분획물을 얻었다.
DPPH 자유 라디칼 소거능 측정 – 분획물을 농도별로 조제하여 각 시료를 96 well plate에 분주하고, 0.2 mM의 1,1-diphenyl-2-picrylhydrazyl (DPPH) 에탄올 용액을 가하여 10초간 진탕한 후 25℃에서 30분간 반응시켜고 517 nm에서 microplate reader로 흡광도를 측정하였으며 vitamin C를 대조군으로 사용하였다.13)
예쁜꼬마선충 배양 – 예쁜꼬마선충(Caenorhabditis elegans)은 E. coli OP50를 도말한 후 20℃에서 Nematode Growth Medium (NGM) agar plate에서 배양하여 사용하였으며, DMSO에 용해한 주목 분획 시료를 0.1% (v/v)의 DMSO에 용해한 후 NGM plate에서 가하고 선충을 배양하였다.14)
Lipofuscin 축적 효능 측정 – 시료가 첨가된 plate에서 성장 단계를 동일시 한 N2 선충을 배양하였다. 성체가 된 후 8일째 선충을 4% sodium azide로 마취시켰으며, fluorescence microscope (Olympus, Japan)를 사용하여 선충 체내 자가 형광을 띠는 노화색소인 lipofuscin의 축적량을 측정하였다. 형광 발현강도는 Image J software (USA)를 사용하여 관찰하였다.15)
노화 관련인자 분석 – 시료가 첨가된 NGM plate에서 성장 단계를 동일시 한 N2 선충을 배양하였다. 선충의 음식 섭취량을 알아보기 위해 4일째인 성충을 신선한 NGM plate에 1마리씩 옮겨 1분 동안 선충 인두의 움직임을 측정하였다. 선충의 성장과 움직임의 변화 상태는 성체 4일째에 측정하였다. 성장과 움직임 측정은 Olympus software (Olympus, Japan)를 사용하여 측정하였고 모든 실험은 동일 조건 하에 3회 반복하였다.15,16)
통계 분석 – 통계 자료의 값은 평균값 ± 표준오차(mean ± S.E.M.)로 표시하였고, 통계적 유의성의 검증은 ANOVA를 통해서 분석하였다. 선충의 연속적인 생존도는 Log-rank test 분석 방법을 이용하였고, p값은 *p < 0.05, **p < 0.01 일 때 유의성이 있는 것으로 판단하였다.
결 과
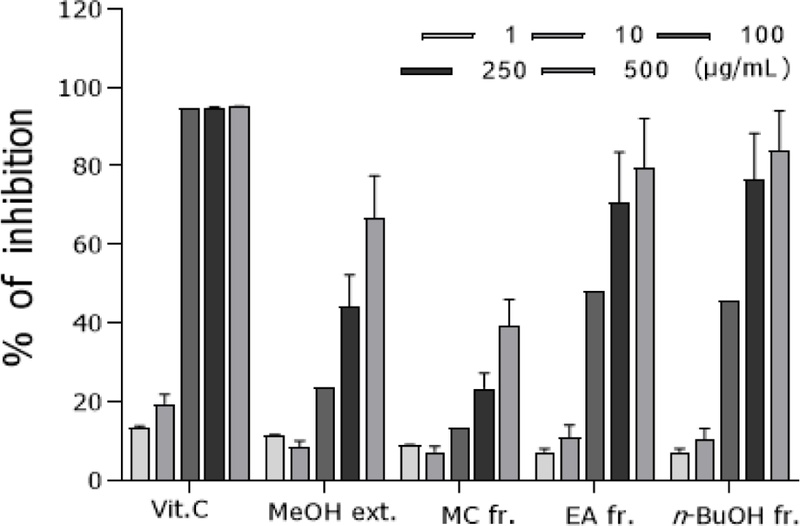
DPPH radical 소거 효과 – 주목 메탄올 추출물 분획의 DPPH radical 소거 효과는 Fig. 1에 나타난 바와 같이 ethyl acetate 분획(IC50 value, 141.3 μg/mL)과 n-butanol 분획(IC50 value, 178.1 μg/mL)이 유사한 효능을 보였으나 ethyl acetate 분획이 더 좋은 radical 소거 효과를 나타냈다(vitamin C, IC50 value, 20.4 μg/mL) (Fig. 1).
lipofuscin 축적량 감소 효능 – 형광 현미경을 이용하여 주목 ethyl acetate 분획이 예쁜꼬마선충 체내 존재하는 노화 색소 lipofuscin의 축적량 감소 효능을 보이는지를 확인하였다. 7일째 선충의 성충을 사용하여 lipofuscin의 형광 발현량을 측정한 결과, 주목 시료를 처리하지 않은 선충군과 비교하여 ethyl acetate 분획 250 μg/mL 처리군에서 21.3% (*p < 0.05), 500 μg/mL 처리군에서 28.8% (*p < 0.05)의 lipofuscin 축적량 감소 효능을 보여주었다(Fig. 2).
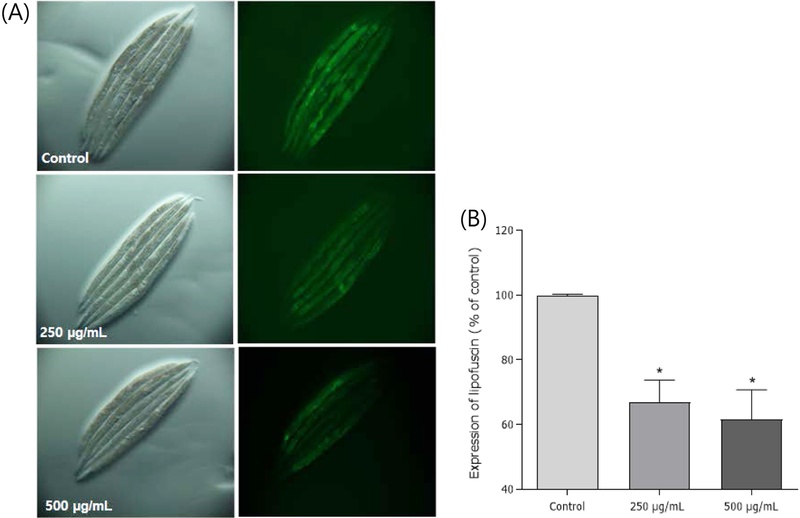
Effects of the ethyl acetate fraction of T. cuspidata on the lipofuscin accumulation in C. elegans. (A) Image of intestinal autofluorescence from lipofuscin accumulation of worms on the 8th adult days. (B) Mean fluorescence intensity of lipofuscin accumulation was expressed as mean ± S.E.M. Differences compared to the control were considered significant at *p < 0.05 by one-way ANOVA.
노화 관련인자의 변화 – 주목 ethyl acetate 분획의 처리가 선충의 수명 관련 인자에 미치는 영향을 확인하기 위해 섭식, 몸길이, 운동량 등을 측정하였다. 대조군에 비하여 선충의 먹이 섭취, 몸길이에 영향을 주지 않았으나, 운동량은 주목 ethyl acetate 분획 처리군이 대조군과 비교하여 ethyl acetate 분획 250 μg/mL 처리군에서 35.0% (*p<0.05), 500 μg/mL 처리군에서 59.3% (*p<0.01)의 운동량이 유의성 있게 증가하는 변화를 보여 주었다(Fig. 3).
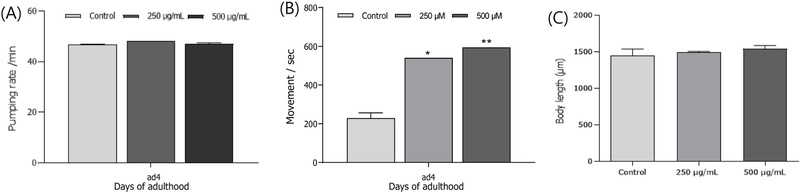
Effects of the ethyl acetate fraction of T. cuspidata on the aging-related factors in C. elegans. (A) On the 4th adult days, the pharynx contraction rates were measured. (B) The body movements were observed under the inverted microscope for 20 seconds. (C) For the growth alteration measurement, photographs were taken of C. elegans, and the body length of worms was analyzed. Data are expressed as the mean ± S.E.M. of three independent experiments. Differences compared to the control were considered significant at *p < 0.05 and **p < 0.05 by one-way ANOVA.
고 찰
예쁜꼬마선충은 1960년대 실험실에 처음 도입된 이래 짧은 수명 주기와 번식의 용이성과 특징적인 발달 계통을 비롯하여 신경계 연결계통이 완전히 밝혀져 있어 동물의 각 기관 발달 과정과 행동을 연구하는데 중요한 모델로 자리 잡았다.17) 선충의 20일 전후의 짧은 수명은 수명 관련 유전자와 신호 전달 기전이 밝혀진 관계로 사람의 노화 연구를 하는데 이용될 수 있다.18) 본 연구는 예쁜꼬마선충 장내에 주로 축적되는 노화 물질인 lipofuscin의 축적양이 주목 ethyl acetate 분획물로 저하되는 효능을 형광 현미경을 통해 확인하고 그 양을 확인하였는데 lipofuscin 값은 대조군에 비해 ethyl acetate 분획 500 μg/mL을 처리한 실험군에서 유의성 있게 감소함을 확인하였다. 또한 노화와 관련되어 나타나는 몇 가지 요인 중 주목 ethyl acetate 분획물을 투여할 때에 변화되는 양상을 확인한 결과 선충의 먹이 섭취량이나 몸길이의 성장은 대조군과 비교하여 유의성 있는 변화를 보이지 않았다. 선충의 운동량은 250 μg/mL과 500 μg/mL 투여군에서 모두 농도 의존적으로 유의성 있는 운동량 증가를 나타내는 것이 관찰되었다. 이러한 결과는 선충의 움직임이 활발해짐으로 lipofuscin의 축적양에 영향을 끼칠 수 있음을 시사한다.19) 추후에 노화 색소인 lipofuscin의 축적 억제 효능을 나타내는 단일 성분의 확인 및 이들 물질에 대한 lipofuscin를 비롯하여 수명연장과 관련된 더 많은 노화 기전연구들이 이루어져야 할 것으로 사료된다.
결 론
Lipofuscin은 유기 생물체에서 노화가 진행될 때 관찰되는 노화색소로 알려져 있다. 예쁜꼬마선충의 장내 lipofuscin 값은 대조군에 비해 주목의 ethyl acetate 분획을 처리한 실험군에서 감소하였다. 노화와 관련된 몇 가지 요인 중에서 주목의 ethyl acetate 분획 처리군이 선충의 식사량이나 성장 및 운동성에 미치는 영향을 확인하기 위해 선충의 인두의 움직임 횟수, 몸길이 및 운동량을 각각 측정하였으며, 먹이 섭취량이나 몸길이의 성장은 대조군과 비교하여 유의성 있는 변화를 보이지 않았으나, 운동량은 대조군에 비해 유의성 있는 증가를 보여 주었다. 추후에 노화 색소인 lipofuscin의 축적 억제 효능을 나타내는 단일 성분의 확인 및 이들 물질에 대한 수명 연장과 관련된 더 많은 노화 기전연구들이 이루어져야 할 것으로 사료된다.
References
-
Terman, A. and Brunk, U. T. (2004) Lipofuscin. Int. J. Biochem. Cell Biol. 36: 1400-1404.
[https://doi.org/10.1016/j.biocel.2003.08.009]

-
Crouch, R. K., Koutalos, Y., Kono, M., Schey, K. and Ablonczy, Z. (2015) A2E and Lipofuscin. Prog. Mol. Biol. Transl. Sci. 134: 449-463.
[https://doi.org/10.1016/bs.pmbts.2015.06.005]

-
Wolf, G. (1993) Lipofuscin, the age pigment. Nutr. Rev. 51: 205-206.
[https://doi.org/10.1111/j.1753-4887.1993.tb03104.x]

- Warburton, S., Davis, W. E., Southwick, K., Xin, H., Woolley, A. T., Burton, G. F. and Thulin, C. D. (2007) Proteomic and phototoxic characterization of melanolipofuscin: correlation to disease and model for its origin. Mol. Vis. 13: 318-329.
-
Boulton, M., Rozanowska, M., Rozanowski, B. and Wess, T. (2004) The photoreactivity of ocular lipofuscin. Photochem. Photobiol. Sci. 3: 759-764.
[https://doi.org/10.1039/b400108g]

-
Kuang, X., Sun, S., Wei, J., Li, Y. and Sun, C. (2019) Iso-Seq analysis of the Taxus cuspidata transcriptome reveals the complexity of taxol biosynthesis. BMC. Plant. Bio. 19: 210.
[https://doi.org/10.1186/s12870-019-1809-8]

-
Gong, Q., Aoki, D., Yoshida, M. and Fukushima, K. (2024) Microscopic distribution of taxanes in freeze-fixed stems of Taxus cuspidata. Front. Chem. 12: 1437141.
[https://doi.org/10.3389/fchem.2024.1437141]

-
Tachibana, S., Ishikawa, H. and Itoh, K. (2005) Antifungal activities of compounds isolated from the leaves of Taxus cuspidata var. nana against plant pathogenic fungi. J. Wood. Sci. 51: 181-184.
[https://doi.org/10.1007/s10086-004-0635-1]

-
Jiang, P., Zhang, Q., Zhao, Y., Xiong, J., Wang, F., Zhang, T. and Zhang, C (2019) Extraction, purification, and biological activities of polysaccharides from branches and leaves of Taxus cuspidata S. et Z. Molecules 24: e2926.
[https://doi.org/10.3390/molecules24162926]

-
Zhang, D., Meng, H. and Yang, H. S. (2012) Antidiabetic activity of Taxus cuspidata polysaccharides in streptozotocin-induced diabetic mice. Int. J. Biol. Macromol. 50: 720-724.
[https://doi.org/10.1016/j.ijbiomac.2011.12.020]

-
Elansary, H. O., Szopa, A., Kubica, P., A Al-Mana, F., Mahmoud, E. A., Zin, E. A. T. K. A., A Mattar, M. and Ekiert, H. (2019) Phenolic compounds of Catalpa speciosa, Taxus cuspidate, and Magnolia acuminata have antioxidant and anti-cancer activity. Molecules 24: e412.
[https://doi.org/10.3390/molecules24030412]

-
Shigemori, H. and Kobayashi, J. (2004) Biological activity and chemistry of taxoids from the Japanese yew, Taxus cuspidata. J. Nat. Prod. 67: 245-256.
[https://doi.org/10.1021/np030346y]

-
Baliyan, S., Mukherjee, R., Priyadarshini, A., Vibhuti, A., Gupta, A., Pandey, R. P. and Chang, C. M. (2022) Determination of antioxidants by DPPH radical scavenging activity and quantitative phytochemical analysis of Ficus religiosa. Molecules 27: 1326.
[https://doi.org/10.3390/molecules27041326]

-
Roux, A. E., Langhans, K., Huynh, W. and Kenyon, C. (2016) Reversible age-related phenotypes induced during larval quiescence in C. elegans. Cell Metab. 23: 1113-1126.
[https://doi.org/10.1016/j.cmet.2016.05.024]

-
Hu, Q., Liu, Z., Guo, Y., Lu, S., Du, H. and Cao, Y. (2021) Antioxidant capacity of flavonoids from Folium Artemisiae Argyi and the molecular mechanism in Caenorhabditis elegans. J. Ethnopharmacol. 279: 114398.
[https://doi.org/10.1016/j.jep.2021.114398]

-
Ji, Y. J., Nam, S., Jin, Y. H., Cha, E. J., Lee, K. S., Choi, K. Y., Song, H. O., Lee, J., Bae, S. C. and Ahnn, J. (2004) RNT-1, the C. elegans homologue of mammalian RUNX transcription factors, regulates body size and male tail development. Dev. Biol. 274: 402-412.
[https://doi.org/10.1016/j.ydbio.2004.07.029]

-
Nechipurenko, I. and Sengupta, P. (2025) C. elegans: An elegant experimental system for the study of cilia biology. Semin. Cell Dev. Biol. 174: 103636.
[https://doi.org/10.1016/j.semcdb.2025.103636]

-
Lin, Y., Lin, C., Cao, Y. and Chen, Y. (2023) Caenorhabditis elegans as an in vivo model for the identification of natural antioxidants with anti-aging actions. Biomed. Pharmacother. 167: 115594.
[https://doi.org/10.1016/j.biopha.2023.115594]

-
Lim, H. J., Han, Y. T., Ahn, J. H., Jeon, Y. D., Jeon, H. and Cha, D. S. (2020) Longevity effects of hispidol in Caenorhabditis elegans. Biofactors 46: 1041-1048.
[https://doi.org/10.1002/biof.1695]